文档内容
物质的分类及转化 达标测试
一、选择题:共16小题,每小题3分,共48分。每小题只有一个选项符合题意。
1.工业上利用 制取盐酸,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.下列变化涉及化学变化的是( )
A.海水提取溴 B.碘的升华 C.切割大理石 D.液氨气化
3.下列化学式或名称表示的物质一定是纯净物的是( )
A. B. C. 丙烯 D. 丁烷
4.当光线通过下列分散系时,能观察到丁达尔效应的是( )
A.稀盐酸 B. 溶液 C.酒精溶液 D. 胶体
5.用特殊方法把固体物质加工到纳米级(1-100nm, )的超细粉末粒子,然后制得
纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A.溶液 B.悬浊液 C.胶体 D.乳浊液
6.下列物质的变化,不能通过一步化学反应完成的是( )
A. B. C. D.
7.下列有关物质分类或归纳正确的是( )
①电解质:明矾、冰醋酸、氯化银、纯碱
②化合物:
③混合物:盐酸、漂白粉、水银
④同素异形体:金刚石、石墨、
A.①② B.②③ C.③④ D.①④
8.下列关于物质分类的正确组合是( )
电解质 盐 碱性氧化物 酸性氧化物
A 硝酸 纯碱 干冰
B 盐酸 食盐 氧化铝 二氧化硫
C 碳酸钙 明矾 氧化镁 二氧化硫
D 氢氧化钠 碳酸钙 生石灰 一氧化碳
A. A B. B C. C D. D
9.下列说法不正确的是( )
A.根据分散系是否具有丁达尔效应将分散系分为溶液、胶体和浊液
B.丁达尔现象可用来区别胶体与溶液
C.胶体的性质主要有丁达尔现象、电泳、渗析和聚沉
D.溶液、胶体、浊液的根本区别是分散质微粒直径的大小10.下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合有( )
序号 X Y Z W
① Si
② Na NaOH NaCl
③ HClO HCl
④ Fe
A.①②③ B.①③④ C.②③ D.①④
11.某化学学习小组讨论辨析以下说法,其中正确的是( )
①福尔马林、聚苯乙烯、油脂、生铁、铝热剂、肥皂均是混合物
②冰和干冰都是酸性氧化物,固体时是分子晶体
③小苏打、硬脂酸钠、 、 都是强电解质
④ 都是非电解质
⑤鸡蛋清溶液、淀粉溶液、烟水晶、雾都是胶体
⑥苯酚、纯碱、胆矾和 分别属于酸、碱、盐和氧化物
A.①③⑤ B.①②④⑤ C.①②③⑤ D.①②③④⑤⑥
12.下列各组物质的分类正确的是( )
①混合物:氯水、氨水、水玻璃、水银、福尔马林、聚乙烯
②电解质:明矾、冰醋酸、石膏、纯碱
③ 均为酸性氧化物, 为碱性氧化物
④同位素:
⑤同素异形体: 、金刚石、石墨
⑥同系物:
⑦同分异构体:乙二酸二乙酯、乙二酸乙二酯
⑧根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
⑨在熔化状态下能导电的化合物为离子化合物
A.②⑤⑨ B.②⑤⑦⑨ C.②④⑤⑥⑦⑨ D.全部正确
13.今有一种固体物质,本身不导电,但其水溶液能够导电。下列说法中不正确的是( )
A.该物质一定为电解质
B.该物质可能为非电解质
C.该物质可能是盐
D.该物质可能是碱
14.下列事实中,与胶体有关的是( )A.家用净水器中活性炭净水
B.饱和 溶液中通入 变浑浊
C.将植物油倒入水中,用力搅拌形成油水混合物
D.一束可见光射入稀豆浆里,从侧面可见一条光亮的“通路”
15.化学与生产、生活及环境密切相关,下列有关说法正确的是( )
A.工业上海水提镁涉及的一系列反应都是氧化还原反应
B.汽车尾气污染物中含有的氮氧化物,是汽油或柴油不完全燃烧造成的
C.江河入海口形成的三角洲与胶体聚沉有关
D.用于光缆通信的光导纤维和制作航天服的聚酯纤维都是新型无机非金属材料
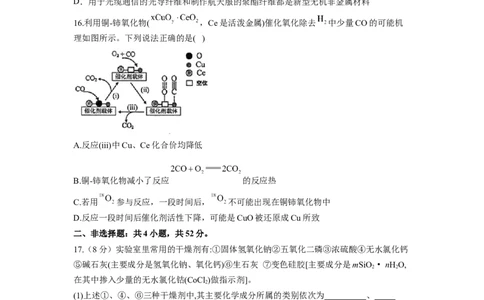
16.利用铜-铈氧化物( ,Ce是活泼金属)催化氧化除去 中少量CO的可能机
理如图所示。下列说法正确的是( )
A.反应(iii)中Cu、Ce化合价均降低
B.铜-铈氧化物减小了反应 的反应热
C.若用 参与反应,一段时间后, 不可能出现在铜铈氧化物中
D.反应一段时间后催化剂活性下降,可能是CuO被还原成Cu所致
二、非选择题:共4小题,共52分。
17.(8分)实验室里常用的干燥剂有:①固体氢氧化钠②五氧化二磷③浓硫酸④无水氯化钙
⑤碱石灰(主要成分是氢氧化钠、氧化钙)⑥生石灰 ⑦变色硅胶[主要成分是mSiO • nHO,
2 2
在其中掺入少量的无水氯化钴(CoCl)做指示剂]。
2
(1)上述①、④、⑥三种干燥剂中,其主要化学成分所属的类别依次为 、
、 (填序号)。
A.酸 B.碱 C.盐 D..氧化物
(2)变色硅胶中无水氯化钴(CoCl)呈蓝色,吸水后变为粉红色的CoCl • 6HO,该变化过程属
2 2 2
于 (填“物理”或“化学”)变化。
(3)生石灰常用做食品干燥剂,久置后易失去干燥能力,其原因为 (用化学方程式表示)。
(4)上述干燥剂中,既可以干燥O,又可以干燥CO 的是 (填序号)。
2 2
18.(8分)分类法是研究物质性质的重要方法。现有 等
物质,根据它们的组成及性质进行如下分类:(1)淡黄色固体最终位于_________组,它的电子式为该物质与水反应,若有2mol电子转
移,则有_________mol该物质参与反应。
(2)写出实验室制备Ⅰ组中气体的化学方程式_________。
(3)B组中的物质能与稀硝酸反应,写出该反应的离子方程式_________。
(4)Ⅱ组中的物质滴入水中后与水剧烈反应产生大量酸雾,写出该反应的化学方程式
_________。
19.(10分)“化学-我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生
活中去”的道理。请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是_______,胶体和溶液的本质区别是
_______。
(2)钠的焰色试验的焰色为_______色,该色的光射程远,透雾力强,据此原理制作的高
压钠灯广泛应用于道路和广场的照明。焰色试验属于_______(填“物理”或“化学”)变化。
过氧化钠是一种淡黄色的固体,可作漂白剂和呼吸面具中的供氧剂,写出过氧化钠和二氧
化碳反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______。
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是_______,原因是_______。
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到
的气体除了挥发的HCl和水蒸气外,还可能有_______(填化学式)。
20.(26分)在通常状况下,A为固态单质。根据如下所示转化关系,回答下列问题。
1.写出A~E的化学式。
A____________;B_________;C________;D__________;E___________。
2.写出下列反应的化学方程式。
①E→C:______________________;
②C→D:_____________________;
③B和C反应:_________________。3.将5 mL 0.10 mol•L-1的C的溶液与5 mL 0.10 mol•L-1的NaOH溶液混合,反应的离子方程
式为____________________。
答案
1.答案:A
解析:
2.答案:A
解析:A.海水提取溴是溴离子变为溴单质,有新物质生成,是化学变化,故A正确; B碘
的升华是物态变化,无新物质生成,是物理变化,故B错误; C切割大理石是发生形变,无新物质生成,是物理变化,故C错误; D液氨气化是物态变化,无新物质生成,故D
错误;故选:A。
3.答案:C
解析:A. 存在同分异构体乙醇和甲醚,不一定为纯净物,故A错误;B. 存
在同分异构体1-氯丙醇,2-氯内醇,不一定为纯净物,故B错误; C丙烯只有一种结构,
为纯净物,故C正确;D.丁烷 存在同分异构体正丁烷和异丁烷,不一定为纯净物,
故D错误;故选:C。
4.答案:D
解析:胶体粒子的微粒直径在1﹣100nm之间,分散质微粒直径小于1﹣100nm的是溶液,
大于1﹣100nm的是浊液; 胶体是胶体,具有丁达尔效应;稀盐酸、 溶液、
酒精溶液是溶液,没有丁达尔效应。
5.答案:C
解析:A.溶液中分散质微粒直径小于1nm,A不选; B.县浊液中分散质微粒直径大于
100nm,B不选; C.胶体中分散质微粒直径在1~100nm之间,C选; D.乳浊液中分散质
微粒直径大于100nm,D不选:
答案选C。
6.答案:B
解析:
7.答案:D
解析:①明矾、冰醋酸、氯化银、纯碱均属于电解质,故选①;
②HT属于单质而非化合物,故不选②;
③水银为汞单质,属于纯净物,故不选③;
④金刚石、石墨以及 互为同素异形体,故选④。
故选①④。
综上所述,本题正确答案为D。
8.答案:C
解析:A.纯碱是碳酸钠,属于盐类化合物, 是过氧化物,不是碱性氧化物,故A错
误;
B.盐酸是氯化氢气体水溶液,为混合物,既不是电解质也不是非电解质,氧化铝是两性氧
化物,故B错误;
C.碳酸钙为电解质,明矾为盐,氧化镁为碱性氧化物,二氧化硫为酸性氧化物,故C正确;
D.一氧化碳是不成盐氧化物,故D错误;
故选:C。
9.答案:B解析:A.丁达尔现象是胶体特有的现象,可用来区别胶体与溶液,A正确;B.分散系根据
分散质粒子直径的大小分为:溶液、胶体和浊液,B错误; C,胶体的性质主要有:丁达
尔现象、电泳、聚沉等,C正确; D.溶液、胶体、浊液的根本区别是分散质微粒直径的大
小,分散质直径介于1nm-100nm的为胶体,小于1nm的为溶液,大于100nm的为浊液,D
正确;故选B。
10.答案:A
解析:① 加热、 、焦炭、Si,满足表中图示物质
在一定条件下一步转化关系,故正确;②Na、水、NaOH、二氧化碳、 、HCl、
NaCl电解Na,满足表中图示物质在一定条件下一步转化关系,故正确;③Fe、氢氧化钙、
、二氧化碳、HClO加热HCl、电解 ,满足表中图示物质在一定条件下一步转
化关系,故正确;④Fe与 反应可生成 , 与Fe反应可得到 , 与
氢氧化钠生成氢氧化亚铁,氢氧化亚铁得不到Fe,故错误;故选A.
11.答案:A
解析: ①福尔马林是甲醛的水溶液,聚苯乙烯属于高聚物,高分子化合物的聚合度是一数
值范围属于混合物,油脂是高级脂防酸甘油酯,属于混合物、生铁属于合金、铝热剂属于
铝和其它金属氧化物的混合物,如铝粉与三氧化二铁的混合物、肥皂通式为RCOOM,式
中RCOO为脂肪酸根,M为金属离子。日用肥皂中的脂肪酸碳数一般为10-18,是混合物,
故①正确;
②冰和干冰固体时都是分子晶体,但冰不是酸性氧化物,故②错误;③小苏打、硬脂酸钠、
是盐,符合强电解质的概念,都是强电解质, 是氧化物属于强电解质,故③
正确;
④ 都是非电解质, 为单质不属于非电解质,故④错误;
⑤鸡蛋清溶液,淀粉溶液,空气,雾分散质微粒符合胶体范围,所以都是胶体,故⑤正确;
⑥苯酚,纯碱分别属于酚、盐,胆矾和 分别属于盐和氧化物,故⑥错误;故选A.
12.答案:A
解析:①纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质,水银是金属
汞单质,故错误;
②在水溶液里或熔融状态下导电的化合物是电解质,明矾、冰醋酸、石膏、纯碱是电解质,
故正确;
③ 不属于酸性氧化物, 是碱性氧化物, 不是碱性氧化物,故错误;
④同位素是指同种元素的不同原子,故错误;
⑤ 、金刚石、石墨都是碳元素形成的不同单质,属于同素异形体,故正确;
⑥ ,结构不一定相似,可能是羧酸也可能是酯,不是
同系物,故错误;⑦乙二酸二乙酯的结构简式: ,乙二酸乙二酯就是一个乙二酸
(HOOCCOOH)和一个乙二醇( )形成的环酯,分子式不同,不是同分异
构体,故错误;
⑧根据酸分子能电离出的氢离子个数,将酸分为一元酸、二元酸等,如 ,1个酸分
子中含有的H原子个数为3个,但电离出1个氢离子,属于一元酸,故错误;
⑨共价化合物在熔化状态下不导电,在熔化状态下能导电的化合物为离子化合物,故正确;
故选A.
13.答案:A
解析:该固体物质本身不导电,溶于水时能够导电,则该物质可能是非电解质如 ,可能是
碱如NaOH,也可能是盐如NaCl。
14.答案:D
解析:A.活性炭净水利用的是活性炭的吸附性,与胶体无关,故A错误; B.饱和
溶液中通入 变浑浊,是二氧化碳与碳酸钠和水反应生成了溶解度较小的碳酸氢钠,与
胶体无关,故B错误; C油水混合物属于浊液,与胶体无关,故C错误; D.一束可见光
射入稀豆浆里,从侧面可见一条光亮的“通路”,是胶体的丁达尔效应,故D正确,故选:
D。
15.答案:C
解析:A.海水提镁时,要把海水中的氯化镁转化为氢氧化镁,氯化镁与碱反应生成氢氧化
镁沉淀的反应属于复分解反应,故A错误;B汽油或柴油属于烃类物质,只含有C、H两
种元素,不含有N元素,汽车尾气污染物中含有的氮氧化物,是空气中的氮气与氧气在高
温下反应生成的,故B错误;C河水中泥土胶粒遇到海水中的电解质会发生聚沉,即在入
海口出聚沉形成沉淀,日积月累形成三角洲,故C正确;D聚酯纤维为有机高分子材料,
光导纤维是传统的无机非金属材料,故D错误,故选C。
16.答案:D
解析:A.反应(iii)中Cu、Ce中的空位结合了氧,氧非金属性较强显负价,则金属元素
Cu、Ce化合价均升高,A错误;B.铜-铈氧化物作为催化剂政变反应速率,不能改变反应
热,B错误;C,由图可知,在反应(iii)中氧分子和催化剂铜-铈氧化物中的空位结合,
反应后1个氧原子进入空位,故一段时间后, 可能出现在铜-铈氧化物中,C错误;D.
一氧化碳具有还原性,会把氧化铜还原为铜单质,反应一段时间后催化剂活性下降,可能
是CuO被还原成Cu所致,D正确;故选D。
17.答案:(1)B;C;D (2)化学(3)CaO+HO=Ca(OH) (4)②③④⑦
2 2
解析: (1)①固体氢氧化钠属于碱,选B,④无水氯化钙属于盐,选C,⑥生石灰属于氧化
物,选D。(2)无 水氯化钴(CoCl )呈蓝色,吸水后变为粉红色的CoCl • 6HO,有新物质
2 2 2
生成,属于化学变化。(3)氧化钙能与水反 应:CaO+HO=Ca(OH)。(4)①固体氢氧化钠和二
2 2
氧 化碳反应,不能用来干燥二氧化碳;②五氧化二磷是酸性干 燥剂,可以干燥氧气和二氧化碳;③浓硫酸和二氧化碳、氧气不反应,可以干燥二氧化碳和氧气;④无水氯化钙是中性
干燥剂,可以干燥二氧化碳和氧气;⑤碱石灰的主要成分是氢氧化钠、氧化钙,可以和二氧
化碳反应,不能干燥二氧化 碳气体;⑥生石灰能和二氧化碳反应,不能干燥二氧化碳气 体;
⑦变色硅胶的主要成分是mSiO2·nHO,在其中掺入 少量的无水氯化钴(CoCl )做指示剂,和
2 2
氧气、二氧化碳不反应,可以干燥二氧化碳和氧气。
18.答案:(1)Ⅰ; ;2
(2)
(3)
(4)
解析:由图中信息可推出甲组物质为单质,乙组物质为化合物,A组为 ,B组为Cu,C
组为CO,Ⅰ组为 ,Ⅱ组为 。
(1)淡黄色固体为 ,可与水反应生成NaOH和氧气,最终位于Ⅰ组, 是由
钠离子和过氧根离子构成的离子化合物,其电子式为 ,根据
可知, 与水反应,若有2mol电子转移,则有2
mol 参与反应。
(2)Ⅰ组中的气体为 ,实验室通过加热氟化铵和 固体混合物制备氢气,其
化学方程式为 。
(3)B组中的物质为铜,铜能与稀硝酸发生氧化还原反应,其离子方程式为
。
(4)Ⅱ组中的物质为 , 与水反应生成HCl和二氧化硫,其化学反应方程式为
。
19.答案:(1) ①. 丁达尔效应 ②. 分散质粒子直径大小不同(2) ①. 黄 ②. 物理 ③.
(3) ①. 有色花瓣变成无色 ②. 氯气和水反应生成了盐酸和次氯酸,次氯酸具有漂
白性
(4)
解析: (1)云、雾属于胶体,鉴别胶体和溶液的方法是∶丁达尔效应,胶体和溶液的本质
区别是∶分散质粒子直径大小不同,
(2)钠的焰色试验的焰色为黄色,焰色试验属于物理变化,过氧化钠和二氧化碳反应的化学
方程式为∶ ,过氧化钠中氧元素化合价-1价升高到0价,
降低到-2 价,结合电子守恒用双线桥法表示电子转移的方向和数目为∶
(3)氯气和水反应生成了盐酸和次氯酸,次氯酸具有漂白性,将新鲜的有色花瓣放入干燥
的氯气中,可观察到的现象是:有色花瓣变成无色,
(4)漂白粉暴露在空气中易变质,次氯酸钙和二氧化碳、水反应生成碳酸钙和次氯酸,次
氯酸分解生成氯化氢和氧气,若向暴露在空气中的漂白粉中加入浓盐酸,氯化钙和次氯酸
钙反应生成氯气,反应的离子方程式为: ,可能收集到的气
体除了挥发的HCl和水蒸气外,还可能有∶ 。
20.答案:1.S;HS;SO ;SO;HSO (浓)
2 2 3 2 4
2.① Cu+2H SO (浓) CusO +SO↑+2H O
2 4 4 2 2
②2SO +O 2SO
2 2 3
③2HS+SO=3S↓+2H O
2 2 2
3.H SO +OH-= +H O
2 3 2
解析:固体单质A能和氧气反应,也能和氢气反应,说明是非金属单质。根据其氧化产物
可继续和氧气反应判断,A是S,和氢气反应生成硫化氢,硫化氢燃烧即生成SO 。硫和氧
2
气反应生成SO ,SO 和氧气反应生成三氧化硫,三氧化硫溶于水生成硫酸。浓硫酸在加热
2 2
的条件下和铜发生氧化还原反应,生成硫酸铜、SO 和水。硫化氢中硫元素的化合价是-2,
2
处于最低价,具有还原性,SO 具有弱氧化性,二者发生氧化还原反应,生成硫单质和水。
2