文档内容
离子反应 达标测试
一、选择题:共15小题,每小题3分,共45分。
1.钠元素在自然界中分布很广,储量极为丰富。金属钠的性质活泼,可与 等物质反
应,钠的化合物 等在生产、生活中应用广泛。
下列物质不属于电解质的是 ( )
A.Na B. C. D.NaOH
2.下列物质在水溶液中的电离方程式错误的是( )
A. B.
C. D.
3.下列物质能导电,但不属于电解质的是( )
A.浓硝酸 B.熔融的NaCl C. 晶体 D.液氨
4.下列物质溶于水不能导电的是( )
A. B. C. D.
5.离子方程式: 中的 不可能来自下列物质中的是
( )
①HCl ② ③ ④ ⑤
A.⑤ B.①④⑤ C.①②③ D.②③⑤
6.下列离子方程式中,书写正确的是 ( )
A. 稀硫酸和铁的反应:2Fe+6H+=2Fe3++3H ↑
2
B. 盐酸和碳酸氢钠溶液反应:2H++ =H O+CO↑
2 2
C. 硫酸铜和氢氧化钡溶液反应: +Ba2+=BaSO ↓
4
D. 铁片插入硫酸铜溶液:Fe+Cu2+=Fe2++Cu
7.在甲、乙两烧杯溶液中,分别含有大量 6种离子中的3
种,已知甲烧杯的溶液呈碱性,则乙烧杯溶液中大量存在的离子是( )
A. 、 、 B. 、 、
C. 、 、Cl- D. 、 、
8.室温时,下列有关电解质的说法正确的是( )
A. pH相等的 和HCN两种酸溶液中,B. NaHB溶液呈酸性,可推知 在水中不能完全电离
C. 往 溶液中加入镁粉,可生成两种气体
D. 溶液中通入 所得的中性溶液中:
9.下列化学用语表示正确的是( )
A.小苏打电离方程式:
B. 的结构示意图:
C. 的电子式:
D. 的名称:乙醚
10.下列反应对应的离子方程式正确的是( )
A. 溶液中滴入稀硝酸:
B.小苏打溶液中加入足量澄清石灰水:
C.酸性高锰酸钾溶液与稀草酸反应:
D. 溶液中加入过量NaOH溶液加热:
11.下列各组离子在溶液中能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
( )
选项 离子 加入试剂 离子方程式
A 稀硫酸
氢氧化钠
B
溶液
少量稀硫
C
酸
过量氢氧
D
化钠溶液
A.A B.B C.C D.D
12.由水电离产生的 为 的溶液中,能大量共存的离子组是( )A. B.
C. D.
13.含氮化合物在水体中过多蓄积会导致水体富营养化,需将其从水体中除去,该过程称为
脱氮。常用的脱氮方法有吹脱法和折点氯化法。
吹脱法:调节水体pH至8左右,然后持续向水中吹入空气。
折点氯化法:调节水体pH至6左右,向水中加入适量 。
下列分析不正确的是( )
A.含氨和铵盐的水体中存在平衡:
B.吹脱法的原理是通过鼓气降低 浓度,从而降低水中 与 的含量
C.折点氯化法除 的原理为:
D.吹脱法无法对含 的水体脱氮,但折点氯化法可以对含 的水体脱氮
14.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是( )
A.滴加石蕊试液显红色的溶液:
B.pH为1的溶液:
C.pH为13的溶液:
D.所含溶质为 的溶液:
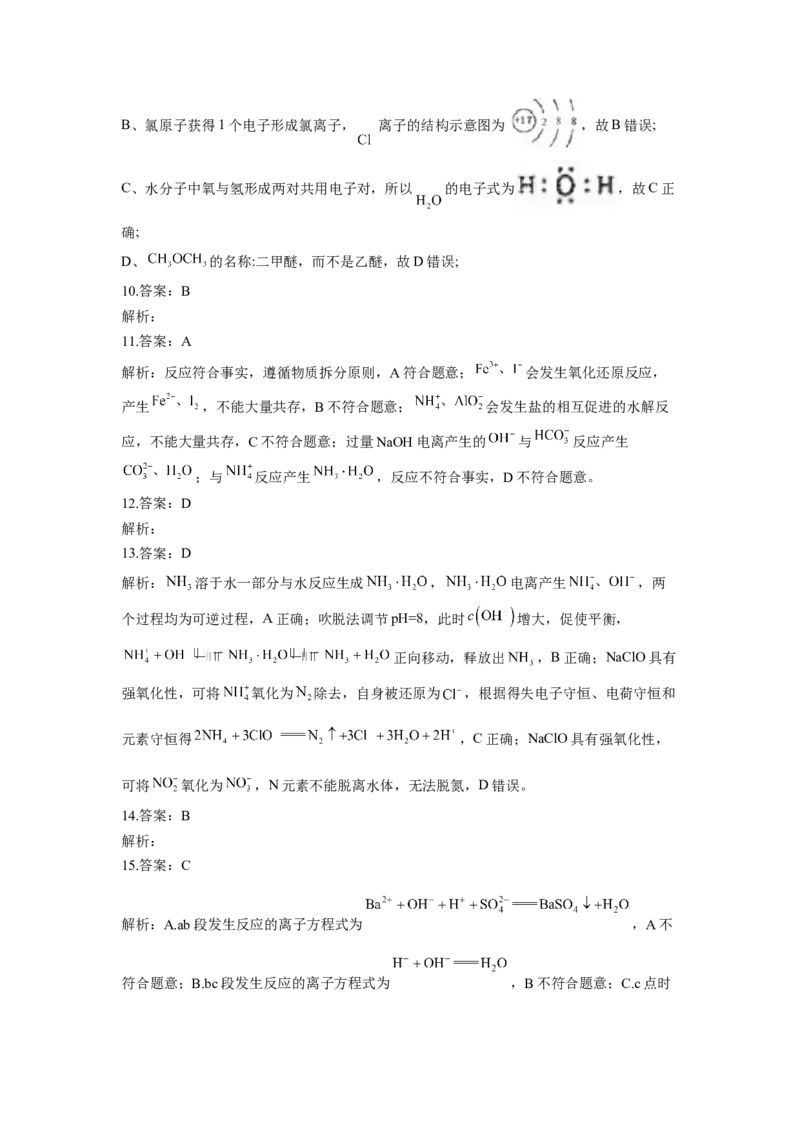
15.向一定浓度的 溶液中滴加 溶液,溶液电导率随滴入 溶液的体
积变化的曲线如图所示。下列分析正确的是( )
A.ab段发生反应的离子方程式
B.bc段发生反应的离子方程式:
C.c点溶液中大量存在的离子是
D.b、d两点对应溶液中的离子总数目相等二、非选择题:共5小题,共55分。
16.(10分)(1)常温下,0.1mol/LNaHB溶液中存在的离子有: 、 、 、 、
,存在的分子只有 ;且 ,则:
①写出酸 的电离方程式___________________。
②常温下,0.1mol/L 溶液 ______0.11mol/L(填 、 或 )。解述理由
___________________。
(2) 时,已知0.1mol/LHCl溶液中 ,现将0.2mol/L的硫酸氢钠
和等浓度的氢氧化钡溶液等体积混合,充分反应后溶液的pH=______。
(3)25℃时,部分物质的电离平衡常数如下表所示:
弱酸化学式
电离平衡常数
下列微粒能大量共存的是______。
A. 、 B. 、
C. 、 D. 、
(4)常温下,等物质的量浓度的 、 、 三种溶液的pH由小到大
的顺序是___________________。
17.(6分)有 、 、 、 四种强电解质,它们在水中电离时可产生下列离子(每种物
质只含一种阴离子且互不重复)。
阳离子 、 、
阴离子 、 、 、
已知:① 、 溶液的 均大于7, 、 的溶液中水的电离程度相同;
② 溶液和 溶液相遇时只生成白色沉淀, 溶液和 溶液相遇时只生成刺激性气味的气
体, 溶液和 溶液混合时无明显现象。
① 是 , 是 。
②用离子方程式表示 溶液呈碱性的原
因 。
18.(16分) 是中学化学中常用试剂。
(1)在 溶液中滴加少量的溴水,振荡,溶液褪色并逸出气体。写出该反应的离子
方程式: 。
(2)测定0.1 mol·L-1 溶液的pH与温度关系如表所示。
时刻 a b c d温度/℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
①用“>”“<”或“=”填空:
水的离子积: (a) (d);水解常数: (a) (b)。
②分别取a、d时刻的溶液各10 mL,加入足量的盐酸酸化的 溶液做对比实验d产生
的白色沉淀比a多。该白色沉淀的化学式是 ;沉淀比a多的原因是 。
③数据显示:a→c的过程中, (填“浓度”或“温度”)对水解平衡移动方向的
影响程度更大。
④为了证明上述规律普遍性,可以选择下列物质做类似实验:该物质是 (填字
母)。
A. B. C. D.
19.(15分)化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择。
阳离子
阴离子
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合加热
后产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝色的气体。
①B的化学式为__________,生成的气体的电子式为___________________。
②A、B溶液混合加热时发生反应的离子方程式为________________。
(2)若A的水溶液呈浅绿色,B的水溶液为无色且其焰色反应为黄色。向A的水溶液中加入
稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合无明显变化。
①A的化学式为________________。
②经分析上述过程中溶液变黄的原因可能有两种:Ⅰ._____________________、Ⅱ.
_____________。(用离子方程式表示)
③请用一种简易方法证明上述溶液变黄的原因___________________________。
20.(8分)甲、乙、丙、丁四种易溶于水的物质,分别由 、Ba2+、Mg2+、H+、OH−、
Cl−、 、 中的不同阳、阴离子各一种组成,已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙容器中滴入AgNO 溶液有不溶于稀HNO 的白色沉淀生成.
3 3
(1)甲是________,乙是________,丙是________,丁是________.
(2)50mL含NaSO 、NaCO 的混合溶液中加入过量的甲溶液,得到14.51g白色沉淀,
2 4 2 3
向白色沉淀中加入过量的稀HNO 充分反应后,沉淀减少到4.66g,并有气体产生.
3
a、写出产生气体的离子方程式_______________________________;
b、混合溶液中Na+的物质的量的浓度是________.答案
1.答案:A
解析:A.钠是单质,既不是电解质也不是非电解质,故A正确;
B氧化钠在熔融状态下能导电,属于电解质,故B错误;
C. 在水溶液中能导电,属于电解质,故C错误;
D. NaOH在水溶液中能导电,属于电解质,故D错误;
故选: A.
2.答案:D
解析:A.氯化钙为强电解质,电离方程式为: ,故A正确; B.硫酸
氢钠为强电解质,在水中完全电离,电离方程式: ,故B正确;
C.硝酸为强电解质,电离方程式为: ,故C正确; D.氯酸钾为强电
解质,电离方程式: ,故D错误;故选:D.
3.答案:A
解析:A.浓硝酸是硝酸的水溶液,能导电,浓硝酸是混合物,既不是电解质又不是非电解
质,故选A;B.熔融的NaCl中离子能自由移动,能导电,NaCl是电解质,故不选B;C.
晶体中离子不能自由移动,不能导电, 晶体属于电解质, 故不选C;D.液氨自
身不能电离,不导电,液氨是非电解质,故不选D;选A。
4.答案:A
解析:A.乙醇属于非电解质,溶于水不导电,故A正确;
B.硝酸钾溶于水电离生成离子,可以导电,故B错误;
C.氢氧化钡属于电解质,溶于水可导电,故C错误;
D.氯气既不是电解质,也不是非电解质,但是氯气溶于水会生成氯化氢和次氯酸,属于电
解质,能导电,故D错误;
故选: A。
5.答案:D
解析:离子方程式: 表示碳酸钡与强酸反应生成可溶
性钡盐、二氧化碳和水。①HCl在水溶液中完全电离,能够与碳酸钡反应生成氯化钡、二氧化碳和水,不符合题意;②硫酸在水溶液中完全电离生成氢离子和硫酸根离子,与碳酸
钡反应时会有硫酸钡沉淀生成,符合题意;③硫酸氢钠在水溶液中完全电离生成钠离子、
氢离子和硫酸根离子,与碳酸钡反应时会有硫酸钡沉淀生成,符合题意;④硝酸属于强酸,
在水溶液中完全电离生成氢离子和硝酸根离子,与碳酸钡反应生成硝酸钡、二氧化碳和水,
不符合题意;⑤碳酸属于弱酸,在离子方程式中写为化学式,符合题意,D正确。
6.答案:D
解析:A.稀硫酸和铁的反应的离子反应为 ,故A错误; B.盐酸和
碳酸氢钠溶液反应的离子反应为 ,故B错误;C.硫酸铜和氢
氧化钡溶液反应的离子反应为 ,故C
错误; D.铁片插入硫酸铜溶液的离子反应为 ,故D正确;故选:D
7.答案:D
解析:甲烧杯的溶液呈碱性,说明甲烧杯中含有 ,与 反应的 、 只能存在
于乙烧杯中,任何溶液都满足电中性,则乙烧杯中必须还有 中的1种阴离子,
由于 与 、 不能共存,乙烧杯中含有的阴离子只能为C,所以乙烧杯溶液中大
量存在的离子是 、 、 ,故选:D。
8.答案:C
解析:本题考查弱电解质的电离平衡、水解平衡。pH相等的 和HCN两种酸溶液中,
相等,根据电荷守恒可知 ,A项错误;NaHB溶液呈酸性,可能
是 ,对应的 在水中能完全电离,B项错误; 溶液中 水解生成
和 ,加入镁粉,镁粉与 反应生成 ,会促进 水解,生成的
较多时会转化为 ,C项正确; 溶液中通入 ,溶液中存在电荷守
恒关系: ,溶液呈中性时,
,则 ,D项错误。
9.答案:C
解析:A. 是弱酸的酸式盐,氢离子不能拆开,小苏打的电离方程式∶
,故A错误;B、氯原子获得1个电子形成氯离子, 离子的结构示意图为 ,故B错误;
C、水分子中氧与氢形成两对共用电子对,所以 的电子式为 ,故C正
确;
D、 的名称:二甲醚,而不是乙醚,故D错误;
10.答案:B
解析:
11.答案:A
解析:反应符合事实,遵循物质拆分原则,A符合题意; 会发生氧化还原反应,
产生 ,不能大量共存,B不符合题意; 会发生盐的相互促进的水解反
应,不能大量共存,C不符合题意;过量NaOH电离产生的 与 反应产生
;与 反应产生 ,反应不符合事实,D不符合题意。
12.答案:D
解析:
13.答案:D
解析: 溶于水一部分与水反应生成 , 电离产生 ,两
个过程均为可逆过程,A正确;吹脱法调节pH=8,此时 增大,促使平衡,
正向移动,释放出 ,B正确;NaClO具有
强氧化性,可将 氧化为 除去,自身被还原为 ,根据得失电子守恒、电荷守恒和
元素守恒得 ,C正确;NaClO具有强氧化性,
可将 氧化为 ,N元素不能脱离水体,无法脱氮,D错误。
14.答案:B
解析:
15.答案:C
解析:A.ab段发生反应的离子方程式为 ,A不
符合题意;B.bc段发生反应的离子方程式为 ,B不符合题意;C.c点时氢氧化钡和硫酸完全反应,只有溶质硫酸钠,C符合题意;D.两点中b点溶液体积小于d
点溶液体积,D不符合题意;故答案为:C。
16.答案:(1). 、 ; < ; 第一步电离产生的 抑制第二
步电离 (2). 12 (3). A (4). 、 、NaHS
解析:本题主要考查弱电解质的电离平衡、盐类水解的应用。
(1)①由于溶液不存在H B,说明H B的第一步电离是完全电离,第二步二元弱酸,则
2 2
电离方程式为H B H HB 、 。
2
HB
H B2
② 电离方程式为H B H HB 、 ,由物料守恒可知
2
H
2
B HB
H B2
c
HB
c
B2
c
Na
0.1mol/L,0.1molL1 H B中由于H B第一步电离中 抑制
2 2
第二步电离,则0.1molL1 H B溶液中c H 0.11molL1。
2
(2)t℃时,0.1molL1 HCl溶液中c OH 11012 molL1 ,此温度下
K 1.01013 mol/L,0.2molL1的硫酸氢钠溶液中c
H
0.2mol/L,等浓度的氢氧
w
化钡溶液中c
OH
0.4mol/L,两者混合后碱过量,溶液显碱性,故混合后溶液中的
c OH 0.40.2 mol/L0.1mol/L,故溶液中的c H 1013 mol/L1012 mol/L,
2 0.1
故溶液的pHlgc
H
12。
(3)电离平衡常数KH C O K HC O KCH COOHKH SK HS ,酸性
2 2 4 2 4 3 2
H C O HC O CH COOHH SHS。
2 2 4 2 4 3 2
A项,CH COOH、C O2之间不反应,能大量共存,故选A项;
3 2 4
B项,HC O、S2反应生成C O2、H S,不能大量共存,故不选B项;
2 4 2 4 2
C项,CH COOH、HS反应生成CH COO、H S而不能大量共存,故不选C项;
3 3 2
D项,HC O、CH COO反应生成C O2、CH COOH而不能大量共存,故不选D项。
2 4 3 2 4 3
综上所述,本题正确答案为A。
(4)电离平衡常数KH C O K HC O KCH COOHKH SK HS ,酸性
2 2 4 2 4 3 2
H C O HC O CH COOHH SHS,水解程度:
2 2 4 2 4 3 2
HC O C O2 CH COO HS S2,则等物质的量浓度的
2 4 2 4 3CH COONa、Na C O 、NaHS三种溶液的pH由小到大的顺序为
3 2 2 4
Na C O CH COONaNaHS。
2 2 4 3
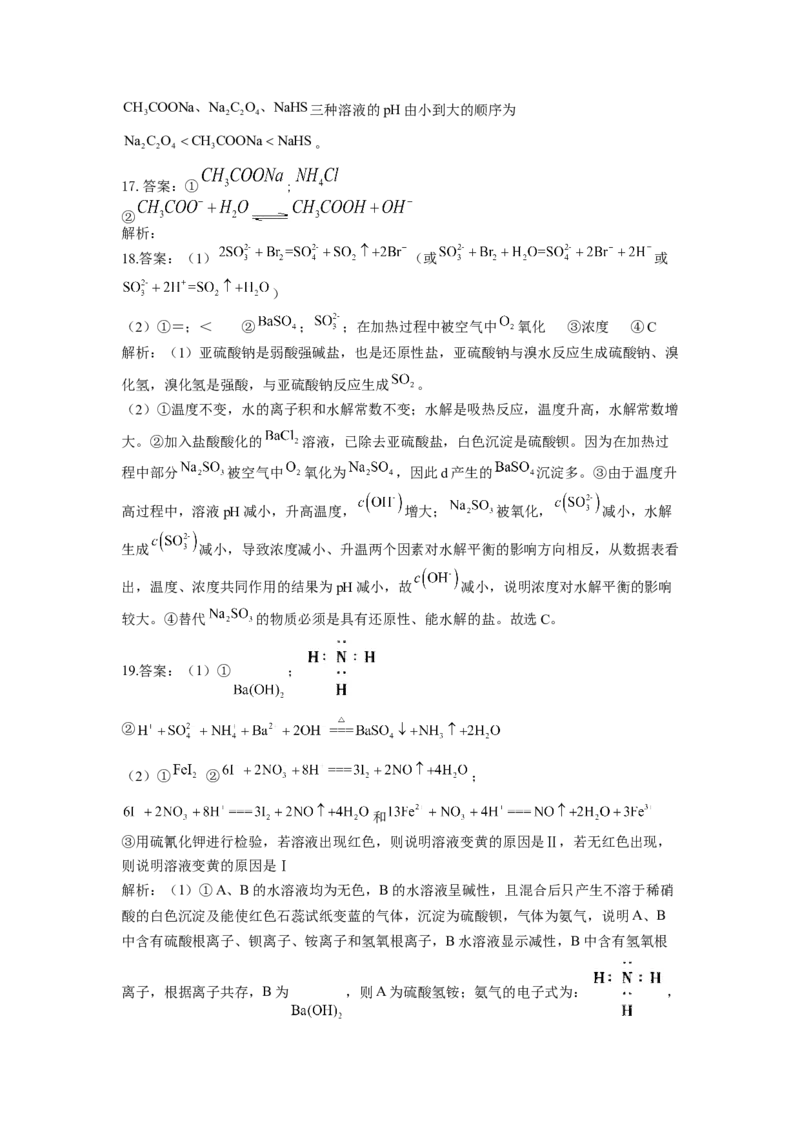
17.答案:① ;
②
解析:
18.答案:(1) (或 或
)
(2)①=;< ② ; ;在加热过程中被空气中 氧化 ③浓度 ④C
解析:(1)亚硫酸钠是弱酸强碱盐,也是还原性盐,亚硫酸钠与溴水反应生成硫酸钠、溴
化氢,溴化氢是强酸,与亚硫酸钠反应生成 。
(2)①温度不变,水的离子积和水解常数不变;水解是吸热反应,温度升高,水解常数增
大。②加入盐酸酸化的 溶液,已除去亚硫酸盐,白色沉淀是硫酸钡。因为在加热过
程中部分 被空气中 氧化为 ,因此d产生的 沉淀多。③由于温度升
高过程中,溶液pH减小,升高温度, 增大; 被氧化, 减小,水解
生成 减小,导致浓度减小、升温两个因素对水解平衡的影响方向相反,从数据表看
出,温度、浓度共同作用的结果为pH减小,故 减小,说明浓度对水解平衡的影响
较大。④替代 的物质必须是具有还原性、能水解的盐。故选C。
19.答案:(1)① ;
②
(2)① ② ;
和
③用硫氰化钾进行检验,若溶液出现红色,则说明溶液变黄的原因是Ⅱ,若无红色出现,
则说明溶液变黄的原因是Ⅰ
解析:(1)①A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝
酸的白色沉淀及能使红色石蕊试纸变蓝的气体,沉淀为硫酸钡,气体为氨气,说明A、B
中含有硫酸根离子、钡离子、铵离子和氢氧根离子,B水溶液显示减性,B中含有氢氧根
离子,根据离子共存,B为 ,则A为硫酸氢铵;氨气的电子式为: ,故答案为 ; ;②硫酸氢铵与氢氧化钡按照物质的量1:1反应,反应
后的溶液显示中性,反应的离子方程式为
,故答案为
;
(2)①A的水溶液呈浅绿色,则A溶液中含有 ,B的水溶液无色且其焰色反应为黄
色,则B溶液中含有Na;向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,
说明A、B中一定存在硝酸根离子,由于向A的水溶液中加入稀盐酸无明显现象,说明硝
酸根离子在B中,即B为 ;能够与亚铁离子形成可溶性的物质有 ,由于
“A、B的水溶液混合亦无明显变化”说明A中一定不含氢离子,所以A为 ,故答案
为: ;②A溶液中的亚铁离子和碘离子都具有还原性,且碘离子还原性强于亚铁离子,
若硝酸根离子不足,溶液变黄的原因碘离子被氧化成碘单质使溶液呈黄色,发生的离子反
应为
;若硝酸根离子足量,氧化完碘离子后还有剩余,
能够继续氧化发生的离子反应为 和
,故答案为
和 ;
③若反应后的溶液中存在铁离子,证明Ⅲ合理,操作方法为:取少量变黄溶液于试管中,
滴加几滴KSCN溶液,若变红则Ⅱ合理,否则Ⅰ合理,故答案为:取少量变黄溶液于试管
中,滴加几滴KSCN溶液,若变红则Ⅲ合理,否则Ⅰ合理。
20.答案:(1)Ba(OH) ; HSO ; MgCl ; (NH )CO
2 2 4 2 4 2 3
(2)BaCO +2H+=Ba2++H O+CO↑; 2.8mol/L
3 2 2