文档内容
热点强化 7 臭氧和过氧化氢
1.臭氧
(1)组成:臭氧的分子式为O,与 O 互为同素异形体。
3 2
(2)物理性质:常温常压下,臭氧是一种有特殊臭味的淡蓝色气体,密度比氧气大,比氧气
易溶于水。吸入少量臭氧对人体无害,吸入过量臭氧对人体健康有一定危害。
(3)化学性质
O 不稳定,容易分解,反应的化学方程式为2O===3O,在放电条件下
3 3 2
不稳定性
空气中的O 可以转化为O,反应的化学方程式为 3O=====2O
2 3 2 3
O 容易使淀粉-KI溶液变蓝色,反应的化学方程式为 2KI+O+
3 3
强氧化性
HO===I+2KOH+O
2 2 2
漂白性 O 因其强氧化性能使有色物质褪色
3
(4)用途
①可用作脱色剂和消毒剂;
②臭氧层可以吸收来自太阳的紫外线,是人类和其他生物的保护伞。
2.过氧化氢
(1)结构
电子式: ,结构式:H—O—O—H。
(2)化学性质
加热、光照或加催化剂都能加快其分解:2HO=====2HO+O↑,因此
2 2 2 2
不稳定性
HO 应保存在棕色瓶中并放置在阴凉处
2 2
弱酸性 相当于二元弱酸:HOH++HO,HOH++O
2 2
①工业上用10%的HO 作为漂白剂,医疗上用3%的HO 作为消毒杀菌剂;
2 2 2 2
②氧化Fe2+、SO等还原性物质:HO+2Fe2++2H+===2Fe3++2HO,HO
2 2 2 2 2
强氧化性
+NaSO ===NaSO +HO;
2 3 2 4 2
③使湿润的淀粉-KI试纸变蓝:HO+2I-+2H+===I+2HO
2 2 2 2
HO 中-1价的氧遇强氧化剂可失去电子转化成0价氧而被氧化,如与酸性
2 2
弱还原性 KMnO 溶液反应:2KMnO +5HO+3HSO ===KSO +2MnSO +5O↑+
4 4 2 2 2 4 2 4 4 2
8HO
2
提醒 ①除MnO 外,Fe3+、Mn2+、Cu2+、Cr3+等也能催化HO 的分解;HO 在碱性环境
2 2 2 2 2
中的分解远比在酸性环境中快。②HO 作氧化剂时,其还原产物一般为水,不引入杂质且对环境无污染,因而又称为绿色
2 2
氧化剂,常用于除去具有还原性的杂质离子。
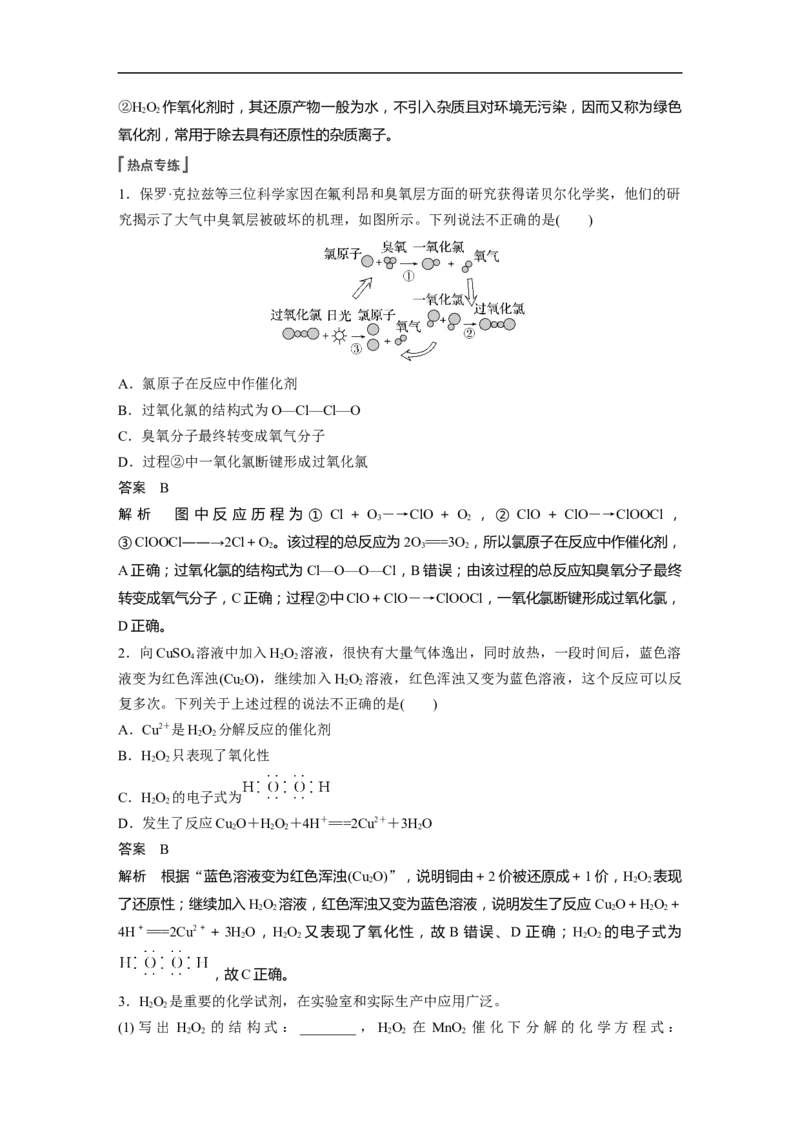
1.保罗·克拉兹等三位科学家因在氟利昂和臭氧层方面的研究获得诺贝尔化学奖,他们的研
究揭示了大气中臭氧层被破坏的机理,如图所示。下列说法不正确的是( )
A.氯原子在反应中作催化剂
B.过氧化氯的结构式为O—Cl—Cl—O
C.臭氧分子最终转变成氧气分子
D.过程②中一氧化氯断键形成过氧化氯
答案 B
解 析 图 中 反 应 历 程 为 ① Cl + O―→ClO + O , ② ClO + ClO―→ClOOCl ,
3 2
③ClOOCl――→2Cl+O 。该过程的总反应为2O===3O ,所以氯原子在反应中作催化剂,
2 3 2
A正确;过氧化氯的结构式为Cl—O—O—Cl,B错误;由该过程的总反应知臭氧分子最终
转变成氧气分子,C正确;过程②中ClO+ClO―→ClOOCl,一氧化氯断键形成过氧化氯,
D正确。
2.向CuSO 溶液中加入HO 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶
4 2 2
液变为红色浑浊(Cu O),继续加入HO 溶液,红色浑浊又变为蓝色溶液,这个反应可以反
2 2 2
复多次。下列关于上述过程的说法不正确的是( )
A.Cu2+是HO 分解反应的催化剂
2 2
B.HO 只表现了氧化性
2 2
C.HO 的电子式为
2 2
D.发生了反应Cu O+HO+4H+===2Cu2++3HO
2 2 2 2
答案 B
解析 根据“蓝色溶液变为红色浑浊(Cu O)”,说明铜由+2价被还原成+1价,HO 表现
2 2 2
了还原性;继续加入HO 溶液,红色浑浊又变为蓝色溶液,说明发生了反应 Cu O+HO +
2 2 2 2 2
4H+===2Cu2++3HO,HO 又表现了氧化性,故 B 错误、D 正确;HO 的电子式为
2 2 2 2 2
,故C正确。
3.HO 是重要的化学试剂,在实验室和实际生产中应用广泛。
2 2
(1)写出 HO 的结构式:________,HO 在 MnO 催化下分解的化学方程式:
2 2 2 2 2________________________________________________________________________。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入 HO 后,则可使铜顺利溶解,写出
2 2
该反应的离子方程式:___________________________________________________
________________________________________________________________________。
②在“海带提碘”的实验中,利用酸性HO 得到碘单质的离子方程式是________________。
2 2
③你认为HO 被称为绿色氧化剂的主要原因是
2 2
________________________________________________________________________
________________________________________________________________________。
(3)H O 还有一定的还原性,能使酸性KMnO 溶液褪色。
2 2 4
①写出反应的离子方程式:_____________________________________________
________________________________________________________________________。
②实验室常用酸性 KMnO 标准液测定溶液中 HO 的浓度,酸性 KMnO 溶液应盛放在
4 2 2 4
______(填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是_________________。
(4)H O 是一种二元弱酸,写出其第一步电离的方程式:______________________,
2 2
它与过量的Ba(OH) 反应的化学方程式为___________________________________
2
________________________________________________________________________。
答案 (1)H—O—O—H 2HO=====2HO+O↑
2 2 2 2
(2)①HO +Cu+2H+===Cu2++2HO ②HO +2I-+2H+===2HO+I ③还原产物为水,
2 2 2 2 2 2 2
对环境无污染
(3)①5HO+2MnO+6H+===5O↑+2Mn2++8HO
2 2 2 2
②酸式 滴入最后一滴酸性KMnO 标准液后,溶液变浅紫色,且30 s 内不褪色
4
(4)H OH++HO HO+Ba(OH) ===BaO+2HO
2 2 2 2 2 2 2