文档内容
热点强化 9 亚硝酸及亚硝酸钠的性质
1.亚硝酸(HNO)
2
亚硝酸是弱酸。向亚硝酸钠溶液中加酸,生成亚硝酸(HNO)。亚硝酸不稳定,仅存在于冷
2
的稀溶液中,微热甚至常温下也会分解,产生红棕色的二氧化氮气体。
NaNO +HSO (稀)===NaHSO+HNO
2 2 4 4 2
2HNO===NO↑+NO ↑+HO
2 2 2
2.亚硝酸钠(NaNO )
2
(1)亚硝酸钠的物理性质及用途
亚硝酸钠的化学式为NaNO ,是可溶性盐。其熔点为271 ℃,分解温度为320 ℃。
2
亚硝酸钠在建筑业中常用作混凝土掺加剂,以促进混凝土凝固,提高其强度,防止在冬天低
温施工时混凝土发生冻结。
亚硝酸钠还是一种食品添加剂,用作食品防腐剂和肉类食品的发色剂。
(2)亚硝酸钠的氧化性
在亚硝酸钠中,氮的化合价为+3,处于中间价态。因此,亚硝酸钠与强还原性物质反应时,
表现出氧化性。如亚硝酸钠与碘化钾反应可生成单质碘。
2NO+2I-+4H+===2NO↑+I+2HO
2 2
析出的碘可以使淀粉溶液变蓝色,据此可以检验NO的存在。
亚硝酸钠与FeCl 溶液反应,生成棕黄色的FeCl 溶液。
2 3
NO+Fe2++2H+===NO↑+Fe3++HO
2
(3)亚硝酸钠的还原性
亚硝酸钠与强氧化性物质反应时,表现出还原性。如亚硝酸钠与KCr O 酸性溶液反应时,
2 2 7
Cr O被还原成Cr3+,KCr O 溶液由橙色变为绿色。
2 2 2 7
Cr O +3NO+8H+===3NO+2Cr3++4HO
2 2
(4)亚硝酸钠与氯化钠的鉴别
与氯化钠不同,亚硝酸钠与AgNO 溶液反应生成的AgNO 沉淀可溶于稀硝酸。
3 2
1.NaNO 像食盐一样有咸味,有很强的毒性,误食亚硝酸钠(NaNO )会使人中毒。已知亚
2 2
硝酸钠能发生如下反应:2NaNO +4HI===2NO↑+I +2NaI+2HO。下列说法正确的是(
2 2 2
)
A.该反应的氧化剂为HI
B.反应产物中能使淀粉变蓝的物质有I、NaI
2
C.该反应中氧化剂与还原剂的物质的量之比为1∶1D.人误食亚硝酸钠中毒时,可以服用HI溶液解毒
答案 C
2.(1)鉴别NaNO 、NaCl可选用的物质有①水、②淀粉-KI试纸、③淀粉、④白酒、⑤食醋。
2
根据上述反应,你认为必须选用的物质有________(填序号)。
(2)某厂废液中,含有2%~5%的NaNO ,直接排放会造成污染,下列试剂能使NaNO 转化
2 2
为N 的是________(填字母)。
2
A.NaCl B.NH Cl
4
C.HNO D.浓HSO
3 2 4
(3)已知反应10Al+6NaNO +4NaOH===10NaAlO +3N↑+2HO。若该反应过程中转移
3 2 2 2
5 mol e-,则生成标准状况下N 的体积为____ L。
2
答案 (1)②⑤ (2)B (3)11.2
解析 (1)水、淀粉、白酒与NaNO 都不反应,所以无明显现象;KI与NaNO 必须在酸性条
2 2
件下才能反应得到I,食醋会电离出氢离子,故必须选用的物质有②⑤。(2)NaNO ―→N,
2 2 2
NaNO 被 还 原 , 必 须 加 还 原 剂 , 故 选 NH Cl 。 (3) 在 反 应 10Al + 6NaNO +
2 4 3
4NaOH===10NaAlO +3N↑+2HO中溶解 10 mol Al 转移 30 mol 电子,同时生成 3 mol
2 2 2
N 。若反应过程中转移5 mol e-,则生成标准状况下N 的体积为5 mol××22.4 L·mol-1=
2 2
11.2 L。
3.信息1:亚硝酸(HNO)是一种弱酸,既具有氧化性又具有还原性;亚硝酸不稳定,易分
2
解为硝酸、水和NO。信息2:亚硝酸钠又名“工业盐”,常被大量用作高分子材料的发泡
剂和偶氮染料的原料等,该物质有毒,但其颜色、形状、味道和食盐相似,很容易因误食而
中毒;亚硝酸银为难溶于水的白色沉淀。
根据上述信息,回答下列问题:
(1)甲组同学取一份可能是NaCl或NaNO 的样品,用蒸馏水溶解,通过下列实验操作鉴别样
2
品成分。在待检验溶液中滴加AgNO 溶液的现象是________________,倒出上清液,在沉
3
淀中加入硝酸,振荡,沉淀溶解,则该样品为______________(写化学式),沉淀溶解的离子
方程式为________________________________________________________________________
________________________________________________________________________。
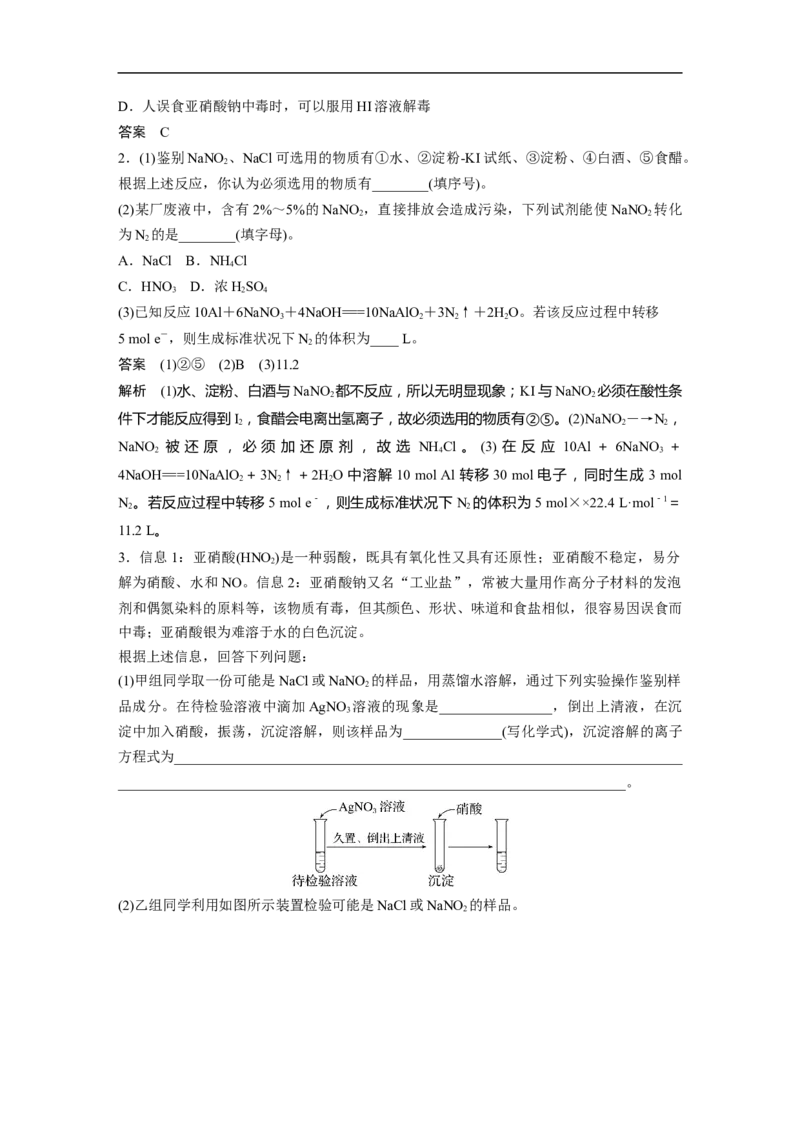
(2)乙组同学利用如图所示装置检验可能是NaCl或NaNO 的样品。
2①A装置中盛装稀硫酸的仪器名称是______________,打开该仪器的活塞,使稀硫酸缓缓滴
下,若样品为NaNO ,则在B装置中可观察到的现象为____________________,检验B装
2
置中有NO的操作及产生的现象是________________________。
②C装置中盛有的试剂名称是________________,作用是_____________________。
(3)设计实验证明。
①亚硝酸为弱酸:_______________________________________________________。
②亚硝酸具有还原性:___________________________________________________。
答案 (1)产生白色沉淀 NaNO 3AgNO +2H+===3Ag++2NO↑+NO+HO (2)①分液
2 2 2
漏斗 出现较淡的红棕色气体 打开止水夹,鼓入空气,红棕色变深 ②NaOH溶液(答案
合理即可) 吸收尾气 (3)①取NaNO 溶液,用pH试纸检验,对照标准比色卡知pH>7(其
2
他合理答案也可)
②在酸性KMnO 溶液中加入过量NaNO 溶液,溶液褪色(其他合理答案也可)
4 2
解析 (1)AgCl和AgNO 均为白色难溶于水的物质,故加入AgNO 溶液后出现白色沉淀。
2 3
AgCl难溶于硝酸,而AgNO 与硝酸反应可生成HNO,该物质不稳定,又分解生成硝酸、
2 2
水和NO。(2)①A装置和B装置中残留的空气与A装置中生成的NO反应生成NO 。由于B
2
装置中主要含NO,故其内气体颜色较淡,打开止水夹,鼓入空气,NO完全转化为NO ,
2
使B装置内NO 浓度增大,红棕色变深。②氮的氧化物有毒,可用碱液(如NaOH溶液)吸收。
2
(3)①检验HNO 的弱酸性,可检验其强碱盐的pH,也可以直接检验其一定浓度稀溶液的pH
2
等。②检验HNO 的还原性需要用到氧化剂,故在酸性KMnO 溶液中加入过量NaNO 溶液,
2 4 2
KMnO 被还原,从而使溶液褪色。
4