文档内容
必做实验提升(四) 不同价态含硫物质的转化
1.-2价S→0价S
实验步骤:在两支试管中分别加入1 mL硫化钠溶液,向其中一支边振荡边滴加亚硫酸溶液,
另一支边振荡边滴加酸性高锰酸钾溶液,用浸有氢氧化钠溶液的棉团塞住试管口,观察并记
录实验现象。
答案 硫化钠转化为单质硫,硫元素化合价由-2价转化为0价,观察到的现象是有淡黄色
沉淀生成。
2.根据硫元素的化合价分析HSO 具有氧化性还是还原性?怎样利用实验验证HSO 具有
2 3 2 3
的性质?
答案 硫元素的最高正价是+6价,最低负价是-2价,HSO 中硫元素为+4价,因此
2 3
HSO 既有氧化性又有还原性。可以利用HSO 与NaS或HS反应,验证HSO 具有氧化性;
2 3 2 3 2 2 2 3
利用HSO 与酸性KMnO 溶液反应,验证HSO 具有还原性。
2 3 4 2 3
3.+6价S→+4价S
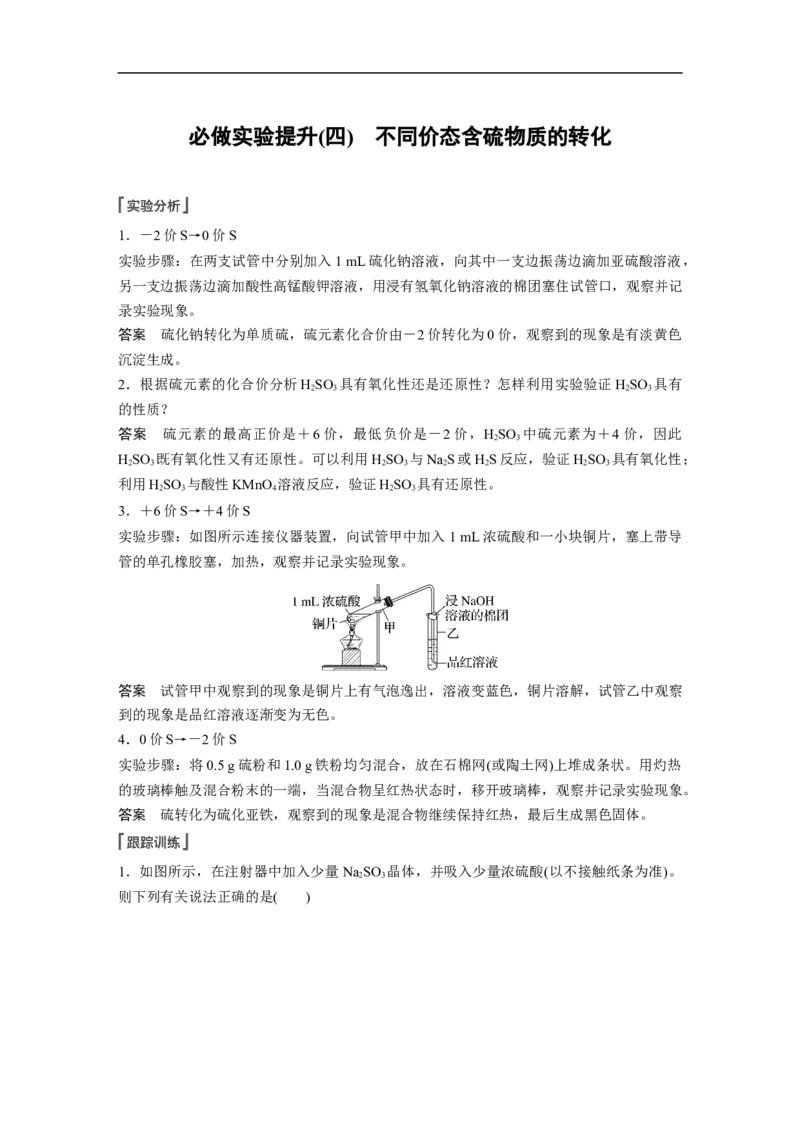
实验步骤:如图所示连接仪器装置,向试管甲中加入1 mL浓硫酸和一小块铜片,塞上带导
管的单孔橡胶塞,加热,观察并记录实验现象。
答案 试管甲中观察到的现象是铜片上有气泡逸出,溶液变蓝色,铜片溶解,试管乙中观察
到的现象是品红溶液逐渐变为无色。
4.0价S→-2价S
实验步骤:将0.5 g硫粉和1.0 g铁粉均匀混合,放在石棉网(或陶土网)上堆成条状。用灼热
的玻璃棒触及混合粉末的一端,当混合物呈红热状态时,移开玻璃棒,观察并记录实验现象。
答案 硫转化为硫化亚铁,观察到的现象是混合物继续保持红热,最后生成黑色固体。
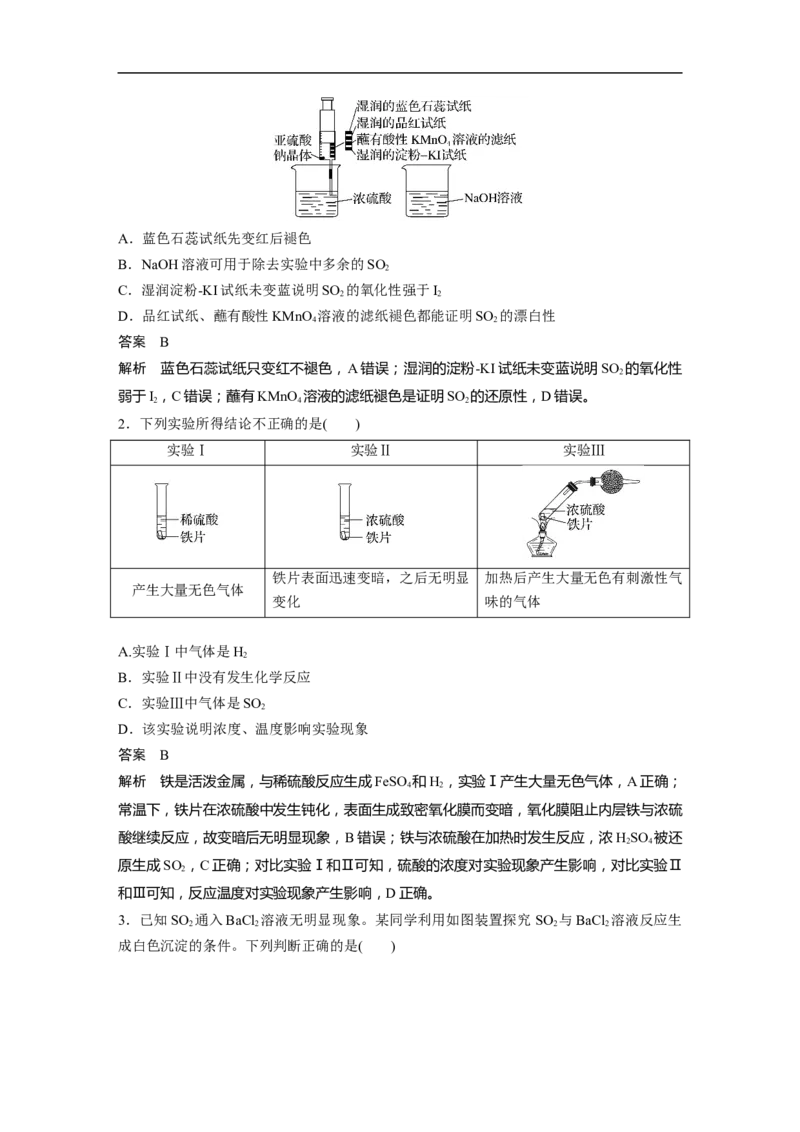
1.如图所示,在注射器中加入少量NaSO 晶体,并吸入少量浓硫酸(以不接触纸条为准)。
2 3
则下列有关说法正确的是( )A.蓝色石蕊试纸先变红后褪色
B.NaOH溶液可用于除去实验中多余的SO
2
C.湿润淀粉-KI试纸未变蓝说明SO 的氧化性强于I
2 2
D.品红试纸、蘸有酸性KMnO 溶液的滤纸褪色都能证明SO 的漂白性
4 2
答案 B
解析 蓝色石蕊试纸只变红不褪色,A错误;湿润的淀粉-KI试纸未变蓝说明SO 的氧化性
2
弱于I,C错误;蘸有KMnO 溶液的滤纸褪色是证明SO 的还原性,D错误。
2 4 2
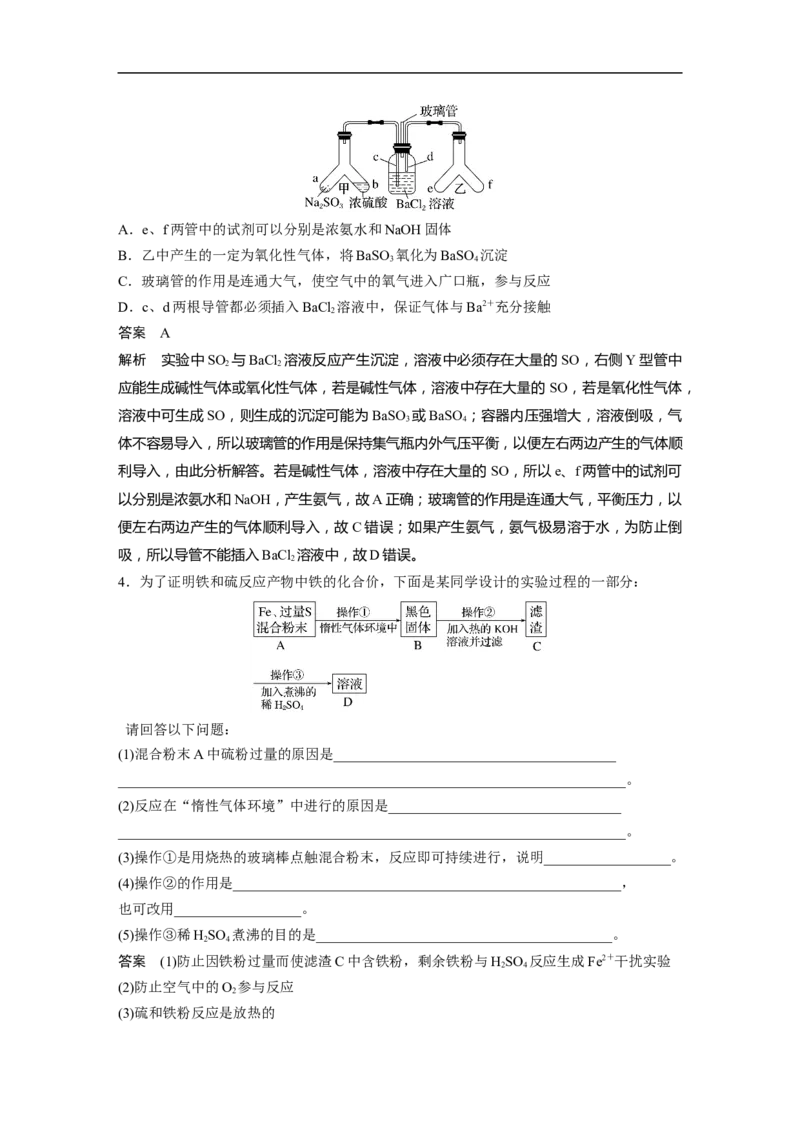
2.下列实验所得结论不正确的是( )
实验Ⅰ 实验Ⅱ 实验Ⅲ
铁片表面迅速变暗,之后无明显 加热后产生大量无色有刺激性气
产生大量无色气体
变化 味的气体
A.实验Ⅰ中气体是H
2
B.实验Ⅱ中没有发生化学反应
C.实验Ⅲ中气体是SO
2
D.该实验说明浓度、温度影响实验现象
答案 B
解析 铁是活泼金属,与稀硫酸反应生成FeSO 和H,实验Ⅰ产生大量无色气体,A正确;
4 2
常温下,铁片在浓硫酸中发生钝化,表面生成致密氧化膜而变暗,氧化膜阻止内层铁与浓硫
酸继续反应,故变暗后无明显现象,B错误;铁与浓硫酸在加热时发生反应,浓HSO 被还
2 4
原生成SO ,C正确;对比实验Ⅰ和Ⅱ可知,硫酸的浓度对实验现象产生影响,对比实验Ⅱ
2
和Ⅲ可知,反应温度对实验现象产生影响,D正确。
3.已知SO 通入BaCl 溶液无明显现象。某同学利用如图装置探究SO 与BaCl 溶液反应生
2 2 2 2
成白色沉淀的条件。下列判断正确的是( )A.e、f两管中的试剂可以分别是浓氨水和NaOH固体
B.乙中产生的一定为氧化性气体,将BaSO 氧化为BaSO 沉淀
3 4
C.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
D.c、d两根导管都必须插入BaCl 溶液中,保证气体与Ba2+充分接触
2
答案 A
解析 实验中SO 与BaCl 溶液反应产生沉淀,溶液中必须存在大量的SO,右侧Y型管中
2 2
应能生成碱性气体或氧化性气体,若是碱性气体,溶液中存在大量的 SO,若是氧化性气体,
溶液中可生成SO,则生成的沉淀可能为BaSO 或BaSO ;容器内压强增大,溶液倒吸,气
3 4
体不容易导入,所以玻璃管的作用是保持集气瓶内外气压平衡,以便左右两边产生的气体顺
利导入,由此分析解答。若是碱性气体,溶液中存在大量的 SO,所以e、f两管中的试剂可
以分别是浓氨水和NaOH,产生氨气,故A正确;玻璃管的作用是连通大气,平衡压力,以
便左右两边产生的气体顺利导入,故C错误;如果产生氨气,氨气极易溶于水,为防止倒
吸,所以导管不能插入BaCl 溶液中,故D错误。
2
4.为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
请回答以下问题:
(1)混合粉末A中硫粉过量的原因是________________________________________
________________________________________________________________________。
(2)反应在“惰性气体环境”中进行的原因是_________________________________
________________________________________________________________________。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明__________________。
(4)操作②的作用是_______________________________________________________,
也可改用__________________。
(5)操作③稀HSO 煮沸的目的是__________________________________________。
2 4
答案 (1)防止因铁粉过量而使滤渣C中含铁粉,剩余铁粉与HSO 反应生成Fe2+干扰实验
2 4
(2)防止空气中的O 参与反应
2
(3)硫和铁粉反应是放热的(4)除去混合物中的硫粉 CS
2
(5)防止稀HSO 溶液溶解的氧气氧化生成的Fe2+
2 4
5.亚硫酸钠中有+4价的硫,它既有氧化性又有还原性。现有试剂:溴水、NaS溶液、
2
NaSO 溶液、稀HSO 、NaOH溶液、氨水。
2 3 2 4
(1)要证明 NaSO 具有还原性,应选用的试剂有____________________,看到的现象是
2 3
____________________,反应的化学方程式为_______________________________
________________________________________________________________________。
(2)要证明 NaSO 具有氧化性,应选用的试剂有____________________,看到的现象是
2 3
____________________,反应的离子方程式为_______________________________
________________________________________________________________________。
答案 (1)Na SO 溶液、溴水 溴水褪色 NaSO +Br +HO===NaSO +2HBr
2 3 2 3 2 2 2 4
(2)Na SO 溶液、NaS溶液和稀硫酸 生成浅黄色沉淀 2S2-+SO+6H+===3S↓+3HO
2 3 2 2
6.某小组同学设计如下实验实现几种价态硫元素间的转化。
任务Ⅰ.从以下试剂中选择合适的试剂实现S(+6)→S(+4)的转化。
试剂:①浓HSO ②稀HSO ③酸性KMnO 溶液 ④NaSO 溶液 ⑤Cu ⑥品红溶液
2 4 2 4 4 2 3
(1)写出实现转化的化学方程式:___________________________________________
________________________________________________________________________。
(2)设计实验,证明实现了该转化(写出操作和现象):_________________________。
任务Ⅱ.实现硫元素化合价在0、+2、+4价之间的转化。
查阅资料:+2价硫元素在酸性条件下不稳定,自身易发生氧化还原反应。
SO ――→NaSO 溶液――→NaSO――→X
2 2 3 2 2 3
(3)①中加入的物质是______________,该转化利用的是SO __________的性质。
2
(4)写出③的离子方程式:_________________________________________________。
答案 (1)Cu+2HSO (浓)=====CuSO +SO ↑+2HO (2)将产生的气体通入品红溶液中,
2 4 4 2 2
溶液褪色 (3)NaOH溶液 酸性氧化物 (4)2H++SO===S↓+SO ↑+HO
2 2 2
解析 (4)根据题干信息,+2价硫元素在酸性条件下不稳定,自身易发生氧化还原反应,即
发生歧化反应,+2价的硫元素化合价既升高又降低,结合步骤②中亚硫酸钠和X反应生成
硫代硫酸钠分析,可得X中硫元素的化合价应低于+2价,则X为硫单质,③的离子方程式
为2H++SO===S↓+SO ↑+HO。
2 2 2