文档内容
专项特训 6 弱电解质电离常数计算与图像分析
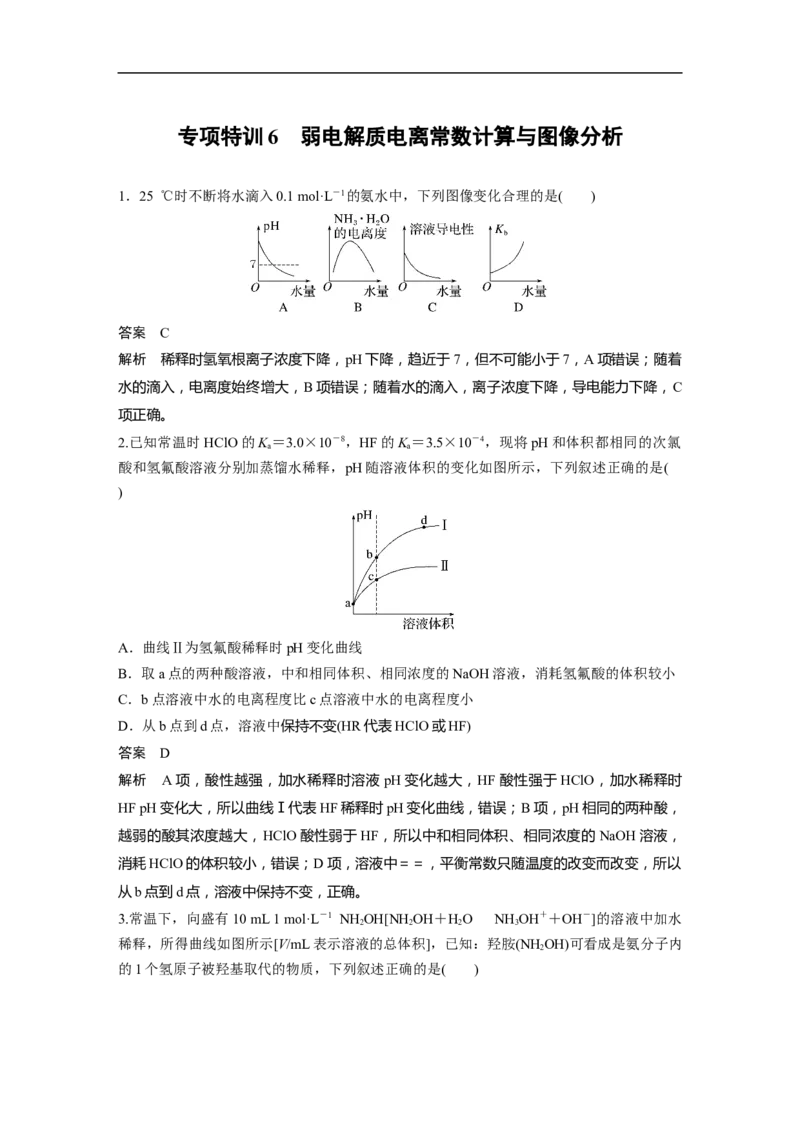
1.25 ℃时不断将水滴入0.1 mol·L-1的氨水中,下列图像变化合理的是( )
答案 C
解析 稀释时氢氧根离子浓度下降,pH下降,趋近于7,但不可能小于7,A项错误;随着
水的滴入,电离度始终增大,B项错误;随着水的滴入,离子浓度下降,导电能力下降,C
项正确。
2.已知常温时HClO的K=3.0×10-8,HF的K=3.5×10-4,现将pH和体积都相同的次氯
a a
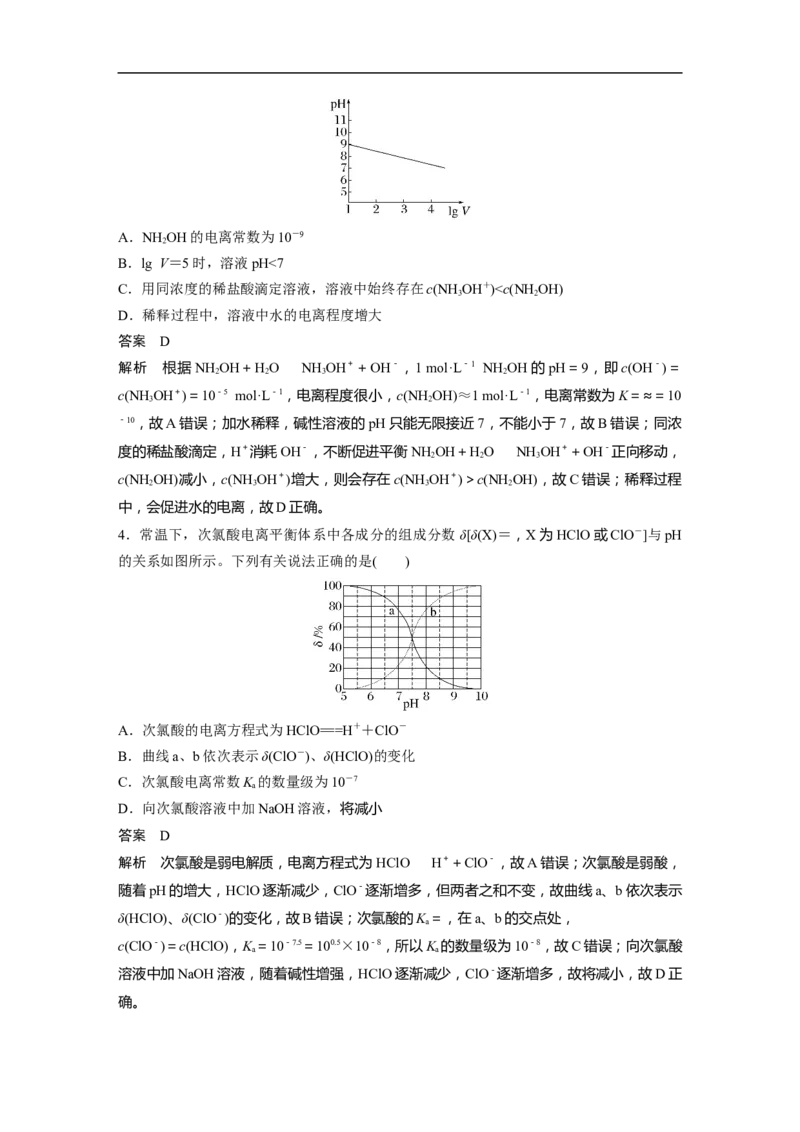
酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是(
)
A.曲线Ⅱ为氢氟酸稀释时pH变化曲线
B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中保持不变(HR代表HClO或HF)
答案 D
解析 A项,酸性越强,加水稀释时溶液pH变化越大,HF酸性强于HClO,加水稀释时
HF pH变化大,所以曲线Ⅰ代表HF稀释时pH变化曲线,错误;B项,pH相同的两种酸,
越弱的酸其浓度越大,HClO酸性弱于HF,所以中和相同体积、相同浓度的 NaOH溶液,
消耗HClO的体积较小,错误;D项,溶液中==,平衡常数只随温度的改变而改变,所以
从b点到d点,溶液中保持不变,正确。
3.常温下,向盛有10 mL 1 mol·L-1 NH OH[NH OH+HONH OH++OH-]的溶液中加水
2 2 2 3
稀释,所得曲线如图所示[V/mL表示溶液的总体积],已知:羟胺(NH OH)可看成是氨分子内
2
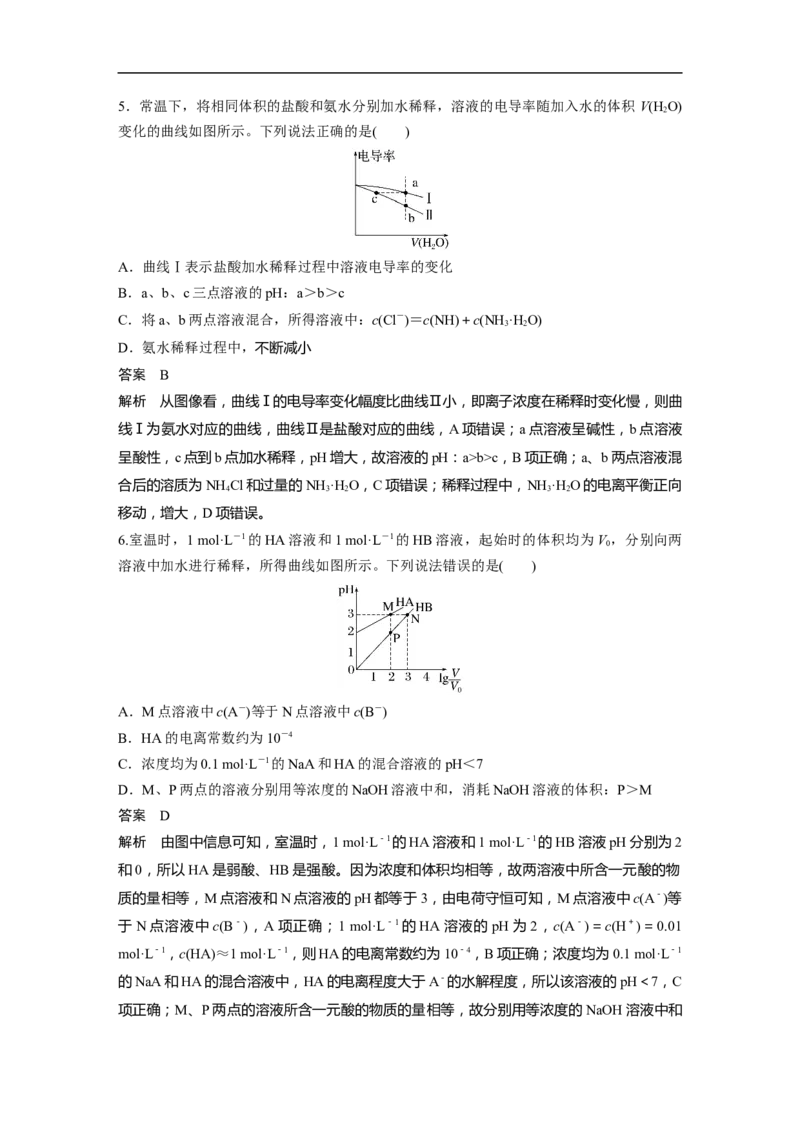
的1个氢原子被羟基取代的物质,下列叙述正确的是( )A.NH OH的电离常数为10-9
2
B.lg V=5时,溶液pH<7
C.用同浓度的稀盐酸滴定溶液,溶液中始终存在c(NH OH+)b>c,B项正确;a、b两点溶液混
合后的溶质为NH Cl和过量的NH ·H O,C项错误;稀释过程中,NH ·H O的电离平衡正向
4 3 2 3 2
移动,增大,D项错误。
6.室温时,1 mol·L-1的HA溶液和1 mol·L-1的HB溶液,起始时的体积均为V ,分别向两
0
溶液中加水进行稀释,所得曲线如图所示。下列说法错误的是( )
A.M点溶液中c(A-)等于N点溶液中c(B-)
B.HA的电离常数约为10-4
C.浓度均为0.1 mol·L-1的NaA和HA的混合溶液的pH<7
D.M、P两点的溶液分别用等浓度的NaOH溶液中和,消耗NaOH溶液的体积:P>M
答案 D
解析 由图中信息可知,室温时,1 mol·L-1的HA溶液和1 mol·L-1的HB溶液pH分别为2
和0,所以HA是弱酸、HB是强酸。因为浓度和体积均相等,故两溶液中所含一元酸的物
质的量相等,M点溶液和N点溶液的pH都等于3,由电荷守恒可知,M点溶液中c(A-)等
于N点溶液中c(B-),A项正确;1 mol·L-1的HA溶液的pH为2,c(A-)=c(H+)=0.01
mol·L-1,c(HA)≈1 mol·L-1,则HA的电离常数约为10-4,B项正确;浓度均为0.1 mol·L-1
的NaA和HA的混合溶液中,HA的电离程度大于A-的水解程度,所以该溶液的pH<7,C
项正确;M、P两点的溶液所含一元酸的物质的量相等,故分别用等浓度的NaOH溶液中和时,消耗NaOH溶液的体积相等,D项错误。
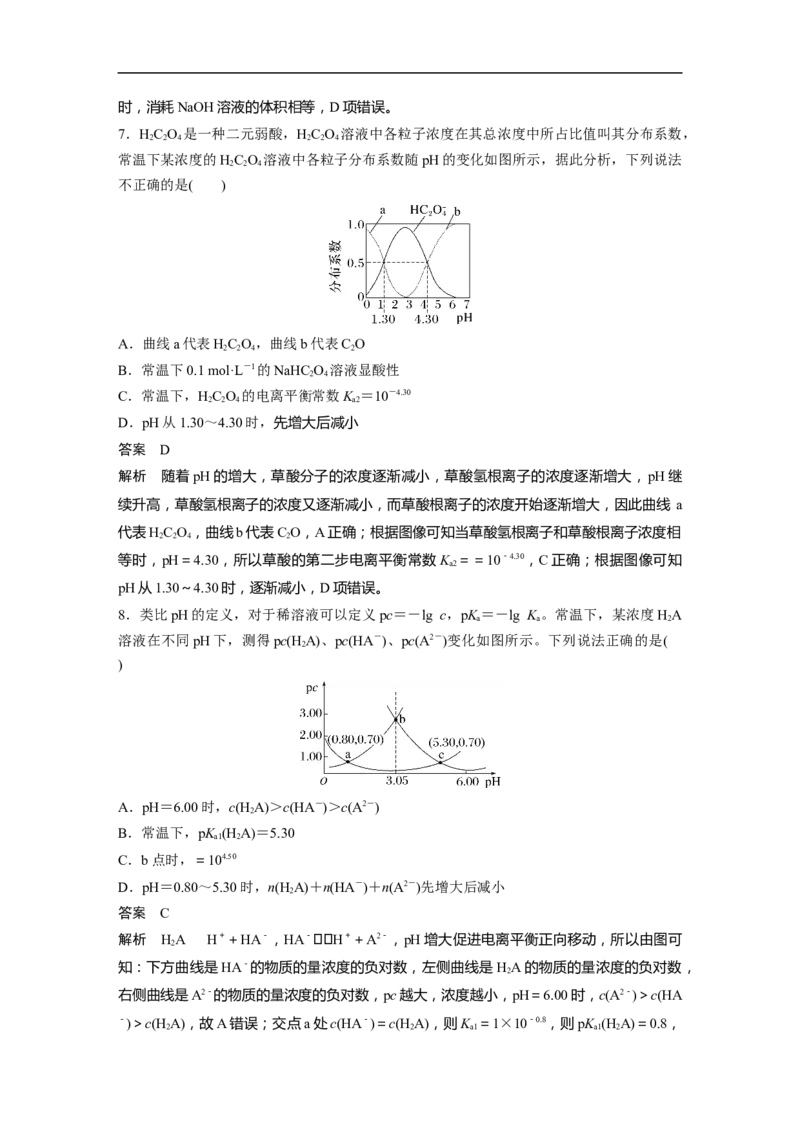
7.HC O 是一种二元弱酸,HC O 溶液中各粒子浓度在其总浓度中所占比值叫其分布系数,
2 2 4 2 2 4
常温下某浓度的HC O 溶液中各粒子分布系数随pH的变化如图所示,据此分析,下列说法
2 2 4
不正确的是( )
A.曲线a代表HC O,曲线b代表C O
2 2 4 2
B.常温下0.1 mol·L-1的NaHC O 溶液显酸性
2 4
C.常温下,HC O 的电离平衡常数K =10-4.30
2 2 4 a2
D.pH从1.30~4.30时,先增大后减小
答案 D
解析 随着pH的增大,草酸分子的浓度逐渐减小,草酸氢根离子的浓度逐渐增大,pH继
续升高,草酸氢根离子的浓度又逐渐减小,而草酸根离子的浓度开始逐渐增大,因此曲线 a
代表HC O,曲线b代表C O,A正确;根据图像可知当草酸氢根离子和草酸根离子浓度相
2 2 4 2
等时,pH=4.30,所以草酸的第二步电离平衡常数K ==10-4.30,C正确;根据图像可知
a2
pH从1.30~4.30时,逐渐减小,D项错误。
8.类比pH的定义,对于稀溶液可以定义pc=-lg c,pK=-lg K。常温下,某浓度HA
a a 2
溶液在不同pH下,测得pc(H A)、pc(HA-)、pc(A2-)变化如图所示。下列说法正确的是(
2
)
A.pH=6.00时,c(H A)>c(HA-)>c(A2-)
2
B.常温下,pK (H A)=5.30
a1 2
C.b点时,=104.50
D.pH=0.80~5.30时,n(H A)+n(HA-)+n(A2-)先增大后减小
2
答案 C
解析 HAH++HA-,HA-H++A2-,pH增大促进电离平衡正向移动,所以由图可
2
知:下方曲线是HA-的物质的量浓度的负对数,左侧曲线是 HA的物质的量浓度的负对数,
2
右侧曲线是A2-的物质的量浓度的负对数,pc越大,浓度越小,pH=6.00时,c(A2-)>c(HA
-)>c(H A),故A错误;交点a处c(HA-)=c(H A),则K =1×10-0.8,则pK (H A)=0.8,
2 2 a1 a1 2故B错误;b点时c(H A)=c(A2-),====104.50,故C正确;根据物料守恒可知,n(H A)
2 2
+n(HA-)+n(A2-)始终不变,故D错误。
9.(1)一定温度下,用水吸收SO 气体时,溶液中水的电离平衡__________移动(填“向左”
2
“向右”或“不”);若得到pH=4的HSO 溶液,试计算溶液中=___________。SO 可用
2 3 2
足量小苏打溶液吸收,反应的离子方程式是_________________________________。(已知该
温度下,HSO 的电离常数:K =4.5×10-2,K =2.5×10-7,HCO 的电离常数:K =
2 3 a1 a2 2 3 a1
8.4×10-7,K =1.2×10-10)
a2
(2)调节溶液pH可实现工业废气CO 的捕获和释放。已知25 ℃时碳酸的电离常数为K 、
2 a1
K ,当溶液pH=12时,c(H CO)∶c(HCO)∶c(CO)=1∶__________∶__________(用K 、
a2 2 3 a1
K 表示)。
a2
答案 (1)向左 400 HCO+SO ===HSO+CO (2)1012·K 1024·K ·K
2 2 a1 a1 a2
解析 (1)用水吸收SO 气体生成了亚硫酸,亚硫酸电离出氢离子抑制水的电离,使水的电
2
离平衡向左移动;亚硫酸的电离方程式为 HSO HSO+H+,HSOH++SO,得到pH
2 3
=4的HSO 溶液,c(H+)=10-4 mol·L-1,由于 K =,===400;由于 K (H SO )>
2 3 a2 a1 2 3
K (H CO)>K (H SO ),所以SO 可用足量小苏打溶液吸收,反应产生亚硫酸氢钠和二氧化
a1 2 3 a2 2 3 2
碳,反应的离子方程式为HCO+SO ===HSO+CO。
2 2
(2)pH=12,即c(H+)=10-12 mol·L-1,由K =,得c(HCO)==1012·K ·c(H CO);由K
a1 a1 2 3 a2
= , 得 c(CO) = = 1024·K ·K ·c(H CO) ; c(H CO)∶c(HCO)∶c(CO) =
a1 a2 2 3 2 3
1∶1012·K ∶1024·K ·K 。
a1 a1 a2
10.联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为
__________(已知:NH +H+NH的K=8.7×107;K =1.0×10-14)。联氨与硫酸形成的
2 4 2 w
酸式盐的化学式为______________________________________________________。
答案 8.7×10-7 NH(HSO )
2 6 4 2
解析 联氨为二元弱碱,在水中的电离方式与氨相似,则联氨第一步电离的方程式为 NH
2 4
+HONH+OH-,再根据已知:NH +H+NH的K=8.7×107及K =1.0×10-14,故
2 2 2 4 2 w
联氨第一步电离平衡常数为K====K·K =8.7×107×1.0×10-14=8.7×10-7;联氨为二元
w
弱碱,酸碱发生中和反应生成盐,则联氨与硫酸形成酸式盐的化学式为NH(HSO )。
2 6 4 2