文档内容
热点强化 17 强酸(碱)与弱酸(碱)的比较
弱酸与强酸的根本区别在于弱酸不完全电离,存在电离平衡,常涉及下列几种问题的比较。
1.一元强酸(HCl)与一元弱酸(CHCOOH)的比较
3
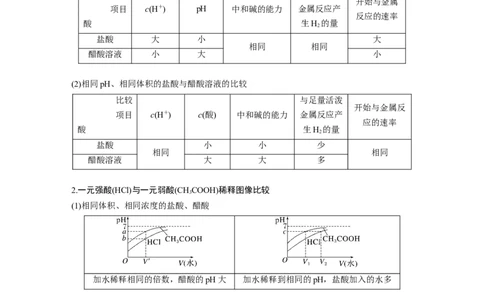
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较 与足量活泼
开始与金属
项目 c(H+) pH 中和碱的能力 金属反应产
反应的速率
酸 生H 的量
2
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较 与足量活泼
开始与金属反
项目 c(H+) c(酸) 中和碱的能力 金属反应产
应的速率
酸 生H 的量
2
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
2.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
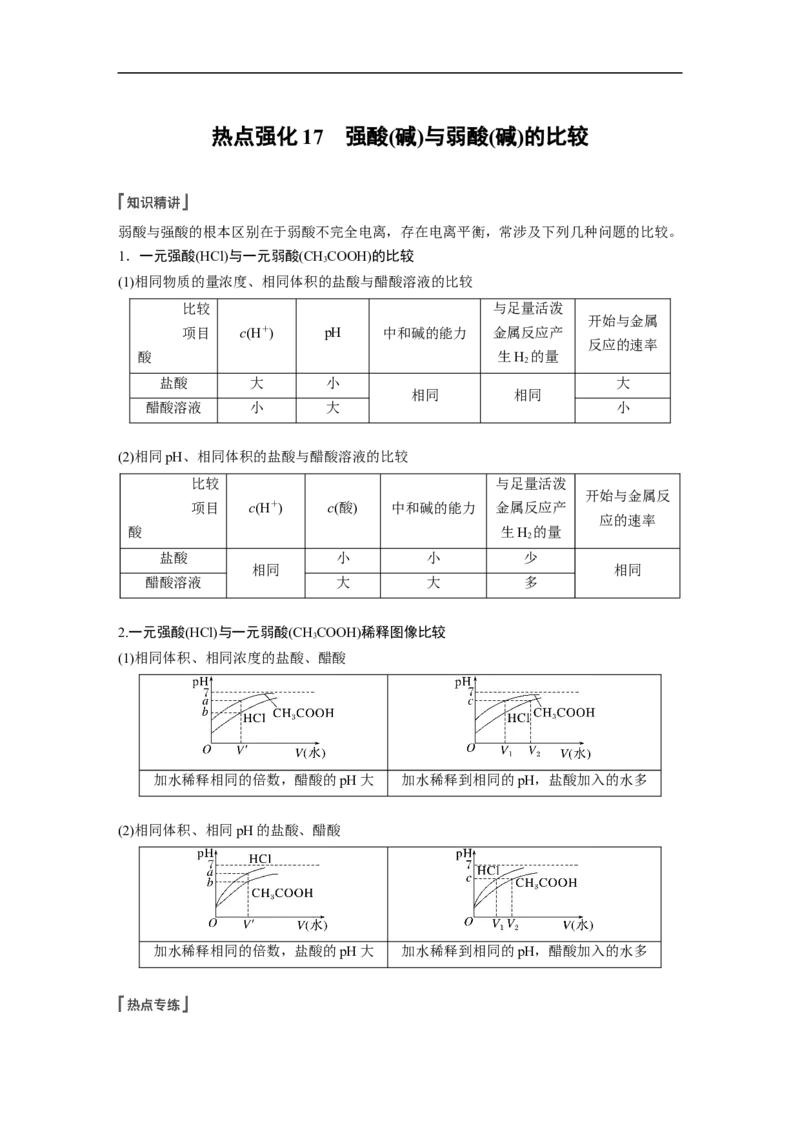
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH大 加水稀释到相同的pH,盐酸加入的水多
(2)相同体积、相同pH的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH大 加水稀释到相同的pH,醋酸加入的水多题组一 判断弱酸或弱碱的方法
1.为了证明HR是弱电解质,某同学开展了题为“HR是弱电解质的实验探究”的探究活动。
该同学设计了如下方案,其中正确的是________(填序号)。
(1)先配制0.10 mol·L-1 HR溶液,再测溶液的pH,若pH大于1,则可证明HR为弱电解质
(2)先配制0.01 mol·L-1和0.10 mol·L-1的HR,再分别用pH计测它们的pH,若两者的pH相
差小于1个单位,则可证明HR是弱电解质
(3)取等体积、等pH的HR溶液和盐酸分别与足量锌反应,测得反应过程中 HR产生H 速率
2
较慢且最终产生H 较多,则可证明HR为弱电解质
2
(4)配制一定量的NaR溶液,测其pH,若常温下pH大于7,则可证明HR是弱电解质
(5)25 ℃时,pH=2的HR和pH=12的Ba(OH) 溶液等体积混合后,溶液显酸性,则HR为
2
弱酸
答案 (1)(2)(4)(5)
解析 (3)取等体积、等c(H+)的HR溶液和盐酸分别与足量锌反应,测得反应过程中 HR产
生H 速率较快且最终产生H 较多,则可证明HR为弱电解质,错误;(5)两溶液等体积混合
2 2
后,若HR为强酸,溶液显中性,若HR为弱酸,弱酸过量,溶液显酸性,可证明 HR为弱
酸,正确。
2.为了证明HF是弱酸,甲、乙、丙三位同学分别设计以下实验进行探究。
(1)甲同学取一定体积的HF溶液,滴入2滴紫色石蕊溶液,显红色,再加入NaF固体观察到
的现象是__________________,则证明HF为弱酸。
(2)乙同学取10 mL未知浓度的HF溶液,测其pH为a(a<5),然后用蒸馏水稀释至1 000
mL。再测其pH为b,若要认为HF为弱酸,则a、b应满足的关系是b<________(用含a的
代数式表示)。
(3)丙同学用pH试纸测得室温下0.10 mol·L-1的HF溶液的pH为2,则测定HF为弱酸,由
丙同学的实验数据可得室温下HF的电离平衡常数约为________。
答案 (1)红色变浅 (2)a+2 (3)1.1×10-3
解析 (1)加入NaF固体,HF的电离平衡向逆反应方向移动,氢离子浓度减小,溶液的红色
变浅,证明HF存在电离平衡,即HF为弱酸。(2)弱酸加水稀释会促进弱酸的电离,稀释
102倍,pH变化小于2个单位,所以稀释后pH=b1。
角度二:弱电解质溶液中存在电离平衡,条件改变,平衡移动,如pH=1的CHCOOH加
3
水稀释10倍后,1<pH<2。
角度三:弱电解质形成的盐类能水解,如判断CHCOOH为弱酸可根据下面两个实验现象:
3
①配制某浓度的醋酸钠溶液,向其中加入几滴酚酞溶液,溶液变为浅红色。
②用玻璃棒蘸取一定浓度的醋酸钠溶液滴在pH试纸上,测其pH,pH>7。
题组二 强酸(碱)与弱酸(碱)的比较
3.(2022·北京高三模拟)关于室温下pH相同、体积相同的氨水与氢氧化钠两种稀溶液,下
列叙述正确的是( )
A.氨水中的c(NH)与NaOH溶液中的c(Na+)相同
B.温度均升高20 ℃(不考虑挥发),两溶液的pH均不变
C.加水稀释相同的倍数后,两种溶液的pH仍相同
D.与等物质的量浓度的盐酸反应,恰好中和时所消耗的盐酸的体积相同
答案 A
解析 温度升高20 ℃,促进NH ·H ONH+OH-正向移动,c(OH-)增大,pH增大,
3 2
NaOH溶液pH不变,故B错误;pH相同的氨水与NaOH两种稀溶液,加水稀释相同的倍数
后,促进NH ·H O的电离,所以氨水中c(OH-)大,两种溶液的pH不相同,故C错误;pH
3 2
相同、体积相同,与等物质的量浓度的盐酸反应,氨水所消耗的盐酸的体积大,故D错误。
4.在两个密闭的锥形瓶中,0.05 g形状相同的镁条(过量)分别与2 mL 2 mol·L-1的盐酸和醋
酸反应,测得容器内压强随时间的变化曲线如图。下列说法正确的是( )
A.①代表的是盐酸与镁条反应时容器内压强随时间的变化曲线
B.任意相同时间段内,盐酸与Mg反应的化学反应速率均快于醋酸与Mg反应的化学反应
速率
C.反应中醋酸的电离被促进,两种溶液最终产生的氢气总量基本相等
D.1 mol·L-1 NaOH溶液完全中和上述两种酸溶液,盐酸消耗NaOH溶液的体积更大
答案 C
解析 2 mL 2 mol·L-1的盐酸和醋酸,盐酸中c(H+)大,与镁条反应的速率快,相同时间内
产生的氢气多,容器内压强大,反应先结束,故②代表的是盐酸与镁条反应时容器内压强随
时间的变化曲线,故A错误;从图像可以看出,100 s后,醋酸与镁的反应速率更大,此时
盐酸与镁已接近反应结束,c(H+)较小,反应速率较小,故B错误;由于盐酸和醋酸的浓度和体积均相同,则二者物质的量相同,故反应结束时,产生的氢气总量基本相等,用1 mol·
L-1 NaOH溶液完全中和上述两种酸溶液时,盐酸与醋酸消耗NaOH溶液的体积相等,故C
正确、D错误。
5.常温下,分别向体积相同、浓度均为 1 mol·L-1的HA、HB两种酸溶液中不断加水稀释,
酸溶液的pH与酸溶液浓度的对数(lg c)间的关系如图。下列对该过程相关分析正确的是(
)
A.HB的电离常数(K)数量级为10-3
a
B.其钠盐的水解常数(K )大小关系是:NaB>NaA
h
C.a、b两点溶液中,水的电离程度:b