文档内容
第 44 讲 水的电离和溶液的 pH
复习目标 1.了解水的电离、离子积常数(K )。2.了解溶液pH的含义及其测定方法,能进
w
行pH的简单计算。
考点一 水的电离与水的离子积常数
1.水的电离
(1)水是极弱的电解质,水的电离方程式为 HO+HOHO++OH-或简写为HOH++
2 2 3 2
OH-。
(2)25 ℃时,纯水中c(H+)=c(OH-)= 1 × 10 - 7 _ mol·L - 1 ;任何水溶液中,由水电离出的c(H
+)与c(OH-)都相等。
2.水的离子积常数
3.填写外界条件对水的电离平衡的具体影响
改变条件 平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小
NaCO 正 不变 增大 增大 减小
2 3
NH Cl 正 不变 增大 减小 增大
4
NaHSO 逆 不变 减小 减小 增大
4
加热 正 增大 增大 增大 增大
1.水的电离平衡常数与水的离子积相等( )
2.25 ℃时CHCOONa溶液的K 大于100 ℃时NaOH溶液的K ( )
3 w w3.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
4.温度一定时,在纯水中通入少量SO ,水的电离平衡不移动,K 不变( )
2 w
5.室温下,0.1 mol·L-1的HCl溶液与0.1 mol·L-1的NaOH溶液中水的电离程度相等( )
答案 1.× 2.× 3.× 4.× 5.√
1.室温下,计算下列溶液中水电离出的 。
(1)0.01 mol·L-1的盐酸中, =___________________________________。
(2)pH=4的亚硫酸溶液中, =___________________________________。
(3)pH=10的KOH溶液中, =___________________________________。
(4)pH=4的NH Cl溶液中, =__________________________________。
4
(5)pH=10的CHCOONa溶液中, =______________________________。
3
答案 (1)1×10-12 mol·L-1 (2)1×10-10 mol·L-1 (3)1×10-10 mol·L-1 (4)1×10-4 mol·L
-1
(5)1×10-4 mol·L-1
2.常温时,纯水中由水电离出的c(H+)=a mol·L-1,pH=1的盐酸中由水电离出的c(H+)=
b mol·L-1,0.1 mol·L-1的盐酸与0.1 mol·L-1的氨水等体积混合后,由水电离出的c(H+)=
c mol·L-1,则a、b、c的关系正确的是( )
A.a>b=c B.c>a>b C.c>b>a D.b>c>a
答案 B
解析 盐酸抑制水的电离,所以ba,故B正确。
3.25 ℃时,在等体积的①pH=0的HSO 溶液、②0.05 mol·L-1的Ba(OH) 溶液、③pH=
2 4 2
10的NaS溶液、④pH=5的NH NO 溶液中,发生电离的水的物质的量之比是( )
2 4 3
A.1∶10∶1010∶109 B.1∶5∶(5×109)∶(5×108)
C.1∶20∶1010∶109 D.1∶10∶104∶109
答案 A
解析 HSO 与Ba(OH) 抑制水的电离,NaS与NH NO 促进水的电离。25 ℃时,pH=0的
2 4 2 2 4 3
HSO 溶液中:c(H O) =c(OH-)= mol·L-1=10-14 mol·L-1;0.05 mol·L-1的Ba(OH) 溶液
2 4 2 电离 2
中:c(H O) =c(H+)= mol·L-1=10-13 mol·L-1;pH=10 的 NaS 溶液中:
2 电离 2
c(H O) =c(OH-)=10-4 mol·L-1;pH=5的NH NO 的溶液中:c(H O) =c(H+)=10-
2 电离 4 3 2 电离5mol·
L-1。它们的物质的量之比为10-14∶10-13∶10-4∶10-5=1∶10∶1010∶109,故A正确。
溶液中 或 的计算及应用(以室温为例)
(1)酸、碱抑制水的电离,酸溶液中求c(OH-),即 = =c(OH-),碱溶
液中求c(H+),即 = =c(H+)。
(2)水解的盐促进水的电离,故 等于显性离子的浓度。
(3)酸式盐溶液
酸式根以电离为主: = =c(OH-)。
酸式根以水解为主: = =c(OH-)。
二、水的电离曲线
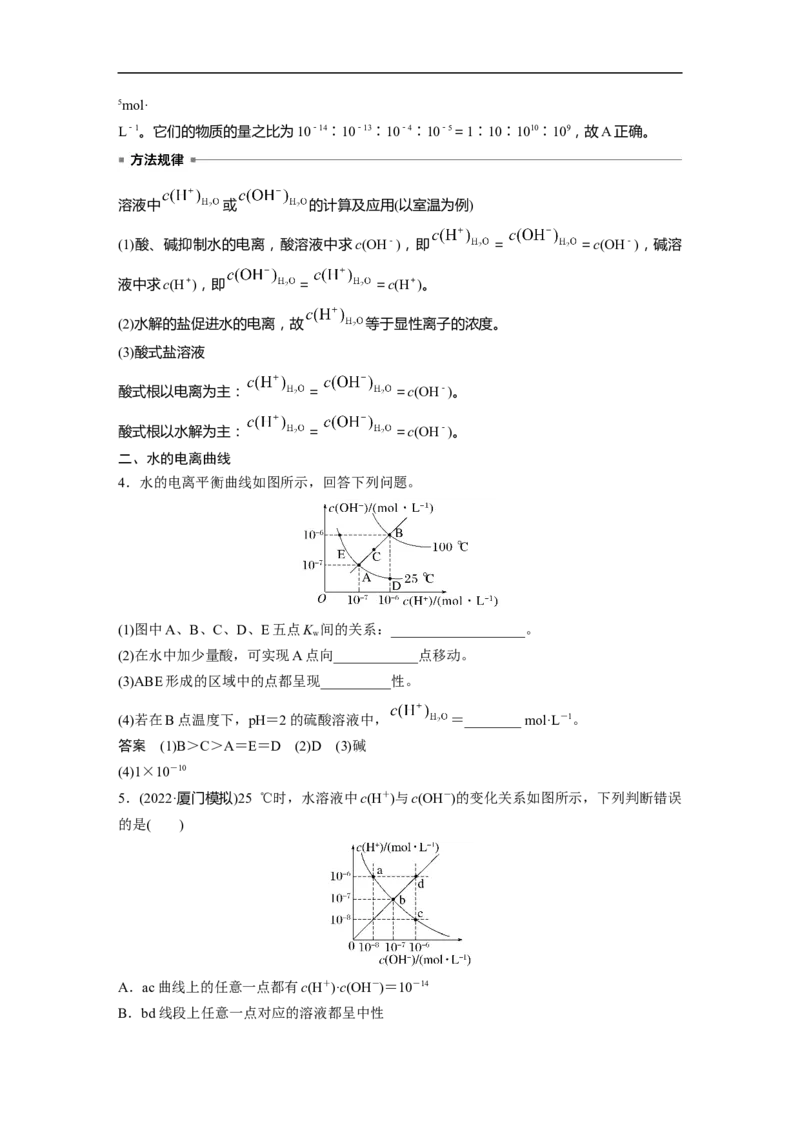
4.水的电离平衡曲线如图所示,回答下列问题。
(1)图中A、B、C、D、E五点K 间的关系:___________________。
w
(2)在水中加少量酸,可实现A点向____________点移动。
(3)ABE形成的区域中的点都呈现__________性。
(4)若在B点温度下,pH=2的硫酸溶液中, =________ mol·L-1。
答案 (1)B>C>A=E=D (2)D (3)碱
(4)1×10-10
5.(2022·厦门模拟)25 ℃时,水溶液中c(H+)与c(OH-)的变化关系如图所示,下列判断错误
的是( )
A.ac曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.bd线段上任意一点对应的溶液都呈中性C.d点对应溶液的温度高于25 ℃,pH<7
D.c点溶液不可能是盐溶液
答案 D
解析 ac曲线上的任意一点,由于温度相同,所以水的离子积常数相同,根据b点可知,
c(H+)·c(OH-)=10-14,A项正确;bd线段上任意一点都满足c(H+)=c(OH-),溶液一定呈中
性,B项正确;d点时,c(H+)=c(OH-)=1×10-6 mol·L-1>1×10-7 mol·L-1,溶液的pH=
6,水的电离为吸热反应,所以 d点温度高于25 ℃,C项正确;在c点c(H+)=1×10-8
mol·L-1,c(OH-)=1×10-6 mol·L-1,溶液显碱性,而醋酸钠溶液显碱性,所以c点可能为
醋酸钠溶液,D项错误。
正确理解水的电离平衡曲线
(1)曲线上的任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度相同,改变酸碱性;实现曲线上点与曲线外点之间
的转化一定改变温度。
考点二 溶液的酸碱性与 pH
1.溶液的酸碱性 pH概念
(1)pH计算公式:pH= - l g_ c (H + ) 。
(2)溶液呈酸碱性的本质:溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
溶液的酸碱性 c(H+)与c(OH-)比较 常温下溶液pH
酸性溶液 c(H+)>c(OH-) <7
中性溶液 c(H+)=c(OH-) =7
碱性溶液 c(H+)<c(OH-) >7
2.pH的测定
(1)酸碱指示剂法
该法只能测其pH的大致范围,常见指示剂变色范围如下表:
指示剂 变色范围的pH
<5.0 5.0~8.0 >8.0
石蕊
红色 紫色 蓝色
甲基橙 <3.1 3.1~4.4 >4.4橙色
红色 黄色
<8.2 8.2~10.0 >10.0
酚酞
无色 浅红色 红色
(2)pH试纸法
用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液点在试纸的中央,
变色后与标准比色卡对照。
(3)pH计测定
3.计算25 ℃时下列溶液的pH
(1)0.005 mol·L-1的HSO 溶液的pH=__________。
2 4
(2)0.001 mol·L-1的NaOH溶液的pH=____________。
(3)pH=2的盐酸加水稀释到1 000倍,溶液的pH=__________。
(4)将 pH=8 的 NaOH 溶液与 pH=10 的 NaOH 溶液等体积混合,混合溶液的 pH=
__________。
(5)0.015 mol·L-1的硫酸与 0.01 mol·L-1的 NaOH 溶液等体积混合,混合溶液的 pH=
_______。
答案 (1)2 (2)11 (3)5 (4)9.7 (5)2
解析 (1)c(H SO )=0.005 mol·L-1,c(H+)=2×c(H SO )=0.01 mol·L-1,pH=2。(2)c(OH-)
2 4 2 4
=1×10-3 mol·L-1,c(H+)= mol·L-1=10-11 mol·L-1,pH=11。(3)pH=2的盐酸加水稀释
到1 000倍,所得溶液的pH=2+3=5。(4)由pH=8、pH=10可得两溶液等体积混合后,
c(OH-)= mol·L-1=×10-6 mol·L-1,c(H+)= mol·L-1≈ 2.0×10-10 mol·L-1,pH≈9.7。
(5)混合后c(H+)= mol·L-1=0.01 mol·L-1,则pH=2。
溶液pH计算的一般思维模型
1.任何温度下,利用H+和OH-浓度的相对大小均可判断溶液的酸碱性( )2.pH<7的溶液一定显酸性( )
3.c(H+)=的溶液一定显中性( )
4.常温下能使甲基橙显黄色的溶液一定显碱性( )
5.用广泛pH试纸测得某溶液的pH为3.4( )
6.用pH试纸测得某氯水的pH为5( )
7.用湿润的pH试纸测定盐酸和醋酸溶液的pH,醋酸溶液的误差更大( )
答案 1.√ 2.× 3.√ 4.× 5.× 6.× 7.×
一、混合溶液酸碱性的判断
1.常温下,两种溶液混合后酸碱性的判断(在括号中填“酸性”“碱性”或“中性”)。
(1)相同浓度的HCl和NaOH溶液等体积混合( )
(2)相同浓度的CHCOOH和NaOH溶液等体积混合( )
3
(3)相同浓度的NH ·H O和HCl溶液等体积混合( )
3 2
(4)pH=2的HSO 和pH=12的NaOH溶液等体积混合( )
2 4
(5)pH=3的HCl和pH=10的NaOH溶液等体积混合( )
(6)pH=3的HCl和pH=12的NaOH溶液等体积混合( )
(7)pH=2的CHCOOH和pH=12的NaOH溶液等体积混合( )
3
(8)pH=2的HSO 和pH=12的NH ·H O等体积混合( )
2 4 3 2
答案 (1)中性 (2)碱性 (3)酸性 (4)中性 (5)酸性 (6)碱性 (7)酸性 (8)碱性
酸碱溶液混合后酸碱性的判断规律
(1)等浓度等体积的一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)室温下c (H+)=c (OH-),即pH之和等于14时,一强一弱等体积混合——“谁弱谁过
酸 碱
量,谁弱显谁性”。
(3)已知强酸和强碱的pH,等体积混合(25 ℃时):
①pH之和等于14,呈中性;
②pH之和小于14,呈酸性;
③pH之和大于14,呈碱性。
二、溶液稀释、混合的pH计算
2.常温下,关于溶液稀释的下列说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.pH=4的HSO 溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
C.将1 L 0.1 mol·L-1的Ba(OH) 溶液稀释为2 L,pH=13
2
D.pH=8的NaOH溶液稀释100倍,其pH=6答案 C
解析 A 项,pH=3 的醋酸溶液在稀释过程中电离平衡正向移动,稀释 100 倍时,
32且pH<7,则HR是弱酸
C.25 ℃时,若测得HR溶液pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,测得
pH=b,b-a<1,则HR是弱酸
D.25 ℃时,若测得NaR溶液pH=a,取该溶液10.0 mL,升温至50 ℃,测得pH=b,
a>b,则HR是弱酸
答案 B
解析 25 ℃时,若测得0.01 mol·L-1NaR溶液pH=7,可知NaR为强酸强碱盐,则HR为
强酸,A错误;25 ℃时,若测得 0.01 mol·L-1HR 溶液 pH>2 且pH<7,可知溶液中 c(H
+)<0.01 mol·
L-1,HR未完全电离,所以HR为弱酸,B正确;假设HR为强酸,取pH=6的该溶液
10.0 mL,加蒸馏水稀释至100.0 mL,测得此时溶液pH<7,C错误;假设HR为强酸,则
NaR为强酸强碱盐,溶液呈中性,升温至50 ℃,促进水的电离,水的离子积常数增大,pH
减小,D错误。
2.(2020·浙江7月选考,17)下列说法不正确的是( )
A.2.0×10-7 mol·L-1的盐酸中c(H+)=2.0×10-7 mol·L-1
B.将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
答案 A
解析 对于2.0×10-7 mol·L-1的盐酸中,水电离出的c(H+)相对来说不是很小,不能忽略,
故该盐酸中c(H+)>2.0×10-7 mol·L-1,A错误;升高温度,水的电离程度增大,K 增大,
w
水电离出的c(H+)增大,则溶液的pH减小,由于KCl是强酸强碱盐,不水解,故其溶液仍
呈中性,B正确;常温下,NaCN溶液呈碱性,说明CN-发生了水解,则HCN为弱电解质,
C正确;常温下,pH为3的醋酸溶液中加入CHCOONa固体,c(CHCOO-)增大,醋酸的电
3 3离平衡逆向移动,c(H+)减小,由于K 不变,则溶液中c(OH-)增大,溶液pH增大,D正确。
w
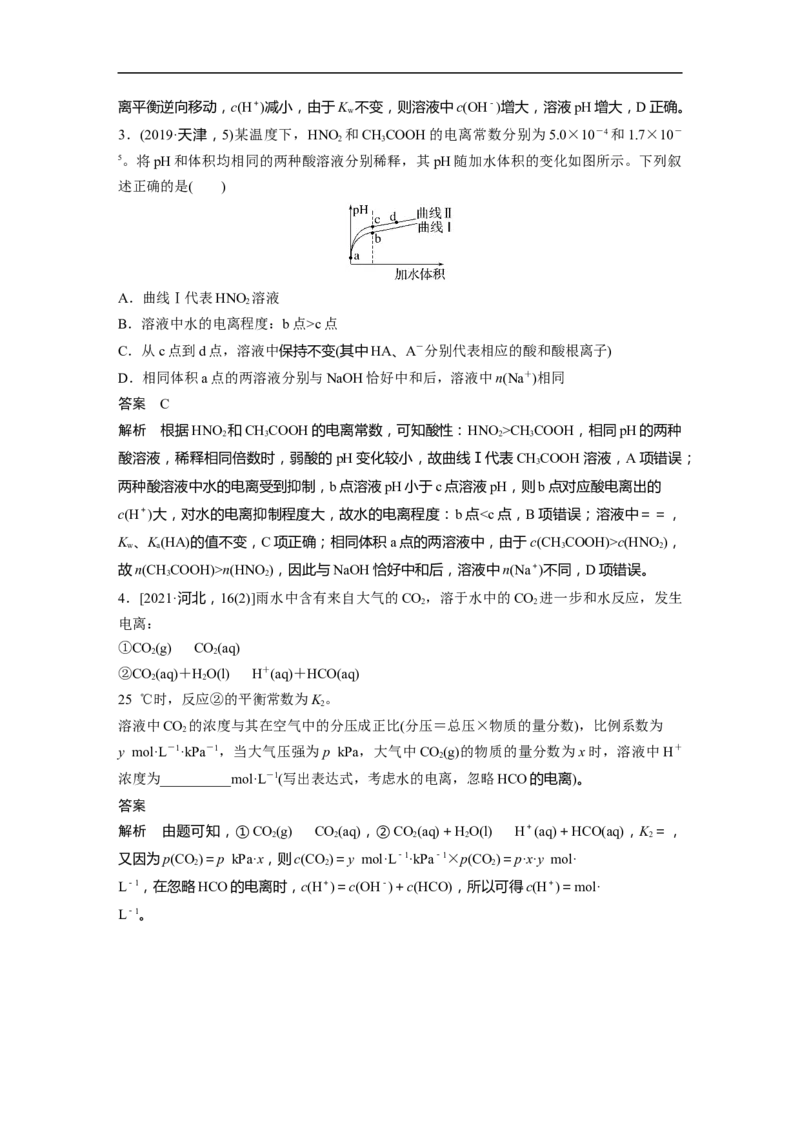
3.(2019·天津,5)某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-
2 3
5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙
述正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
答案 C
解析 根据HNO 和CHCOOH的电离常数,可知酸性:HNO>CH COOH,相同pH的两种
2 3 2 3
酸溶液,稀释相同倍数时,弱酸的pH变化较小,故曲线Ⅰ代表CHCOOH溶液,A项错误;
3
两种酸溶液中水的电离受到抑制,b点溶液pH小于c点溶液pH,则b点对应酸电离出的
c(H+)大,对水的电离抑制程度大,故水的电离程度:b点c(HNO),
w a 3 2
故n(CHCOOH)>n(HNO),因此与NaOH恰好中和后,溶液中n(Na+)不同,D项错误。
3 2
4.[2021·河北,16(2)]雨水中含有来自大气的CO ,溶于水中的CO 进一步和水反应,发生
2 2
电离:
①CO(g)CO(aq)
2 2
②CO(aq)+HO(l)H+(aq)+HCO(aq)
2 2
25 ℃时,反应②的平衡常数为K 。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
2
y mol·L-1·kPa-1,当大气压强为p kPa,大气中CO(g)的物质的量分数为x时,溶液中H+
2
浓度为__________mol·L-1(写出表达式,考虑水的电离,忽略HCO的电离)。
答案
解析 由题可知,①CO(g)CO(aq),②CO(aq)+HO(l)H+(aq)+HCO(aq),K =,
2 2 2 2 2
又因为p(CO)=p kPa·x,则c(CO)=y mol·L-1·kPa-1×p(CO)=p·x·y mol·
2 2 2
L-1,在忽略HCO的电离时,c(H+)=c(OH-)+c(HCO),所以可得c(H+)=mol·
L-1。课时精练
1.25 ℃时,水的电离达到平衡:HOH++OH-。下列叙述错误的是( )
2
A.向水中通入氨气,平衡逆向移动,c(OH-)增大
B.向水中加入少量稀硫酸,c(H+)增大,K 不变
w
C.将水加热平衡正向移动,K 变大
w
D.升高温度,平衡正向移动,c(H+)增大,pH不变
答案 D
解析 升高温度,能促进水的电离,c(H+)增大,pH减小,D项错误。
2.其他条件不变,升高温度,下列数据不一定增大的是( )
A.可逆反应的化学平衡常数K
B.电离常数K
C.水的离子积常数K
w
D.弱电解质的电离度α
答案 A
解析 A项,若正反应为放热反应,升高温度平衡向逆反应方向移动,化学平衡常数减小;
若正反应为吸热反应,升高温度平衡向正反应方向移动,化学平衡常数增大。
3.已知液氨的性质与水相似。T ℃时,NH +NH NH+NH,NH的平衡浓度为1×
3 3
10-15 mol·L-1,则下列说法正确的是( )
A.在此温度下液氨的离子积为1×10-17
B.在液氨中放入金属钠,可生成NaNH
2
C.恒温下,在液氨中加入NH Cl,可使液氨的离子积减小
4
D.降温,可使液氨电离平衡逆向移动,且c(NH)<c(NH)
答案 B
解析 由电离方程式知,NH与NH的离子平衡浓度相等,都为1×10-15 mol·L-1,根据水
的离子积得液氨的离子积K=c(NH)·c(NH)=1×10-30,A项错误;由水的离子积可以知道,
其大小只与温度有关,与离子浓度无关,C项错误;因为电离是吸热反应,所以降温平衡逆
向移动,c(NH)=c(NH)都减小,D项错误。
4.室温下,下列说法正确的是( )
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的
大小关系是a>b>c
B.KNO 溶液和CHCOONH 溶液pH均为7,但两溶液中水的电离程度不相同
3 3 4
C.5.0×10-3 mol·L-1KHA溶液的pH=3.75,该溶液中c(A2-)c>b,A错误;CHCOONH 溶液中的铵根离子与醋酸根离子均发生水解,促进水的电离,
3 4
所以CHCOONH 溶液中水的电离程度大于KNO 溶液中水的电离程度,B正确;5.0×10-
3 4 3
3mol·
L-1 KHA 溶液的 pH=3.75,显酸性,HA-的电离程度大于其水解程度,所以 c(A2
-)>c(H A),C 错误;醋酸为弱酸,浓度越小,电离程度越大,故 0.01 mol·L-1与0.001
2
mol·L-1的CHCOOH溶液中c(H+)之比小于10∶1,D错误。
3
5.(2022·温州模拟)常温下,下列有关说法不正确的是( )
A.pH=11的氨水、NaOH溶液中,水电离产生的c(H+)后者大
B.pH=3的HCl溶液与pH=11的氨水等体积混合,混合后溶液的pH大于7
C.pH=3的盐酸、CHCOOH溶液中,c(Cl-)=c(CHCOO-)
3 3
D.往10 mL pH=3的盐酸中分别加入pH=11的氨水、NaOH溶液至中性,消耗氨水的体
积小
答案 A
解析 pH=11的氨水、NaOH溶液中,c(OH-)都为1×10-3 mol·L-1,对水的电离抑制程度
相同, 相等,A项错误。
6.常温下,0.1 mol·L-1某一元酸(HA)溶液中=1×10-8,下列叙述正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中由水电离出的c(H+)=1×10-11 mol·L-1
C.该溶液中水的离子积常数为1×10-22
D.用0.1 mol·L-1的NaOH溶液V L与V L 0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶
1 2
液的pH=7,则V>V
1 2
答案 B
解析 将c(OH-)=代入题中关系式,可得=1×10-8,解得c(H+)=1×10-3 mol·
L-1,所以该溶液的pH=3,A项错误;由酸溶液中水的电离程度看c(OH-),c(OH-)
= mol·L-1=1×10-11 mol·L-1,所以由水电离出的c(H+)=1×10-11 mol·L-1,B项正确;
温度一定,水的离子积常数一定,常温下K =1×10-14,C项错误;由于HA是一元弱酸,
w
二者若等体积混合,生成NaA,溶液呈碱性,若pH=7,应有V<V,D项错误。
1 2
7.在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+
b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
序号 NaOH溶液体积 盐酸体积 溶液pH
① 20.00 0.00 8
② 20.00 20.00 6
假设溶液混合前后的体积变化忽略不计,则c为( )A.1 B.4 C.5 D.6
答案 B
解析 据题意可知在该温度下水的离子积常数是 1×10-12。通过①可知,此NaOH溶液中
c(OH-)=10-4 mol·L-1。由②可知,加入20 mL盐酸后溶液的pH=6,此时恰好完全中和,
则c(H+)==1×10-4 mol·L-1,则c=4。
8.25 ℃时,体积为V、pH=a的某一元强酸溶液与体积为V、pH=b的某一元强碱溶液均
a b
匀混合后,溶液的pH=7,已知b=6a,V<V,下列有关a的说法正确的是( )
a b
A.a可能等于1 B.a一定大于2
C.a一定小于2 D.a一定等于2
答案 C
解析 由b=6a>7得a>,由混合溶液的pH=7得n(H+)=n(OH-),即V×10-a=V×
a b
10b-14,得=10a+b-14;由于V<V ,即10a+b-14<1,得a+b-14<0,结合b=6a得a<2,
a b
综合知,<a<2,故选C项。
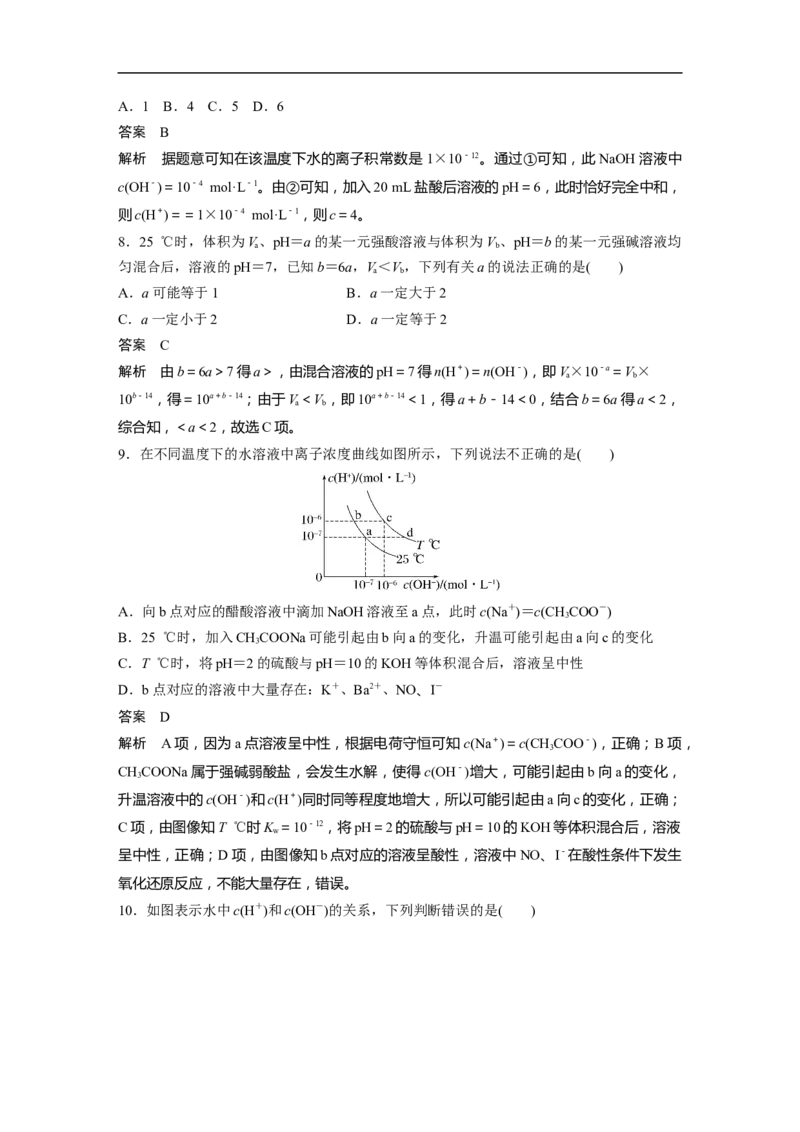
9.在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )
A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CHCOO-)
3
B.25 ℃时,加入CHCOONa可能引起由b向a的变化,升温可能引起由a向c的变化
3
C.T ℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性
D.b点对应的溶液中大量存在:K+、Ba2+、NO、I-
答案 D
解析 A项,因为a点溶液呈中性,根据电荷守恒可知 c(Na+)=c(CHCOO-),正确;B项,
3
CHCOONa属于强碱弱酸盐,会发生水解,使得 c(OH-)增大,可能引起由b向a的变化,
3
升温溶液中的c(OH-)和c(H+)同时同等程度地增大,所以可能引起由a向c的变化,正确;
C项,由图像知T ℃时K =10-12,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液
w
呈中性,正确;D项,由图像知b点对应的溶液呈酸性,溶液中NO、I-在酸性条件下发生
氧化还原反应,不能大量存在,错误。
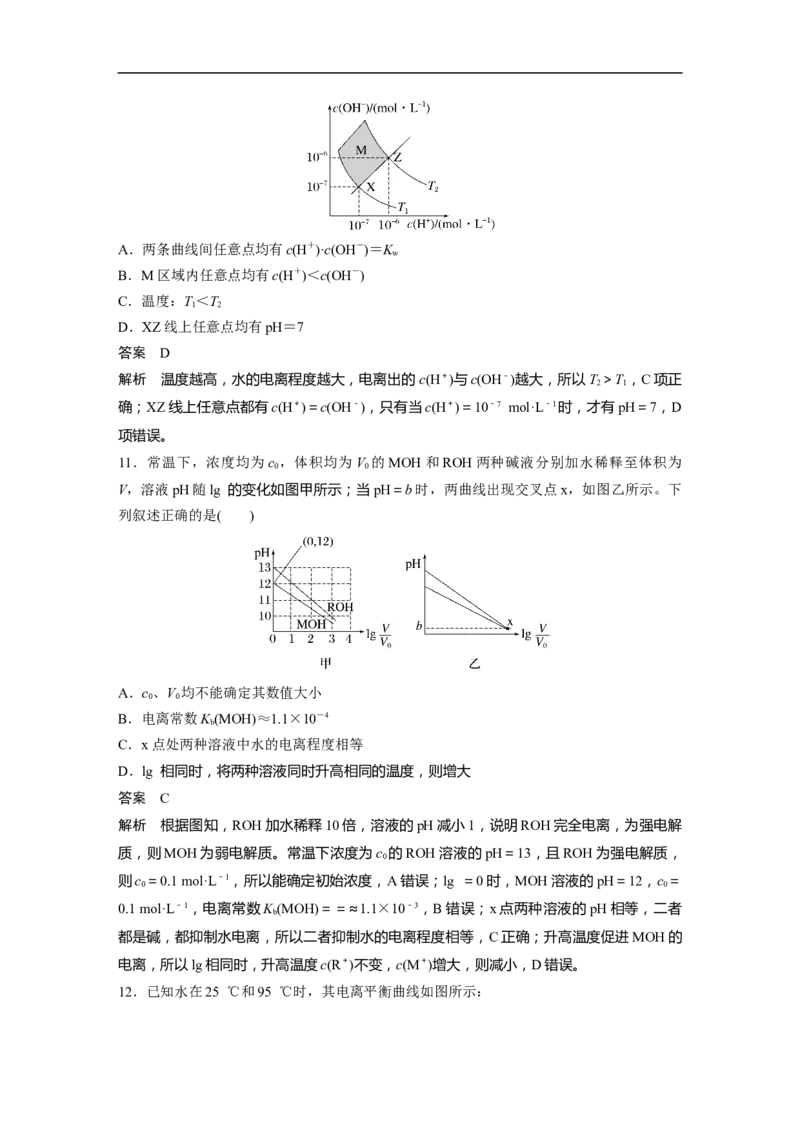
10.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )A.两条曲线间任意点均有c(H+)·c(OH-)=K
w
B.M区域内任意点均有c(H+)<c(OH-)
C.温度:T<T
1 2
D.XZ线上任意点均有pH=7
答案 D
解析 温度越高,水的电离程度越大,电离出的c(H+)与c(OH-)越大,所以T >T ,C项正
2 1
确;XZ线上任意点都有c(H+)=c(OH-),只有当c(H+)=10-7 mol·L-1时,才有pH=7,D
项错误。
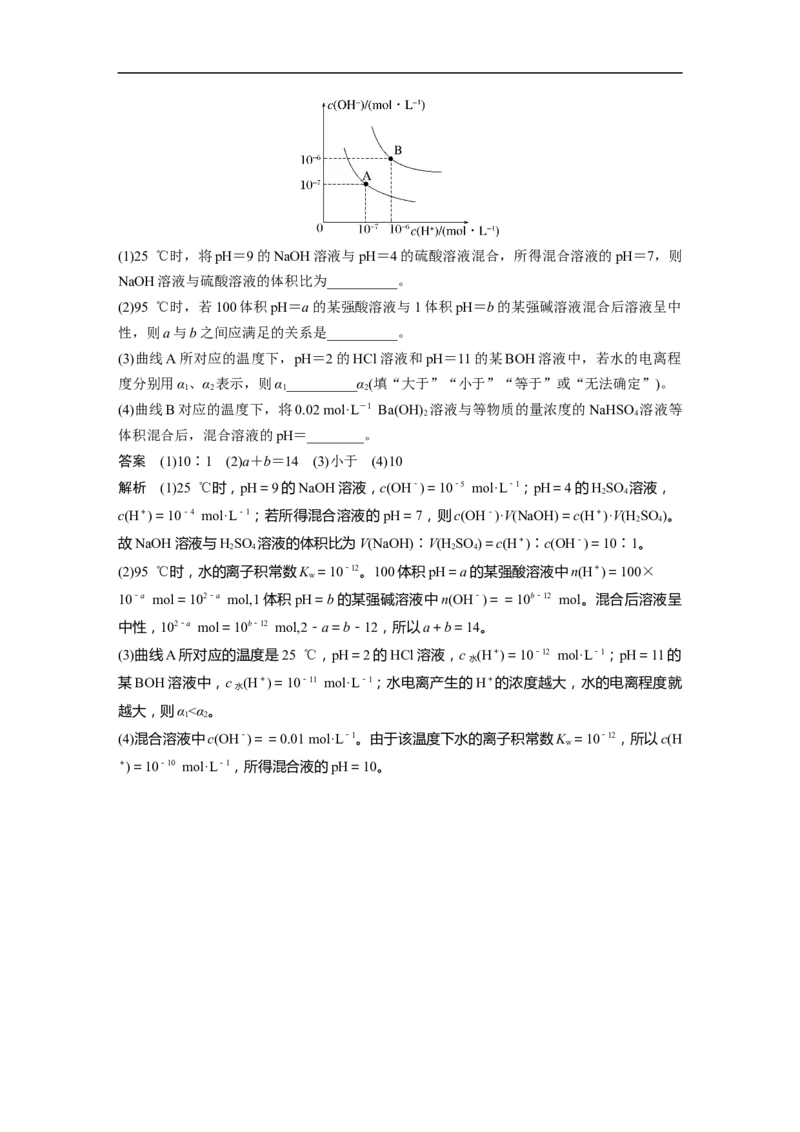
11.常温下,浓度均为c ,体积均为V 的MOH和ROH两种碱液分别加水稀释至体积为
0 0
V,溶液pH随lg 的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下
列叙述正确的是( )
A.c、V 均不能确定其数值大小
0 0
B.电离常数K (MOH)≈1.1×10-4
b
C.x点处两种溶液中水的电离程度相等
D.lg 相同时,将两种溶液同时升高相同的温度,则增大
答案 C
解析 根据图知,ROH加水稀释10倍,溶液的pH减小1,说明ROH完全电离,为强电解
质,则MOH为弱电解质。常温下浓度为c 的ROH溶液的pH=13,且ROH为强电解质,
0
则c =0.1 mol·L-1,所以能确定初始浓度,A错误;lg =0时,MOH溶液的pH=12,c =
0 0
0.1 mol·L-1,电离常数K (MOH)==≈1.1×10-3,B错误;x点两种溶液的pH相等,二者
b
都是碱,都抑制水电离,所以二者抑制水的电离程度相等,C正确;升高温度促进MOH的
电离,所以lg相同时,升高温度c(R+)不变,c(M+)增大,则减小,D错误。
12.已知水在25 ℃和95 ℃时,其电离平衡曲线如图所示:(1)25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则
NaOH溶液与硫酸溶液的体积比为__________。
(2)95 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中
性,则a与b之间应满足的关系是__________。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程
度分别用α、α 表示,则α__________α(填“大于”“小于”“等于”或“无法确定”)。
1 2 1 2
(4)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液等
2 4
体积混合后,混合溶液的pH=________。
答案 (1)10∶1 (2)a+b=14 (3)小于 (4)10
解析 (1)25 ℃时,pH=9的NaOH溶液,c(OH-)=10-5 mol·L-1;pH=4的HSO 溶液,
2 4
c(H+)=10-4 mol·L-1;若所得混合溶液的pH=7,则c(OH-)·V(NaOH)=c(H+)·V(H SO )。
2 4
故NaOH溶液与HSO 溶液的体积比为V(NaOH)∶V(H SO )=c(H+)∶c(OH-)=10∶1。
2 4 2 4
(2)95 ℃时,水的离子积常数K =10-12。100体积pH=a的某强酸溶液中n(H+)=100×
w
10-a mol=102-a mol,1体积pH=b的某强碱溶液中n(OH-)==10b-12 mol。混合后溶液呈
中性,102-a mol=10b-12 mol,2-a=b-12,所以a+b=14。
(3)曲线A所对应的温度是25 ℃,pH=2的HCl溶液,c (H+)=10-12 mol·L-1;pH=11的
水
某BOH溶液中,c (H+)=10-11 mol·L-1;水电离产生的H+的浓度越大,水的电离程度就
水
越大,则α<α。
1 2
(4)混合溶液中c(OH-)==0.01 mol·L-1。由于该温度下水的离子积常数K =10-12,所以c(H
w
+)=10-10 mol·L-1,所得混合液的pH=10。