文档内容
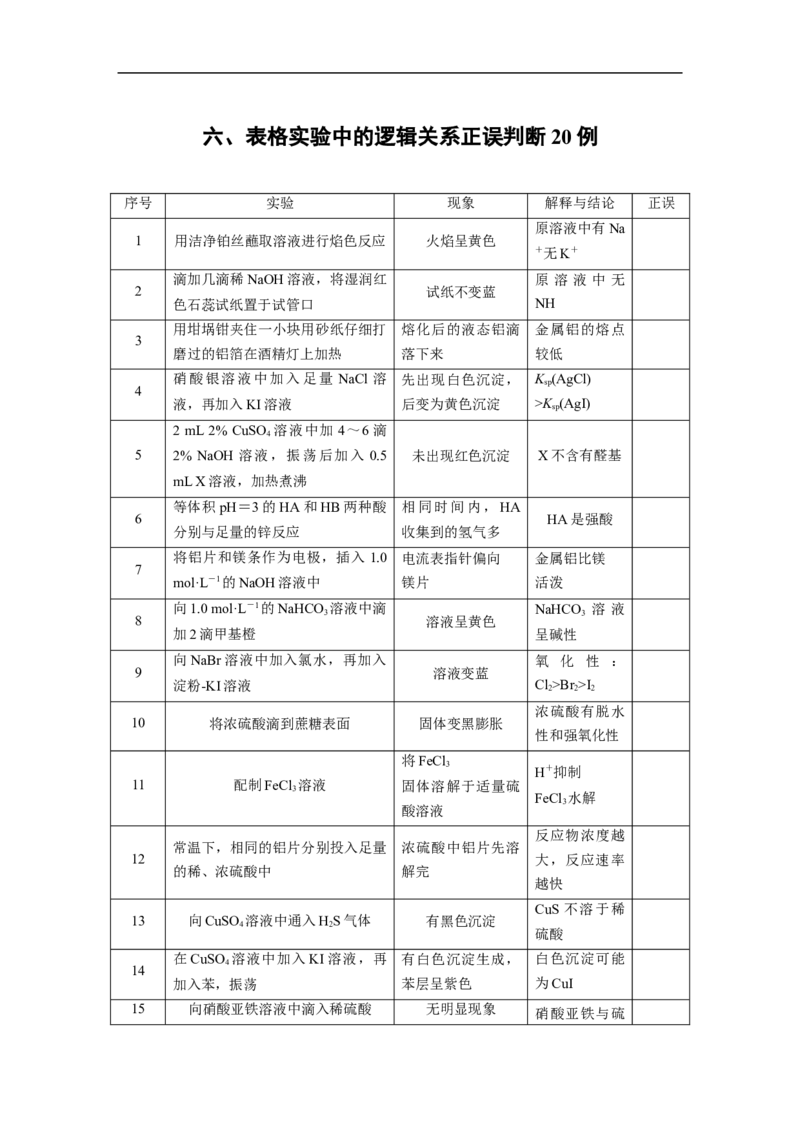
六、表格实验中的逻辑关系正误判断 20 例
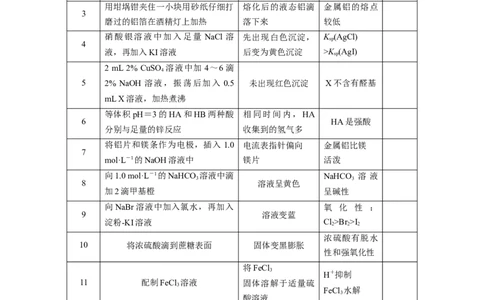
序号 实验 现象 解释与结论 正误
原溶液中有Na
1 用洁净铂丝蘸取溶液进行焰色反应 火焰呈黄色
+无K+
滴加几滴稀NaOH溶液,将湿润红 原 溶 液 中 无
2 试纸不变蓝
色石蕊试纸置于试管口 NH
用坩埚钳夹住一小块用砂纸仔细打 熔化后的液态铝滴 金属铝的熔点
3
磨过的铝箔在酒精灯上加热 落下来 较低
硝酸银溶液中加入足量 NaCl 溶 先出现白色沉淀, K (AgCl)
sp
4
液,再加入KI溶液 后变为黄色沉淀 >K (AgI)
sp
2 mL 2% CuSO 溶液中加 4~6 滴
4
5 2% NaOH 溶液,振荡后加入 0.5 未出现红色沉淀 X不含有醛基
mL X溶液,加热煮沸
等体积pH=3的HA和HB两种酸 相同时间内,HA
6 HA是强酸
分别与足量的锌反应 收集到的氢气多
将铝片和镁条作为电极,插入 1.0 电流表指针偏向 金属铝比镁
7
mol·L-1的NaOH溶液中 镁片 活泼
向1.0 mol·L-1的NaHCO 溶液中滴 NaHCO 溶 液
3 3
8 溶液呈黄色
加2滴甲基橙 呈碱性
向NaBr溶液中加入氯水,再加入 氧 化 性 :
9 溶液变蓝
淀粉-KI溶液 Cl>Br >I
2 2 2
浓硫酸有脱水
10 将浓硫酸滴到蔗糖表面 固体变黑膨胀
性和强氧化性
将FeCl
3 H+抑制
11 配制FeCl 溶液 固体溶解于适量硫
3
FeCl 水解
3
酸溶液
反应物浓度越
常温下,相同的铝片分别投入足量 浓硫酸中铝片先溶
12 大,反应速率
的稀、浓硫酸中 解完
越快
CuS 不溶于稀
13 向CuSO 溶液中通入HS气体 有黑色沉淀
4 2
硫酸
在CuSO 溶液中加入KI溶液,再 有白色沉淀生成, 白色沉淀可能
4
14
加入苯,振荡 苯层呈紫色 为CuI
15 向硝酸亚铁溶液中滴入稀硫酸 无明显现象 硝酸亚铁与硫酸不反应
HCO的水解程
常温下,用pH试纸测定一定浓度 比对后,测得
16 度小于其电离
的NaHCO 溶液的pH pH=8
3
程度
向一定量的浓硫酸中加入过量的锌 该气体成分仅
17 产生气泡
粒,微热至反应结束 为SO
2
将澄清石灰水滴入可能混有 该溶液中一定
18 有白色沉淀产生
NaCO 的NaHCO 溶液中 含有NaCO
2 3 3 2 3
构成原电池,
表面变黑的银器浸泡到盛有食盐水 铝作负极,硫
19 银器变得光亮如新
的铝制容器中,银器与铝接触 化银得电子被
还原成单质银
浓 硝 酸 将 Fe
氧化成Fe3+,
向足量的浓硝酸中加入铁片,一段 有气体生成,溶液
20 生成NO ,Cu
2
时间后加入铜粉 呈蓝绿色
与Fe3+反应生
成Cu2+
答案 1.× 2.× 3.× 4.√ 5.× 6.× 7.× 8.× 9.× 10.√ 11.× 12.×
13.√
14.√ 15.× 16.× 17.× 18.× 19.√ 20.×