文档内容
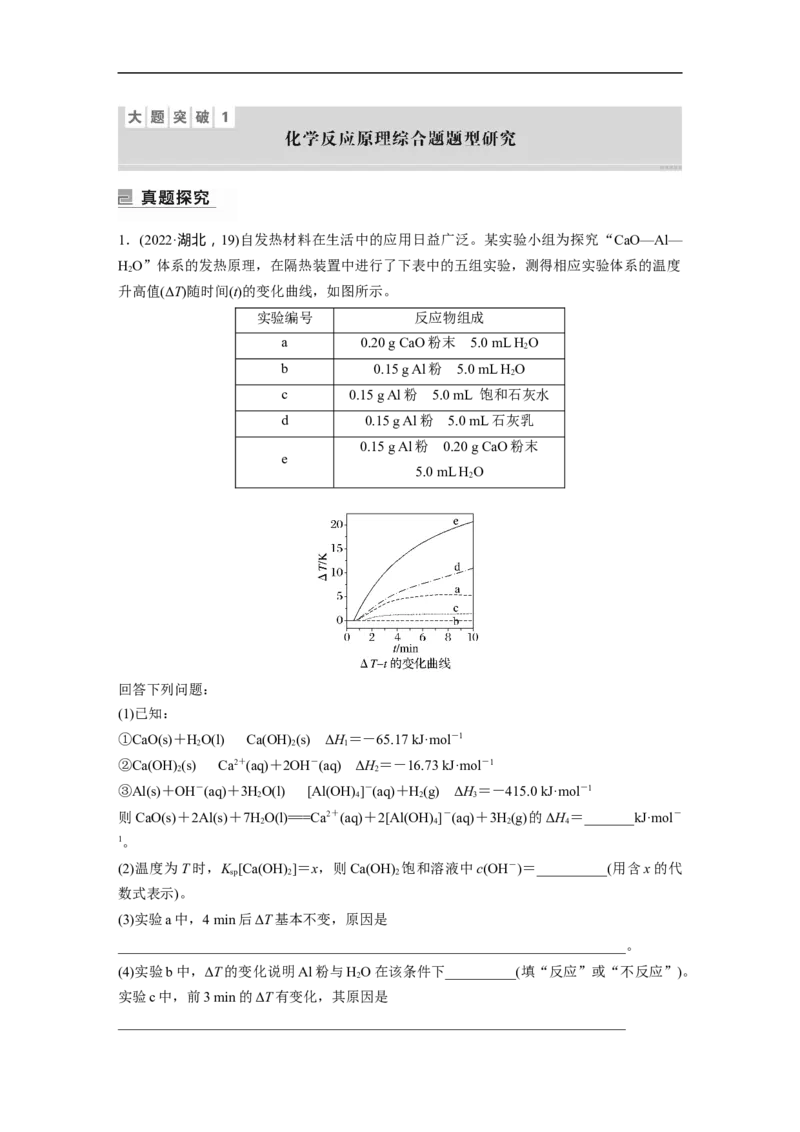
1.(2022·湖北,19)自发热材料在生活中的应用日益广泛。某实验小组为探究“CaO—Al—
HO”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度
2
升高值(ΔT)随时间(t)的变化曲线,如图所示。
实验编号 反应物组成
a 0.20 g CaO粉末 5.0 mL H O
2
b 0.15 g Al粉 5.0 mL H O
2
c 0.15 g Al粉 5.0 mL 饱和石灰水
d 0.15 g Al粉 5.0 mL石灰乳
0.15 g Al粉 0.20 g CaO粉末
e
5.0 mL H O
2
回答下列问题:
(1)已知:
①CaO(s)+HO(l)Ca(OH) (s) ΔH=-65.17 kJ·mol-1
2 2 1
②Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH=-16.73 kJ·mol-1
2 2
③Al(s)+OH-(aq)+3HO(l)[Al(OH) ]-(aq)+H(g) ΔH=-415.0 kJ·mol-1
2 4 2 3
则CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH) ]-(aq)+3H(g)的ΔH =_______kJ·mol-
2 4 2 4
1。
(2)温度为T时,K [Ca(OH) ]=x,则Ca(OH) 饱和溶液中c(OH-)=__________(用含x的代
sp 2 2
数式表示)。
(3)实验a中,4 min后ΔT基本不变,原因是
________________________________________________________________________。
(4)实验b中,ΔT的变化说明Al粉与HO在该条件下__________(填“反应”或“不反应”)。
2
实验c中,前3 min的ΔT有变化,其原因是
________________________________________________________________________________________________________________________________________________;
3 min后ΔT基本不变,其原因是____________________________________________
________________________________________________________________________
微粒的量有限。
(5)下列说法不能解释实验d在10 min内温度持续升高的是__________(填标号)。
A.反应②的发生促使反应①平衡右移
B.反应③的发生促使反应②平衡右移
C.气体的逸出促使反应③向右进行
D.温度升高导致反应速率加快
(6)归纳以上实验结果,根据实验e的特征,用文字简述其发热原理________________
________________________________________________________________________。
答案 (1)-911.9 (2) mol·L-1 (3)Ca(OH) 在水中的溶解度小,反应①达到了平衡状态
2
(4)不反应 Al和溶液中的OH-发生了反应 OH- (5)A (6)实验e中,发生反应①、②和
③,反应③中有气体生成,气体的逸出促使反应③向右进行,反应③的发生使得溶液中OH
-的浓度减小,促使反应②平衡右移,反应②的发生促使反应①平衡右移,这三步反应都是
放热反应,温度升高导致反应速率加快,温度持续升高
解析 (1)根据盖斯定律,①+②+2×③可得反应CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+
2
2[Al(OH)]-(aq)+3H(g),则ΔH =ΔH +ΔH +2ΔH =(-65.17 kJ·mol-1)+(-16.73 kJ·mol-1)
4 2 4 1 2 3
+2×(-415.0 kJ·mol-1)=-911.9 kJ·mol-1。(2)温度为 T 时,Ca(OH) 饱和溶液中,
2
Ca(OH) (s)Ca2+(aq)+2OH-(aq), c(OH-)=2c(Ca2+),K [Ca(OH) ]=c(Ca2+)·c2(OH-)=x,
2 sp 2
则c(OH-)= mol·L-1。(4)实验b中,ΔT几乎不变,说明Al粉与HO在该条件下不反应;
2
实验c中,前3 min的ΔT有变化,是因为Al和溶液中的OH-发生了反应,3 min后ΔT基本
不变,是因为饱和石灰水中OH-的浓度较低,OH-的量有限。(5)实验d中,发生反应②和
③,反应③中有气体生成,气体的逸出促使反应③向右进行,反应③的发生使得溶液中OH
-的浓度减小,促使反应②平衡右移,这两步反应都是放热反应,温度升高导致反应速率加
快;综上所述,实验d在10 min内温度持续升高与反应①无关,故选A。
2.(2022·海南,16)某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
CO(g)+4H(g)2HO(g)+CH(g)
2 2 2 4
回答问题:
(1)已知:电解液态水制备1 mol O (g),电解反应的ΔH=+572 kJ·mol-1。由此计算H(g)的
2 2
燃烧热(焓)ΔH=______ kJ·mol-1。
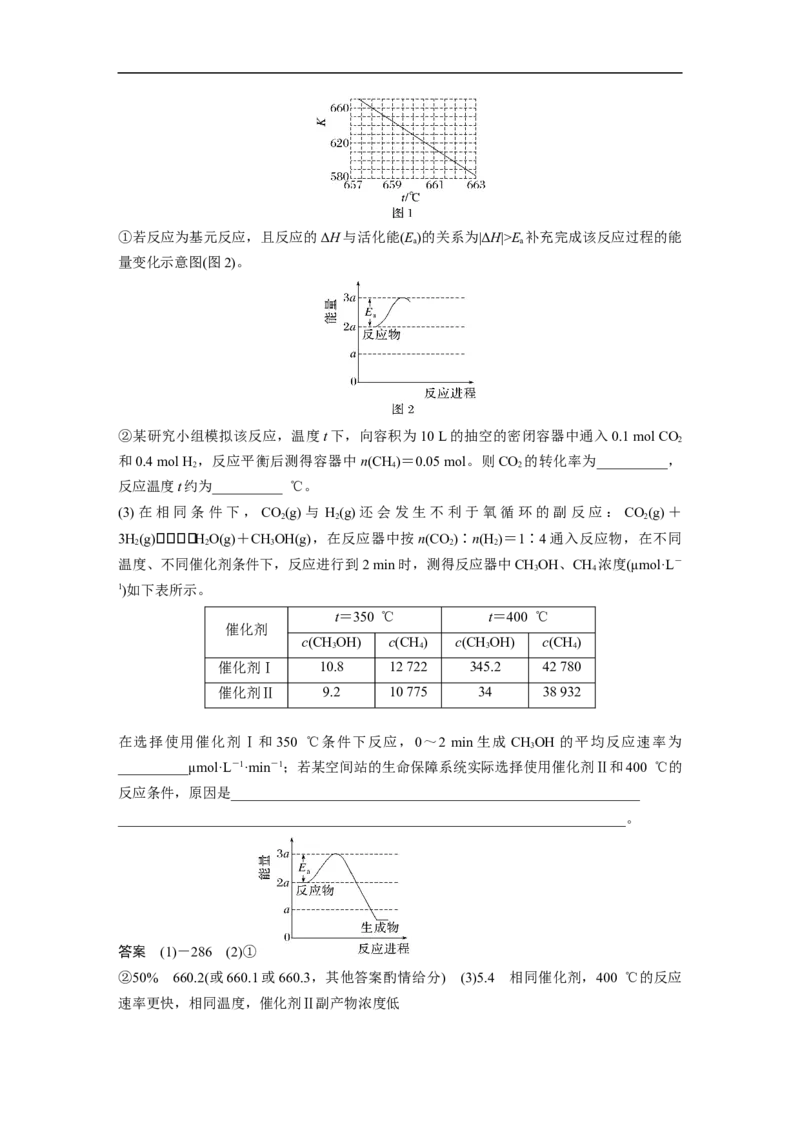
(2)已知:CO(g)+4H(g)2HO(g)+CH(g)的平衡常数(K)与反应温度(t)之间的关系如图
2 2 2 4
1所示。①若反应为基元反应,且反应的ΔH与活化能(E)的关系为|ΔH|>E 补充完成该反应过程的能
a a
量变化示意图(图2)。
②某研究小组模拟该反应,温度t下,向容积为10 L的抽空的密闭容器中通入0.1 mol CO
2
和0.4 mol H ,反应平衡后测得容器中n(CH)=0.05 mol。则CO 的转化率为__________,
2 4 2
反应温度t约为__________ ℃。
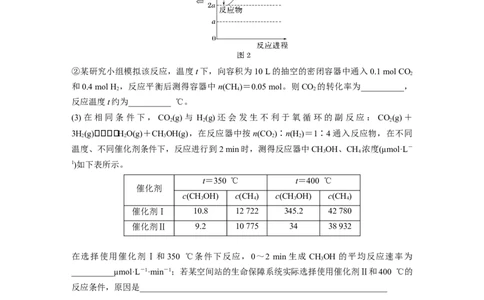
(3)在相同条件下,CO(g)与 H(g)还会发生不利于氧循环的副反应: CO(g)+
2 2 2
3H(g)HO(g)+CHOH(g),在反应器中按n(CO)∶n(H )=1∶4通入反应物,在不同
2 2 3 2 2
温度、不同催化剂条件下,反应进行到2 min时,测得反应器中CHOH、CH 浓度(μmol·L-
3 4
1)如下表所示。
t=350 ℃ t=400 ℃
催化剂
c(CHOH) c(CH) c(CHOH) c(CH)
3 4 3 4
催化剂Ⅰ 10.8 12 722 345.2 42 780
催化剂Ⅱ 9.2 10 775 34 38 932
在选择使用催化剂Ⅰ和 350 ℃条件下反应,0~2 min 生成 CHOH 的平均反应速率为
3
__________μmol·L-1·min-1;若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400 ℃的
反应条件,原因是__________________________________________________________
________________________________________________________________________。
答案 (1)-286 (2)①
②50% 660.2(或660.1或660.3,其他答案酌情给分) (3)5.4 相同催化剂,400 ℃的反应
速率更快,相同温度,催化剂Ⅱ副产物浓度低解析 (1)电解液态水制备1 mol O (g),电解反应的ΔH=+572 kJ·mol-1,由此可以判断,2
2
mol H(g)完全燃烧消耗1 mol O (g),生成液态水的同时放出的热量为572 kJ,故1 mol H (g)
2 2 2
完全燃烧生成液态水放出的热量为286 kJ,因此,H(g)的燃烧热(焓)ΔH=-286 kJ·mol-1。
2
(2)①由CO(g)+4H(g)2HO(g)+CH(g)的平衡常数(K)与反应温度(t)之间的关系图可
2 2 2 4
知,K随着温度升高而减小,故该反应为放热反应。若反应为基元反应,则反应为一步完成,
由于反应的ΔH与活化能(E)的关系为|ΔH|>E ,由图2信息可知E =a kJ·mol-1,则|ΔH|>a
a a a
kJ·mol-1,该反应为放热反应,生成物的总能量小于反应物的,因此该反应过程的能量变化
示意图为 。②温度t下,向容积为10 L的抽空的密闭容器中通入
0.1 mol CO 和0.4 mol H ,反应平衡后测得容器中n(CH)=0.05 mol,则CO 的转化率为
2 2 4 2
×100%=50%,根据C元素守恒可知,CO 的平衡量为0.05 mol,H 的平衡量为0.2 mol,
2 2
HO(g)的平衡量是CH(g)的2倍,则n(H O)=0.1 mol,CO(g)、H(g)、HO(g)、CH(g)的平
2 4 2 2 2 2 4
衡浓度分别为0.005 mol·L-1、0.02 mol·L-1、0.01 mol·L-1、0.005 mol·L-1,则该反应的平衡
常数K==625,根据图1中的信息可知,反应温度t约为660.2 ℃。(3)在选择使用催化剂
Ⅰ和350 ℃条件下反应,由表中信息可知,0~2 min CH OH的浓度由0增加到10.8 μmol·L-
3
1,因此,0~2 min生成CHOH的平均反应速率为=5.4 μmol·L-1·min-1;由表中信息可知,
3
相同催化剂,400 ℃的反应速率更快,相同温度,催化剂Ⅱ副产物浓度低。
化学反应原理主要考查热化学、电化学、化学反应速率和化学平衡等主干理论知识,主要命
题点有盖斯定律的应用、反应速率和化学平衡的分析、化学平衡常数的表达式书写与计算、
反应条件的分析选择、生产生活中的实际应用等,试题常以填空、读图、作图、计算等形式
呈现。试题一般以与生产、生活紧密联系的物质为背景材料命制组合题,各小题之间又有一
定的独立性。主要考查学生的信息处理能力、学科内综合分析能力,应用反应原理解决生产
实际中的具体问题,体现了“变化观念与平衡思想”的核心素养。在近几年的相关考题中,
对单一因素影响的考查已经越来越少了,主要以“多因素影响”出现,考查考生的综合分析
判断能力。以实际情景(场景)为背景,更能体现核心素养的要求。而在实际生产过程中,影
响因素是多元化、多方位和多层次的。
(2022·安徽模拟)处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物NO的反应为CO(g)+NO(g)CO(g)+N(g)。在Zn+作用下该
2 2 2 2
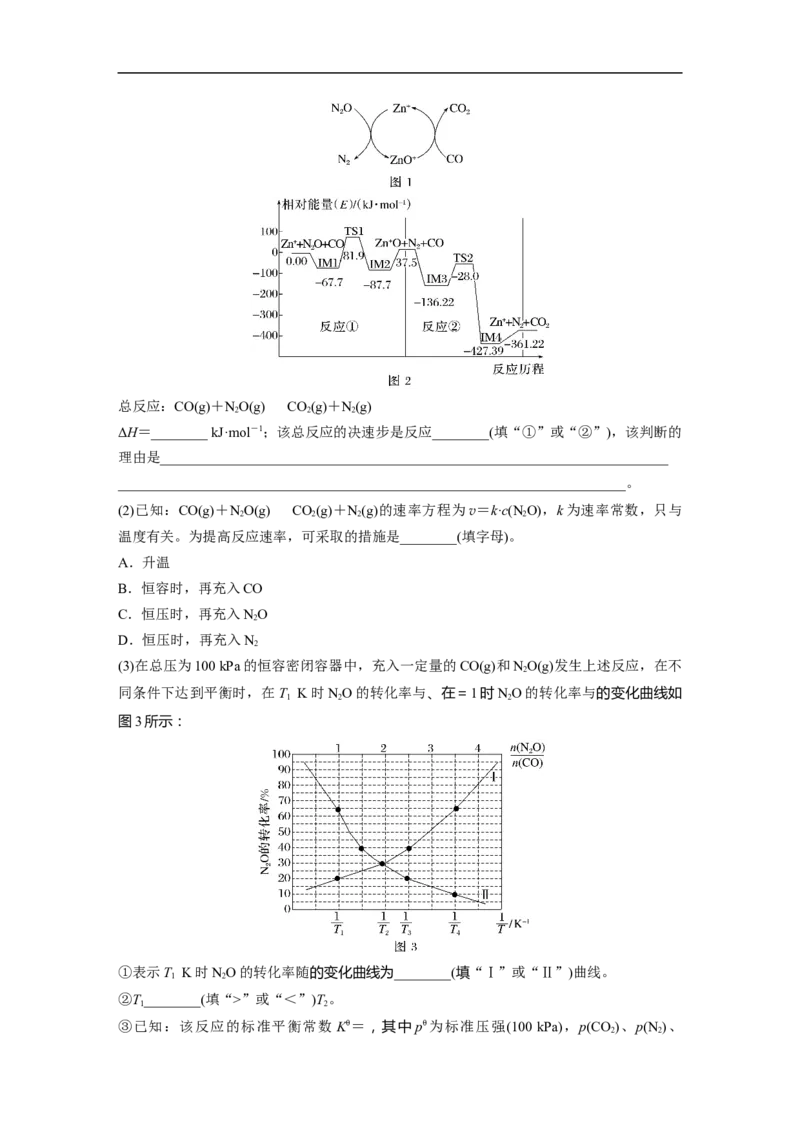
反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。总反应:CO(g)+NO(g)CO(g)+N(g)
2 2 2
ΔH=________ kJ·mol-1;该总反应的决速步是反应________(填“①”或“②”),该判断的
理由是________________________________________________________________________
________________________________________________________________________。
(2)已知:CO(g)+NO(g)CO(g)+N(g)的速率方程为v=k·c(N O),k为速率常数,只与
2 2 2 2
温度有关。为提高反应速率,可采取的措施是________(填字母)。
A.升温
B.恒容时,再充入CO
C.恒压时,再充入NO
2
D.恒压时,再充入N
2
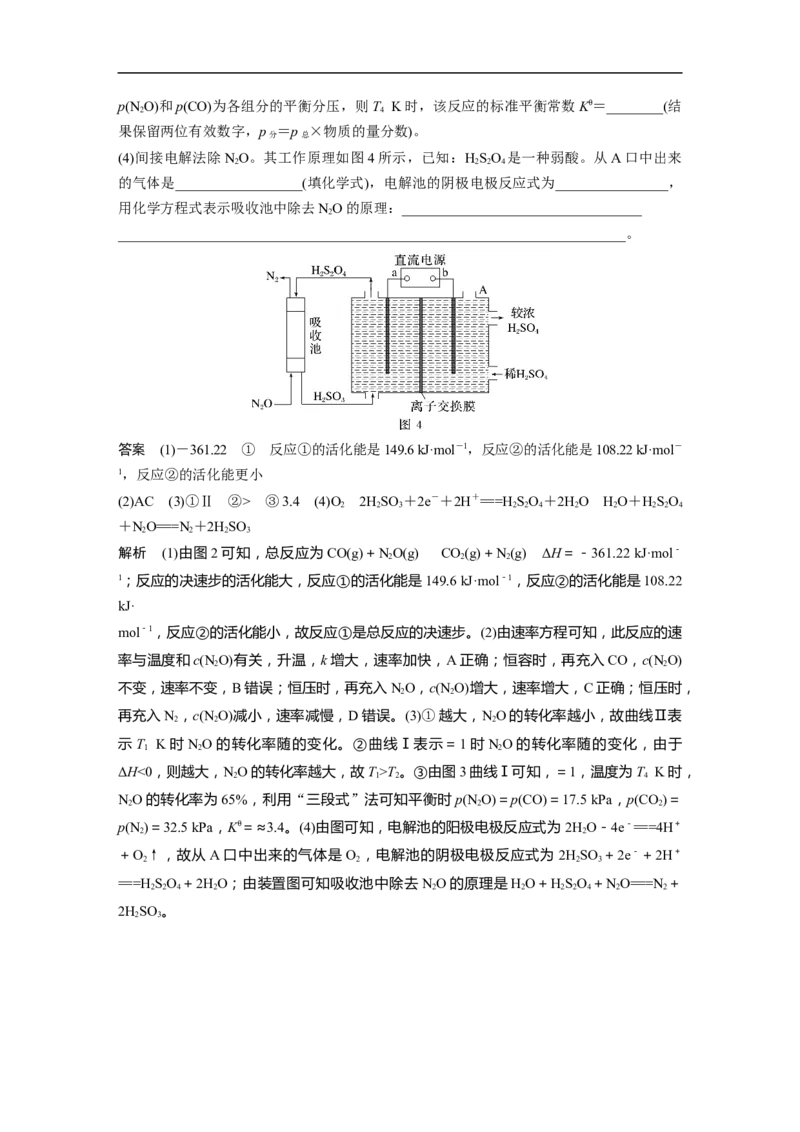
(3)在总压为100 kPa的恒容密闭容器中,充入一定量的CO(g)和NO(g)发生上述反应,在不
2
同条件下达到平衡时,在T K时NO的转化率与、在=1时NO的转化率与的变化曲线如
1 2 2
图3所示:
①表示T K时NO的转化率随的变化曲线为________(填“Ⅰ”或“Ⅱ”)曲线。
1 2
②T________(填“>”或“<”)T。
1 2
③已知:该反应的标准平衡常数 Kθ=,其中 pθ为标准压强(100 kPa),p(CO)、p(N )、
2 2p(N O)和p(CO)为各组分的平衡分压,则T K时,该反应的标准平衡常数Kθ=________(结
2 4
果保留两位有效数字,p =p ×物质的量分数)。
分 总
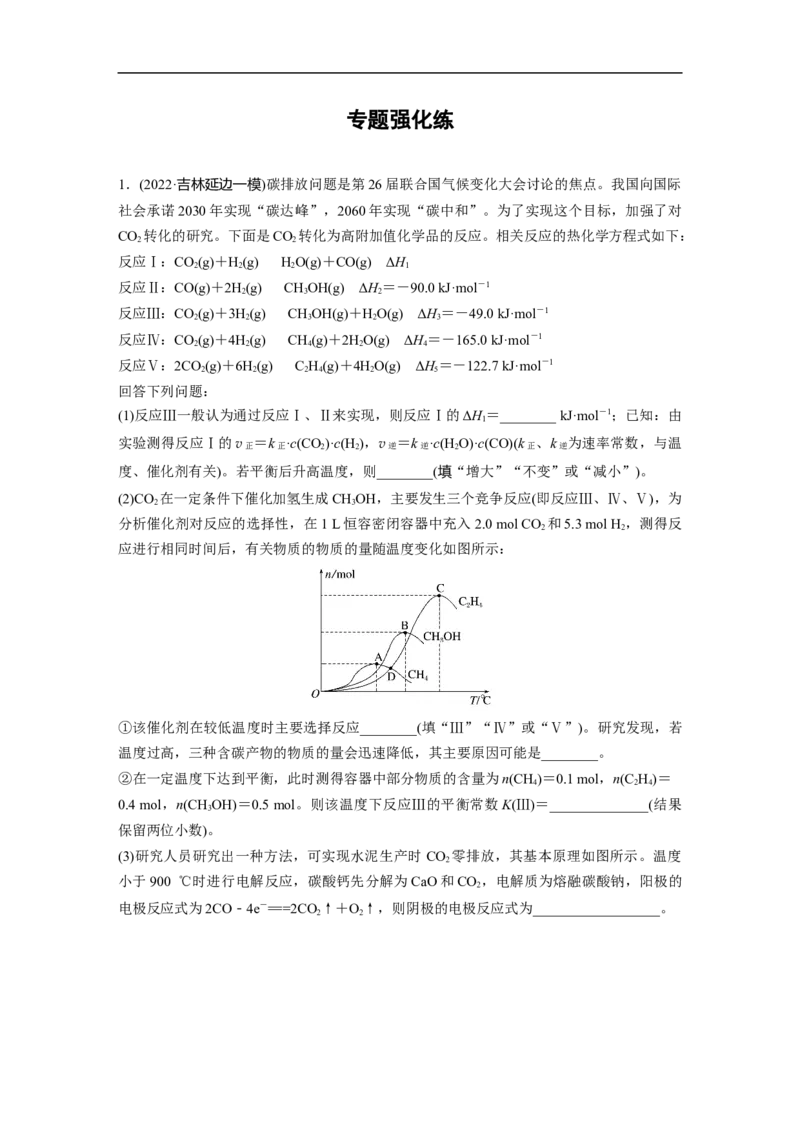
(4)间接电解法除NO。其工作原理如图4所示,已知:HSO 是一种弱酸。从A口中出来
2 2 2 4
的气体是__________________(填化学式),电解池的阴极电极反应式为________________,
用化学方程式表示吸收池中除去NO的原理:__________________________________
2
________________________________________________________________________。
答案 (1)-361.22 ① 反应①的活化能是149.6 kJ·mol-1,反应②的活化能是108.22 kJ·mol-
1,反应②的活化能更小
(2)AC (3)①Ⅱ ②> ③3.4 (4)O 2HSO +2e-+2H+===HSO +2HO HO+HSO
2 2 3 2 2 4 2 2 2 2 4
+NO===N+2HSO
2 2 2 3
解析 (1)由图2可知,总反应为CO(g)+NO(g)CO(g)+N(g) ΔH=-361.22 kJ·mol-
2 2 2
1;反应的决速步的活化能大,反应①的活化能是149.6 kJ·mol-1,反应②的活化能是108.22
kJ·
mol-1,反应②的活化能小,故反应①是总反应的决速步。(2)由速率方程可知,此反应的速
率与温度和c(N O)有关,升温,k增大,速率加快,A正确;恒容时,再充入CO,c(N O)
2 2
不变,速率不变,B错误;恒压时,再充入NO,c(N O)增大,速率增大,C正确;恒压时,
2 2
再充入N ,c(N O)减小,速率减慢,D错误。(3)①越大,NO的转化率越小,故曲线Ⅱ表
2 2 2
示T K时NO的转化率随的变化。②曲线Ⅰ表示=1时NO的转化率随的变化,由于
1 2 2
ΔH<0,则越大,NO的转化率越大,故T>T 。③由图3曲线Ⅰ可知,=1,温度为T K时,
2 1 2 4
NO的转化率为65%,利用“三段式”法可知平衡时p(N O)=p(CO)=17.5 kPa,p(CO)=
2 2 2
p(N )=32.5 kPa,Kθ=≈3.4。(4)由图可知,电解池的阳极电极反应式为 2HO-4e-===4H+
2 2
+O↑,故从A口中出来的气体是 O ,电解池的阴极电极反应式为 2HSO +2e-+2H+
2 2 2 3
===HSO +2HO;由装置图可知吸收池中除去 NO的原理是HO+HSO +NO===N +
2 2 4 2 2 2 2 2 4 2 2
2HSO 。
2 3专题强化练
1.(2022·吉林延边一模)碳排放问题是第26届联合国气候变化大会讨论的焦点。我国向国际
社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。为了实现这个目标,加强了对
CO 转化的研究。下面是CO 转化为高附加值化学品的反应。相关反应的热化学方程式如下:
2 2
反应Ⅰ:CO(g)+H(g)HO(g)+CO(g) ΔH
2 2 2 1
反应Ⅱ:CO(g)+2H(g)CHOH(g) ΔH=-90.0 kJ·mol-1
2 3 2
反应Ⅲ:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-49.0 kJ·mol-1
2 2 3 2 3
反应Ⅳ:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165.0 kJ·mol-1
2 2 4 2 4
反应Ⅴ:2CO(g)+6H(g)C H(g)+4HO(g) ΔH=-122.7 kJ·mol-1
2 2 2 4 2 5
回答下列问题:
(1)反应Ⅲ一般认为通过反应Ⅰ、Ⅱ来实现,则反应Ⅰ的ΔH=________ kJ·mol-1;已知:由
1
实验测得反应Ⅰ的v正 =k
正
·c(CO
2
)·c(H
2
),v逆 =k
逆
·c(H
2
O)·c(CO)(k
正
、k
逆
为速率常数,与温
度、催化剂有关)。若平衡后升高温度,则________(填“增大”“不变”或“减小”)。
(2)CO 在一定条件下催化加氢生成CHOH,主要发生三个竞争反应(即反应Ⅲ、Ⅳ、Ⅴ),为
2 3
分析催化剂对反应的选择性,在1 L恒容密闭容器中充入2.0 mol CO 和5.3 mol H ,测得反
2 2
应进行相同时间后,有关物质的物质的量随温度变化如图所示:
①该催化剂在较低温度时主要选择反应________(填“Ⅲ”“Ⅳ”或“Ⅴ”)。研究发现,若
温度过高,三种含碳产物的物质的量会迅速降低,其主要原因可能是________。
②在一定温度下达到平衡,此时测得容器中部分物质的含量为n(CH)=0.1 mol,n(C H)=
4 2 4
0.4 mol,n(CHOH)=0.5 mol。则该温度下反应Ⅲ的平衡常数K(Ⅲ)=______________(结果
3
保留两位小数)。
(3)研究人员研究出一种方法,可实现水泥生产时 CO 零排放,其基本原理如图所示。温度
2
小于900 ℃时进行电解反应,碳酸钙先分解为CaO和CO ,电解质为熔融碳酸钠,阳极的
2
电极反应式为2CO-4e-===2CO↑+O↑,则阴极的电极反应式为__________________。
2 2答案 (1)+41.0 减小 (2)①Ⅳ 温度升高,催化剂活性降低 ②1.92 (3)3CO +4e-
2
===C+2CO
解析 (1)根据盖斯定律,反应Ⅲ-反应Ⅱ可得CO (g)+H (g)H O(g)+CO(g) ΔH =-
2 2 2 1
49.0 kJ·mol-1+90.0 kJ·mol-1=+41.0 kJ·mol-1;反应Ⅰ属于吸热反应,升温平衡正向移动,
K=增大,则减小。
(2)①由图知,在较低温度时主要生成甲烷,该催化剂在较低温度时主要选择反应Ⅳ。研究
发现,若温度过高,三种含碳产物的物质的量会迅速降低,其主要原因可能是温度升高,催
化剂活性降低。
② CO(g)+3H(g)CHOH(g)+HO(g)
2 2 3 2
0.5 1.5 0.5 0.5
CO(g)+4H(g)CH(g)+2HO(g)
2 2 4 2
0.1 0.4 0.1 0.2
2CO(g)+6H(g)C H(g)+4HO(g)
2 2 2 4 2
0.8 2.4 0.4 1.6
平衡时,c(H O)=(0.5+0.2+1.6) mol·L-1=2.3 mol·L-1,c(H )=(5.3-1.5-0.4-2.4) mol·L-
2 2
1=1 mol·L-1,c(CO)=(2.0-0.5-0.1-0.8) mol·L-1=0.6 mol·L-1,K(Ⅲ)==≈1.92。
2
(3)温度小于900 ℃时进行电解反应,碳酸钙先分解为CaO和CO ,电解质为熔融碳酸钠,
2
熔融碳酸钠中的碳酸根离子移向阳极,阳极的电极反应式为 2CO-4e-===2CO↑+O↑,
2 2
阴极得电子发生还原反应生成碳,则阴极的电极反应式为3CO+4e-===C+2CO。
2
2.(2022·重庆模拟)碳达峰是指我国承诺2030年前,二氧化碳的排放不再增长。因此,诸多
科学家都在大力研究利用CO 和CO以减少碳的排放。
2
(1)“神十三”中航天员们呼吸产生的CO 用一种循环方案处理,即CO(g)+2H(g)C(s)
2 2 2
+2HO(g) ΔH,然后电解水又得氢气和氧气。在温度为T时,向一恒容密闭容器中,按物
2
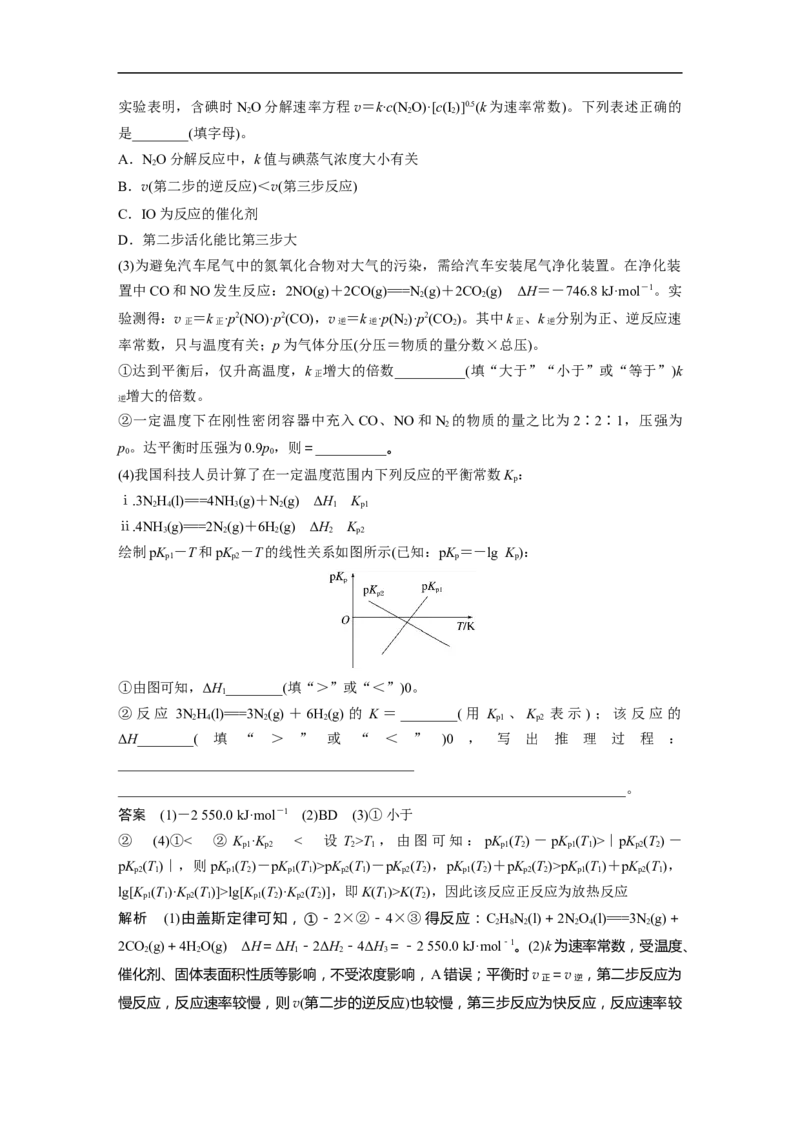
质的量之比为2∶1通入H 和CO ,测得反应过程中压强(p)随时间(t)的变化如图中a所示。
2 2
若其他条件不变,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图中b所示。①能说明容器中的反应已达到平衡状态的是__________(填字母)。
A.容器内气体的平均相对分子质量不变
B.CO 和H 的转化率相等
2 2
C.H(g)与C(s)的物质的量之比保持不变
2
D.v(H )=v(H O)
2 2
②ΔH________(填“>”“<”或“不确定”)0;理由是
________________________________________________________________________
________________________________________________________________________。
③改变的条件是__________________________________________________________。
(2)CO 经催化加氢可以生成低碳有机物,主要有以下反应:
2
反应Ⅰ:CO(g)+3H(g)CHOH(g)+HO(g)
2 2 3 2
ΔH=-49.6 kJ·mol-1
反应Ⅱ:2CO(g)+6H(g)CHOCH (g)+3HO(g) ΔH=-122.6 kJ·mol-1
2 2 3 3 2
①反应Ⅱ的活化能E(正)________(填“>”“<”或“=”)E(逆)。
a a
②在T 温度下,将3 mol CO 和7 mol H 充入2 L的恒容密闭容器中发生反应Ⅰ和Ⅱ,达到
1 2 2
平衡状态时CHOH(g)和CHOCH (g)的物质的量分别为1 mol和0.5 mol。则T 温度时反应
3 3 3 1
Ⅰ的平衡常数K=__________。
(3)工业上利用废气中的CO 、CO联合制取烧碱、氯代烃和甲醇的流程如图。已知 B中的装
2
置使用了阳离子交换膜。
①B中发生的总反应的离子方程式为___________________________________________
________________________________________________________________________。
②若某废气中含有的 CO 和 CO 的体积比为 1∶1,废气中 CO 和 CO 的体积分数共为
2 2
8.96%。假设A中处理了标准状况下10 m3的废气,其中CO 和CO全部转化成CHOH,理
2 3
论上可制得C HCl________ kg。
2 4 2
答案 (1)①AC ②< 随着反应进行,压强先变大后变小,说明反应为放热反应,使得开
始的温度升高,压强增大 ③加入催化剂 (2)①< ②10(3)①2HO+2Cl-=====H↑+2OH-+Cl↑
2 2 2
②9.9
解析 (1)①容器内气体的质量和物质的量均是变化的量,气体的平均相对分子质量不变,
说明反应已达到平衡状态,A符合题意;CO 和H 的投料比等于化学计量数之比,故两者
2 2
的转化率相等,不能说明反应达到平衡状态,B不符合题意;H(g)与C(s)的物质的量之比随
2
着反应的进行不断变化,当该比例保持不变时,说明反应已达到平衡状态,C符合题意;
v(H )=v(H O)时,由于未指明两个速率的反应方向,故不能说明反应达到平衡状态,D不符
2 2
合题意。②由图可知,随着反应进行,压强先变大后变小,5 min时达到平衡状态,说明反
应为放热反应,使得开始的温度升高,压强变大,故ΔH<0。③改变的条件使化学反应速
率加快,而平衡没有移动,说明加入了催化剂。(2)①反应Ⅱ为放热反应,生成物的能量低
于反应物的能量,则反应Ⅱ的活化能E(正)<E(逆)。②由题可得:
a a
CO(g)+3H(g)CHOH(g)+HO(g)
2 2 3 2
1 3 1 1
2CO(g)+6H(g)CHOH (g)+3HO(g)
2 2 3 3 2
1 3 0.5 1.5
在T 温度下,2 L的恒容密闭容器中平衡时CO 、H 、CHOH、HO的物质的量分别为3
1 2 2 3 2
mol-1 mol-1 mol=1 mol、7 mol-3 mol-3 mol=1 mol、1 mol、1 mol+1.5 mol=2.5
mol;则T 温度时反应Ⅰ的平衡常数K==10。
1
(3)①由图可知,B中发生的总反应为电解氯化钠溶液的反应,离子方程式为 2HO+2Cl-
2
=====H↑+2OH-+Cl↑。
2 2
②10 m3的废气中CO 和CO总体积为10×103 L×8.96%=896 L,CO 和CO的体积均为448
2 2
L,两者的物质的量均为20 mol,CO 和CO全部转化成CHOH,CO ~6e-、CO~4e-,则
2 3 2
转移电子的总物质的量为200 mol;C H 生成C HCl ,C H ~2e-,则根据电子转移守恒可
2 4 2 4 2 2 4
知,生成C HCl 的物质的量为100 mol,质量为100 mol×99 g·mol-1=9 900 g=9.9 kg。
2 4 2
3.(2022·安徽马鞍山二中模拟)研究含氮元素物质的反应对生产、生活、科研等方面具有重
要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C HN)。
2 8 2
已知:①C HN(l)+4O(g)===2CO(g)+N(g)+4HO(l) ΔH=-2 765.0 kJ·mol-1
2 8 2 2 2 2 2 1
②2O(g)+N(g)===NO(l) ΔH=-19.5 kJ·mol-1
2 2 2 4 2
③HO(g)===HO(l) ΔH=-44.0 kJ·mol-1
2 2 3
则C HN(l)+2NO(l)===3N(g)+2CO(g)+4HO(g)的ΔH为__________。
2 8 2 2 4 2 2 2
(2)碘蒸气存在能大幅度提高NO的分解速率,反应历程为
2
第一步:I(g)―→2I(g)(快反应)
2
第二步:I(g)+NO(g)―→N(g)+IO(g)(慢反应)
2 2
第三步:IO(g)+NO(g)―→N(g)+O(g)+I(g)(快反应)
2 2 2实验表明,含碘时NO分解速率方程v=k·c(N O)·[c(I)]0.5(k为速率常数)。下列表述正确的
2 2 2
是________(填字母)。
A.NO分解反应中,k值与碘蒸气浓度大小有关
2
B.v(第二步的逆反应)<v(第三步反应)
C.IO为反应的催化剂
D.第二步活化能比第三步大
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装
置中CO和NO发生反应:2NO(g)+2CO(g)===N(g)+2CO(g) ΔH=-746.8 kJ·mol-1。实
2 2
验测得:v正 =k
正
·p2(NO)·p2(CO),v逆 =k
逆
·p(N
2
)·p2(CO
2
)。其中k
正
、k
逆
分别为正、逆反应速
率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k 增大的倍数__________(填“大于”“小于”或“等于”)k
正
增大的倍数。
逆
②一定温度下在刚性密闭容器中充入CO、NO和N 的物质的量之比为2∶2∶1,压强为
2
p。达平衡时压强为0.9p,则=__________。
0 0
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数K :
p
ⅰ.3N H(l)===4NH (g)+N(g) ΔH K
2 4 3 2 1 p1
ⅱ.4NH(g)===2N(g)+6H(g) ΔH K
3 2 2 2 p2
绘制pK -T和pK -T的线性关系如图所示(已知:pK =-lg K ):
p1 p2 p p
①由图可知,ΔH________(填“>”或“<”)0。
1
②反应 3NH(l)===3N(g)+6H(g)的 K =________(用 K 、K 表示 );该反应的
2 4 2 2 p1 p2
ΔH________( 填 “ > ” 或 “ < ” )0 , 写 出 推 理 过 程 :
__________________________________________
________________________________________________________________________。
答案 (1)-2 550.0 kJ·mol-1 (2)BD (3)①小于
② (4)①< ② K ·K < 设 T>T ,由图可知:pK (T)-pK (T)>∣pK (T)-
p1 p2 2 1 p1 2 p1 1 p2 2
pK (T)∣,则pK (T)-pK (T)>pK (T)-pK (T),pK (T)+pK (T)>pK (T)+pK (T),
p2 1 p1 2 p1 1 p2 1 p2 2 p1 2 p2 2 p1 1 p2 1
lg[K (T)·K (T)]>lg[K (T)·K (T)],即K(T)>K(T),因此该反应正反应为放热反应
p1 1 p2 1 p1 2 p2 2 1 2
解析 (1)由盖斯定律可知,①-2×②-4×③得反应:C HN(l)+2NO(l)===3N(g)+
2 8 2 2 4 2
2CO(g)+4HO(g) ΔH=ΔH -2ΔH -4ΔH =-2 550.0 kJ·mol-1。(2)k为速率常数,受温度、
2 2 1 2 3
催化剂、固体表面积性质等影响,不受浓度影响,A错误;平衡时v =v ,第二步反应为
正 逆
慢反应,反应速率较慢,则v(第二步的逆反应)也较慢,第三步反应为快反应,反应速率较快,故v(第二步的逆反应)<v(第三步反应),B正确;IO为中间过程产物,不是反应的催化
剂,C错误;活化能越大反应越慢,第二步反应为慢反应,第三步反应为快反应,故第二步
活化能比第三步大,D 正确。(3)① 达到平衡后,v =v 即 k ·p2(NO)·p2(CO)=k
正 逆 正
·p(N )·p2(CO),反应的平衡常数K ==,反应为放热反应,升高温度,平衡逆向移动,K
逆 2 2 p p
值减小,则仅升高温度,k 增大的倍数小于k 增大的倍数。②一定温度下在刚性密闭容器
正 逆
中充入CO、NO和N 的物质的量之比为2∶2∶1,设初始CO、NO和N 的物质的量分别为
2 2
2 mol、2 mol、1 mol,生成N 的物质的量为x mol,
2
2NO(g)+2CO(g)N(g)+2CO(g)
2 2
起始/mol 2 2 1 0
转化/mol 2x 2x x 2x
平衡/mol 2-2x 2-2x 1+x 2x
则反应后总物质的量为(5-x) mol,初始压强为p ,达平衡时压强为0.9p ,则=,x=0.5,
0 0
平衡时CO、NO、N、CO 的物质的量分别为1 mol、1 mol、1.5 mol、1 mol,总物质的量为
2 2
4.5 mol,则K ===。(4)①由图可知,K 随着温度的升高而减小,则平衡逆向移动,正反
p p1
应为放热反应,ΔH<0。②由盖斯定律可知,ⅰ+ⅱ得反应3NH(l)===3N(g)+6H(g),则
1 2 4 2 2
该反应的K=K ·K 。
p1 p2
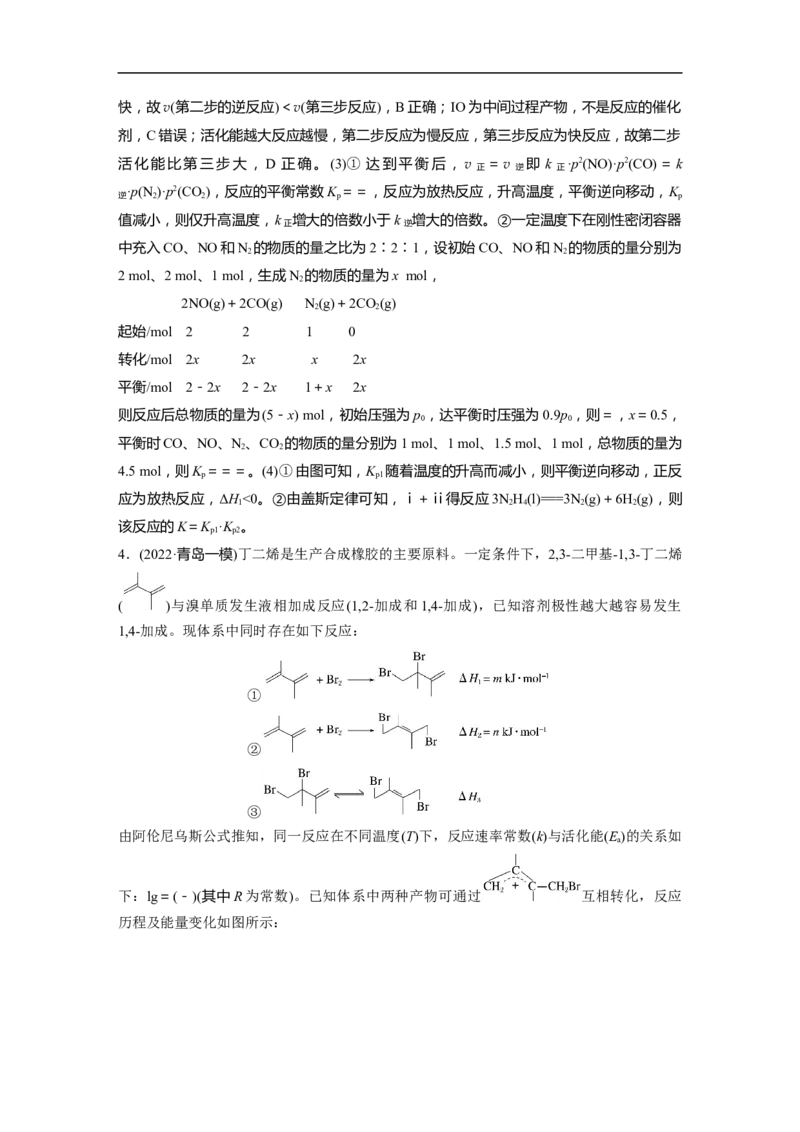
4.(2022·青岛一模)丁二烯是生产合成橡胶的主要原料。一定条件下,2,3-二甲基-1,3-丁二烯
( )与溴单质发生液相加成反应(1,2-加成和1,4-加成),已知溶剂极性越大越容易发生
1,4-加成。现体系中同时存在如下反应:
①
②
③
由阿伦尼乌斯公式推知,同一反应在不同温度(T)下,反应速率常数(k)与活化能(E)的关系如
a
下:lg=(-)(其中R为常数)。已知体系中两种产物可通过 互相转化,反应
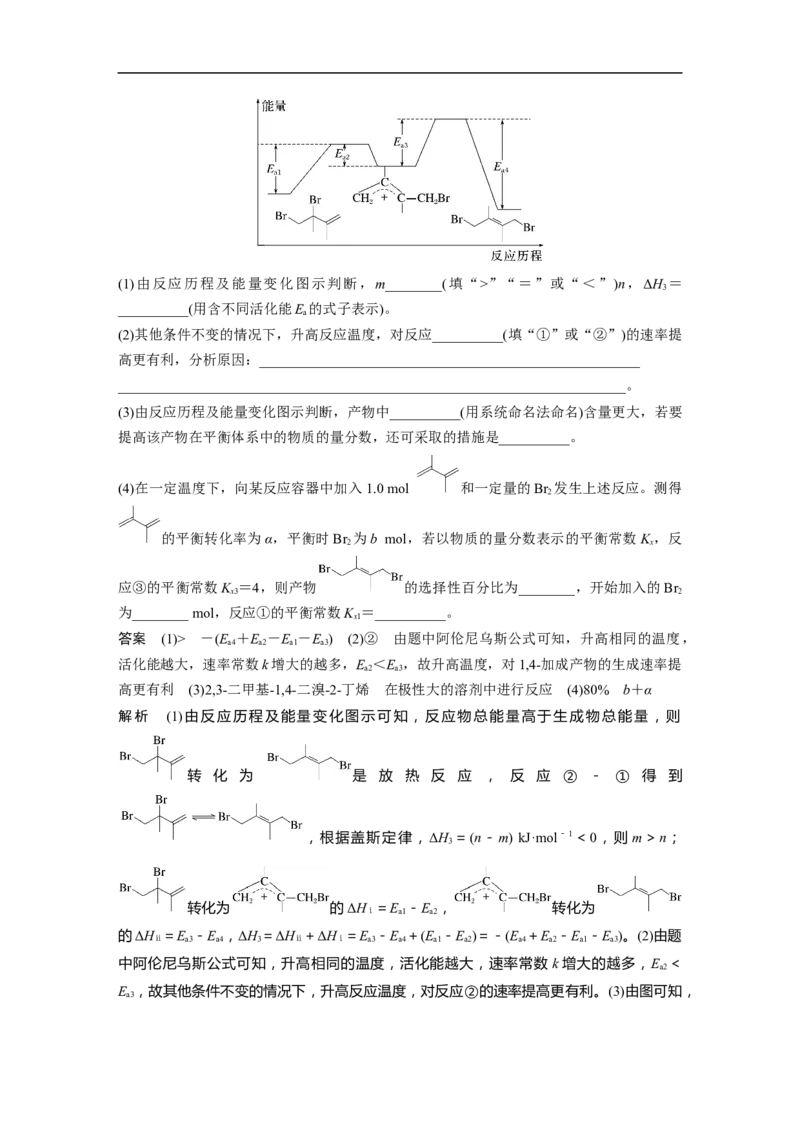
历程及能量变化如图所示:(1)由反应历程及能量变化图示判断,m________(填“>”“=”或“<”)n,ΔH =
3
__________(用含不同活化能E 的式子表示)。
a
(2)其他条件不变的情况下,升高反应温度,对反应__________(填“①”或“②”)的速率提
高更有利,分析原因:______________________________________________________
________________________________________________________________________。
(3)由反应历程及能量变化图示判断,产物中__________(用系统命名法命名)含量更大,若要
提高该产物在平衡体系中的物质的量分数,还可采取的措施是__________。
(4)在一定温度下,向某反应容器中加入1.0 mol 和一定量的Br 发生上述反应。测得
2
的平衡转化率为α,平衡时Br 为b mol,若以物质的量分数表示的平衡常数K,反
2 x
应③的平衡常数K =4,则产物 的选择性百分比为________,开始加入的Br
x3 2
为________ mol,反应①的平衡常数K =__________。
x1
答案 (1)> -(E +E -E -E ) (2)② 由题中阿伦尼乌斯公式可知,升高相同的温度,
a4 a2 a1 a3
活化能越大,速率常数k增大的越多,E <E ,故升高温度,对1,4-加成产物的生成速率提
a2 a3
高更有利 (3)2,3-二甲基-1,4-二溴-2-丁烯 在极性大的溶剂中进行反应 (4)80% b+α
解析 (1)由反应历程及能量变化图示可知,反应物总能量高于生成物总能量,则
转 化 为 是 放 热 反 应 , 反 应 ② - ① 得 到
,根据盖斯定律,ΔH =(n-m) kJ·mol-1<0,则 m>n;
3
转化为 的ΔH =E -E , 转化为
ⅰ a1 a2
的ΔH =E -E ,ΔH =ΔH +ΔH =E -E +(E -E )=-(E +E -E -E )。(2)由题
ⅱ a3 a4 3 ⅱ ⅰ a3 a4 a1 a2 a4 a2 a1 a3
中阿伦尼乌斯公式可知,升高相同的温度,活化能越大,速率常数 k增大的越多,E <
a2
E ,故其他条件不变的情况下,升高反应温度,对反应②的速率提高更有利。(3)由图可知,
a3的能量低于 , 较稳定,反应生成的 容易
转化为 ,则反应达平衡后,产物中 含量更大,主链含有4个C
原子,1、4号C原子上含有Br原子,2、3号C原子上含有甲基,2号C原子含有碳碳双键,
则该物质的名称为2,3-二甲基-1,4-二溴-2-丁烯;由题目中信息可知,溶剂极性越大越容易发
生1,4-加成,故若要提高该产物在平衡体系中的物质的量分数,还可采取的措施是在极性大
的溶剂中进行反应。(4)设反应生成x mol ,反应③的平衡常数K =4,则生成
x3
的物质的量为 4x mol,则产物 的选择性百分比为×100%=
80%;反应开始时,加入1.0 mol , 的平衡转化率为α,则消耗 的物质
的量为α mol,则消耗Br 的物质的量为α mol,平衡时Br 为b mol,故开始加入的Br 为(b
2 2 2
+α) mol;消耗 的物质的量为α mol,生成 和 的总物质的量
为α mol,产物 的选择性百分比为80%,则生成 的物质的量为(1-
80%)×α mol=0.2α mol,平衡时, 的物质的量为(1-α) mol,Br 为b mol,各物质
2
总物质的量为(1+b) mol,则反应①的平衡常数K ==。
x1
5.(2022·辽宁丹东一模)合成氨反应N(g)+3H(g)2NH (g)是目前最有效的工业固氮方法,
2 2 3
解决了数亿人口生存问题。
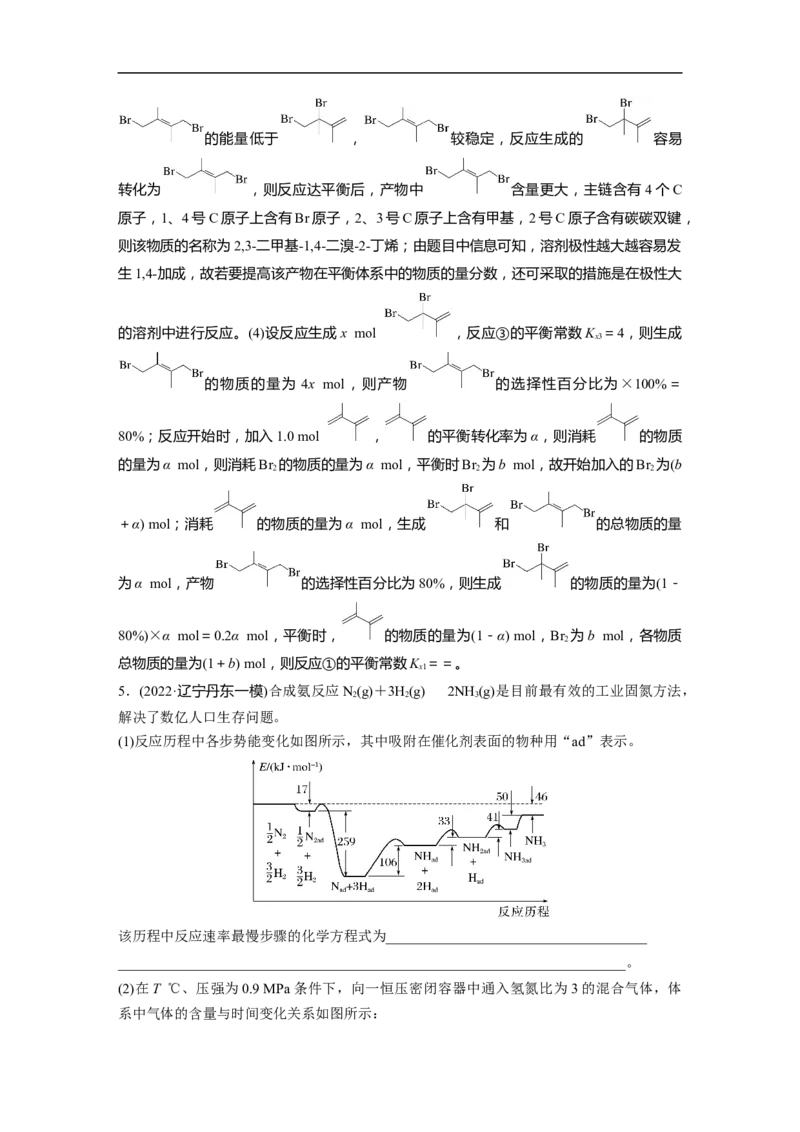
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用“ad”表示。
该历程中反应速率最慢步骤的化学方程式为_____________________________________
________________________________________________________________________。
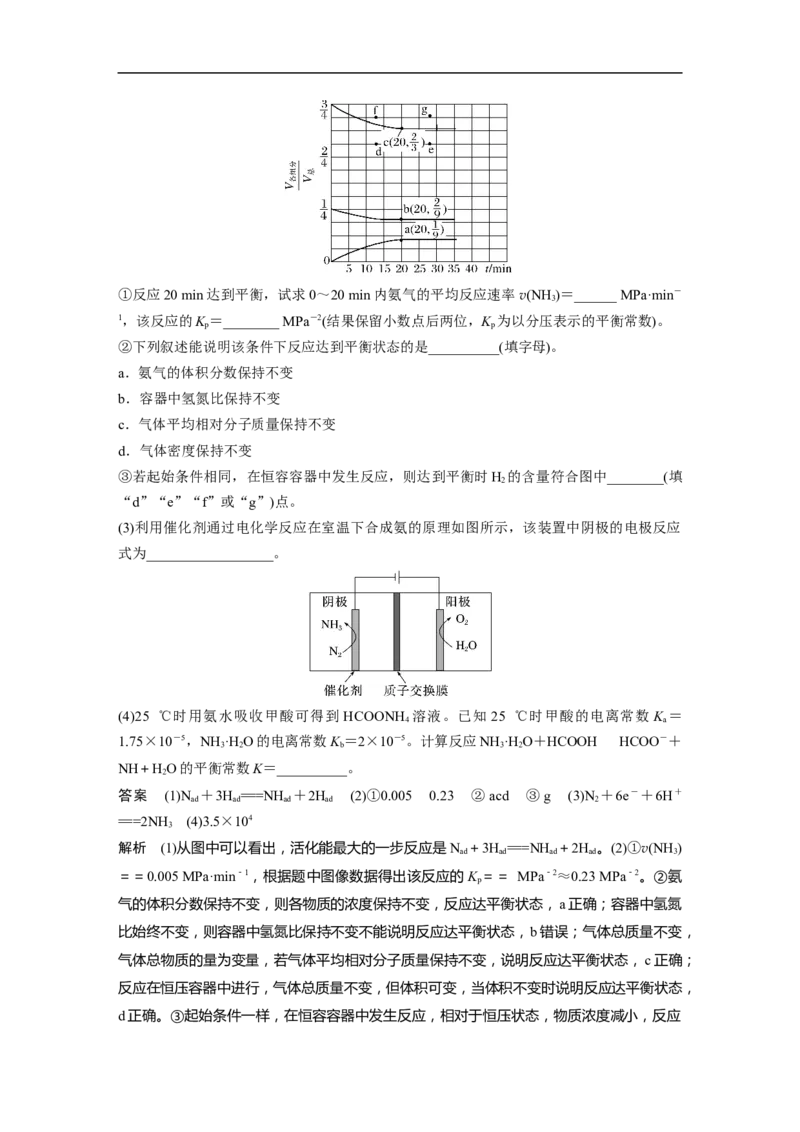
(2)在T ℃、压强为0.9 MPa条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体
系中气体的含量与时间变化关系如图所示:①反应20 min达到平衡,试求0~20 min内氨气的平均反应速率v(NH )=______ MPa·min-
3
1,该反应的K =________ MPa-2(结果保留小数点后两位,K 为以分压表示的平衡常数)。
p p
②下列叙述能说明该条件下反应达到平衡状态的是__________(填字母)。
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H 的含量符合图中________(填
2
“d”“e”“f”或“g”)点。
(3)利用催化剂通过电化学反应在室温下合成氨的原理如图所示,该装置中阴极的电极反应
式为__________________。
(4)25 ℃时用氨水吸收甲酸可得到 HCOONH 溶液。已知 25 ℃时甲酸的电离常数 K =
4 a
1.75×10-5,NH ·H O的电离常数K =2×10-5。计算反应NH ·H O+HCOOHHCOO-+
3 2 b 3 2
NH+HO的平衡常数K=__________。
2
答案 (1)N +3H ===NH +2H (2)①0.005 0.23 ② acd ③ g (3)N +6e-+6H+
ad ad ad ad 2
===2NH (4)3.5×104
3
解析 (1)从图中可以看出,活化能最大的一步反应是N +3H ===NH +2H 。(2)①v(NH )
ad ad ad ad 3
==0.005 MPa·min-1,根据题中图像数据得出该反应的K == MPa-2≈0.23 MPa-2。②氨
p
气的体积分数保持不变,则各物质的浓度保持不变,反应达平衡状态,a正确;容器中氢氮
比始终不变,则容器中氢氮比保持不变不能说明反应达平衡状态,b错误;气体总质量不变,
气体总物质的量为变量,若气体平均相对分子质量保持不变,说明反应达平衡状态,c正确;
反应在恒压容器中进行,气体总质量不变,但体积可变,当体积不变时说明反应达平衡状态,
d正确。③起始条件一样,在恒容容器中发生反应,相对于恒压状态,物质浓度减小,反应速率减慢,且恒容相当于减小压强,平衡逆向移动,H 的百分含量增大,所以g点符合要
2
求。(3)根据图中信息可知,阴极上氮气得电子生成氨气,电极反应式为 N +6e-+6H+
2
===2NH 。(4)反应 NH ·H O+HCOOHHCOO-+NH+HO 的平衡常数 K====
3 3 2 2
3.5×104。