文档内容
第四章 物质结构 元素周期律
第三节 化学键
第一课时 离子键
【学习目标】1.以氯化钠的形成过程为例,从微观角度分析宏观物质的形成过程,认识离子键的形
成,建立共价键的概念,初步建立化学键的概念,培养宏观辨识与微观探析的化学核心素养。
2.通过阅读思考,讨论交流,理解离子键的形成过程和形成条件,能用电子式对离子键进行表征,能
熟练地用电子式表示离子化合物的形成过程。
【学习重点】离子键、离子化合物的概念及判断;用电子式表示离子化合物及离子化合物的形成过
程。
【学习难点】用电子式表示离子化合物的形成过程。
【课前预习】
旧知回顾:1.写出钠原子结构示意图为 ,氯原子的原子结构示意图为 ,二者
均为 不稳定 结构,钠原子容易通过 失去 电子,将次外层变成 最外 层,形成最外层 8 电子稳定结
构,而氯原子容易 得到 电子,形成最外层 8 电子稳定结构。
2.金属Na常温下与氧气反应方程式 4Na + O == =2Na O ,在加热条件下与氧气反应方程式 2Na +
2 2
O ==== = N aO ,Na与Cl(在点燃条件下)反应的现象: 产生大量白烟 ,产物为 氯化钠 。化学方程式:
2 2 2 2
2Na + Cl ===== 2NaCl 。
2
新知预习:1.根据钠原子和氯原子的核外电子排布,钠原子要达到8电子的稳定结构,需 失去 1 个电
子;而氯原子要达到8电子稳定结构则需 得到 1 个电子。钠与氯气反应时,钠原子的最外电子层上的1个
电子转移到氯原子的 最外电子层 上,形成带 正电荷 的钠离子和带 负电荷 的氯离子。带相反电荷的
钠离子和氯离子,通过 静电作用 结合在一起,从而形成与单质钠和氯气性质完全不同的氯化钠。
2.离子键是 带相反电荷的离子之间的相互作用 , 含有离子键的化合物 叫离子化合物。常见含有离
子键的化合物有 强碱 :如 NaOH 、 KOH 、 Ba(OH ) 等、绝大多数 盐 :如 NaC l 、 KNO 、 NH Cl 等、
2 3 4
金属氧化物 :如 N a O 、 CaO 、 MgO 等。
2
【课中探究】
情景导入:由元素周期表可知,到目前为止,已经发现的元素有一百多种。然而,由这一百多种元素
的原子构成的物质已超过1亿种。那么,元素的原子之间通过什么作用形成如此丰富的物质呢?如氢分子
是由氢原子构成,要想使氢分子分解成氢原子需要加热到温度高达2000℃,它的分解率仍不到1%,说明
在氢分子里氢原子与氢原子之间存在强烈的相互作用,这种强烈的相互作用就是今天我们要学习的化学
键,化学键有多种类型,在此先讨论离子键。一、离子键
活动一、氯化钠的形成过程
任务一、思考交流:氧化还原反应的本质是什么?有哪些具体表现?
【答案要点】①氧化还原反应的本质是有电子的转移,包括电子得失和共用电子对偏移两个方面。
②如通过钠原子失去电子,氯原子得到电子形成NaCl;通过形成共用电子对,并偏向氯原子,偏离氢
原子形成HCl。
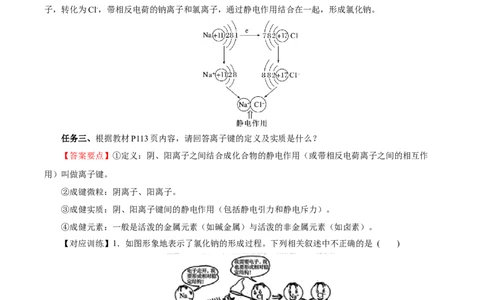
任务二、阅读教材P113页内容,观看钠原子与氯原子形成氯化钠的动画模拟,思考从微观角度如何
理解氯化钠的形成过程?
【答案要点】不稳定的钠原子失去最外层1个电子转化为Na+,不稳定的氯原子得到钠失去的一个电
子,转化为Cl-,带相反电荷的钠离子和氯离子,通过静电作用结合在一起,形成氯化钠。
任务三、根据教材P113页内容,请回答离子键的定义及实质是什么?
【答案要点】①定义:阴、阳离子之间结合成化合物的静电作用(或带相反电荷离子之间的相互作
用)叫做离子键。
②成键微粒:阴离子、阳离子。
③成健实质:阴、阳离子键间的静电作用(包括静电引力和静电斥力)。
④成健元素:一般是活泼的金属元素(如碱金属)与活泼的非金属元素(如卤素)。
【对应训练】1.如图形象地表示了氯化钠的形成过程。下列相关叙述中不正确的是 ( )
A.钠原子易失去一个电子,氯原子易得到一个电子
B.钠离子与钠原子有相似的化学性质
C.钠原子与氯原子作用生成NaCl后,其稳定性增强
D.构成氯化钠的粒子是钠离子和氯离子
【答案】B
【解析】钠原子最外层只有1个电子,当它失去1个电子后形成的Na+具有最外层8个电子的稳定结
构,氯原子最外层有7个电子,当它得到1个电子后形成的Cl-具有最外层8个电子的稳定结构,Na+和Cl-通过静电作用形成离子键,从而构成离子化合物NaCl。
2.下列说法不正确的是( )
A.凡金属元素跟非金属元素化合时都能形成离子键
B.原子间先通过得失电子变成阴阳离子后,阴阳离子间才能形成离子键
C.具有强得电子能力的原子与具有强失电子能力的原子相遇时能形成离子键
D.一般情况下,活泼金属(第Ⅰ A、Ⅱ A族金属)和活泼的非金属(第Ⅵ A、Ⅶ A族非金属)之
间化合时,易形成离子键
【答案】A
【解析】A.氯元素和铝元素化合时形成共价键,故A符合题意;B.原子间通过得失电子变成阴阳
离子后形成离子键,故B不符合题意;C.具有强得电子能力的原子与具有强失电子能力的原子相遇时,
能形成离子键,故C不符合题意;D.一般情况下,活泼金属(第Ⅰ A、Ⅱ A族金属)和活泼的非金属
(第Ⅵ A、Ⅶ A族非金属)它们之间化合时,都易形成离子键,例如氯化钠,故D不符合题意;故答案
为:A。
活动二、离子键的形成条件及存在
任务一、讨论交流:根据离子键的成键实质,思考离子键的形成条件是什么?
【答案要点】①活泼金属元素和活泼非金属元素,如ⅠA、ⅡA族的金属元素和ⅥA、ⅦA族的非金
属元素。如NaCl、MgCl 、KCl、NaO、MgO等。
2 2
②金属阳离子或NH +和某些带负电荷的原子和原子团。如NaOH、NaSO 、NH Cl等。
4 2 4 4
任务二、问题探究:形成离子键的原因是什么?从物质类别看离子键可能存在于哪些物质中?
【答案要点】①形成离子键的原因是原子间相互得失电子形成稳定的阴、阳离子,使体系的总能量降
低。
②离子键存在于强碱,如NaOH、KOH等;活泼金属氧化物,如NaO、KO、CaO、MgO等;绝大多
2 2
数盐类,如NaCl、NH Cl、BaSO 等。
4 4
注意:少部分盐例外。如AlCl 等。
3
【对应训练】1.下列叙述错误的是( )
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属元素原子间不可能形成离子键
【答案】D
【解析】A.带相反电荷离子之间的相互作用称为离子键,故A正确;B.金属元素与非金属元素化
合时,可能形成离子键或共价键,如NaCl为离子键,氯化铝为共价键,故B正确;C.某元素的原子最外
层只有一个电子,可能为H,跟卤素结合所形成的化学键为共价键,故C正确;D.非金属原子间可能形成离子键,如铵盐中存在离子键,故D错误;故选D。
2.下列说法正确的是( )
A.钠原子与氯原子反应生成食盐后,其结构的稳定性增强
B.阴、阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距离相当小
C.失电子难的原子获得电子的能力一定强
D.任何离子键在形成过程中必定有电子的得与失
【答案】A
【解析】 A.金属钠和非金属氯气反应生成离子化合物氯化钠后,各原子都变成8电子稳定结构的离
子,A项正确;B.在离子键中,既有阴、阳离子的相互吸引,又有电子与电子、原子核与原子核之间的排
斥作用,B项错误;C. 失电子难的原子获得电子的能力不一定强,如稀有气体原子既难失电子,又难得电
子,C项错误;D.在离子相交换过程中及在离子化合物从溶液中结晶过程中所形成的离子键,并没有电子
得失(如Ba2++SO2—=BaSO ↓),D项错误;答案选A。
4 4
二、离子化合物
活动一、离子化合物的概念及形成条件
任务一、阅读教材P113页6、6自然段,回答什么是离子化合物?
【答案要点】①由离子键构成的化合物叫做离子化合物,通常由活泼金属和活泼非金属或铵根离子和
酸根离子形成。如NaF、NaS、Al O、NaCO、NH Cl、NH Br 等化合物。
2 2 3 2 3 4 4
②判断方法:a.活泼金属阳离子和活泼非金属阴离子形成的化合物;
b.活泼金属阳离子和酸根离子形成的盐;
c.铵根离子和酸根离子(或活泼非金属阴离子)形成的盐。
任务二、拓展提升:结合氯化钠的性质,思考离子化合物在组成和性质上有哪些特点?
【答案要点】①在离子化合物里阳离子所带的正电荷总数等于阴离子所带的负电荷总数,整个化合物
呈电中性;
②多数离子化合物在固态(或晶态)时不能导电,而它的水溶液或熔化状态则能导电;
③离子化合物一般说来,熔点和沸点较高,硬度较大,质脆,难于压缩,难挥发;
④离子化合物由阴阳离子构成,阴阳离子之间通过离子键连接。如氯化钠中不存在单个的NaCl分
子,阴阳离子个数比是1:1,所以NaCl是表示离子个数比的化学式,而不是表示分子组成的分子式。
【对应训练】1.下列关于离子化合物的叙述正确的是( )
A.离子化合物中可能存在共价键 B.离子化合物中阳离子一定是金属离子
C.离子化合物的水溶液一定能导电 D.离子键在形成过程中一定有电子的得失
【答案】A
【解析】离子化合物中存在离子键也可能同时存在共价键,例如过氧化钠中含有离子键和共价键,A
正确;离子化合物中阳离子不一定是金属离子,例如氯化铵中的铵根离子,B错误;溶液导电的原因是存在自由移动的离子,离子化合物的水溶液不一定能导电,例如难溶性硫酸钡的溶液几乎不导电,C错误;
离子键是阴阳离子通过静电作用形成的,在形成过程中不涉及电子的得失,在离子形成的过程中涉及电子
得失,D错误。
2.下列关于离子键和离子化合物的说法正确的是 ( )
A.阴、阳离子间通过静电引力形成离子键
B.阴、阳离子间通过离子键一定能形成离子化合物
C.离子化合物都能导电,它们都是电解质杨sir化学,侵权必究
D.只有活泼金属元素和活泼非金属元素化合时,才能形成离子键
【答案】B
【解析】A.离子键是阴、阳离子间的静电引力与静电斥力,达到平衡时的一种静电作用,故错误;B.离
子化合物是阴、阳离子通过离子键而形成的化合物,故正确;C.离子化合物固态时不能导电,其水溶液或
熔融状态下能导电,都是电解质;D.非金属元素原子间可能形成离子键,如氯化铵中的铵根离子与氯离子
形成离子键,故错误。故选B。
活动二、电子式及书写方法
任务一、阅读教材P113页“资料卡片”,回答什么是电子式?原子、离子及离子化合物的电子式有
何特点?完成表格内容。
【答案要点】①定义:在元素符号的周围用“.”或“×”来表示原子的最外层电子(价电子)的式子叫电
子式。
②电子式的书写方法:
书写 先写出元素符号,再在元素符号的周围用“.”或“×”来表示原子的最外层电子
数,但应注意(a)一个“”或“”代表一个电子,原子的电子式中“”(或“”)的个
规则 数即原子的最外层电子数。(b)同一原子的电子式不能既用“”又用“”表示。
原子
示例
(1)简单阳离子是原子失去最外层电子后形成的,其电子式就是阳离子。
(2)简单阴离子得到电子后最外层一般为8电子结构,书写时要在元素符号周围
书写
标出电子,用“[ ]”括起来,并在右上角注明所带电荷数。
简单 规则
离子
注意:复杂的阳离子用“[ ]”加电荷数表示。如铵根离子 等。
示例 Na+ Mg2+ Al3+
离子 书写 离子化合物的电子式由阴、阳离子的电子式组成,相同的离子不合并,阴阳离子间
规则 隔排列,将阴阳离子(阳离子在前,阴离子在后.)拼在一起。
化合物 示例
任务二、观察教材P113页氯化钠形成观察的电子表示式,思考用电子式表示离子化合物的形成过程
要注意哪些问题?
【答案要点】①用电子式表示离子化合物的形成过程中不但要表示出离子化合物的电子式,还要同时
写成方程式的形式。
②反应物均用原子的电子式表示,而不是用分子式或分子的电子式表示,且反应物中相同原子可以合
并写。生成物是离子化合物的电子式,且化合物中相同原子必须分开写;
③反应物和生成物之间用箭头而不用等号表示,形成符合质量守恒定律;
④得失电子的原子之间要用弯箭头“ ”表示出电子转移的方向(可不用)。如、氯化钠、氯化镁
的形成过程:究
、 。
【对应训练】1.下列有关电子式的叙述正确的是 ( )
A.H、He、Li的电子式分别为H·、·He·、·Li
B.氯原子的电子式为 ,Cl-的电子式为
C.钠离子、镁离子、铝离子的电子式分别为Na+、Mg2+、Al3+
D.NaO的电子式为 ,HO的电子式为
2 2
【答案】C
【解析】A中锂原子的电子式应为 Li·;B中Cl-的电子式应为 ;D中HO的电子式应为
2
;金属阳离子的电子式与离子符号相同,C正确。
2.下列有关化学用语表示正确的是 ( )
A.中子数为10的氧原子: B.Mg2+的结构示意图:
C.硫化钠的电子式: D.HF的电子式:
【答案】B
【解析】中子数为10的氧原子,质量数为18,表示为 ,A错误;Mg2+的核电荷数为12,最外层电
子数为8,B正确;NaS为离子化合物,电子式为 C错误;HF为共价化合物,电子式为
2
D错误。【课后巩固】1.(易)下列关于离子键和离子化合物的说法正确的是( )
A.离子键是指带相反电荷的阴、阳离子之间的相互吸引作用
B.离子键只能在活泼金属和活泼非金属元素原子之间形成
C.离子键的作用仅仅局限于相邻的两个阴、阳离子之间
D.CaO、NaCl、NaOH中均存在离子键,都是离子化合物
【答案】D
【解析】A.离子键是指阴、阳离子之间的静电作用,包括引力和斥力,A错误;B.不是只有活泼的
金属元素和活泼的非金属元素之间才能形成离子键,如铵离子与氯离子也能形成离子键,B错误;C.离
子键的作用不仅局限于相邻的两个阴、阳离子之间,还存在于原子核和电子之间,C错误;D.CaO、
NaCl、NaOH都是由活泼金属阳离子与阴离子构成的,均存在离子键,都是离子化合物,D正确;故答案
为:D。
2.(易)关于离子化合物的下列说法正确的是 ( )
A.离子化合物一定能导电 B.能导电的物质一定是离子化合物
C.离子化合物的水溶液一定能导电 D.溶于水能导电的化合物一定是离子化合物
【答案】C
【解析】离子化合物需要产生自由移动的离子时才能导电,固体状态时并不导电,A错;能导电的物
质也可以是金属单质,B错;离子化合物在溶于水或熔化时均可以产生自由移动离子,均可以导电,C正
确;部分共价化合物溶于水也可以导电,D错误。
3.(中)下列说法正确的是 ( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl 中,两个氯离子之间存在共价键
2
D.含有离子键的化合物一定是离子化合物
【答案】D
【解析】离子键是使阴、阳离子结合成化合物的静电作用,要注意区别静电作用和静电引力,A项错
误;金属与非金属原子之间不一定形成离子键,B项错误;由CaCl 的电子式 可以
2
看出,CaCl 中只存在离子键,C项错误;含有离子键的化合物一定是离子化合物,D项正确。
2
4.(中)下列表示物质结构的化学用语正确的是 ( )
A.H、D、T表示同一种核素
B.MgCl 的形成过程:
2C.Cl-的结构示意图:
D.NH Cl的电子式:
4
【答案】B
【解析】H、D、T是同一种元素的三种核素,故A错误;氯离子是由氯原子得一个电子形成,核电荷
数仍为17,故氯离子的结构示意图为 ,故C错误;氯化铵为离子化合物,氯离子的最外层电子数必
须标出,氯化铵正确的电子式为 故D错误。
5.下列化学用语的书写,正确的是( )
A.氯原子的结构示意图:
B.6个质子8个中子的碳元素的核素符号:12C
C.氯化镁的电子式:
D.用电子式表示氯化氢的形成过程:
【答案】C
【解析】A.氯原子的结构示意图为 ,A错误;B.6个质子8个中子的碳元素的核素符号为
,B错误;C.氯化镁是含有离子键的离子化合物,电子式为 ,C正确;D.氯化氢是
含有极性键的共价化合物,则用电子式表示氯化氢的形成过程为 ,D错误;答
案选C。
6.(中)以下叙述中,错误的是 ( )
A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强
B.在氯化钠中,除氯离子和钠离子的静电吸引作用外,还存在电子与电子,原子核与原子核之间的
排斥作用
C.任何离子键在形成的过程中必定有电子的得与失D.钠与氯反应生成氯化钠后,体系能量降低
【答案】C
【解析】活泼的金属原子和活泼的非金属原子之间形成离子化合物,阴离子和阳离子均达到稳定结
构,这样体系的能量降低,其结构的稳定性增强,故A、D正确,B也正确。离子键的形成只是阴、阳离
子间的静电作用,并不一定发生电子的得失,如Na+与OH-结合成NaOH。
7.(难)X元素的原子最外层有7个电子,Y元素的原子与X元素的原子的次外层上都有8个电子,
X与Y形成的化合物中两离子的电子层结构相同,以下说法正确的是( )
A.两元素形成化合物的化学式一定为YX
B.两元素形成的化合物中一定存在离子键
C.两元素原子形成化合物后体系的能量明显升高
D.如果形成化合物的化学式为YX ,微粒之间不只含有离子键
2
【答案】B
【解析】由题意可知X为Cl元素,Y为K元素或Ca元素,可以形成KCl或CaCl ,微粒之间只存在
2
离子键,一旦形成化合物后体系的能量明显降低。
8.(中)设X、Y、Z代表三种元素。已知:
①X+和Y-两种离子具有相同的电子层结构;
②Z元素原子核内质子数比Y元素原子核内质子数少 9个;
③Y和Z两种元素可以形成四核42个电子的-1价阴离子。
据此,请填空:
(1)写出X、Y、Z三种元素的名称:X______,Y______,Z________。
(2)X 、 Y 两 种 元 素 最 高 价 氧 化 物 对 应 水 化 物 相 互 反 应 的 离 子 方 程 式 为
_____________________________。
(3) 用 电 子 式 表 示 X 、 Z 形 成 化 合 物 的 过 程 :
___________________________________________________。
【答案】 (1)钾 氯 氧 (2)H++OH-===H O
2
(3)