文档内容
五、物质结构与性质必备知识
1.1~36号元素原子的未成对电子数(m)
(1)m=1:ns1(4)、ns2np1(3)、ns2np5(3)、3d14s2(1)、3d104s1(1),共12 种。
(2)m=2:ns2np2(3)、ns2np4(3)、3d24s2(1)、3d84s2(1),共8 种
(3)m=3:ns2np3(3)、3d34s2(1)、3d74s2(1),共5 种。
(4)m=4:3d64s2(1),共1 种。
(5)m=5:3d54s2(1),共1 种。
(6)m=6:3d54s1(1),共1 种。
2.原子光谱
解释原子发光现象
①在××条件,基态电子吸收能量跃迁到激发态。
②由激发态跃迁回基态过程中,释放能量。
③释放的能量以××可见光的形式呈现。
3.根据电负性写水解方程式
(1)水解原理
①电负性大的原子显负价,结合水中的 H + 。
②电负性小的原子显正价,结合水中的 OH - 。
(2)实例
①IBr: IBr + H O == = HIO + HBr 。
2
②NCl :NCl + 3H O == = NH + 3HClO 。
3 3 2 3
4.键角大小的比较
(1)中心原子和配位原子均相同:中心原子上孤电子对越多,孤电子对对键角的压缩作用越
大,键角越小。
如键角:HO<HO+,NH<NH <[Zn(NH )]2+,CH>—CH>CH,NO>NO >NO。
2 3 3 3 6 3 2
(2)中心原子不同或配位原子不完全相同
①中心原子电负性大:中心原子的电负性越大,中心原子对键角的拉伸作用越大,键角越大。
如NH >PH ,HO>HS。
3 3 2 2
②配位原子电负性大:配位原子的电负性越大,配位原子对键角的压缩作用越大,键角越小。
如NF <NCl 。
3 3
5.氢键
(1)氢键的存在
①三种气态氢化物:HO、HF、NH 。
2 3
②含羟基物质:含氧酸、含氧酸的酸式盐、醇、酸、酚及它们的水溶液。
③含氨基物质:NH 、NH、DNA双螺旋体。
3 2 4(2)氢键的类型
①分子间氢键:
链状:如NH ·H O: 。
3 2
环状:分子中含多个N、O、F原子,如二聚乙酸: 。
②分子内氢键:含多个N、O、F原子,且为邻位关系,如邻硝基苯酚: 。
6.晶体的有关计算
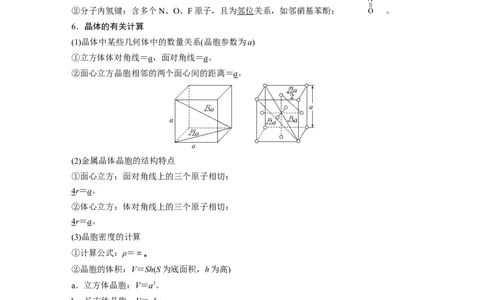
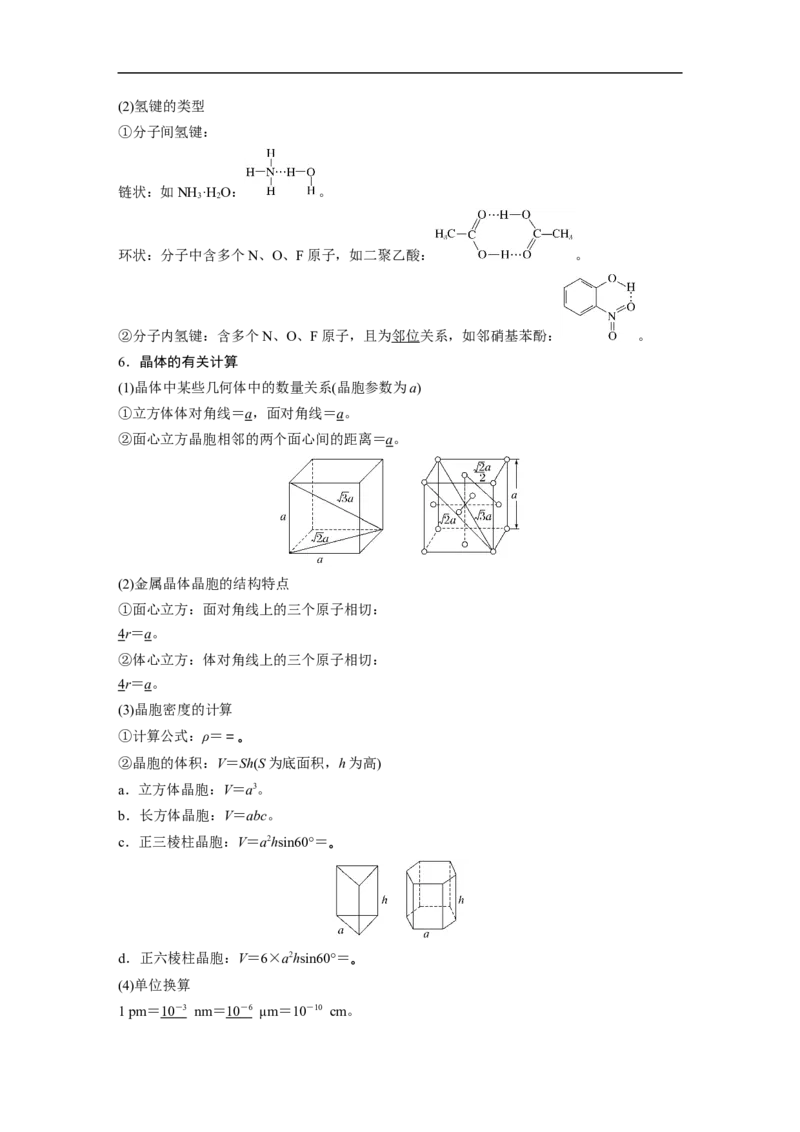
(1)晶体中某些几何体中的数量关系(晶胞参数为a)
①立方体体对角线=a,面对角线=a。
②面心立方晶胞相邻的两个面心间的距离=a。
(2)金属晶体晶胞的结构特点
①面心立方:面对角线上的三个原子相切:
4r=a。
②体心立方:体对角线上的三个原子相切:
4r=a。
(3)晶胞密度的计算
①计算公式:ρ==。
②晶胞的体积:V=Sh(S为底面积,h为高)
a.立方体晶胞:V=a3。
b.长方体晶胞:V=abc。
c.正三棱柱晶胞:V=a2hsin60°=。
d.正六棱柱晶胞:V=6×a2hsin60°=。
(4)单位换算
1 pm= 10 - 3 nm= 10 - 6 μm=10-10 cm。