文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题10
1.在甲、乙两烧杯溶液中,分别含有下列离子中的三种:Cu2+、Na+、H+、SO CO OH-。已
、 、
知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是
A.CO OH-、SO .Na+、H+、SO
、 B
C.Cu2+、H+、SO .Na+、OH-、CO
D
答案:D
解析:甲烧杯中溶液呈蓝色,一定含Cu2+,则和Cu2+不能共存的CO OH-在乙烧杯中,H+在
、
甲烧杯中,根据电荷守恒,甲烧杯中还含有、SO Na+,所以乙烧杯中大量存在的离子是
,乙烧杯中还含有
Na+、OH-、CO D。
,答案选
2.反应8NH +3Cl=N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比为
3 2 2 4 3 2
A.2∶3 B.8∶3 C.6∶3 D.3∶2
答案:A
解析:该氧化还原反应用双线桥表示为 ,可知实际升价的N原
子为2个,所以2个NH 被氧化,同时Cl 全部被还原,观察计量数,Cl 为3个,因而被氧化的
3 2 2
NH 与被还原的Cl 的物质的量之比为2:3。
3 2
3.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 使甲基橙试液变红的溶液:Al3+、Na+、NO Cl-
、
B. 通入足量SO 的溶液:Na+、NH、MnO SO
2 、
C. 通入足量NH 的溶液:K+、Cu2+、SO Cl-
3 、
D. 水电离的c(H+)=10-13mol·L-1的溶液:K+、Na+、Cr O、NO
2
答案:A
解析:A.使甲基橙试液变红的溶液为酸性溶液,酸性溶液中,Al3+、Na+、NO Cl-之间互不
、
反应,能大量共存,故A符合题意;
B. SO 具有还原性,能与MnO B不符合题意;
2 发生氧化还原反应,不能大量共存,故
C.通入足量NH 的溶液中:Cu2+会反应生成[Cu]NH )]2+,不能大量共存,故C不符合题意;
3 3 2
D.水电离的c(H+)=10-13mol·L-1的溶液可能呈酸性,也可能呈碱性,Cr O存在Cr O+HO
2 2 2
2CrO+2H+,当溶液呈碱性时,该平衡正向移动,主要以CrO形式存在,故D不符合题意;
4. “科学技术是第一生产力”,高科技的发展与化学密切相关。下列说法错误的是
A. CO 可人工合成葡萄糖和脂肪酸,葡萄糖属于单糖
2
B. 氘氚核聚变可实现“人造太阳”,氘和氚互为同位素
C. 利用全新原理可实现海水直接电解制氢,氢气是可再生能源
D. 涤纶纤维可制作飞船着陆器的降落伞,涤纶是无机非金属材料
答案:D解析:A.通过电催化将CO 高效还原合成高浓度乙酸,并进一步利用微生物发酵生产葡萄糖
2
和长链脂肪酸,葡萄糖属于单糖,故A正确;
B.氘氚核聚变可实现“人造太阳”,氘和氚互为同位素,故B正确;
C.利用全新原理可实现海水直接电解制氢,氢气燃烧后又生成水,氢气是可再生能源,故C
正确;
D.涤纶是有机高分子材料,故D错误;
5.室温下,下列各组离子在指定溶液中一定能大量共存的是
A. 在NH SCN溶液中:K+、Fe3+、Cl-、SO
4
B. 含大量H+的溶液中:Zn2+、Cu2+、NO SO
、
C. 加入Al产生H 的溶液中:Na+、Mg2+、NO HCO
2 、
D. 由水电离的c(OH-)=10-12mol·L-1的溶液中:K+、Ca2+、Cl-、ClO-
答案:B
解析:A.铁离子和SCN-离子生成红色物质,不共存,A不符合题意;
B.H+、Zn2+、Cu2+、NO SO B符合题意;
、 相互之间不反应,能共存,
C.加入Al产生H 的溶液为酸性或碱性,若为碱性溶液氢氧根离子会和镁离子、碳酸氢根离
2
子反应不共存;若为酸性氢离子会和HCO C不符合题意;
反应不共存,
D.由水电离的c(OH-)=10-12mol·L-1的溶液为酸性或碱性,酸性溶液中氢离子、氯离子、次
氯酸根离子会发生氧化还原反应生成氯气,不共存,D不符合题意;
6. 关于反应4Cu2++8OH-+NH=2Cu O↓+N↑+6HO,下列说法正确的是
2 4 2 2 2
A. N 是还原产物 B. 氧化剂与还原剂的物质的量之比为1∶4
2
C. NH 既是氧化剂又是还原剂 D. 生成28g N ,转移4mol电子
2 4 2
答案:D
解析:A. 分析方程式中的化合价可知,NH 中N元素的化合价为-2,N 中的N元素的化合价
2 4 2
为0,N元素的化合价升高,N 为氧化产物,故A错误;
2
B. 分析方程式中的化合价可知,Cu元素化合价降低,Cu2+为氧化剂,N元素化合价升高,
NH 为还原剂,氧化剂与还原剂的物质的量之比为4∶1,故B错误;
2 4
C. NH 中有且只有N元素化合价升高,所以NH 仅为还原剂,故C错误;
2 4 2 4
D. 分析方程式可知,每生成1mol N,转移的电子数为4mol,28g N ,正好为1mol N,故D
2 2 2
正确;
7.下列反应的离子方程式不正确的是
A. 少量的Cl 通入亚硫酸钠溶液:SO Cl+HO=SO 2Cl-+2H+
2 + 2 2 +
B. 惰性电极电解饱和硫酸锌溶液:2Zn2++2HO=====2Zn+4H++O↑
2 2
C. 浓硝酸与铜的反应:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
D. 用NaCO 溶液处理水垢中的CaSO:CaSO+CO CaCO +SO
2 3 4 4 3
答案:A
解析:A.亚硫酸钠溶液为碱性,少量的Cl 通入亚硫酸钠溶液发生反应生成硫酸钠和氯化钠,
2离子方程式为:SO Cl+2OH-=SO 2Cl-+HO,故A错误;
+ 2 + 2
B.饱和硫酸锌溶液呈碱性,惰性电极电解饱和硫酸锌溶液,Zn2+在阴极得到电子生成Zn,
HO在阳极失去电子生成O,电极方程式为:2Zn2++2HO=====2Zn+4H++O↑,故B正确;
2 2 2 2
C.浓硝酸与铜反应生成硝酸铜和二氧化氮,离子方程式为:Cu+4H++2NO Cu2++2NO ↑+
= 2
2HO,故C正确;
2
D.由于CaCO 的溶解度小于CaSO 的溶解度,用NaCO 溶液处理水垢中的CaSO,CaSO 会
3 4 2 3 4 4
转化为CaCO ,离子方程式为:CaSO+CO CaCO +SO,故D正确;
3 4 3
8.下列物质中属于难溶于水的碱性氧化物的是
A. SiO B. Fe O C. CuO D. Al O
2 3 4 2 3
答案:C
解析:A.SiO 是酸性氧化物,A不符合;
2
B.Fe O 虽然能与酸反应生成亚铁盐、铁盐和水,但不存在对应的碱,不属于碱性氧化物,B
3 4
不符合;
C.CuO难溶于水,与酸反应生成铜离子和水,属于碱性氧化物,C符合;
D.Al O 是两性氧化物,D不符合;
2 3
9.关于反应CHCHOH+Cr O+H++HO—→CHCOOH+Cr(HO)(未配平),下列说法不正确的
3 2 2 2 3 2
是
A. 生成1mol CHCOOH,转移6mol电子 B. CHCOOH是氧化产物
3 3
C. 该反应类型属于氧化还原反应 D. Cr(HO)的配体中形成配位键的原子是O
2
答案:A
解析:A.CHCHOH中C为-2价,CHCOOH中C为0价,有2个C原子发生变价,生成
3 2 3
1mol CHCOOH,转移4mol电子,故A错误;
3
B.碳元素化合价升高,CHCHOH是还原剂,CHCOOH是氧化产物,故B正确;
3 2 3
C.该反应中C、Cr元素化合价发生变化,属于氧化还原反应,故C正确;
D.HO中O原子提供孤对电子对与Cr3+提供空轨道形成配位键,故D正确;
2
10.下列反应的离子方程式的正确是
A. 磁铁矿溶于稀硝酸:3Fe2++4H++NO 3Fe3++NO↑+2HO
= 2
B. 将NaAlO 溶液与NaHCO 溶液混合:HCO +HO=Al(OH) ↓+CO
2 3 +AlO 2 3
C. 在亚硫酸中加入过量的次氯酸钠溶液:HSO +ClO-=Cl-+2H++SO
2 3
D. 往硫酸氢铵溶液滴加过量NaOH溶液:H++OH-=HO
2
答案:B
解析:A.磁铁的主要成分是四氧化三铁,硝酸可以把其中的二价铁氧化为三价铁,方程式为:
3Fe O+28H++NO 9Fe3++NO↑+14HO,A错误;
3 4 = 2
B.两者混合发生双水解反应,得到氢氧化铝沉淀和碳酸钠,离子方程式为:HCO +HO=
+AlO 2
Al(OH) ↓+CO
3 ,B正确;
C.亚硫酸有还原性,次氯酸钠有氧化性,两者发生氧化还原反应,但是次氯酸钠过量,最终会生成次氯酸,离子方程式为:HSO +3ClO-=Cl-+2HClO+SO,C错误;
2 3
D.硫酸氢铵溶液与过量氢氧化钠溶液反应生成硫酸钠、一水合氨和水,反应的离子方程式为:
NH+H++2OH-=NH ∙HO+HO,D错误;
3 2 2
11.铟(In)是制备酞菁铟、磷化铟等半导体的重要基础材料,广泛应用于军工、航天航空、平
面显示、光电信息、太阳能电池等领域。从铅锌冶炼烟灰(主要含InO、InS、ZnO、PbO、Fe O)
2 3 2 3 2 3
中提取金属铟的流程如图:
已知:氧化酸浸后铟以In3+的形式存在。“萃取”过程中的萃取剂可用HA 表示,其在酸性溶
2 2
液中可萃取三价金属离子。
回答下列问题:
(1)“氧化酸浸”过程中InS 的硫元素被氧化为SO,则氧化剂与还原剂的物质的量之比为
2 3
___________,滤渣除含过量MnO 外,还有___________(填化学式)。
2
(2)一个配体中有两个配位原子的配体叫双齿配体,C O就是一种双齿配体。“净化”时加入
2
HC O 的主要作用是络合Fe3+,Fe3+的配位数是6,则“净化”时的离子方程式是___________。
2 2 4
(3)萃取过程的反应方程式为:In3++3HA In(HA )+3H+,平衡常数为K。一定温度下萃取
2 2 2 3
率(E%)与c(H+)的关系如下:lg=lgK-lg。当pH=2.30时,萃取率为50%;若将萃取率提升到
95%,应调节溶液的pH=___________[已知lg19=1.28。忽略萃取剂浓度c(H A)在萃取过程中随
2 2
pH的变化。结果保留小数点后两位]。
(4)锌可以从___________中进行回收(填字母)。
a.滤渣 b.水相 c.有机相 d.滤液
(5)酞菁铟是有机分子酞菁与铟原子形成的复杂分子,结构简式如图所示,该分子中不存在的化
学键为___________(填字母)。
a.σ键 b.π键 c.离子键 d.配位键
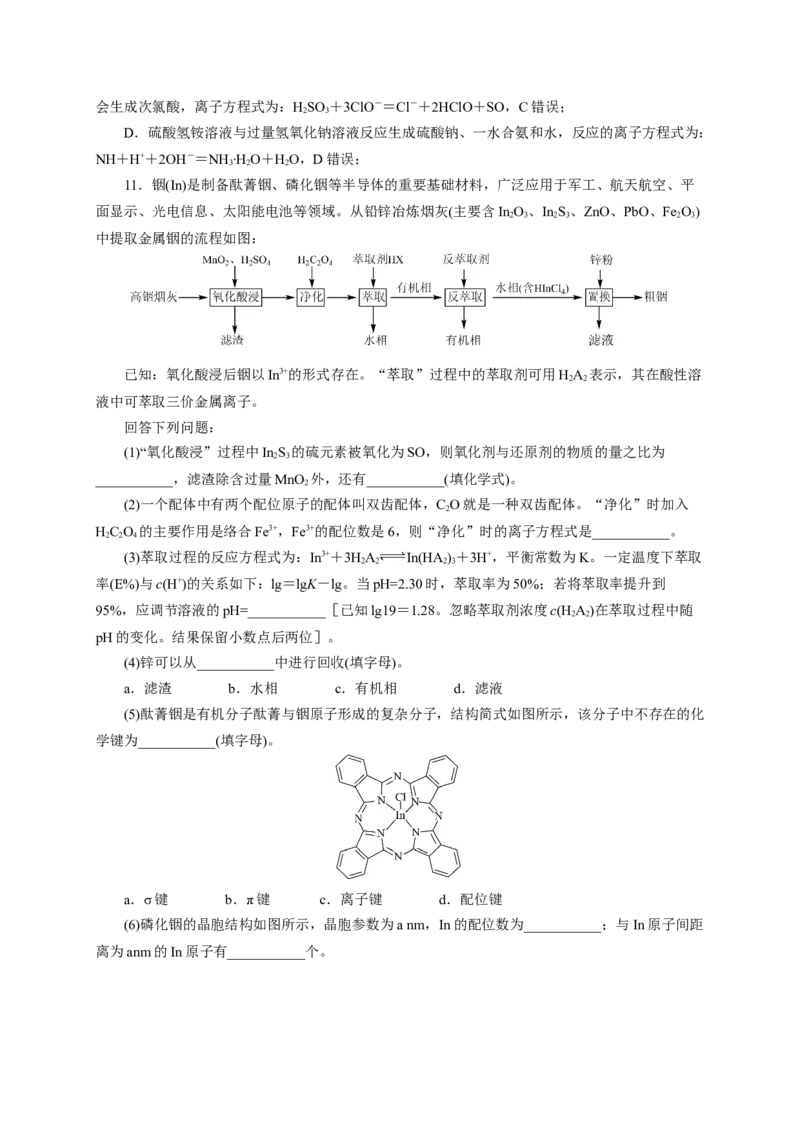
(6)磷化铟的晶胞结构如图所示,晶胞参数为a nm,In的配位数为___________;与In原子间距
离为anm的In原子有___________个。答案:(1) 12∶1 PbSO (2) Fe3++3HC O=[Fe(C O)]3-+6H+
4 2 2 4 2 4 3
(3)2.73 (4)b (5)c (6) 4 12
解析:高铟烟灰(主要含ZnO、PbO、Fe O、 InO、 InS),在高铟烟灰加入硫酸、二氧化锰
2 3 2 3 2 3
进行酸浸氧化,将InS 氧化为硫酸根离子和In3+, ZnO、PbO、Fe O 分别和硫酸反应转化为
2 3 2 3
ZnSO、PbSO 沉淀和Fe ( SO) ,InO 和硫酸反应变为In3+,则滤渣为硫酸铅;过滤,向滤液中
4 4 2 4 3 2 3
加入草酸,还原铁离子,防止加入萃取剂时,铁离子进入有机相;加入萃取剂萃取In3+,则Zn2+、
Fe2+均进入水相,经一系列操作得到粗铟,据此分析。
(1)氧化酸浸过程中MnO 只将InS 中的硫元素氧化为硫酸根离子,S的化合价由-2价变为+6价,
2 2 3
共失去24个电子, Mn的化合价由+4价变为+2价,得到2个电子,根据得失电子总数相等,则氧
化剂与还原剂的物质的量之比为24 : 2,滤渣除了过量的二氧化锰外还有硫酸铅。
(2)草酸根离子为双齿配体,铁离子的配位数为6,故形成的配位离子为[Fe(C O)]3-,该净化
2 4 3
的离子方程式为:Fe3++3HC O=[Fe(C O)]3-+6H+
2 2 4 2 4 3
(3) lg=lgK-lg。当pH=2.30时,萃取率为50%;则lg=lgK-lg lg=lgK-lg,得lgK=lg,若
将萃取率提升到95%,则lg=lgK-lg=lg19,将lgK代入,则有lg19=lg-lg=lg×=lg,
lgc(H+)=-2.73,则应调节溶液的pH=2.73。
(4)Zn2+、Fe2+均进入水相,故锌可以从水相中进行回收。
(5)In3+和氮原子之间存在配位键、共价键,单键为键,双键为一个σ键和一个π键,所以不含
c。
(6)磷周围有4个In原子形成正四面体结构,磷的配位数为4,晶胞中In为8×+6×=4,磷原子
数为4,磷原子和In个数相等,故In的配位数也为4,晶胞参数为a nm,与In原子间距离为anm
的In原子在晶胞面对角线上,每个顶点为8个晶胞共用,每个面为2个晶胞共用,则与In原子间
距离为anm的In原子数为3×8×=12
12.工业上以铬铁矿[主要成分为Fe(CrO ),含少量Al O、CuO杂质]为主要原料制备红矾钾
2 2 2 3
(K Cr O)的工艺流程如图所示:
2 2 7
请回答下列问题:(1)已知“高温连续焙烧”阶段Cr元素转化为CrO。
①焙烧时采取“多层逆流焙烧”,即将固体粉末从炉顶投料,氧气从炉底鼓入,这样做的优点
为__________________________________。
②Al O 与纯碱反应的化学方程式为________________________________________。
2 3
(2)滤液Ⅱ中发生反应的离子方程式为_______________________________________。
(3)一系列操作包括:50℃蒸发溶剂至_______,停止加热、_______抽滤、重结晶。
(4)生产过程中产生的KCr O 酸性废液可通过钡盐沉淀法处理,其过程为:先将KCr O 酸性
2 2 7 2 2 7
废液碱化处理,再加入BaCl 。废液需进行碱化处理的目的是_______[已知:BaCrO(s) Ba2+(aq)
2 4
+CrO(aq) K (BaCrO)=1.2×10-10 ]。
sp 4
(5)除了“一系列操作”中所得母液可循环利用外,上述流程中可循环利用的物质还有
NaHCO 、_______(填化学式)。
3
答案:(1)增大反应物接触面积,提高反应速率,从而提高原料的利用率
Al O+NaCO=====2NaAlO +CO↑
2 3 2 3 2 2
(2)2Na++2CrO+2CO+HO=Cr O+2NaHCO ↓
2 2 2 3
(3)有晶膜出现 冷却至室温
(4)促进Cr O转化为CrO,CrO浓度升高,有利于与Ba2+生成BaCrO 沉淀 (5)CO
2 4 2
解析:铬铁矿中加入NaCO、通入氧气,高温连续焙烧,Cr元素转化为CrO,Fe转化为
2 3
Fe O,Al O 与NaCO 反应生成NaAlO 同时生成二氧化碳,CuO不参与反应,水浸后Fe O、CuO
2 3 2 3 2 3 2 2 3
不溶于水生成沉淀过滤除去,滤液Ⅰ中含有NaAlO 和NaCrO,滤液Ⅰ通入CO 调节pH至8.3,此
2 2 4 2
时NaAlO 与CO、HO反应生成Al(OH) 沉淀除去,滤液Ⅱ中主要为NaCrO,往滤液Ⅱ中通入过
2 2 2 3 2 4
量CO,NaCrO 与CO 反应生成NaCr O 和NaHCO ,NaHCO 结晶析出,滤液Ⅲ中主要为
2 2 4 2 2 2 7 3 3
NaCr O,滤液Ⅲ中加入KCl,再经过一系列操作得到KCr O。
2 2 7 2 2 7
(1)①焙烧时固体粉末从炉顶投料,氧气从炉底鼓入,这样可以增大反应物的接触面积,提高
反应速率,从而提高原料的利用率。
②Al O 与纯碱反应生成NaAlO 和CO,化学方程式为Al O+NaCO=====2NaAlO +
2 3 2 2 2 3 2 3 2
CO↑。
2
(2)滤液Ⅱ中NaCrO 与CO、HO反应生成NaCr O 和NaHCO ,碳酸氢钠在水中溶解度较小
2 4 2 2 2 2 7 3
结晶析出,因此该反应的离子方程式为2Na++2CrO+2CO+HO=Cr O+2NaHCO ↓。
2 2 2 3
(3)从KCr O 溶液中得到KCr O 晶体,采用蒸发浓缩、冷却结晶,抽滤、重结晶的方式,
2 2 7 2 2 7
50℃蒸发溶剂至有晶膜出现,停止加热、冷却至室温,再抽滤重结晶得到KCr O 晶体。
2 2 7
(4)将KCr O 酸性废液碱化处理,促使Cr O+H O 2CrO+2H+化学平衡正向移动,可使Cr O
2 2 7 2 2 2
转化为CrO,CrO浓度升高,有利于与Ba2+反应生成BaCrO 沉淀。
4
(5)高温连续焙烧生成了CO,NaHCO 分解制NaCO 时也会生成CO,生成的CO 可用于与滤
2 3 2 3 2 2
液Ⅰ中偏铝酸钠反应,也可与滤液Ⅱ中CrO反应,因此上述流程中可循环利用的物质还有CO。
2