文档内容
平衡移动&图象作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 3,7 题为三星,1-2,4-6,8-20 为四星。
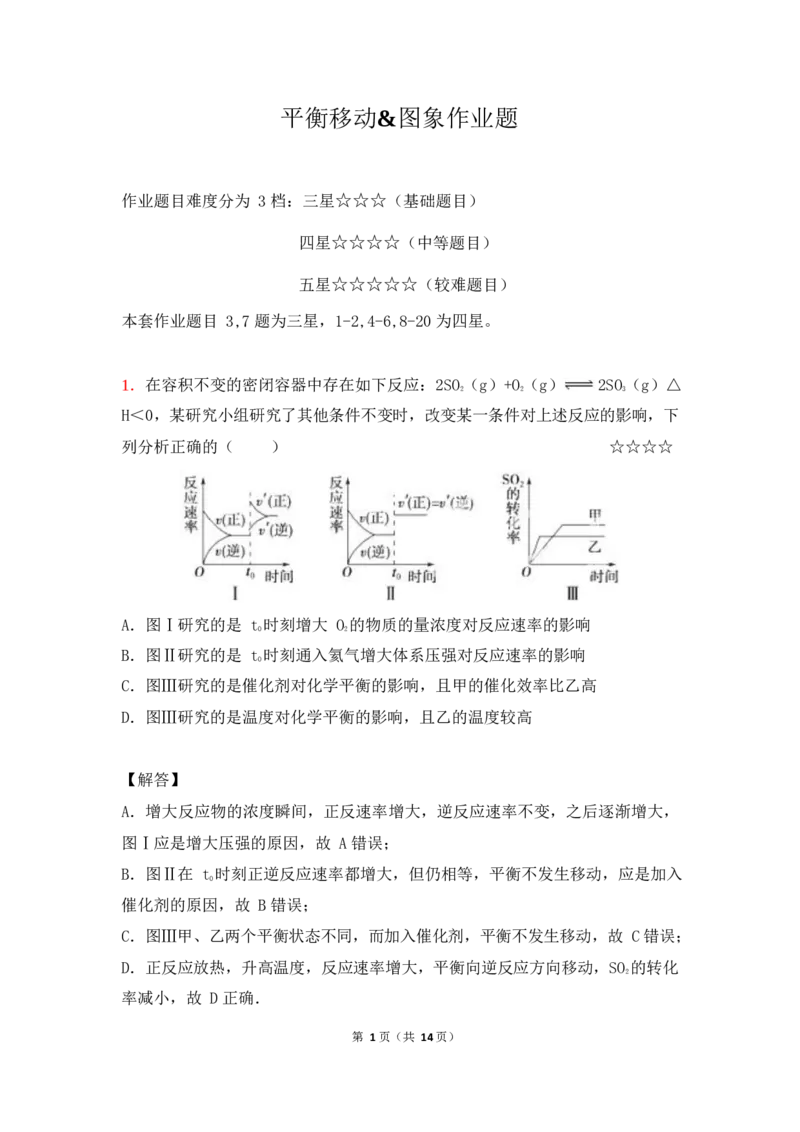
1.在容积不变的密闭容器中存在如下反应:2SO(g)+O(g) 2SO(g)△
2 2 3
H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下
列分析正确的( ) ☆☆☆☆
A.图Ⅰ研究的是 t 时刻增大 O 的物质的量浓度对反应速率的影响
0 2
B.图Ⅱ研究的是 t 时刻通入氦气增大体系压强对反应速率的影响
0
C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
【解答】
A.增大反应物的浓度瞬间,正反速率增大,逆反应速率不变,之后逐渐增大,
图Ⅰ应是增大压强的原因,故 A 错误;
B.图Ⅱ在 t 时刻正逆反应速率都增大,但仍相等,平衡不发生移动,应是加入
0
催化剂的原因,故 B 错误;
C.图Ⅲ甲、乙两个平衡状态不同,而加入催化剂,平衡不发生移动,故 C 错误;
D.正反应放热,升高温度,反应速率增大,平衡向逆反应方向移动,SO 的转化
2
率减小,故 D 正确.
第 1页(共 14页)故选:D.
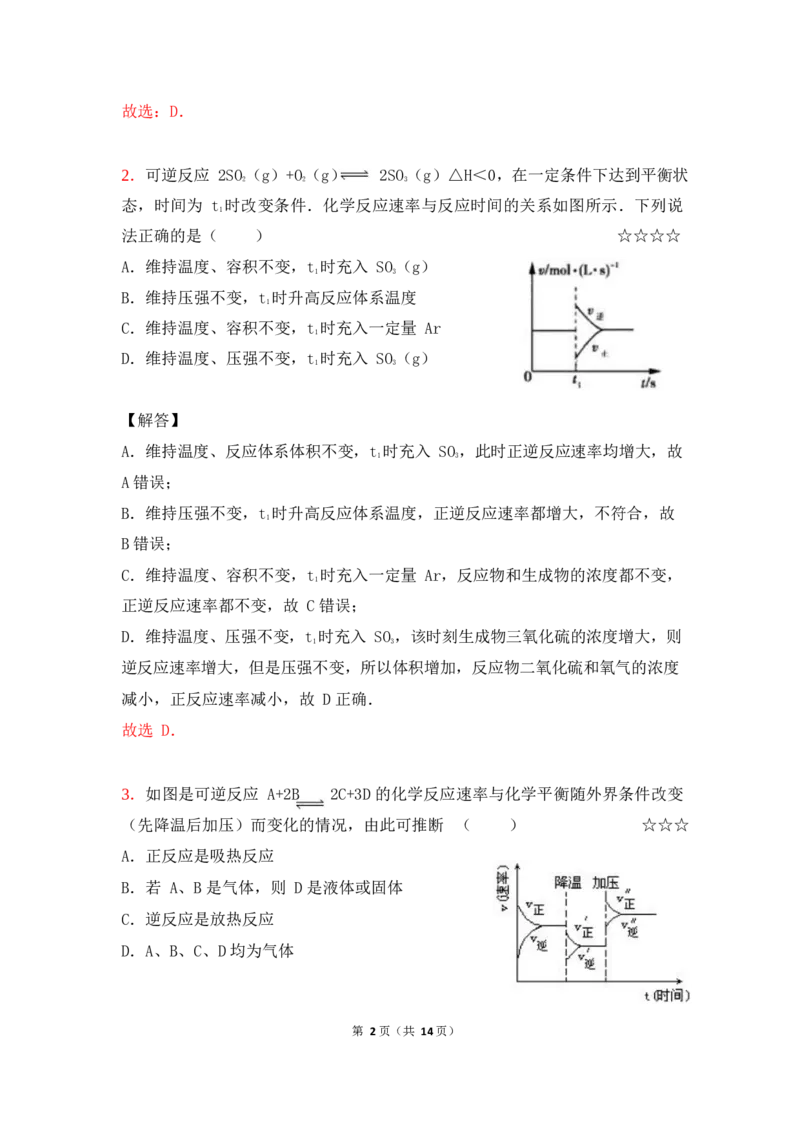
2.可逆反应 2SO(g)+O(g) 2SO(g)△H<0,在一定条件下达到平衡状
2 2 3
态,时间为 t 时改变条件.化学反应速率与反应时间的关系如图所示.下列说
1
法正确的是( ) ☆☆☆☆
A.维持温度、容积不变,t 时充入 SO(g)
1 3
B.维持压强不变,t 时升高反应体系温度
1
C.维持温度、容积不变,t 时充入一定量 Ar
1
D.维持温度、压强不变,t 时充入 SO(g)
1 3
【解答】
A.维持温度、反应体系体积不变,t 时充入 SO,此时正逆反应速率均增大,故
1 3
A 错误;
B.维持压强不变,t 时升高反应体系温度,正逆反应速率都增大,不符合,故
1
B 错误;
C.维持温度、容积不变,t 时充入一定量 Ar,反应物和生成物的浓度都不变,
1
正逆反应速率都不变,故 C 错误;
D.维持温度、压强不变,t 时充入 SO,该时刻生成物三氧化硫的浓度增大,则
1 3
逆反应速率增大,但是压强不变,所以体积增加,反应物二氧化硫和氧气的浓度
减小,正反应速率减小,故 D 正确.
故选 D.
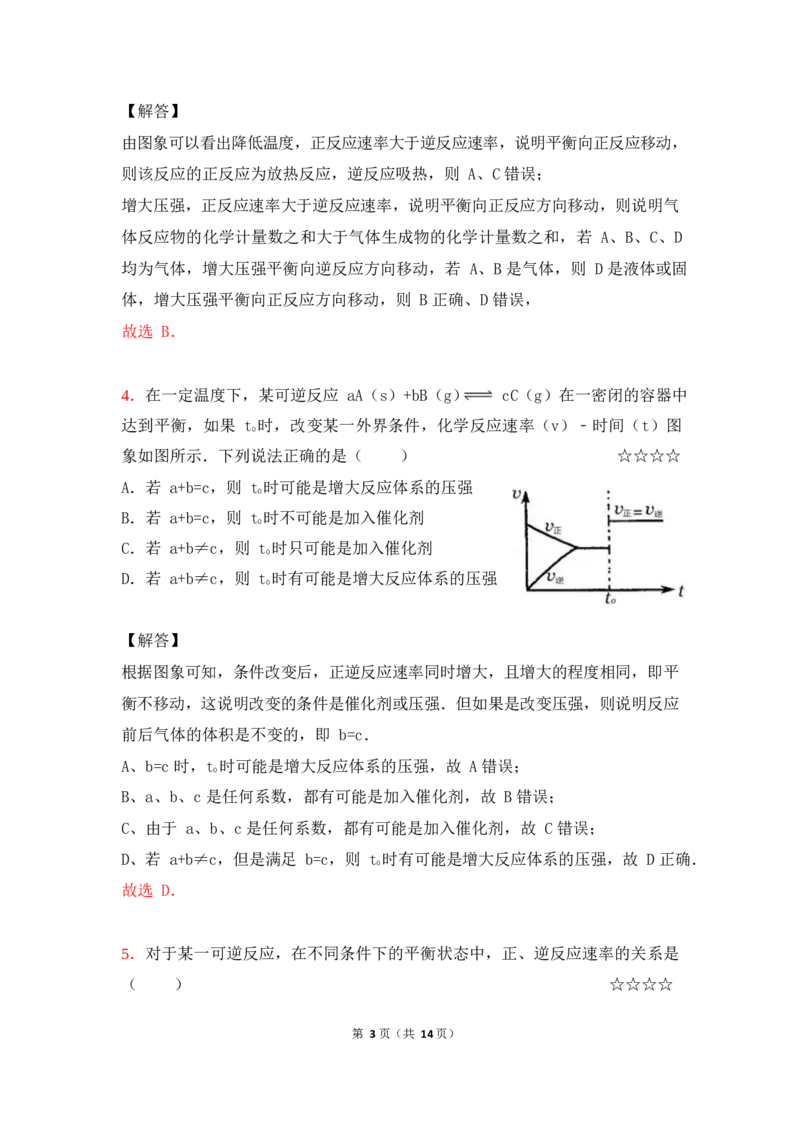
3.如图是可逆反应 A+2B 2C+3D 的化学反应速率与化学平衡随外界条件改变
(先降温后加压)而变化的情况,由此可推断 ( ) ☆☆☆
A.正反应是吸热反应
B.若 A、B 是气体,则 D 是液体或固体
C.逆反应是放热反应
D.A、B、C、D 均为气体
第 2页(共 14页)【解答】
由图象可以看出降低温度,正反应速率大于逆反应速率,说明平衡向正反应移动,
则该反应的正反应为放热反应,逆反应吸热,则 A、C 错误;
增大压强,正反应速率大于逆反应速率,说明平衡向正反应方向移动,则说明气
体反应物的化学计量数之和大于气体生成物的化学计量数之和,若 A、B、C、D
均为气体,增大压强平衡向逆反应方向移动,若 A、B 是气体,则 D 是液体或固
体,增大压强平衡向正反应方向移动,则 B 正确、D 错误,
故选 B.
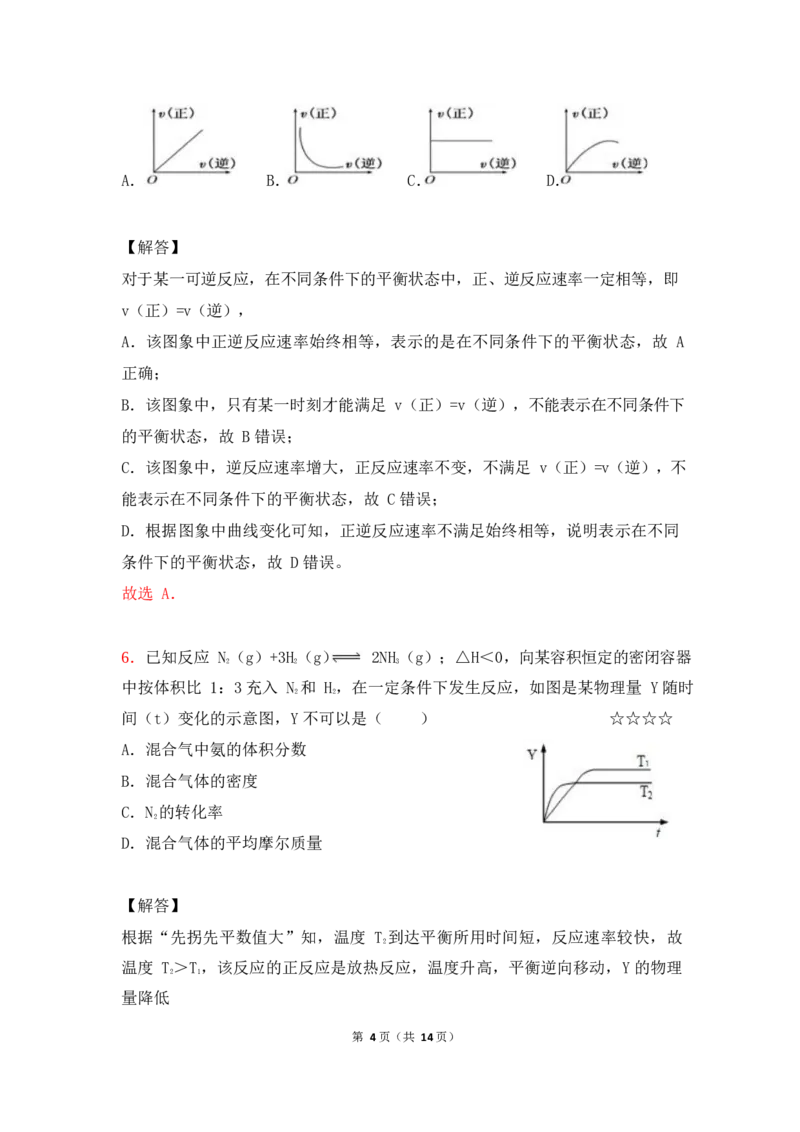
4.在一定温度下,某可逆反应 aA(s)+bB(g) cC(g)在一密闭的容器中
达到平衡,如果 t 时,改变某一外界条件,化学反应速率(v)﹣时间(t)图
0
象如图所示.下列说法正确的是( ) ☆☆☆☆
A.若 a+b=c,则 t 时可能是增大反应体系的压强
0
B.若 a+b=c,则 t 时不可能是加入催化剂
0
C.若 a+b≠c,则 t 时只可能是加入催化剂
0
D.若 a+b≠c,则 t 时有可能是增大反应体系的压强
0
【解答】
根据图象可知,条件改变后,正逆反应速率同时增大,且增大的程度相同,即平
衡不移动,这说明改变的条件是催化剂或压强.但如果是改变压强,则说明反应
前后气体的体积是不变的,即 b=c.
A、b=c 时,t 时可能是增大反应体系的压强,故 A 错误;
0
B、a、b、c 是任何系数,都有可能是加入催化剂,故 B 错误;
C、由于 a、b、c 是任何系数,都有可能是加入催化剂,故 C 错误;
D、若 a+b≠c,但是满足 b=c,则 t 时有可能是增大反应体系的压强,故 D 正确.
0
故选 D.
5.对于某一可逆反应,在不同条件下的平衡状态中,正、逆反应速率的关系是
( ) ☆☆☆☆
第 3页(共 14页)A. B. C. D.
【解答】
对于某一可逆反应,在不同条件下的平衡状态中,正、逆反应速率一定相等,即
v(正)=v(逆),
A.该图象中正逆反应速率始终相等,表示的是在不同条件下的平衡状态,故 A
正确;
B.该图象中,只有某一时刻才能满足 v(正)=v(逆),不能表示在不同条件下
的平衡状态,故 B 错误;
C.该图象中,逆反应速率增大,正反应速率不变,不满足 v(正)=v(逆),不
能表示在不同条件下的平衡状态,故 C 错误;
D.根据图象中曲线变化可知,正逆反应速率不满足始终相等,说明表示在不同
条件下的平衡状态,故 D 错误。
故选 A.
6.已知反应 N(g)+3H(g) 2NH(g);△H<0,向某容积恒定的密闭容器
2 2 3
中按体积比 1:3 充入 N 和 H,在一定条件下发生反应,如图是某物理量 Y 随时
2 2
间(t)变化的示意图,Y 不可以是( ) ☆☆☆☆
A.混合气中氨的体积分数
B.混合气体的密度
C.N 的转化率
2
D.混合气体的平均摩尔质量
【解答】
根据“先拐先平数值大”知,温度 T 到达平衡所用时间短,反应速率较快,故
2
温度 T>T,该反应的正反应是放热反应,温度升高,平衡逆向移动,Y 的物理
2 1
量降低
第 4页(共 14页)A.升高温度,平衡逆向移动,生成氨气的物质的量减小,则混合气体中氨气的
体积分数降低,符合图象,故 A 不选;
B.反应前后气体总质量不变、容器体积不变,则密度始终不变,与图象不符,
故 B 选;
C.升高温度,平衡逆向移动,则氮气的转化率降低,符合图象,故 C 不选;
D.升高温度,平衡逆向移动,平衡时混合气体物质的量增大,其平均摩尔质量
减小,符合图象,故 D 不选。
故选 B.
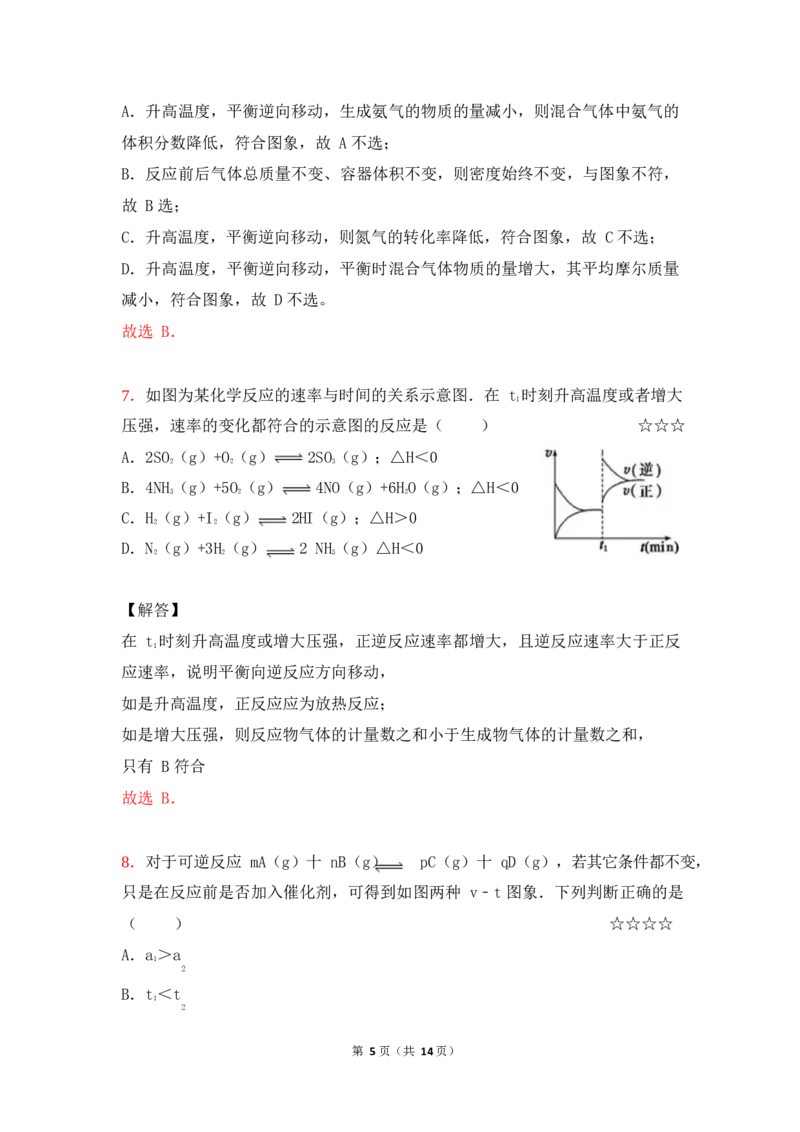
7.如图为某化学反应的速率与时间的关系示意图.在 t 时刻升高温度或者增大
1
压强,速率的变化都符合的示意图的反应是( ) ☆☆☆
A.2SO(g)+O(g) 2SO(g);△H<0
2 2 3
B.4NH(g)+5O(g) 4NO(g)+6HO(g);△H<0
3 2 2
C.H(g)+I(g) 2HI(g);△H>0
2 2
D.N(g)+3H(g) 2 NH(g)△H<0
2 2 3
【解答】
在 t 时刻升高温度或增大压强,正逆反应速率都增大,且逆反应速率大于正反
1
应速率,说明平衡向逆反应方向移动,
如是升高温度,正反应应为放热反应;
如是增大压强,则反应物气体的计量数之和小于生成物气体的计量数之和,
只有 B 符合
故选 B.
8.对于可逆反应 mA(g)十 nB(g) pC(g)十 qD(g),若其它条件都不变,
只是在反应前是否加入催化剂,可得到如图两种 v﹣t 图象.下列判断正确的是
( ) ☆☆☆☆
A.a>a
1
2
B.t<t
1
2
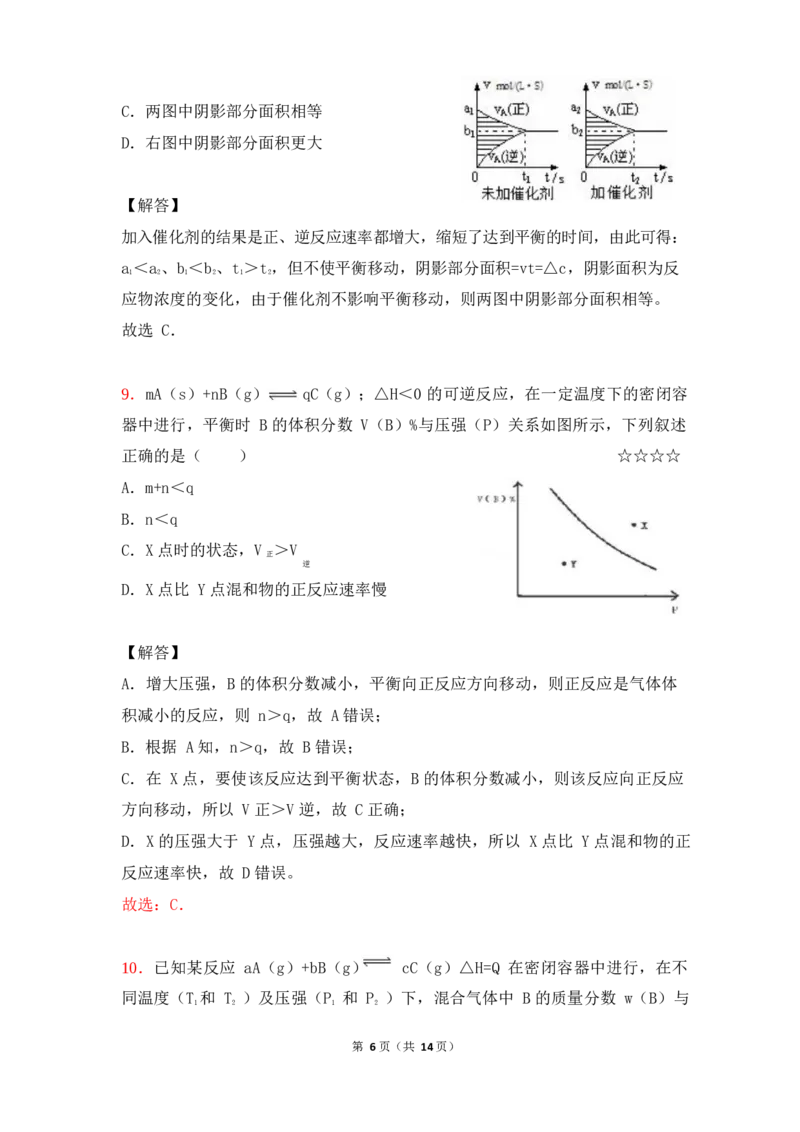
第 5页(共 14页)C.两图中阴影部分面积相等
D.右图中阴影部分面积更大
【解答】
加入催化剂的结果是正、逆反应速率都增大,缩短了达到平衡的时间,由此可得:
a<a、b<b、t>t,但不使平衡移动,阴影部分面积=vt=△c,阴影面积为反
1 2 1 2 1 2
应物浓度的变化,由于催化剂不影响平衡移动,则两图中阴影部分面积相等。
故选 C.
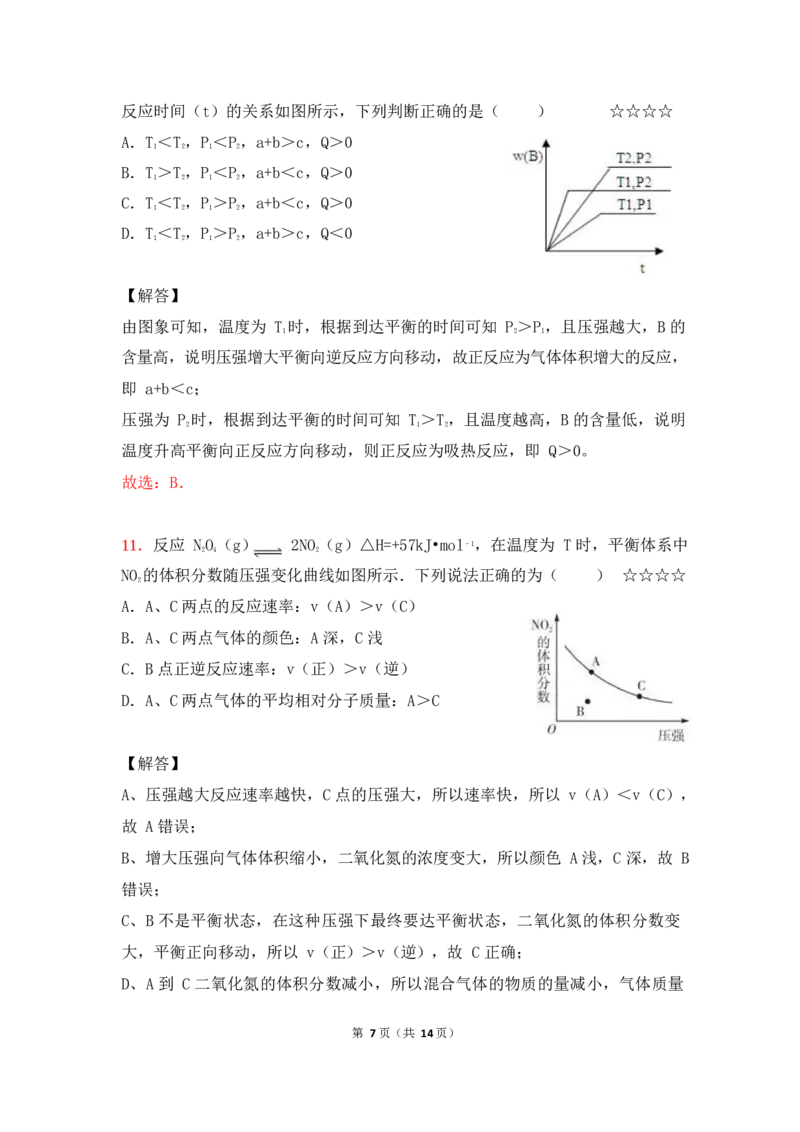
9.mA(s)+nB(g) qC(g);△H<0 的可逆反应,在一定温度下的密闭容
器中进行,平衡时 B 的体积分数 V(B)%与压强(P)关系如图所示,下列叙述
正确的是( ) ☆☆☆☆
A.m+n<q
B.n<q
C.X 点时的状态,V >V
正
逆
D.X 点比 Y 点混和物的正反应速率慢
【解答】
A.增大压强,B 的体积分数减小,平衡向正反应方向移动,则正反应是气体体
积减小的反应,则 n>q,故 A 错误;
B.根据 A 知,n>q,故 B 错误;
C.在 X 点,要使该反应达到平衡状态,B 的体积分数减小,则该反应向正反应
方向移动,所以 V 正>V 逆,故 C 正确;
D.X 的压强大于 Y 点,压强越大,反应速率越快,所以 X 点比 Y 点混和物的正
反应速率快,故 D 错误。
故选:C.
10.已知某反应 aA(g)+bB(g) cC(g)△H=Q 在密闭容器中进行,在不
同温度(T 和 T )及压强(P 和 P )下,混合气体中 B 的质量分数 w(B)与
1 2 1 2
第 6页(共 14页)反应时间(t)的关系如图所示,下列判断正确的是( ) ☆☆☆☆
A.T<T,P<P,a+b>c,Q>0
1 2 1 2
B.T>T,P<P,a+b<c,Q>0
1 2 1 2
C.T<T,P>P,a+b<c,Q>0
1 2 1 2
D.T<T,P>P,a+b>c,Q<0
1 2 1 2
【解答】
由图象可知,温度为 T 时,根据到达平衡的时间可知 P>P,且压强越大,B 的
1 2 1
含量高,说明压强增大平衡向逆反应方向移动,故正反应为气体体积增大的反应,
即 a+b<c;
压强为 P 时,根据到达平衡的时间可知 T>T,且温度越高,B 的含量低,说明
2 1 2
温度升高平衡向正反应方向移动,则正反应为吸热反应,即 Q>0。
故选:B.
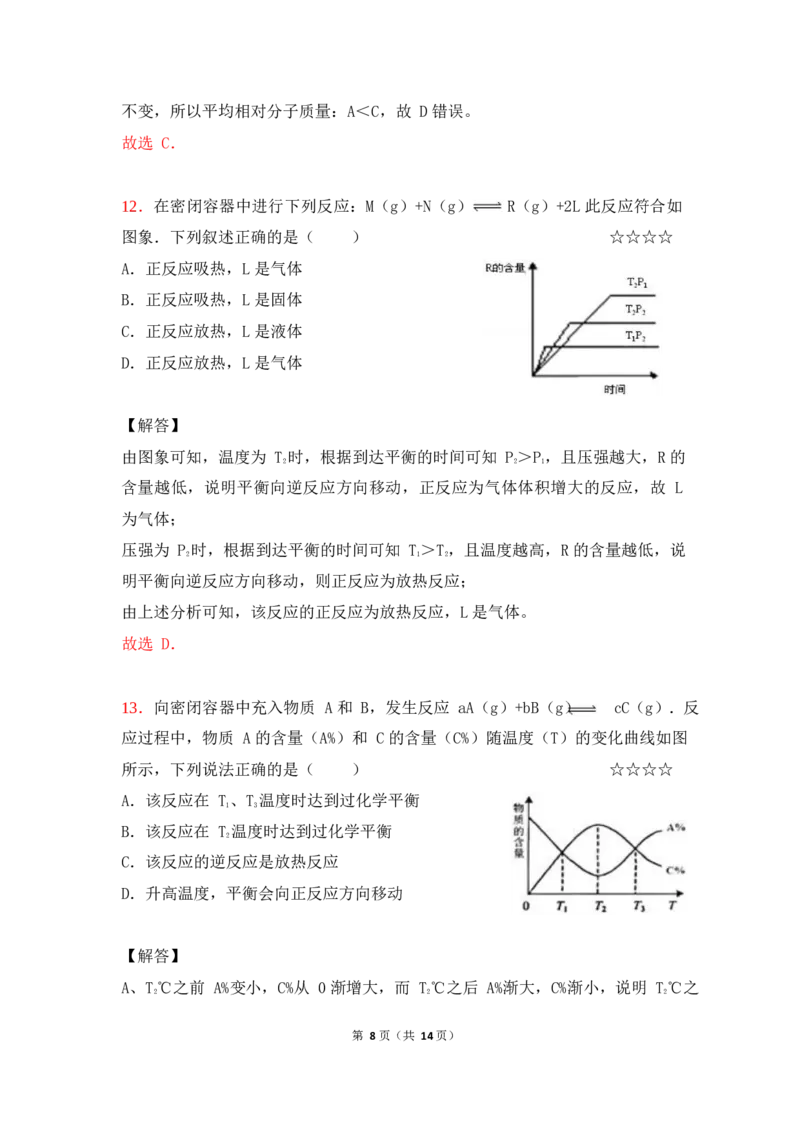
11.反应 NO(g) 2NO(g)△H=+57kJ•mol﹣1,在温度为 T 时,平衡体系中
2 4 2
NO 的体积分数随压强变化曲线如图所示.下列说法正确的为( ) ☆☆☆☆
2
A.A、C 两点的反应速率:v(A)>v(C)
B.A、C 两点气体的颜色:A 深,C 浅
C.B 点正逆反应速率:v(正)>v(逆)
D.A、C 两点气体的平均相对分子质量:A>C
【解答】
A、压强越大反应速率越快,C 点的压强大,所以速率快,所以 v(A)<v(C),
故 A 错误;
B、增大压强向气体体积缩小,二氧化氮的浓度变大,所以颜色 A 浅,C 深,故 B
错误;
C、B 不是平衡状态,在这种压强下最终要达平衡状态,二氧化氮的体积分数变
大,平衡正向移动,所以 v(正)>v(逆),故 C 正确;
D、A 到 C 二氧化氮的体积分数减小,所以混合气体的物质的量减小,气体质量
第 7页(共 14页)不变,所以平均相对分子质量:A<C,故 D 错误。
故选 C.
12.在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L 此反应符合如
图象.下列叙述正确的是( ) ☆☆☆☆
A.正反应吸热,L 是气体
B.正反应吸热,L 是固体
C.正反应放热,L 是液体
D.正反应放热,L 是气体
【解答】
由图象可知,温度为 T 时,根据到达平衡的时间可知 P>P,且压强越大,R 的
2 2 1
含量越低,说明平衡向逆反应方向移动,正反应为气体体积增大的反应,故 L
为气体;
压强为 P 时,根据到达平衡的时间可知 T>T,且温度越高,R 的含量越低,说
2 1 2
明平衡向逆反应方向移动,则正反应为放热反应;
由上述分析可知,该反应的正反应为放热反应,L 是气体。
故选 D.
13.向密闭容器中充入物质 A 和 B,发生反应 aA(g)+bB(g) cC(g).反
应过程中,物质 A 的含量(A%)和 C 的含量(C%)随温度(T)的变化曲线如图
所示,下列说法正确的是( ) ☆☆☆☆
A.该反应在 T、T 温度时达到过化学平衡
1 3
B.该反应在 T 温度时达到过化学平衡
2
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
【解答】
A、T℃之前 A%变小,C%从 0 渐增大,而 T℃之后 A%渐大,C%渐小,说明 T℃之
2 2 2
第 8页(共 14页)前是反应没有达到平衡状态,而 T℃时恰好平衡,T℃之后是温度升高使平衡向
2 2
左移动,所以 T 温度时未达到化学平衡,T 达到化学平衡,故 A 错误;
1 3
B、T℃之前 A%变小,C%从 0 渐增大,而 T℃之后 A%渐大,C%渐小,说明 T℃之
2 2 2
前是反应没有达到平衡状态,故 B 正确;
C、T℃时恰好平衡,T℃之后 A%渐大,C%渐小,说明 T℃之后是温度升高使平
2 2 2
衡向左移动,所以逆反应是吸热反应,故 C 错误;
D、T℃时恰好平衡,T℃之后 A%渐大,C%渐小,说明 T℃之后是温度升高使平
2 2 2
衡向逆反应移动,故 D 错误。
故选 B.
14.在容积不变的密闭容器中存在如下可逆反应 aA(g)+bB(g) cC(g)
+dD(s)△H=Q kJ•mol﹣1,反应过程中,当其他条件不变时,某物质在混合物中
的含量与温度(T)、反应速率(v)与压强的关系如图所示.据图分析,以下说
法正确的是( ) ☆☆☆☆
A.T<T,Q>0
1 2
B.增大压强,B 的转化率减小
C.当混合气体的密度不再变化,反应达平衡状态
D.a+b<c+d
【解答】
A.根据“先拐先平数值大”知,T<T,升高温度平衡向吸热方向移动,升高温
1 2
度产物含量减小,说明平衡逆向移动,则正反应是放热反应,Q<0,故 A 错误;
B.增大压强正逆反应速率都增大,但正反应速率大于逆反应速率,平衡正向移
动,B 的转化率增大,故 B 错误;
C.反应前后气体总质量减小,容器体积不变,则密度减小,但容器内气体密度
不变时正逆反应速率相等,反应达到平衡状态,故 C 正确;
D.增大压强平衡向气体体积减小的方向移动,增大压强平衡正向移动,则 a+b
>c,故 D 错误。
故选 C.
第 9页(共 14页)15.下列图象能正确地表达可逆反应 3A(g)+B(g) 2C(g)△H<0 的是( )
☆☆☆☆
A. B.
C. D.
【解答】
对于可逆反应 3A(g)+B(g) 2C(g)△H<0,反应放热,升高温度,正、逆
⇌
反应速率都增大,逆反应速率增大更多,平衡向逆反应方向移动,则 C%降低,
A%增大,A 的转化率降低.反应物的化学计量数之和大于生成物的化学计量数之
和,增大压强,平衡向正反应方向移动,则 C%增大,A%降低,A 的转化率增大,
A、由图象可知,温度升高 C%增大,说明升高温度平衡向正反应移动,图象与实
际不相符,故 A 错误;
B、由图象可知,温度升高,正反应速率增大比逆反应速率增大更多,平衡向正
反应移动,图象与实际不相符,故 B 错误;
C、由图象可知,压强越大 A%降低,平衡向正反应移动,升高温度 A%降低,平衡
向正反应移动,图象与实际不相符,故 C 错误;
D、由图象可知,压强越大 A 转化率增大,平衡向正反应移动,升高温度 A 的转
化率降低,平衡向逆反应移动,图象与实际相符,故 D 正确。
故选 D.
16.在容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g);△H
<0.某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并
根据实验数据作出下列关系图,下列判断一定错误的是( ) ☆☆☆☆
第 10页(共 14页)A.图 I 研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且乙的压强较高
C.图Ⅲ研究的是温度对反应的影响,且甲的温度较高
D.图 IV 研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
【解答】
A.加入催化剂,平衡不发生移动,甲到达平衡时间短,所以甲使用的催化剂效
率较高,乙使用的催化剂效率较较低,故 A 错误;
B.甲到达平衡时间长,所以甲的压强较低,乙的压强较高,故 B 正确;
C.甲到达平衡时间短,所以甲的温度较高,正反应放热,升高温度,平衡向逆
反应方向移动,所以 B 的转化率减小,故 C 正确;
D.加入催化剂,平衡不发生移动,甲到达平衡时间短,所以甲使用的催化剂效
率较高,故 D 正确。
故选 A.
17.可逆反应 mA(固)+nB(气) pC(气)+qD(气)反应过程中其他条件
不变时 C 的百分含量 C%与温度(T)和压强(P)的关系如图所示,下列叙述中
正确的是( ) ☆☆☆☆
A.达到平衡后,使用催化剂,C%将增大
B.达到平衡后,若升高温度,化学平衡向逆反应方向移动
C.方程式中 n>p+q
D.达到平衡后,增加 A 的量有利于化学平衡向正反应方向移动
【解答】
可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间
第 11页(共 14页)越短.由图象(1)可知 T>T,温度越高,平衡时 C 的体积分数φ(C)越小,
1 2
故此反应的正反应为放热反应;
当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图
(2)可知 p>p,压强越大,平衡时 C 的体积分数φ(C)越小,可知正反应为
2 1
气体物质的量增大的反应,即 n<P+q.
A、催化剂只改变化学反应速率,对平衡移动没有影响,C 的质量分数不变,故 A
错误;
B、由上述分析可知,可逆反应 mA(固)+nB(气)
⇌
Pc (气)+qD(气)正反
应为放热反应,升高温度平衡向吸热方向移动,即向逆反应移动,故 B 正确;
C、由上述分析可知,可逆反应 mA(固)+nB(气)
⇌
Pc (气)+qD(气)正反
应为气体物质的量增大的反应,即 n<P+q,故 C 错误;
D、A 为固体,浓度为定值,达平衡后,增加 A 的量,平衡不移动,故 D 错误。
故选 B.
18.在一定温度不同压强(P<P)下,可逆反应 2X(g) 2Y(g)+Z(g)
1 2
中,生成物 Z 在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下
图示,正确的是( ) ☆☆☆☆
A. B.
C. D.
【解答】
A、图象中压强 p 到达平衡时间短,故图象中 p>p,与题意不符,故 A 错误;
1 1 2
B、图象中压强 p 到达平衡时间短,图象中 p<p,增大压强,平衡时生成物 Z
2 1 2
第 12页(共 14页)的物质的量减小,与实际相符,故 B 正确;
C、图象中压强 p 到达平衡时间短,故图象中 p>p,与题意不符,故 C 错误;
1 1 2
D、图象中压强 p 到达平衡时间短,图象中 p<p,增大压强,平衡时生成物 Z
2 1 2
的物质的量增大,与实际不相符,故 D 错误。
故选 B.
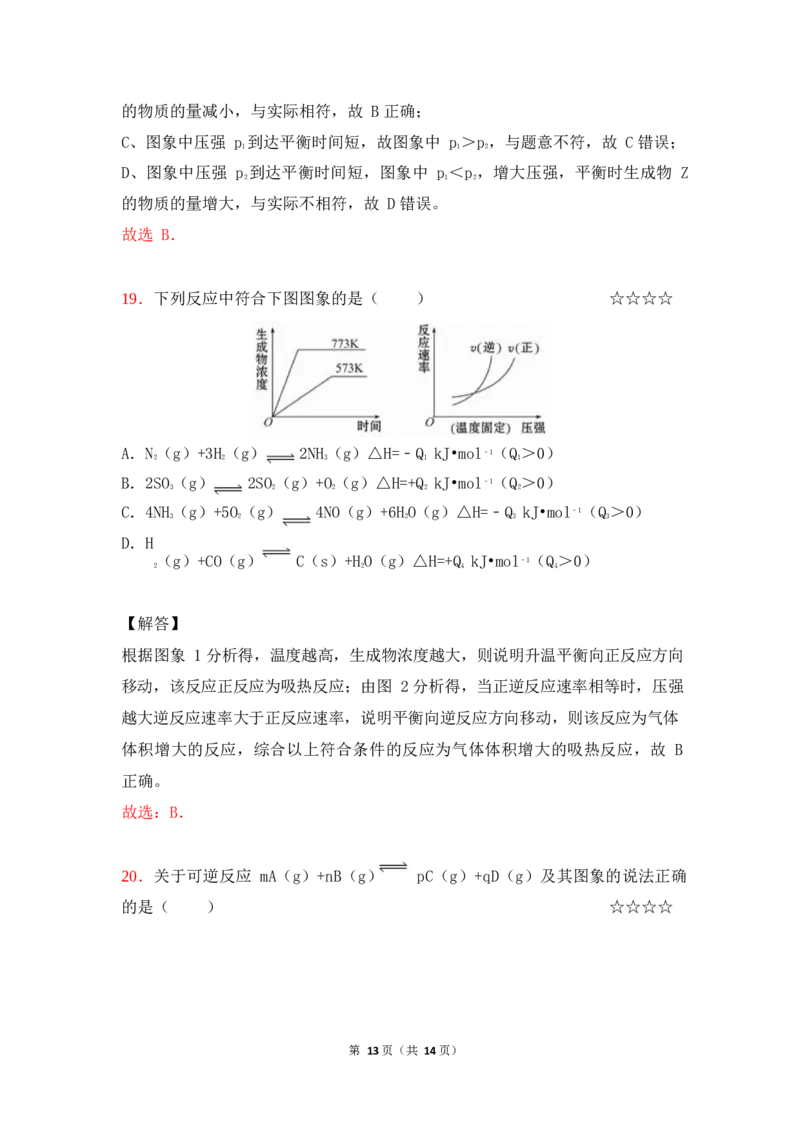
19.下列反应中符合下图图象的是( ) ☆☆☆☆
A.N(g)+3H(g) 2NH(g)△H=﹣Q kJ•mol﹣1(Q>0)
2 2 3 1 1
B.2SO(g) 2SO(g)+O(g)△H=+Q kJ•mol﹣1(Q>0)
3 2 2 2 2
C.4NH(g)+5O(g) 4NO(g)+6HO(g)△H=﹣Q kJ•mol﹣1(Q>0)
3 2 2 3 3
D.H
(g)+CO(g) C(s)+HO(g)△H=+Q kJ•mol﹣1(Q>0)
2 2 4 4
【解答】
根据图象 1 分析得,温度越高,生成物浓度越大,则说明升温平衡向正反应方向
移动,该反应正反应为吸热反应;由图 2 分析得,当正逆反应速率相等时,压强
越大逆反应速率大于正反应速率,说明平衡向逆反应方向移动,则该反应为气体
体积增大的反应,综合以上符合条件的反应为气体体积增大的吸热反应,故 B
正确。
故选:B.
20.关于可逆反应 mA(g)+nB(g) pC(g)+qD(g)及其图象的说法正确
的是( ) ☆☆☆☆
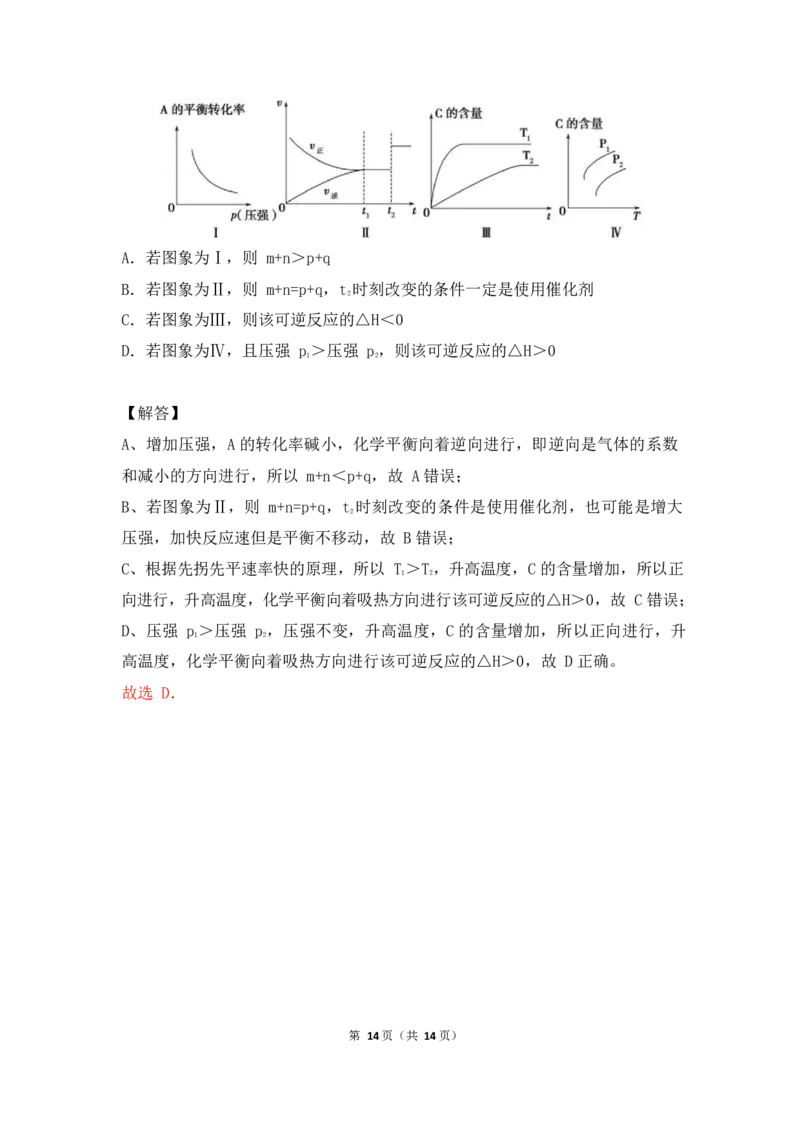
第 13页(共 14页)A.若图象为Ⅰ,则 m+n>p+q
B.若图象为Ⅱ,则 m+n=p+q,t 时刻改变的条件一定是使用催化剂
2
C.若图象为Ⅲ,则该可逆反应的△H<0
D.若图象为Ⅳ,且压强 p>压强 p,则该可逆反应的△H>0
1 2
【解答】
A、增加压强,A 的转化率碱小,化学平衡向着逆向进行,即逆向是气体的系数
和减小的方向进行,所以 m+n<p+q,故 A 错误;
B、若图象为Ⅱ,则 m+n=p+q,t 时刻改变的条件是使用催化剂,也可能是增大
2
压强,加快反应速但是平衡不移动,故 B 错误;
C、根据先拐先平速率快的原理,所以 T>T,升高温度,C 的含量增加,所以正
1 2
向进行,升高温度,化学平衡向着吸热方向进行该可逆反应的△H>0,故 C 错误;
D、压强 p>压强 p,压强不变,升高温度,C 的含量增加,所以正向进行,升
1 2
高温度,化学平衡向着吸热方向进行该可逆反应的△H>0,故 D 正确。
故选 D.
第 14页(共 14页)