文档内容
专练 31 原电池原理及应用一
一、单项选择题
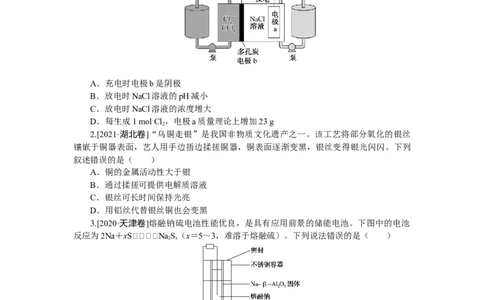
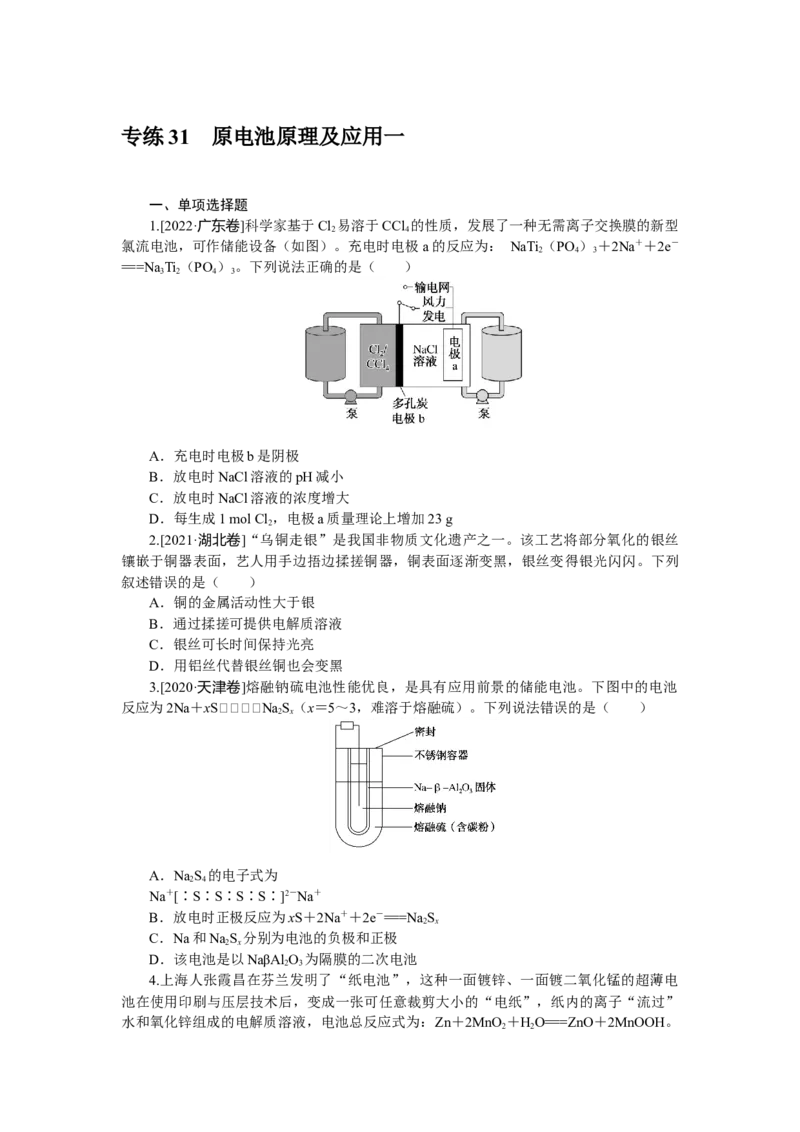
1.[2022·广东卷]科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型
2 4
氯流电池,可作储能设备(如图)。充电时电极 a的反应为: NaTi (PO ) +2Na++2e-
2 4 3
===Na Ti (PO )。下列说法正确的是( )
3 2 4 3
A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1 mol Cl ,电极a质量理论上增加23 g
2
2.[2021·湖北卷]“乌铜走银”是我国非物质文化遗产之一。该工艺将部分氧化的银丝
镶嵌于铜器表面,艺人用手边捂边揉搓铜器,铜表面逐渐变黑,银丝变得银光闪闪。下列
叙述错误的是( )
A.铜的金属活动性大于银
B.通过揉搓可提供电解质溶液
C.银丝可长时间保持光亮
D.用铝丝代替银丝铜也会变黑
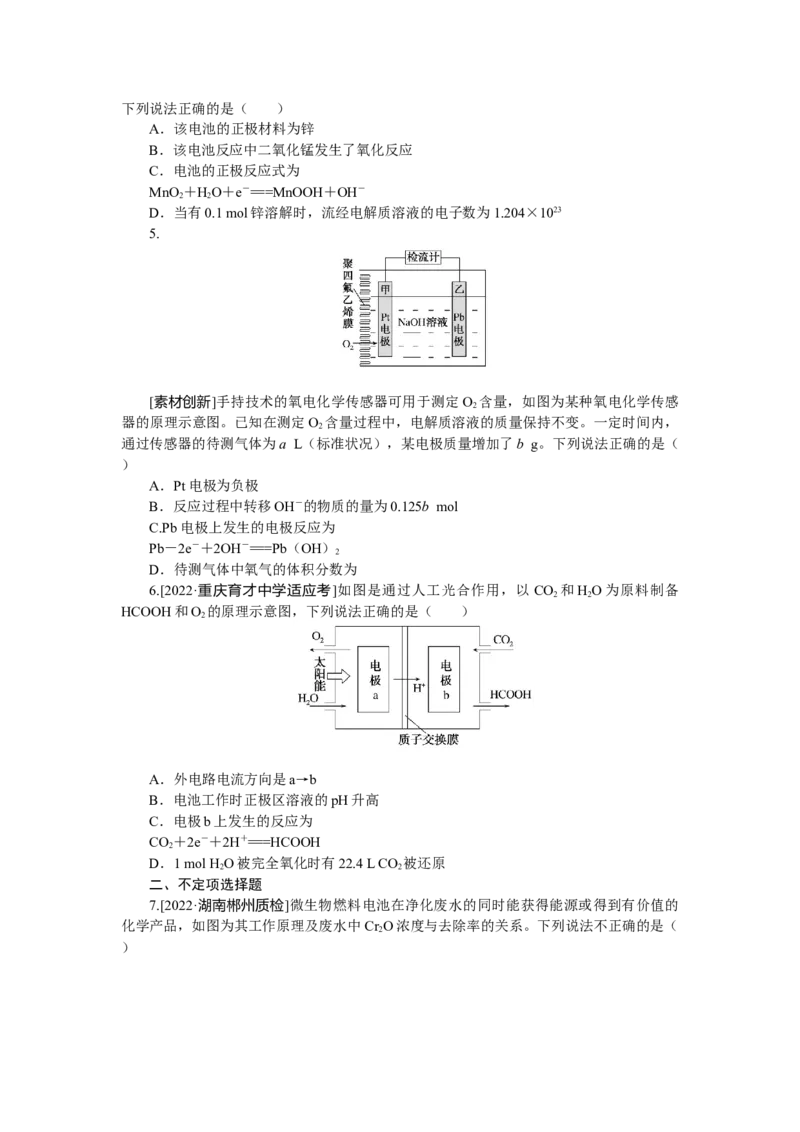
3.[2020·天津卷]熔融钠硫电池性能优良,是具有应用前景的储能电池。下图中的电池
反应为2Na+xSNaS(x=5~3,难溶于熔融硫)。下列说法错误的是( )
2 x
A.NaS 的电子式为
2 4
Na+[∶S∶S∶S∶S∶]2-Na+
B.放电时正极反应为xS+2Na++2e-===Na S
2 x
C.Na和NaS 分别为电池的负极和正极
2 x
D.该电池是以NaβAl O 为隔膜的二次电池
2 3
4.上海人张霞昌在芬兰发明了“纸电池”,这种一面镀锌、一面镀二氧化锰的超薄电
池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,纸内的离子“流过”
水和氧化锌组成的电解质溶液,电池总反应式为:Zn+2MnO +HO===ZnO+2MnOOH。
2 2下列说法正确的是( )
A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为
MnO +HO+e-===MnOOH+OH-
2 2
D.当有0.1 mol锌溶解时,流经电解质溶液的电子数为1.204×1023
5.
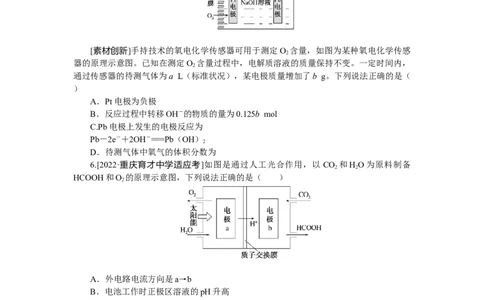
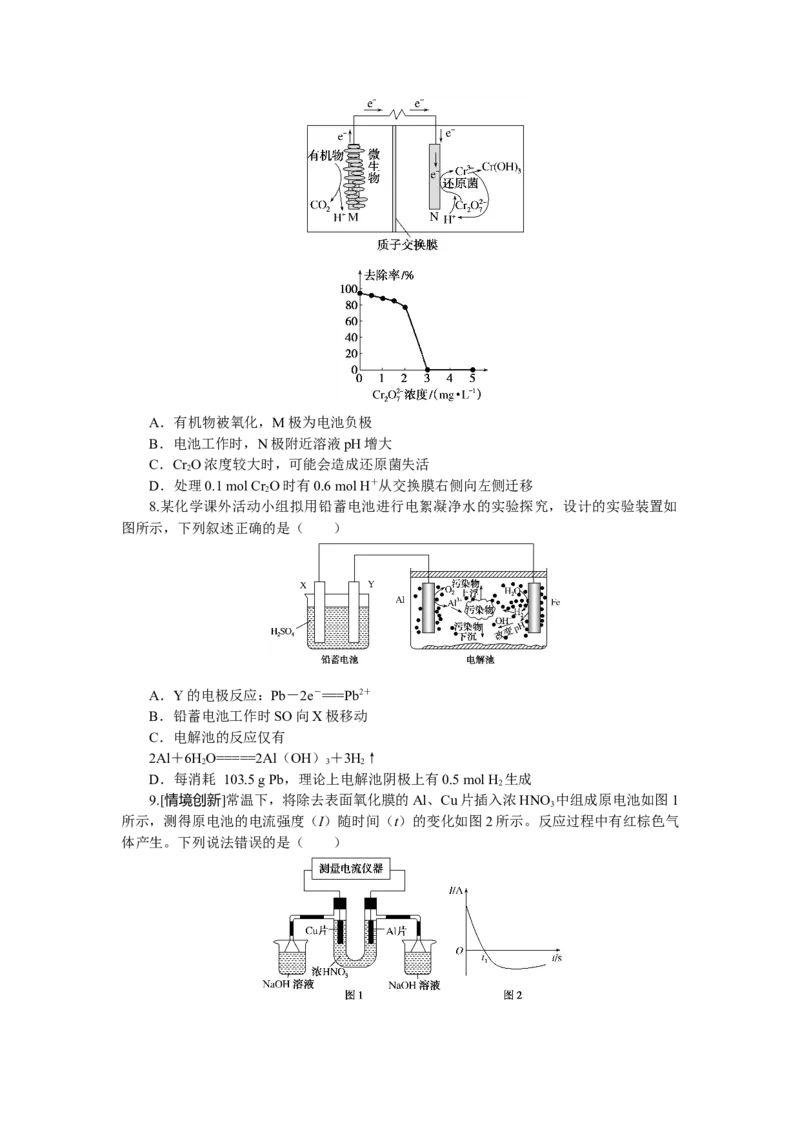
[素材创新]手持技术的氧电化学传感器可用于测定O 含量,如图为某种氧电化学传感
2
器的原理示意图。已知在测定O 含量过程中,电解质溶液的质量保持不变。一定时间内,
2
通过传感器的待测气体为a L(标准状况),某电极质量增加了b g。下列说法正确的是(
)
A.Pt电极为负极
B.反应过程中转移OH-的物质的量为0.125b mol
C.Pb电极上发生的电极反应为
Pb-2e-+2OH-===Pb(OH)
2
D.待测气体中氧气的体积分数为
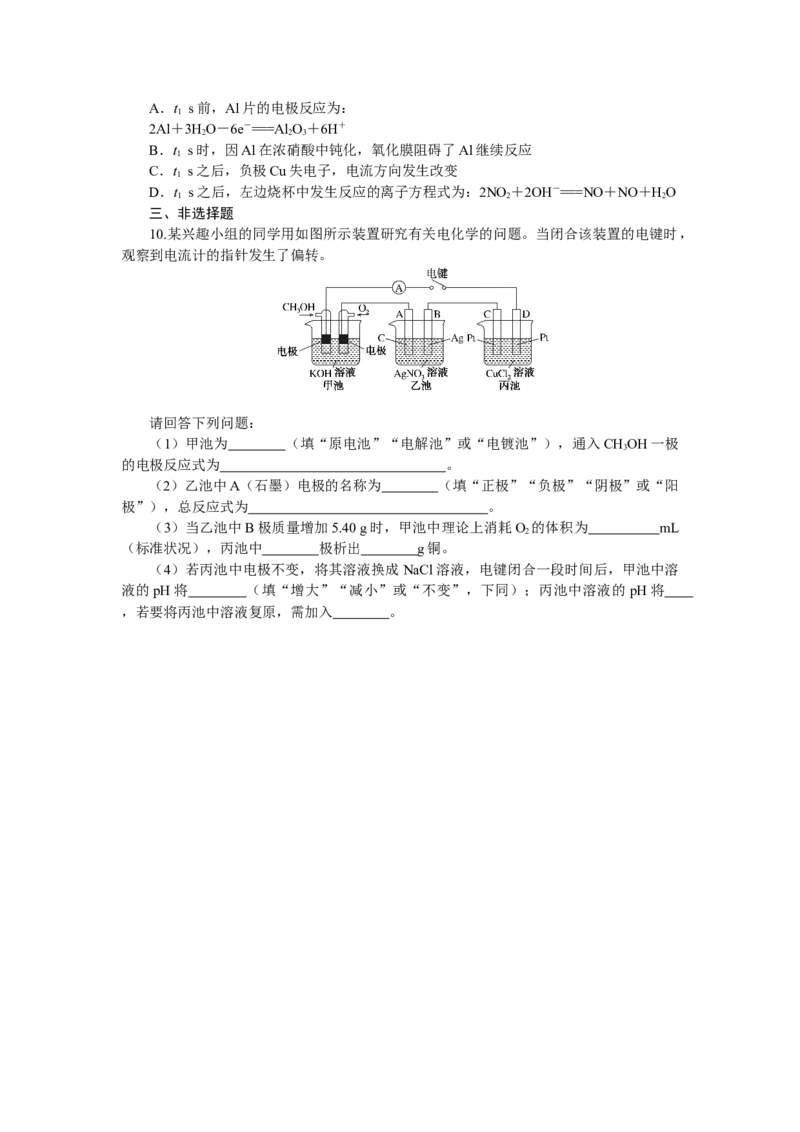
6.[2022·重庆育才中学适应考]如图是通过人工光合作用,以 CO 和HO为原料制备
2 2
HCOOH和O 的原理示意图,下列说法正确的是( )
2
A.外电路电流方向是a→b
B.电池工作时正极区溶液的pH升高
C.电极b上发生的反应为
CO+2e-+2H+===HCOOH
2
D.1 mol H O被完全氧化时有22.4 L CO 被还原
2 2
二、不定项选择题
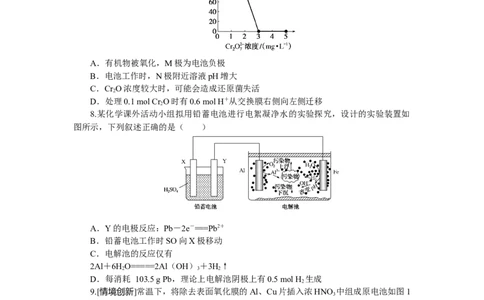
7.[2022·湖南郴州质检]微生物燃料电池在净化废水的同时能获得能源或得到有价值的
化学产品,如图为其工作原理及废水中Cr O浓度与去除率的关系。下列说法不正确的是(
2
)A.有机物被氧化,M极为电池负极
B.电池工作时,N极附近溶液pH增大
C.Cr O浓度较大时,可能会造成还原菌失活
2
D.处理0.1 mol Cr O时有0.6 mol H+从交换膜右侧向左侧迁移
2
8.某化学课外活动小组拟用铅蓄电池进行电絮凝净水的实验探究,设计的实验装置如
图所示,下列叙述正确的是( )
A.Y的电极反应:Pb-2e-===Pb2+
B.铅蓄电池工作时SO向X极移动
C.电解池的反应仅有
2Al+6HO=====2Al(OH)+3H↑
2 3 2
D.每消耗 103.5 g Pb,理论上电解池阴极上有0.5 mol H 生成
2
9.[情境创新]常温下,将除去表面氧化膜的Al、Cu片插入浓HNO 中组成原电池如图1
3
所示,测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气
体产生。下列说法错误的是( )A.t s前,Al片的电极反应为:
1
2Al+3HO-6e-===AlO+6H+
2 2 3
B.t s时,因Al在浓硝酸中钝化,氧化膜阻碍了Al继续反应
1
C.t s之后,负极Cu失电子,电流方向发生改变
1
D.t s之后,左边烧杯中发生反应的离子方程式为:2NO +2OH-===NO+NO+HO
1 2 2
三、非选择题
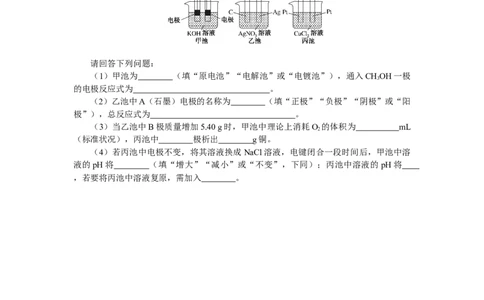
10.某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,
观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为 (填“原电池”“电解池”或“电镀池”),通入CHOH一极
3
的电极反应式为 。
(2)乙池中A(石墨)电极的名称为 (填“正极”“负极”“阴极”或“阳
极”),总反应式为 。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O 的体积为 mL
2
(标准状况),丙池中 极析出 g铜。
(4)若丙池中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲池中溶
液的pH将 (填“增大”“减小”或“不变”,下同);丙池中溶液的pH将
,若要将丙池中溶液复原,需加入 。