文档内容
专练 44 化学反应原理综合题
1.[2022·湖南卷]2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。
回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1mol HO(g),起始压强
2
为0.2 MPa时,发生下列反应生成水煤气:
Ⅰ.C(s)+H
2
O(g)⇌CO(g)+H
2
(g)ΔH
1
=+131.4 kJ·mol-1
Ⅱ.CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)ΔH
2
=-41.1 kJ·mol-1
①下列说法正确的是________;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于
2
D.将炭块粉碎,可加快反应速率
②反应平衡时,HO(g)的转化率为50%,CO的物质的量为0.1 mol。此时,整个体系
2
________(填“吸收”或“放出”)热量________kJ,反应Ⅰ的平衡常数K =________(以分
p
压表示,分压=总压×物质的量分数)。
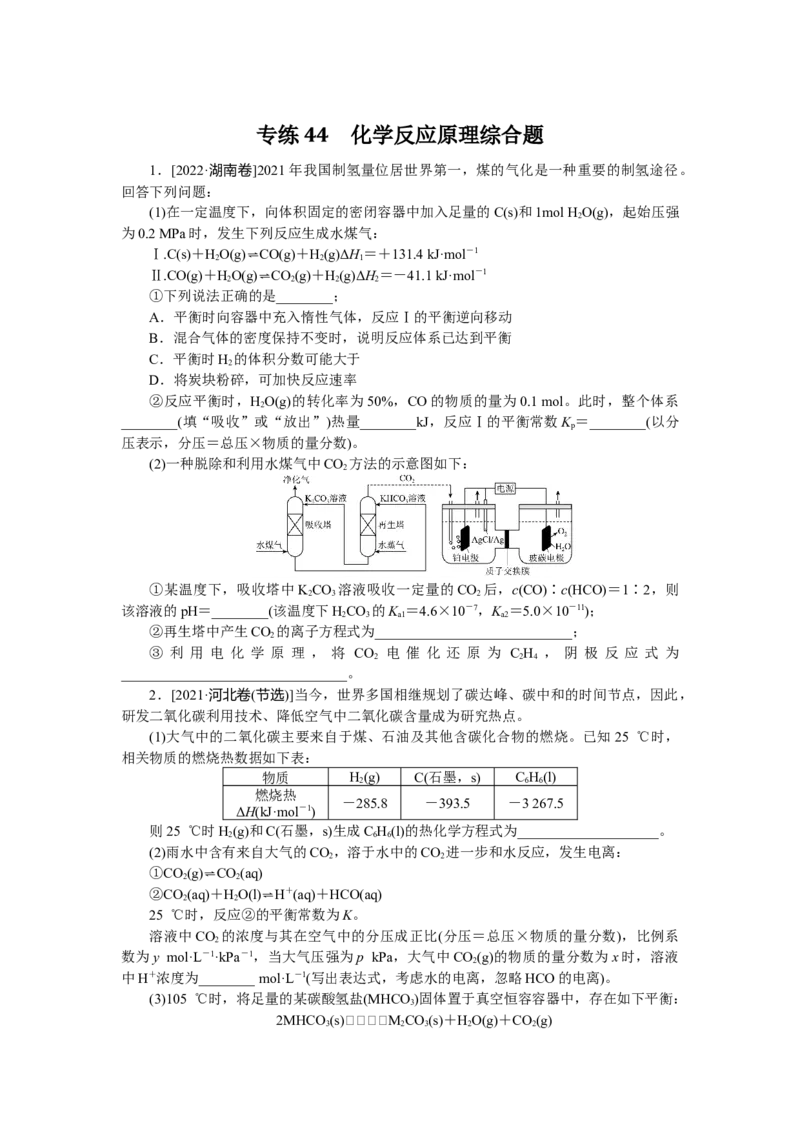
(2)一种脱除和利用水煤气中CO 方法的示意图如下:
2
①某温度下,吸收塔中KCO 溶液吸收一定量的CO 后,c(CO)∶c(HCO)=1∶2,则
2 3 2
该溶液的pH=________(该温度下HCO 的K =4.6×10-7,K =5.0×10-11);
2 3 a1 a2
②再生塔中产生CO 的离子方程式为____________________________;
2
③ 利 用 电 化 学 原 理 , 将 CO 电 催 化 还 原 为 C H , 阴 极 反 应 式 为
2 2 4
________________________________。
2.[2021·河北卷(节选)]当今,世界多国相继规划了碳达峰、碳中和的时间节点,因此,
研发二氧化碳利用技术、降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25 ℃时,
相关物质的燃烧热数据如下表:
物质 H(g) C(石墨,s) C H(l)
2 6 6
燃烧热
-285.8 -393.5 -3 267.5
ΔH(kJ·mol-1)
则25 ℃时H(g)和C(石墨,s)生成C H(l)的热化学方程式为____________________。
2 6 6
(2)雨水中含有来自大气的CO,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO
2
(g)⇌CO
2
(aq)
②CO
2
(aq)+H
2
O(l)⇌H+(aq)+HCO(aq)
25 ℃时,反应②的平衡常数为K。
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系
2
数为y mol·L-1·kPa-1,当大气压强为p kPa,大气中CO(g)的物质的量分数为x时,溶液
2
中H+浓度为________ mol·L-1(写出表达式,考虑水的电离,忽略HCO的电离)。
(3)105 ℃时,将足量的某碳酸氢盐(MHCO )固体置于真空恒容容器中,存在如下平衡:
3
2MHCO (s)MCO(s)+HO(g)+CO(g)
3 2 3 2 2上述反应达平衡时体系的总压为46 kPa。
保持温度不变,开始时在体系中先通入一定量的 CO(g),再加入足量MHCO (s),欲
2 3
使平衡时体系中水蒸气的分压小于5 kPa,CO(g)的初始压强应大于________ kPa。
2
(4)我国科学家研究LiCO 电池,取得了重大科研成果。回答下列问题:
2
①LiCO 电池中,Li为单质锂片,则该电池中的CO 在________(填“正”或“负”)
2 2
极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且 CO 电还原后与锂
2
离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
Ⅰ.2CO +2e-===C O
2 2
Ⅱ.C O===CO +CO
2 2
Ⅲ.________________________
Ⅳ.CO+2Li+===Li CO
2 3
②研究表明,在电解质水溶液中,CO 气体可被电化学还原。
2
CO 在碱性介质中电还原为正丙醇 (CHCHCHOH) 的电极反应方程式为
2 3 2 2
________________________。
3.[2021·全国乙卷]一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反
应,也可用作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而
错过了一种新元素的发现。该元素是________。
(2)氯铂酸钡(BaPtCl )固体加热时部分分解为BaCl 、Pt和Cl ,376.8 ℃时平衡常数K′
6 2 2 p
=1.0×104Pa2。在一硬质玻璃烧瓶中加入过量BaPtCl ,抽真空后,通过一支管通入碘蒸气
6
(然后将支管封闭)。在376.8 ℃,碘蒸气初始压强为20.0 kPa。376.8 ℃平衡时,测得烧瓶
中压强为 32.5 kPa,则 p =________kPa,反应 2ICl(g)===Cl(g)+I(g)的平衡常数 K=
ICl 2 2
________(列出计算式即可)。
(3)McMorris测定和计算了在136~180 ℃范围内下列反应的平衡常数K :
p
2NO(g)+2ICl(g)⇌2NOCl(g)+I
2
(g) K
p1
2NOCl(g)⇌2NO(g)+Cl
2
(g) K
p2
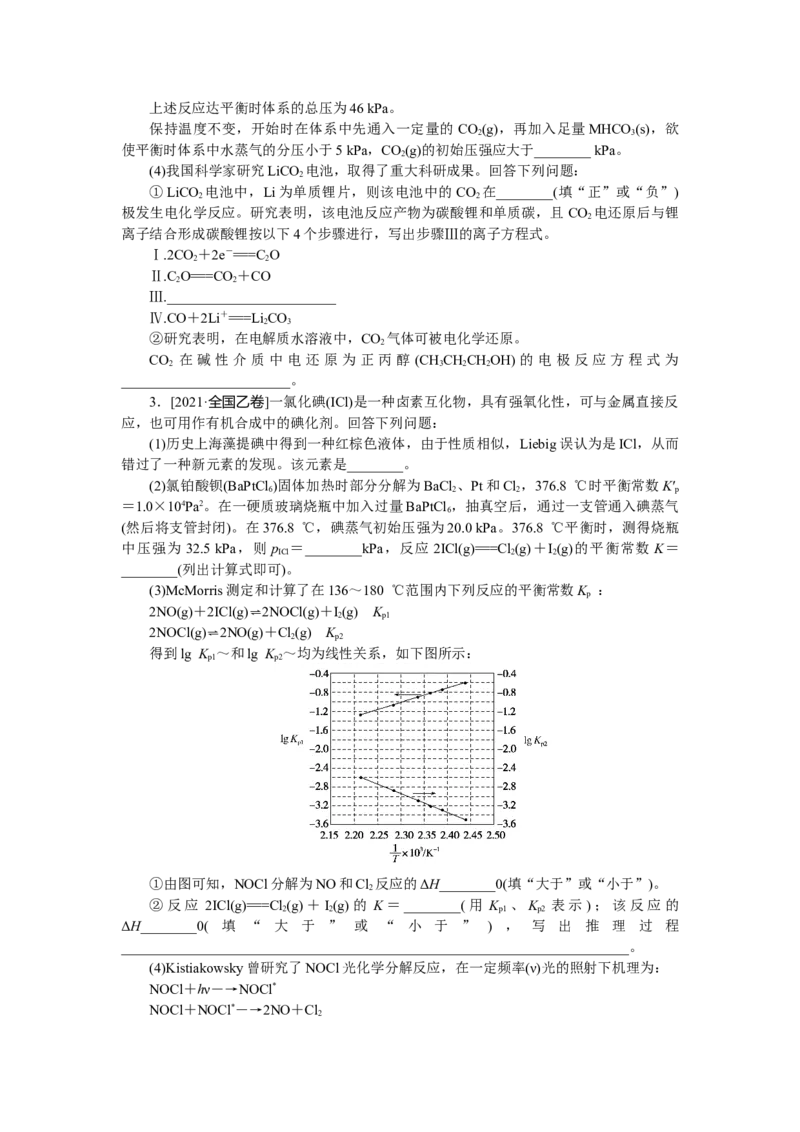
得到lg K ~和lg K ~均为线性关系,如下图所示:
p1 p2
①由图可知,NOCl分解为NO和Cl 反应的ΔH________0(填“大于”或“小于”)。
2
②反应 2ICl(g)===Cl(g)+I(g)的 K=________(用 K 、K 表示);该反应的
2 2 p1 p2
ΔH________0( 填 “ 大 于 ” 或 “ 小 于 ” ) , 写 出 推 理 过 程
________________________________________________________________________。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(ν)光的照射下机理为:
NOCl+hν―→NOCl*
NOCl+NOCl*―→2NO+Cl
2其中hν表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1 mol的NOCl需
要吸收________mol的光子。
4.[2022·浙江卷1月(节选)]工业上,以煤炭为原料,通入一定比例的空气和水蒸气,
经过系列反应可以得到满足不同需求的原料气。
请回答:
(1)在C和O 的反应体系中:
2
反应1 C(s)+O(g)===CO (g) ΔH=-394 kJ·mol-1
2 2 1
反应2 2CO(g)+O(g)===2CO (g) ΔH=-566 kJ·mol-1
2 2 2
反应3 2C(s)+O(g)===2CO(g) ΔH
2 3
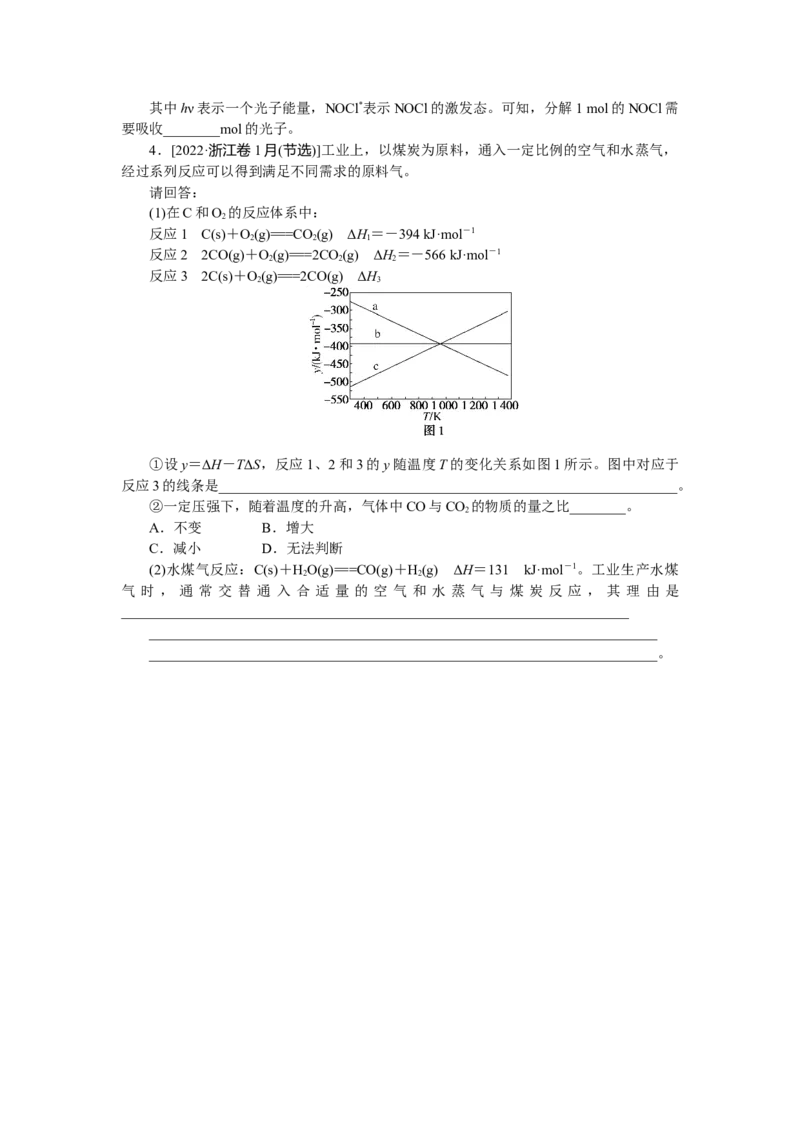
①设y=ΔH-TΔS,反应1、2和3的y随温度T的变化关系如图1所示。图中对应于
反应3的线条是_________________________________________________________________。
②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比________。
2
A.不变 B.增大
C.减小 D.无法判断
(2)水煤气反应:C(s)+HO(g)===CO(g)+H(g) ΔH=131 kJ·mol-1。工业生产水煤
2 2
气 时 , 通 常 交 替 通 入 合 适 量 的 空 气 和 水 蒸 气 与 煤 炭 反 应 , 其 理 由 是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。