文档内容
专练 49 物质的检验、分离、提纯
一、单项选择题
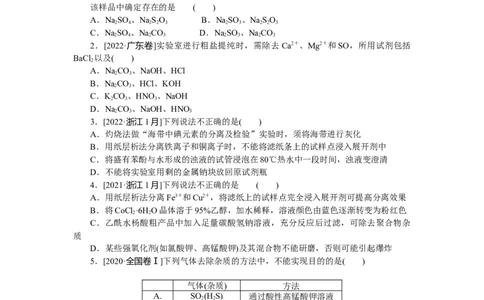
1.[2022·全国乙卷]某白色粉末样品,可能含有NaSO 、NaSO 、NaSO 和NaCO。
2 4 2 3 2 2 3 2 3
取少量样品进行如下实验:
①溶于水,得到无色透明溶液。
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是 ( )
A.NaSO 、NaSO B.NaSO 、NaSO
2 4 2 2 3 2 3 2 2 3
C.NaSO 、NaCO D.NaSO 、NaCO
2 4 2 3 2 3 2 3
2.[2022·广东卷]实验室进行粗盐提纯时,需除去Ca2+、Mg2+和SO,所用试剂包括
BaCl 以及( )
2
A.NaCO、NaOH、HCl
2 3
B.NaCO、HCl、KOH
2 3
C.KCO、HNO、NaOH
2 3 3
D.NaCO、NaOH、HNO
2 3 3
3.[2022·浙江1月]下列说法不正确的是( )
A.灼烧法做“海带中碘元素的分离及检验”实验时,须将海带进行灰化
B.用纸层析法分离铁离子和铜离子时,不能将滤纸条上的试样点浸入展开剂中
C.将盛有苯酚与水形成的浊液的试管浸泡在80℃热水中一段时间,浊液变澄清
D.不能将实验室用剩的金属钠块放回原试剂瓶
4.[2021·浙江1月]下列说法不正确的是 ( )
A.用纸层析法分离Fe3+和Cu2+,将滤纸上的试样点完全浸入展开剂可提高分离效果
B.将CoCl ·6H O晶体溶于95%乙醇,加水稀释,溶液颜色由蓝色逐渐转变为粉红色
2 2
C.乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可除去聚合物杂
质
D.某些强氧化剂(如氯酸钾、高锰酸钾)及其混合物不能研磨,否则可能引起爆炸
5.[2020·全国卷Ⅰ]下列气体去除杂质的方法中,不能实现目的的是( )
气体(杂质) 方法
A. SO (H S) 通过酸性高锰酸钾溶液
2 2
B. Cl(HCl) 通过饱和的食盐水
2
C. N(O ) 通过灼热的铜丝网
2 2
D. NO(NO ) 通过氢氧化钠溶液
2
6.[2022·衡水中学二调]某校化学兴趣小组用如图所示过程除去AlCl 溶液中含有的Mg2
3
+、K+杂质离子并尽可能减少AlCl 的损失。
3
下列说法正确的是( )A.NaOH溶液可以用氨水来代替
B.溶液a中含有Al3+、K+、Cl-、Na+、OH-
C.溶液b中只含有NaCl
D.向溶液a中滴加盐酸需控制溶液的pH
7.[2022·天津三中月考]下列关于物质或离子检验的叙述正确的是( )
A.气体通过无水CuSO ,粉末变蓝,证明原气体中含有水蒸气
4
B.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.向某溶液中加稀盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中存在CO
二、不定项选择题
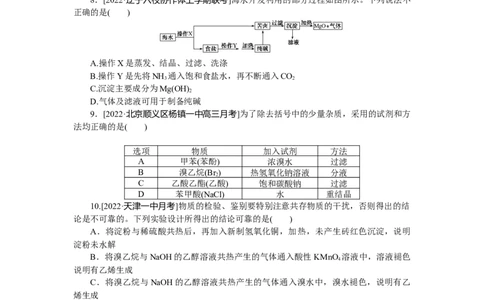
8.[2022·辽宁六校协作体上学期联考]海水开发利用的部分过程如图所示。下列说法不
正确的是( )
A.操作X是蒸发、结晶、过滤、洗涤
B.操作Y是先将NH 通入饱和食盐水,再不断通入CO
3 2
C.沉淀主要成分为Mg(OH)
2
D.气体及滤液可用于制备纯碱
9.[2022·北京顺义区杨镇一中高三月考]为了除去括号中的少量杂质,采用的试剂和方
法均正确的是( )
选项 物质 加入试剂 方法
A 甲苯(苯酚) 浓溴水 过滤
B 溴乙烷(Br) 热氢氧化钠溶液 分液
2
C 乙酸乙酯(乙酸) 饱和碳酸钠 过滤
D 苯甲酸(NaCl) 水 重结晶
10.[2022·天津一中月考]物质的检验、鉴别要特别注意共存物质的干扰,否则得出的结
论是不可靠的。下列实验设计所得出的结论可靠的是( )
A.将淀粉与稀硫酸共热后,再加入新制氢氧化铜,加热,未产生砖红色沉淀,说明
淀粉未水解
B.将溴乙烷与NaOH的乙醇溶液共热产生的气体通入酸性KMnO 溶液中,溶液褪色
4
说明有乙烯生成
C.将溴乙烷与NaOH的乙醇溶液共热产生的气体通入溴水中,溴水褪色,说明有乙
烯生成
D.将苯、液溴、铁粉混合物反应产生的气体通入AgNO 溶液中有淡黄色沉淀产生,
3
说明有HBr生成
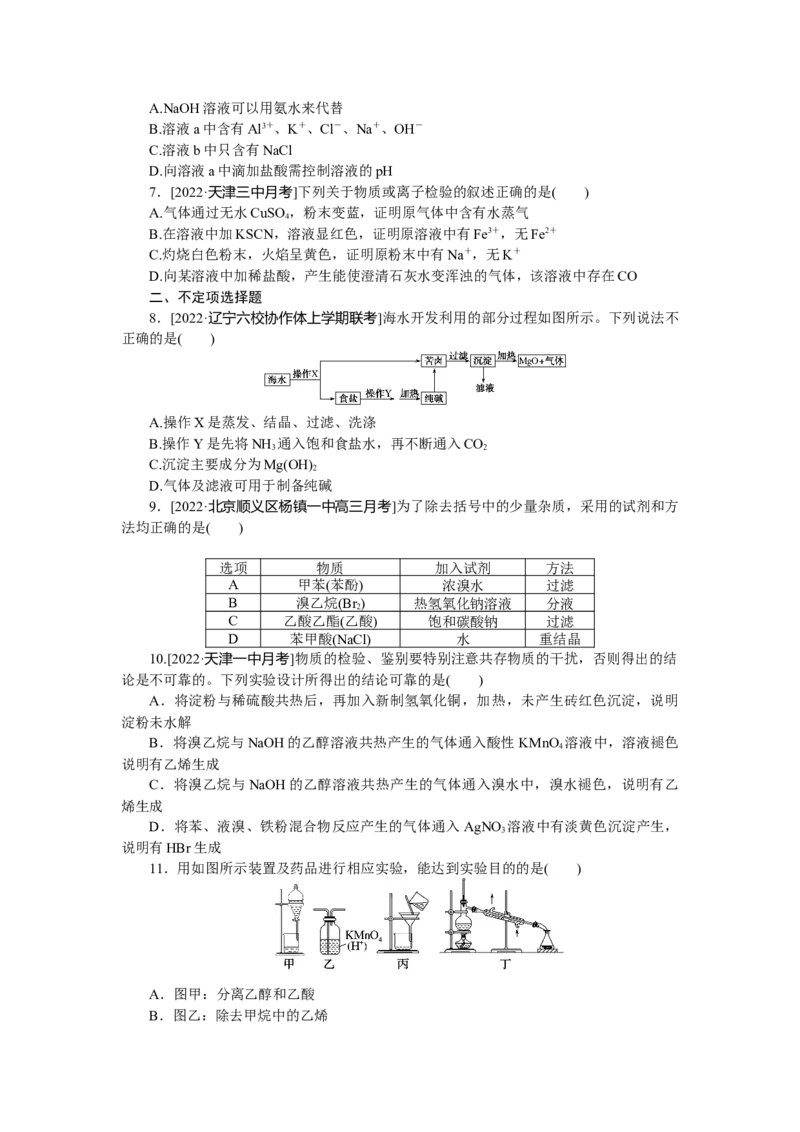
11.用如图所示装置及药品进行相应实验,能达到实验目的的是( )
A.图甲:分离乙醇和乙酸
B.图乙:除去甲烷中的乙烯C.图丙:除去溴苯中的溴单质
D.图丁:除去工业酒精中的甲醇
三、非选择题
12.[2022·德州市武城二中高三月考]
(NH )Fe(SO )·6H O(莫尔盐,浅绿色)是重要的化工原料和化学试剂。某课题小组为了
4 2 4 2 2
探究莫尔盐的分解产物,开展了如下实验:
(1)甲同学猜想:莫尔盐的分解产物可能是N、Fe O、SO 和HO四种物质。你是否同
2 2 3 3 2
意甲同学的猜想,并说明理由:
________________________________________________________________________
________________________________________________________________________。
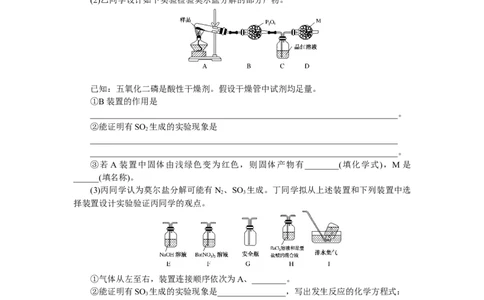
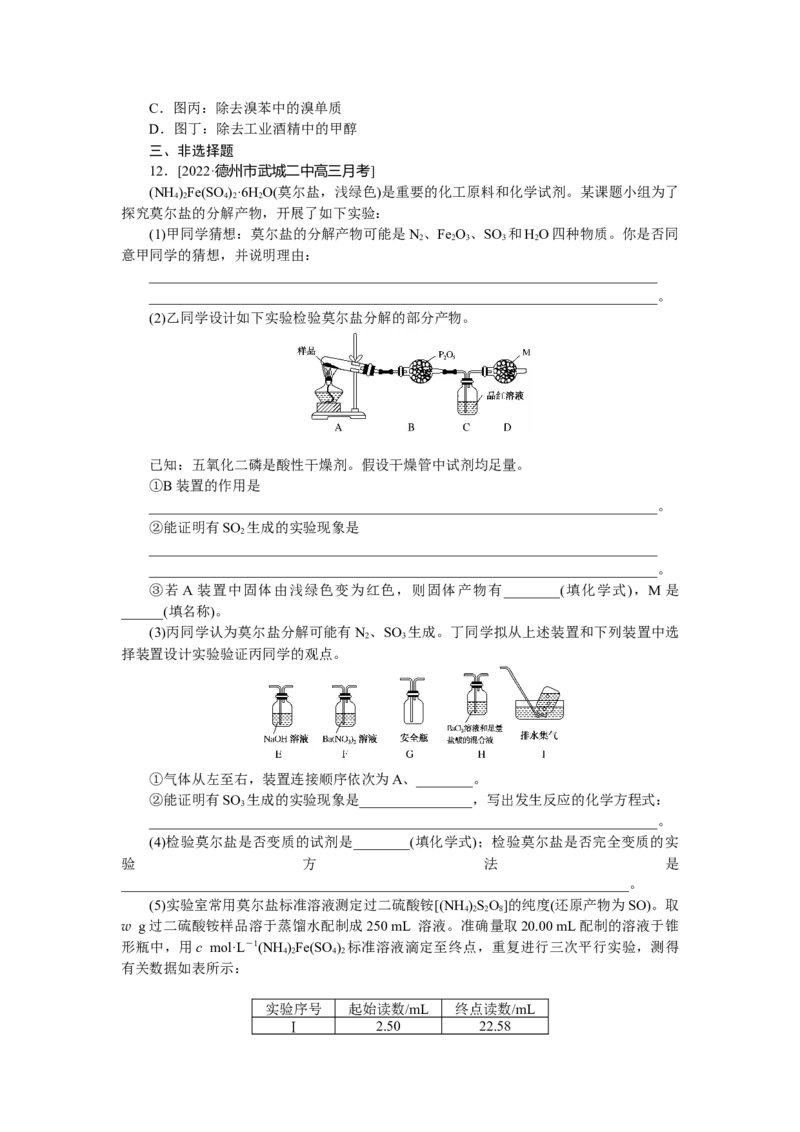
(2)乙同学设计如下实验检验莫尔盐分解的部分产物。
已知:五氧化二磷是酸性干燥剂。假设干燥管中试剂均足量。
①B装置的作用是
________________________________________________________________________。
②能证明有SO 生成的实验现象是
2
________________________________________________________________________
________________________________________________________________________。
③若A装置中固体由浅绿色变为红色,则固体产物有________(填化学式),M是
______(填名称)。
(3)丙同学认为莫尔盐分解可能有N 、SO 生成。丁同学拟从上述装置和下列装置中选
2 3
择装置设计实验验证丙同学的观点。
①气体从左至右,装置连接顺序依次为A、________。
②能证明有SO 生成的实验现象是________________,写出发生反应的化学方程式:
3
________________________________________________________________________。
(4)检验莫尔盐是否变质的试剂是________(填化学式);检验莫尔盐是否完全变质的实
验 方 法 是
________________________________________________________________________。
(5)实验室常用莫尔盐标准溶液测定过二硫酸铵[(NH )SO]的纯度(还原产物为SO)。取
4 2 2 8
w g过二硫酸铵样品溶于蒸馏水配制成250 mL 溶液。准确量取20.00 mL配制的溶液于锥
形瓶中,用c mol·L-1(NH )Fe(SO ) 标准溶液滴定至终点,重复进行三次平行实验,测得
4 2 4 2
有关数据如表所示:
实验序号 起始读数/mL 终点读数/mL
Ⅰ 2.50 22.58Ⅱ 1.00 23.12
Ⅲ 0.00 19.92
①完成上述实验需要三种定量仪器:托盘天平、________和酸式滴定管。准确量取
20.00 mL 过二硫酸铵溶液所用仪器的名称是________。
②写出滴定反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
③根据上述数据计算,样品的纯度为______(用含w、c的代数式表示)。