文档内容
第五篇 水溶液中的离子反应与平衡
专项 31 中和滴定图象
在酸碱电离过程中,溶液的pH会发生变化,对于强酸强碱的反应,开始时由于被中和的酸或碱浓度
较大,加入少量的碱或酸对其pH的影响不大。当反应接近反应终点(pH≈7)时,很少量(一滴,约
0.04mL)的碱或酸就会引起溶液pH突变。酸、碱的浓度不同, pH突变范围不同。
1.强酸与强碱滴定过程中pH曲线(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸
为例)
2滴定曲线特点
氢氧化钠滴定等浓度等体积的盐酸、醋酸的 盐酸滴定等浓度等体积的氢氧化钠、氨水的
滴定曲线 滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强
碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸
反应(强酸与弱碱反应)
室温下pH=7不一定是终点:强碱与强酸反应时,终点是pH=7;强碱与弱酸(强酸与弱碱)
反应时,终点不是pH=7(强碱与弱酸反应终点是pH>7,强酸与弱碱反应终点是pH<7)
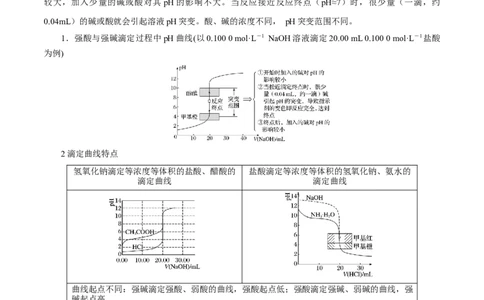
1.(2022•浙江1月选考)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 340mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲
3
线:
下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -
1 3
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
【答案】C
【解析】A项,碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,碳酸钠与盐酸反应
先生成碳酸氢钠,再产生二氧化碳气体,故图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向
2 3
NaHCO 溶液中滴加盐酸,A错误;B项,当滴加盐酸的体积为VmL时(a点、b点),所发生的反应为碳酸
3 1
根离子与氢离子结合生成碳酸氢根离子,离子方程式表示为:CO2-+H+= HCO -,B错误;C项,根据pH—
3 3
V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,故可用酚酞作指示剂;d点的pH在4
左右,符合甲基橙的指示范围,故可用甲基橙作指示剂指示滴定终点,C正确;D项,根据电荷守恒和物
料守恒,则NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO-), NaHCO 溶液中满足c(HCO)-
2 3 2 3 3 3 2 3
c(CO2-)=c(OH-)-c(H+),D错误;故选C。
3
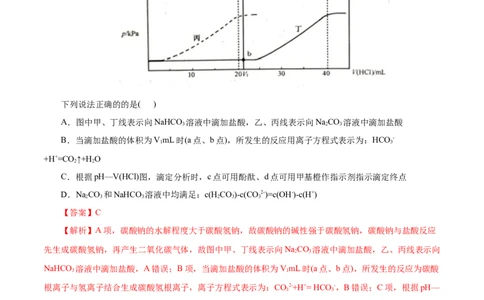
2.(2021•海南选择性考试) 25℃时,向10.00mL0.1000mol·L-1的NaHCO 溶液中滴加.1000mol·L-1的盐
3
酸,溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是( )A. 点,溶液 是由于HCO -水解程度大于电离程度
3
B. 点,c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-)
3 3
C.c 点,溶液中的 主要来自HCO -的电离
3
D.d点,c(Na+)= c(Cl-)= 0.1000mol·L-1
【答案】AB
【解析】A项,HCO -存在水解平衡和电离平衡,a点溶液pH>7是由于HCO -水解程度大于电离程度,
3 3
故A正确;B项,根据电荷守恒c(Na+)+c(H+)=c(HCO -)+2c(CO2-)+c(Cl-)+c(OH―),b点pH=7即c(H+)=
3 3
c(OH-),所以c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-),故B正确;C项,c点,溶质为碳酸氢钠、氯化钠、碳酸,
3 3
溶液中的H+主要来自HCO 的电离,故C错误;D项,d点,碳酸氢钠和盐酸恰好反应,c(Na+)= c(Cl-)=
2 3
0.0500mol·L-1,故D错误;选AB。
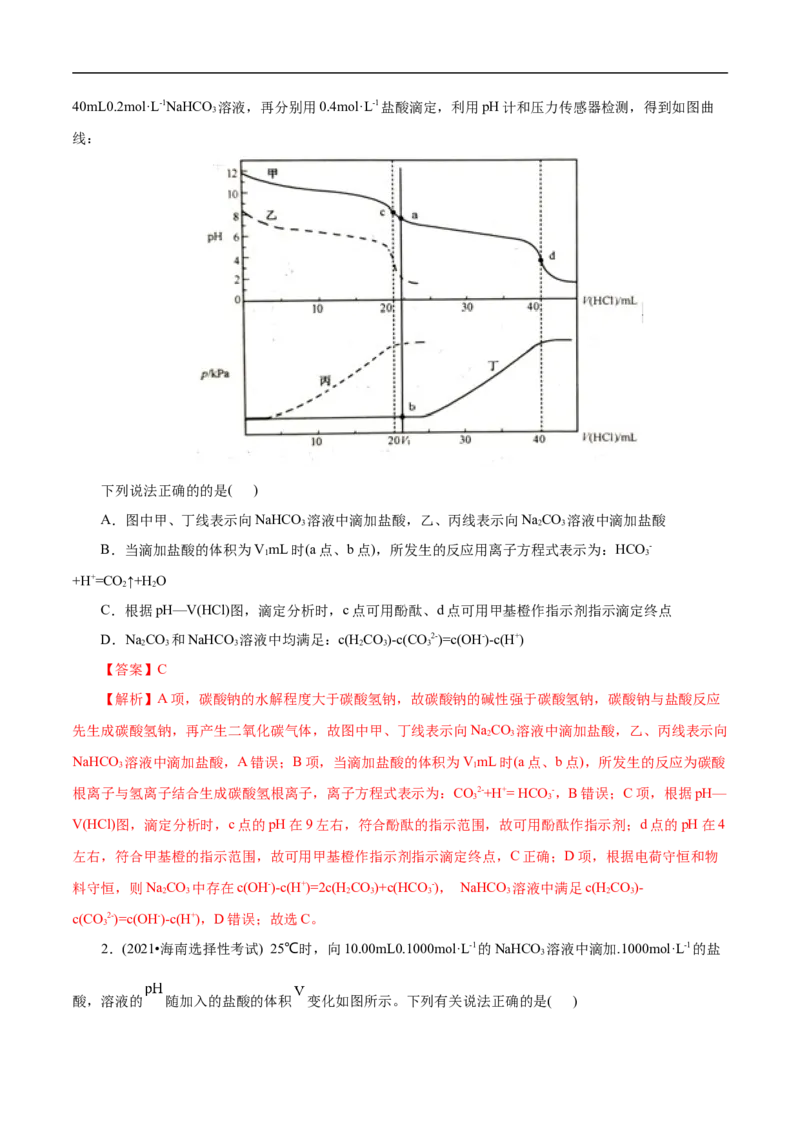
3.(2021•湖南选择性考试)常温下,用0.1000mol•L﹣1的盐酸分别滴定20.00mL浓度均为0.1000mol•L﹣1
的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A.该NaX溶液中:c(Na+)>c(X﹣)>c(OH﹣)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X﹣)=c(Y﹣)=c(Z﹣)
D.分别滴加20.00mL盐酸后,再将三种溶液混合:c(X﹣)+c(Y﹣)+c(Z﹣)=c(H+)﹣c(OH﹣)【答案】C
【解析】A项,因为HX为弱酸,NaX溶液存在水解:X﹣+H O HX+OH﹣,所以c(Na+)>c(X﹣)>
2
c(OH﹣)>c(H+),故A正确;B项,根据盐类水解的规律:越弱越水解可⇌知,相同浓度的强碱弱酸盐溶液中,
一元弱酸越弱,则其盐溶液碱性越强,结合图片可知溶液碱性强弱为:NaX<NaY<NaZ,则酸性强弱为:
HX>HY>HZ,一元弱酸中,酸性越强,电离程度越大,电离平衡常数 K越大,所以有:K(HX)>
a
K(HY)>K(HZ),故B正确;C项,当pH=7时,c(H+)=c(OH﹣),根据电荷守恒,NaX溶液中有:c(H+)
a a
+c(Na+)=c(OH﹣)+c(X﹣)+c(Cl﹣),则有:c(X﹣)=c(Na+)﹣c(Cl﹣),同理有:c(Y﹣)=c(Na+)﹣c(Cl﹣),c(Z﹣)=
c(Na+)﹣c(Cl﹣),又因三种溶液滴定到pH=7时,消耗的HCl的量是不一样的,即溶液中的c(Cl﹣)是不一样
的,所以c(X﹣)≠c(Y﹣)≠c(Z﹣),故C错误;D项,分别滴加20.00mL盐酸后,再将三种溶液混合后存在电荷
0.1mol/L×20mL×3
守恒:c(X﹣)+c(Y﹣)+c(Z﹣)+c(OH﹣)+c(Cl﹣)=c(H+)+c(Na+),又混合溶液中c(Na+)= =
40mL×3
0.1mol/L×20mL×3
0.05mol/L,混合溶液中c(Cl﹣)= =0.05mol/L,代入电荷守恒表达式,有c(X﹣)+c(Y
40mL×3
﹣)+c(Z﹣)=c(H+)﹣c(OH﹣),故D正确。故选C。
4.(2020•浙江1月选考)室温下,向20.00 mL 0.1000mol·L−1盐酸中滴加0.1000mol·L−1 NaOH溶液,溶
液的pH随NaOH溶液体积的变化如图。已知lg5=0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
【答案】C
【解析】A项,NaOH与盐酸恰好完全反应时溶液中的溶质为NaCl,呈中性,室温下 ,故A正
确;B项,选择变色范围在pH突变范围内的指示剂,可减小实验误差,B正确;C项,甲基橙的变色范围在pH突变范围外,误差更大,故C错误;D项, 时,溶液中的溶质为氯化钠和氢
氧化钠,且c(NaOH)= =0.02mol/L,即溶液中c(OH-)=0.02mol,
则c(H+)=5×10-13 mol/L,pH=-lgc(H+)=12.3,故D正确;故选C。
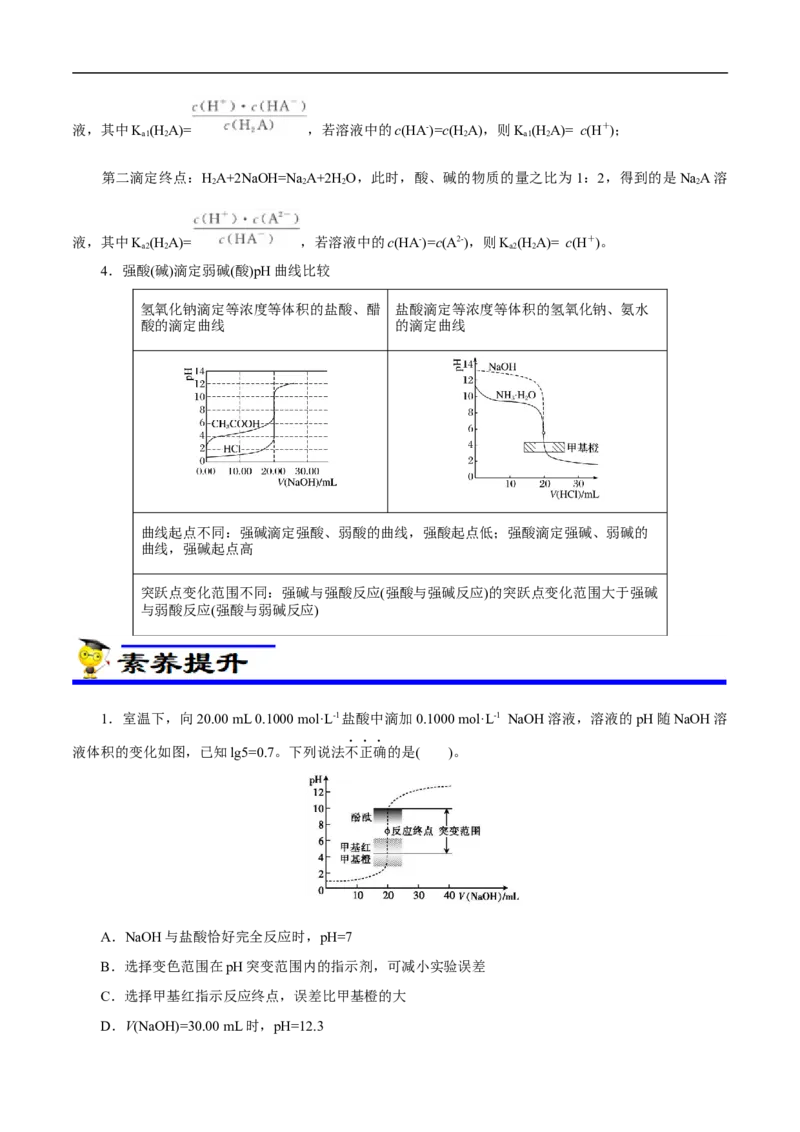
1.中和滴定曲线图像的分析方法
抓反应的“起始”点 判断酸、碱的相对强弱
抓反应的“一半”点 判断是哪种溶质的等量混合
抓溶液的“中性”点 判断溶液中溶质的成分及哪种物质过量或不足
抓“恰好”反应点 判断生成的溶质成分及溶液的酸碱性
抓反应的“过量”点 判断溶液中的溶质,判断哪种物质过量
如:常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CHCOOH溶液所得滴定曲
3
线如图:
2.酸碱中和滴定过程中的粒子浓度关系
常 温 下 , 用 0.1000 不同时刻 溶液中溶质成分及粒子浓度关系
mol·L-1 NaOH溶液滴定
** 错误的表达式 溶质是CHCOOH:
20.00 mL 0.1000 3
**V(NaOH)=0 mL
mol·L-1CHCOOH溶液 c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-)
3 3 3
②V(NaOH)=10 mL 溶质是等物质的量浓度的 CHCOOH 和 CHCOONa:
3 3
c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+)>c(OH-)
3 3
** 错误的表达式 溶质是CHCOONa和少量的CHCOOH:
3 3
**pH=7
c(Na+)=c(CHCOO-)>c(H+)=c(OH-)
3
④V(NaOH)=20 mL 溶质是CHCOONa:
3
c(Na+)>c(CHCOO-)>c(OH-)>c(CHCOOH)>c(H+)
3 3
3.抓“两个滴定点”突破图象
二元弱权(HA)与碱(NaOH)发生反应分两步进行:
2
第一滴定终点:HA+NaOH=NaHA+H O,此时,酸、碱的物质的量之比为1:1,得到的是NaHA溶
2 2液,其中K (H A)= ,若溶液中的c(HA-)=c(H A),则K (H A)= c(H+);
a1 2 2 a1 2
第二滴定终点:HA+2NaOH=Na A+2HO,此时,酸、碱的物质的量之比为1:2,得到的是NaA溶
2 2 2 2
液,其中K (H A)= ,若溶液中的c(HA-)=c(A2-),则K (H A)= c(H+)。
a2 2 a2 2
4.强酸(碱)滴定弱碱(酸)pH曲线比较
氢氧化钠滴定等浓度等体积的盐酸、醋 盐酸滴定等浓度等体积的氢氧化钠、氨水
酸的滴定曲线 的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的
曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱
与弱酸反应(强酸与弱碱反应)
1.室温下,向20.00 mL 0.1000 mol·L-1盐酸中滴加0.1000 mol·L-1 NaOH溶液,溶液的pH随NaOH溶
液体积的变化如图,已知lg5=0.7。下列说法不正确的是( )。
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
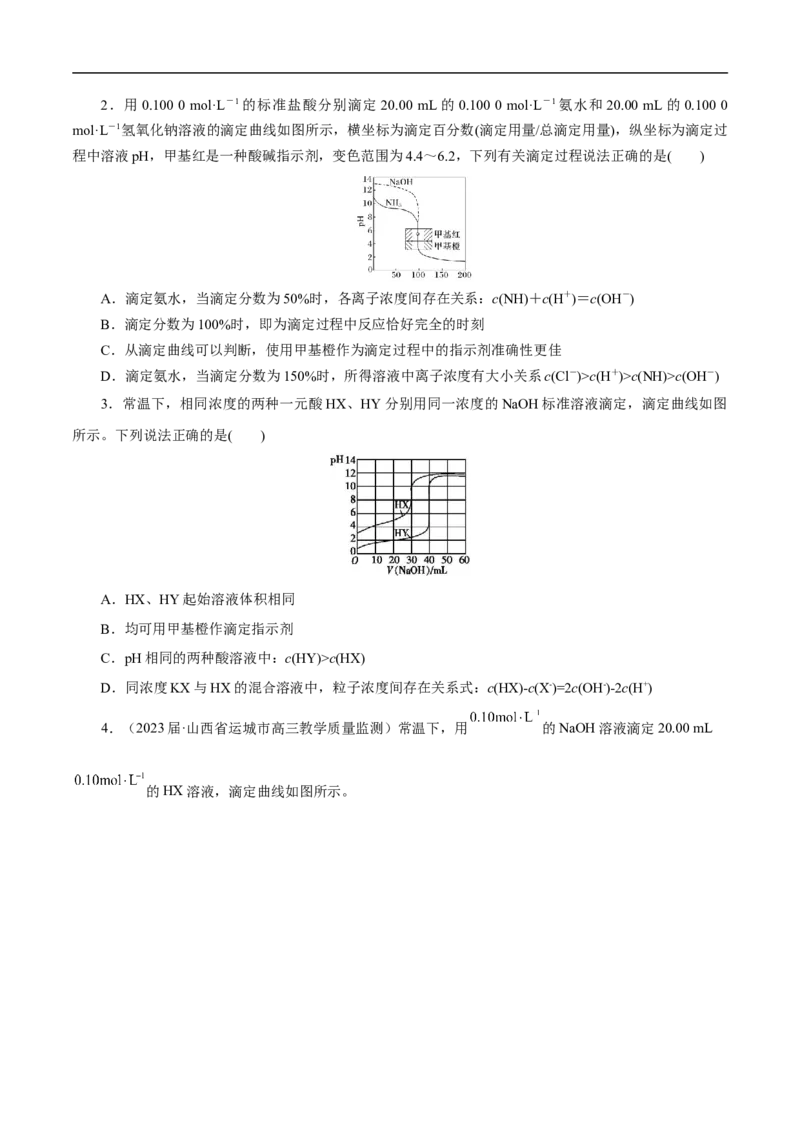
D.V(NaOH)=30.00 mL时,pH=12.32.用0.100 0 mol·L-1的标准盐酸分别滴定 20.00 mL的0.100 0 mol·L-1氨水和20.00 mL的0.100 0
mol·L-1氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过
程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4~6.2,下列有关滴定过程说法正确的是( )
A.滴定氨水,当滴定分数为50%时,各离子浓度间存在关系:c(NH)+c(H+)=c(OH-)
B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D.滴定氨水,当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)>c(NH)>c(OH-)
3.常温下,相同浓度的两种一元酸HX、HY分别用同一浓度的NaOH标准溶液滴定,滴定曲线如图
所示。下列说法正确的是( )
A.HX、HY起始溶液体积相同
B.均可用甲基橙作滴定指示剂
C.pH相同的两种酸溶液中:c(HY)>c(HX)
D.同浓度KX与HX的混合溶液中,粒子浓度间存在关系式:c(HX)-c(X-)=2c(OH-)-2c(H+)
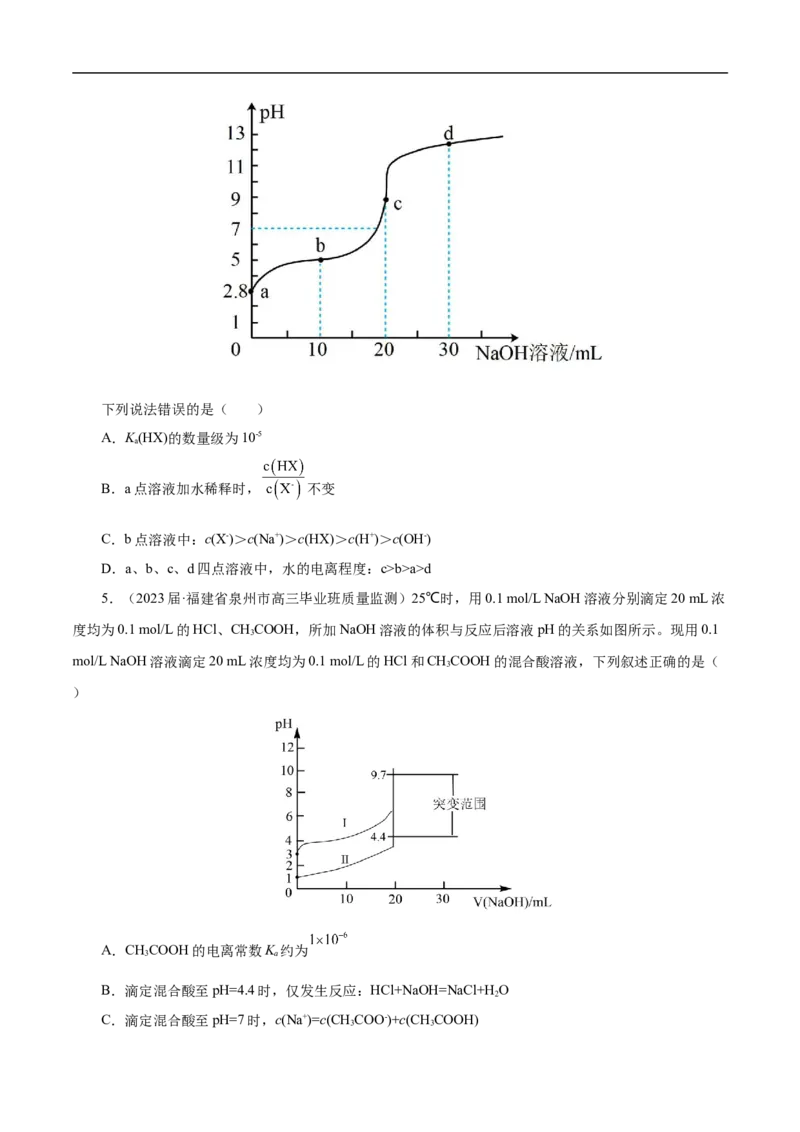
4.(2023届·山西省运城市高三教学质量监测)常温下,用 的NaOH溶液滴定20.00 mL
的HX溶液,滴定曲线如图所示。下列说法错误的是( )
A.K(HX)的数量级为10-5
a
B.a点溶液加水稀释时, 不变
C.b点溶液中:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
D.a、b、c、d四点溶液中,水的电离程度:c>b>a>d
5.(2023届·福建省泉州市高三毕业班质量监测)25℃时,用0.1 mol/L NaOH溶液分别滴定20 mL浓
度均为0.1 mol/L的HCl、CHCOOH,所加NaOH溶液的体积与反应后溶液pH的关系如图所示。现用0.1
3
mol/L NaOH溶液滴定20 mL浓度均为0.1 mol/L的HCl和CHCOOH的混合酸溶液,下列叙述正确的是(
3
)
A.CHCOOH的电离常数K 约为
3 a
B.滴定混合酸至pH=4.4时,仅发生反应:HCl+NaOH=NaCl+H O
2
C.滴定混合酸至pH=7时,c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3D.滴定混合酸至pH=8.2时,c(Na+)>c(Cl-)>c(CHCOO-)>c(OH-)
3
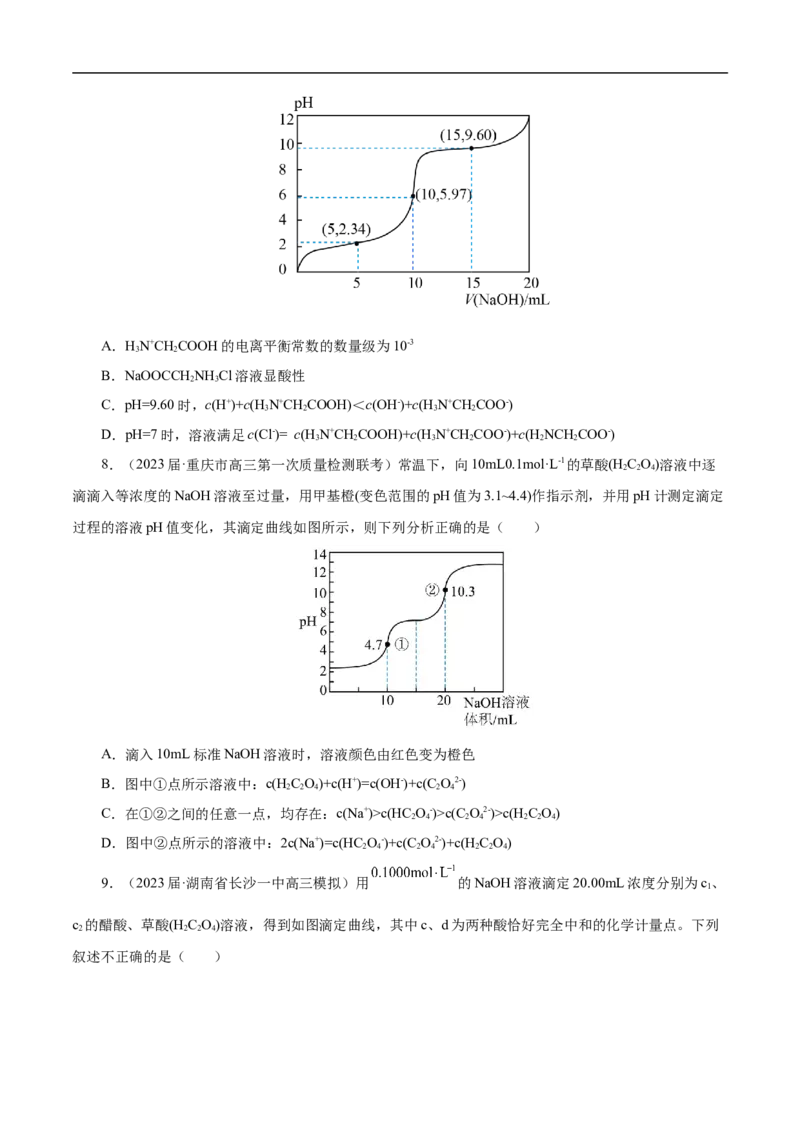
6.(2023届·河南省十所名校高中毕业班尖子生高三第一次考试)25℃时,用0.1000 的
溶液分别滴定体积均为50.00 、浓度均为0.0500 的5.6×10-11 mol·L-1、KHP (邻苯二甲酸氢
钾)及 溶液,其滴定曲线如图所示:
下列说法正确的是( )
A.K(HF )<K(HClO)
a a
B.V(NaOH溶液) 时,②中c(H P)>c(P2-)
2
C.V(NaOH溶液)均为0时,阴离子总数① ② ③
D.分别滴定至 时,c(ClO-)<c(P2-)-c(H P)<c(F-)
2
7.(2023届·河北省邯郸市高三摸底考试)常温下,向 的甘氨酸盐酸盐(化学式为
HOOCCH NH Cl)中逐滴加入 的 溶液,滴定过程中溶液的 与 溶液体积的变化曲
2 3
线如图所示。已知:甘氨酸盐酸盐与溶液的 反应过程为
,下列有关说法错误的是
( )A.HN+CHCOOH的电离平衡常数的数量级为10-3
3 2
B.NaOOCCHNH Cl溶液显酸性
2 3
C.pH=9.60时,c(H+)+c(H N+CHCOOH)<c(OH-)+c(H N+CHCOO-)
3 2 3 2
D.pH=7时,溶液满足c(Cl-)= c(H N+CHCOOH)+c(H N+CHCOO-)+c(H NCH COO-)
3 2 3 2 2 2
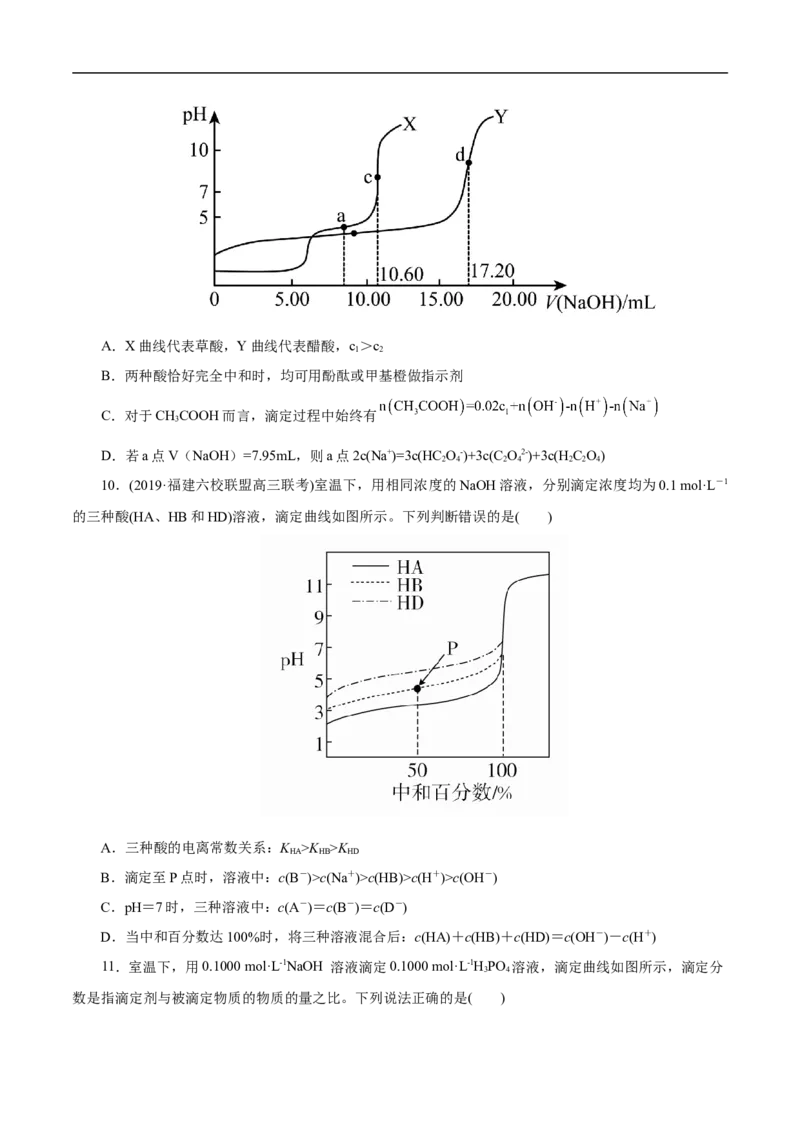
8.(2023届·重庆市高三第一次质量检测联考)常温下,向10mL0.1mol·L-1的草酸(H C O)溶液中逐
2 2 4
滴滴入等浓度的NaOH溶液至过量,用甲基橙(变色范围的pH值为3.1~4.4)作指示剂,并用pH计测定滴定
过程的溶液pH值变化,其滴定曲线如图所示,则下列分析正确的是( )
A.滴入10mL标准NaOH溶液时,溶液颜色由红色变为橙色
B.图中①点所示溶液中:c(HC O)+c(H+)=c(OH-)+c(C O2-)
2 2 4 2 4
C.在①②之间的任意一点,均存在:c(Na+)>c(HC O-)>c(C O2-)>c(H C O)
2 4 2 4 2 2 4
D.图中②点所示的溶液中:2c(Na+)=c(HC O-)+c(C O2-)+c(H C O)
2 4 2 4 2 2 4
9.(2023届·湖南省长沙一中高三模拟)用 的NaOH溶液滴定20.00mL浓度分别为c、
1
c 的醋酸、草酸(H C O)溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。下列
2 2 2 4
叙述不正确的是( )A.X曲线代表草酸,Y曲线代表醋酸,c>c
1 2
B.两种酸恰好完全中和时,均可用酚酞或甲基橙做指示剂
C.对于CHCOOH而言,滴定过程中始终有
3
D.若a点V(NaOH)=7.95mL,则a点2c(Na+)=3c(HC O-)+3c(C O2-)+3c(H C O)
2 4 2 4 2 2 4
10.(2019·福建六校联盟高三联考)室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1
的三种酸(HA、HB和HD)溶液,滴定曲线如图所示。下列判断错误的是( )
A.三种酸的电离常数关系:K >K >K
HA HB HD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
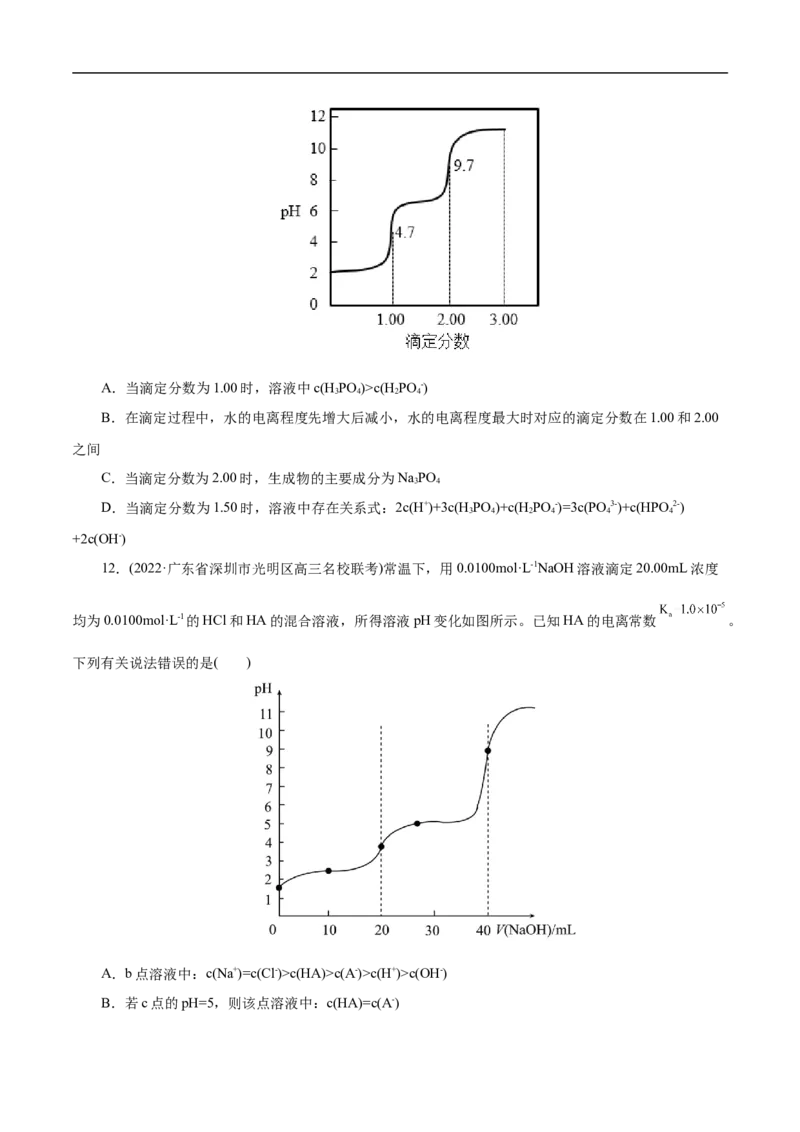
11.室温下,用0.1000 mol·L-1NaOH 溶液滴定0.1000 mol·L-1HPO 溶液,滴定曲线如图所示,滴定分
3 4
数是指滴定剂与被滴定物质的物质的量之比。下列说法正确的是( )A.当滴定分数为1.00时,溶液中c(HPO )>c(H PO -)
3 4 2 4
B.在滴定过程中,水的电离程度先增大后减小,水的电离程度最大时对应的滴定分数在1.00和2.00
之间
C.当滴定分数为2.00时,生成物的主要成分为NaPO
3 4
D.当滴定分数为1.50时,溶液中存在关系式:2c(H+)+3c(H PO )+c(H PO -)=3c(PO3-)+c(HPO 2-)
3 4 2 4 4 4
+2c(OH-)
12.(2022·广东省深圳市光明区高三名校联考)常温下,用0.0100mol·L-1NaOH溶液滴定20.00mL浓度
均为0.0100mol·L-1的HCl和HA的混合溶液,所得溶液pH变化如图所示。已知HA的电离常数 。
下列有关说法错误的是( )
A.b点溶液中:c(Na+)=c(Cl-)>c(HA)>c(A-)>c(H+)>c(OH-)
B.若c点的pH=5,则该点溶液中:c(HA)=c(A-)C.曲线上任何一点溶液中:c(Cl-)=c(A-)+c(HA)
D.在滴定过程中,水的电离程度:d>c>b>a
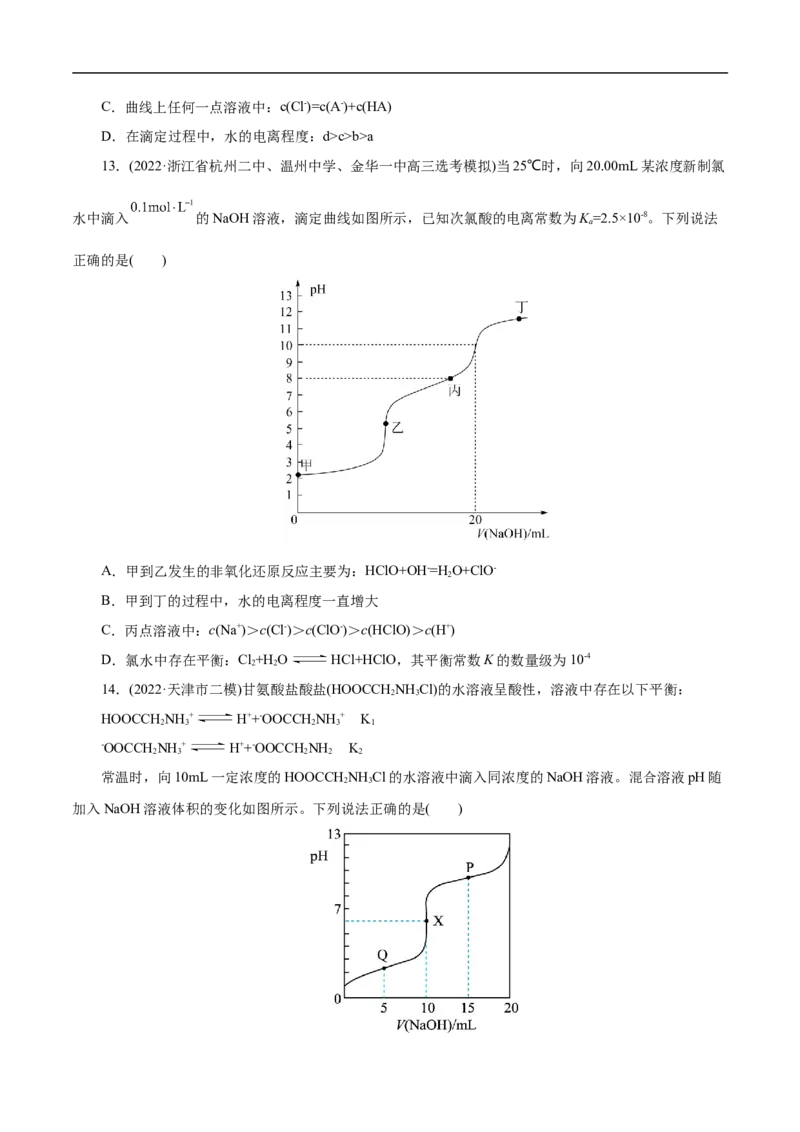
13.(2022·浙江省杭州二中、温州中学、金华一中高三选考模拟)当25℃时,向20.00mL某浓度新制氯
水中滴入 的NaOH溶液,滴定曲线如图所示,已知次氯酸的电离常数为K =2.5×10-8。下列说法
a
正确的是( )
A.甲到乙发生的非氧化还原反应主要为:HClO+OH-=H O+ClO-
2
B.甲到丁的过程中,水的电离程度一直增大
C.丙点溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(HClO)>c(H+)
D.氯水中存在平衡:Cl+H O HCl+HClO,其平衡常数K的数量级为10-4
2 2
14.(2022·天津市二模)甘氨酸盐酸盐(HOOCCH NH Cl)的水溶液呈酸性,溶液中存在以下平衡:
2 3
HOOCCH NH + H++-OOCCH NH + K
2 3 2 3 1
-OOCCH NH + H++-OOCCH NH K
2 3 2 2 2
常温时,向10mL一定浓度的HOOCCH NH Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随
2 3
加入NaOH溶液体积的变化如图所示。下列说法正确的是( )A.水的电离程度:Q>X
B.X→P过程中: 逐渐增大
C.P点的溶液中:c(HOOCCH NH +)+c(H+)=c(-OOCCH NH )+c(OH-)
2 3 2 2
D.当 时,混合溶液中的溶质主要为NaOOCCHNH 和NaCl
2 2
15.298 K时,向20.0 mL 0.10 mol·L-1 HA溶液中滴加0.10 mol·L-1 NaOH溶液,滴定曲线如图所示。
2
下列说法正确的是( )
A.该滴定过程应该选择石蕊溶液作指示剂
B.W点到X点发生的主要反应的离子方程式为HA+2OH-===A2-+2HO
2 2
C.Y点对应的溶液中c(Na+)+c(H+)=c(OH-)+2c(A2-)
D.反应HA+A2- 2HA-的平衡常数K=1.0×107.4
2
16.(2022·浙江省山水联盟高三联考)常温下,用0.10mol/LNaOH溶液分别滴定20.00mL起始浓度
也均为0.1mol/L的一元弱酸HX和HY溶液,已知HX电离程度小于HY,且当 时,可以认为弱
酸达电离平衡时的浓度近似等于起始浓度,其滴定曲线如图所示,下列说法正确的是( )A.图中曲线I对应的为HY,II电离常数为
B.在B 和B 两点对应的溶液中,满足
1 2
C.两条曲线终点坐标分别为C 、C ,两曲线相比,曲线I选用酚酞作终点指示剂误差更小
1 2
D.当溶液pH=7时,曲线Ⅱ加入NaOH物质的量与剩余酸的物质的量之比为1:10