文档内容
专题 01 物质的组成、分类、性质及变化
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 物质的组成分类及变化.......................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
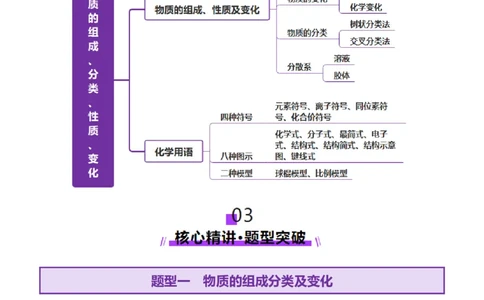
1.物质的宏观组成和微观构成的关系............................................................................................................
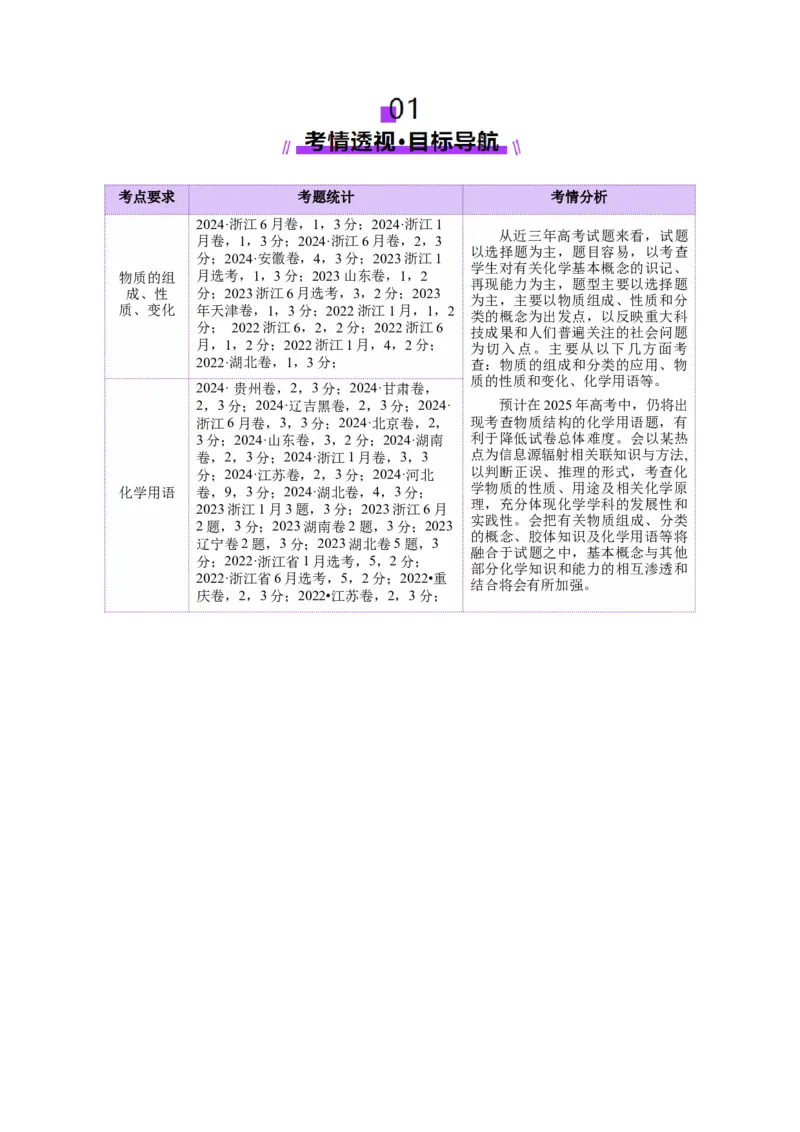
2.物质的分类.....................................................................................................................................................
3.不同类别的无机物之间的转化....................................................................................................................
4.识记易混淆的物理变化、化学变化............................................................................................................
5.胶体的性质及应用.........................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1 物质的组成与分类..................................................................................................................................
考向2 物质的转化..............................................................................................................................................
题型二 化学用语的规范使用.............................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1. 常见的电子式..................................................................................................................................................
2.六种表示物质变化的方程式........................................................................................................................
3.化学用语使用“六”注意............................................................................................................................
【命题预测】...........................................................................................................................................................考点要求 考题统计 考情分析
2024·浙江6月卷,1,3分;2024·浙江1
从近三年高考试题来看,试题
月卷,1,3分;2024·浙江6月卷,2,3
以选择题为主,题目容易,以考查
分;2024·安徽卷,4,3分;2023浙江1
学生对有关化学基本概念的识记、
物质的组 月选考,1,3分;2023山东卷,1,2
再现能力为主,题型主要以选择题
成、性 分;2023浙江6月选考,3,2分;2023
为主,主要以物质组成、性质和分
质、变化 年天津卷,1,3分;2022浙江1月,1,2
类的概念为出发点,以反映重大科
分; 2022浙江6,2,2分;2022浙江6
技成果和人们普遍关注的社会问题
月,1,2分;2022浙江1月,4,2分; 为切入点。主要从以下几方面考
2022·湖北卷,1,3分; 查:物质的组成和分类的应用、物
质的性质和变化、化学用语等。
2024· 贵州卷,2,3分;2024·甘肃卷,
2,3分;2024·辽吉黑卷,2,3分;2024· 预计在2025年高考中,仍将出
浙江6月卷,3,3分;2024·北京卷,2, 现考查物质结构的化学用语题,有
3分;2024·山东卷,3,2分;2024·湖南 利于降低试卷总体难度。会以某热
卷,2,3分;2024·浙江1月卷,3,3 点为信息源辐射相关联知识与方法,
分;2024·江苏卷,2,3分;2024·河北 以判断正误、推理的形式,考查化
学物质的性质、用途及相关化学原
化学用语 卷,9,3分;2024·湖北卷,4,3分;
理,充分体现化学学科的发展性和
2023浙江1月3题,3分;2023浙江6月
实践性。会把有关物质组成、分类
2题,3分;2023湖南卷2题,3分;2023
的概念、胶体知识及化学用语等将
辽宁卷2题,3分;2023湖北卷5题,3
融合于试题之中,基本概念与其他
分;2022·浙江省1月选考,5,2分;
部分化学知识和能力的相互渗透和
2022·浙江省6月选考,5,2分;2022•重
结合将会有所加强。
庆卷,2,3分;2022•江苏卷,2,3分;题型一 物质的组成分类及变化
1.(2024·浙江6月卷,1,3分)按物质组成分类,KAl(SO )·12H O属于( )
4 2 2
A.酸 B.碱 C.盐 D.混合物
【答案】C
【解析】KAl(SO )·12HO是结晶水合物,属于纯净物;是由金属阳离子K+、Al3+和酸根阴离子SO 2-
4 2 2 4
组成的复盐;故选C。2.(2024·浙江1月卷,1,3分)下列物质不属于电解质的是( )
A.CO B. C. D.BaSO
2 4
【答案】A
【解析】A项, CO 在水溶液中能导电,是生成的碳酸电离,不是自身电离,不属于电解质,A符合
2
题意;B.HCl溶于水电离出离子导电,属于电解质,B不符合题意;C.NaOH在水溶液和熔融状态均能
电离离子而导电,属于电解质,C不符合题意;D.BaSO 在熔融状态能电离离子而导电,属于电解质,D
4
不符合题意;故选A。
3.(2024·浙江6月卷,2,3分)下列说法不正确的是( )
A.Al(OH) 呈两性,不能用于治疗胃酸过多
3
B.NaO 能与CO 反应产生O,可作供氧剂
2 2 2 2
C.FeO有还原性,能被氧化成Fe O
3 4
D.HNO 见光易分解,应保存在棕色试剂瓶中
3
【答案】A
【解析】A项,Al(OH) 呈两性,不溶于水,但可以与胃酸反应生成无毒物质,因此其能用于治疗胃酸
3
过多,A不正确;B项,NaO 能与CO 反应产生O,该反应能安全发生且不生成有毒气体,故CO 反应
2 2 2 2 2
产生O 可作供氧剂,B正确;C项,FeO有还原性,其中Fe元素的化合价为+2,用适当的氧化剂可以将其
2
氧化成更高价态的Fe O,C正确;D项,见光易分解的物质应保存在棕色试剂瓶中;Fe O 见光易分解,
3 4 3 4
故其应保存在棕色试剂瓶中,D正确;故选A。
4.(2024·安徽卷,4,3分)下列选项中的物质能按图示路径在自然界中转化。且甲和水可以直接生成
乙的是( )
选项 甲 乙 丙
A Cl NaClO NaCl
2
B SO HSO CaSO
2 2 4 4
C Fe O Fe(OH) FeCl
2 3 3 3D CO HCO Ca(HCO )
2 2 3 3 2
【答案】D
【解析】A项,Cl 与水反应生成HClO和HCl,无法直接生成NaClO,A错误;B项,SO 与水反应生
2 2
成亚硫酸而不是硫酸,B错误;C项,氧化铁与水不反应,不能生成氢氧化铁沉淀,C错误;D项,CO 与
2
水反应生成碳酸,碳酸与碳酸钙反应生成碳酸氢钙,碳酸氢钙受热分解生成二氧化碳气体,D正确;故选
D。
5.(2023·山东卷,1,2分)下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归
为一类的是
A.泰山墨玉 B.龙山黑陶 C.齐国刀币 D.淄博琉璃
【答案】C
【解析】墨玉、黑陶、琉璃均为陶瓷制品,均属于硅酸盐制品,主要成分均为硅酸盐材料,而刀币的
主要成分为青铜,选C。
6.(2022·湖北卷,1,3分)化学与生活密切相关,下列不涉及化学变化的是
A.加入明矾后泥水变澄清 B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜 D.切开的茄子放置后切面变色
【答案】B
【解析】明矾净水的原理为:Al3++3OH- Al(OH) +3H+,Al(OH) 胶体具有吸附性,可以使泥水变澄清,
3 3
涉及化学变化,A错误;水和冰的分子式都是HO,水快速制冰为物理变化,B正确;在炖排骨的过程中,
2
醋会和排骨中在高温下溶解的脂肪进行酯化反应,生成芳香酯,使菜肴的味道更鲜美,涉及化学变化,C
错误;茄子中存在一类叫“酚氧化酶”的物质,它见到氧气之后,发生化学反应产生一些有色的物质。反
应时间越长,颜色越深,D错误。
第一步:读题
(1) 逐字逐句读,挖掘关键字,排除无效信息,找到对解题有价值的信息,并作标记。
(2) 分析题目给出的新信息所考查的内容,对于新信息中所提供的物质要从性质与应用的角度分析。
第二步:联题
(1) 结合题目中的问题或选项分析本题考查的知识板块。
(2) 联系中学化学知识体系中的“知识块”和“化学性质”,找准提取信息 ( 知识、性质、用途 ) 的方向 。
第三步:析题
(1) 思维从新情境回归教材、回归平时学习中。
(2) 回顾解同类题易犯的错误,易漏知识等。
第四步:解题(1) 解题要抓住题目要求和关键词,如“不正确”与“正确”;“一定”与“可能”等易看错内容。
(2) 熟记日常生活中常见物质的重要应用及典型化工流程的基本原理。
1 .物质的宏观组成和微观构成的关系
【易错提醒】
①物质的组成可概括为“宏观一素(元素)、微观六子(原子、分子、离子、质子、中子、电子)”。
②由原子或离子构成的单质和化合物均用化学式表示。
③几乎所有的酸都是共价化合物,都有确定的分子式。
2 .物质的分类
【易错提醒】
(1)由同种元素组成的物质不一定是纯净物。如由O、O 组成的气体就是混合物。
2 3
(2)一种分子式不一定只表示一种物质。如分子式为C H 的结构有正丁烷和异丁烷。
4 10
(3)NO 不属于酸性氧化物。
2
(4)能与酸反应生成盐和水的氧化物就是碱性氧化物,如NaO 不属于碱性氧化物。
2 2
(5)酸性氧化物不一定是非金属氧化物,如MnO 属于酸性氧化物。
2 7
(6)酸的元数与酸的结构中羟基氢原子个数相同,不可简单地认为分子中有几个氢原子就是几元酸。如
HPO 中只有一个羟基氢,为一元酸。
3 23 .不同类别的无机物之间的转化
(1)金属单质及其化合物的转化
金属单质――→碱性氧化物――→碱――→盐
如:Na――→NaO――→NaOH――→NaSO
2 2 4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
(2)非金属单质及其化合物的转化
非金属单质――→酸性氧化物――→酸――→盐
如:S――→SO ――→HSO ――→NaSO
2 2 3 2 3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
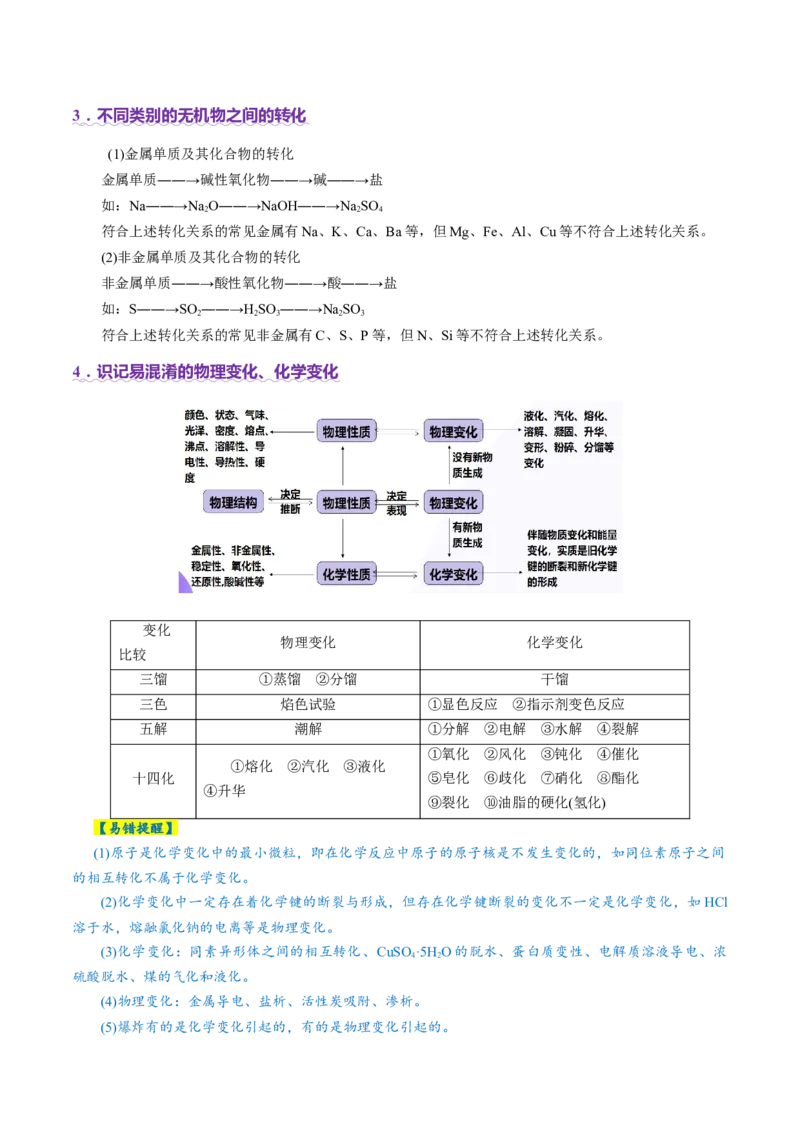
4 .识记易混淆的物理变化、化学变化
变化
物理变化 化学变化
比较
三馏 ①蒸馏 ②分馏 干馏
三色 焰色试验 ①显色反应 ②指示剂变色反应
五解 潮解 ①分解 ②电解 ③水解 ④裂解
①氧化 ②风化 ③钝化 ④催化
①熔化 ②汽化 ③液化
十四化 ⑤皂化 ⑥歧化 ⑦硝化 ⑧酯化
④升华
⑨裂化 ⑩油脂的硬化(氢化)
【易错提醒】
(1)原子是化学变化中的最小微粒,即在化学反应中原子的原子核是不发生变化的,如同位素原子之间
的相互转化不属于化学变化。
(2)化学变化中一定存在着化学键的断裂与形成,但存在化学键断裂的变化不一定是化学变化,如HCl
溶于水,熔融氯化钠的电离等是物理变化。
(3)化学变化:同素异形体之间的相互转化、CuSO ·5H O的脱水、蛋白质变性、电解质溶液导电、浓
4 2
硫酸脱水、煤的气化和液化。
(4)物理变化:金属导电、盐析、活性炭吸附、渗析。
(5)爆炸有的是化学变化引起的,有的是物理变化引起的。5 .胶体的性质及应用
(1)胶体与其他分散系的本质区别是分散质粒子直径的大小(1~100 nm之间),胶体的特性是丁达尔效应;
用渗析法可将胶体粒子和溶液中的溶质粒子进行分离,利用丁达尔效应可以区分胶体和溶液。
(2)胶体不带有电荷,但是某些胶体中的粒子带有电荷。部分有机高分子形成的胶体中,分散质粒子不
带电荷,如淀粉溶液。
(3)Fe(OH) 胶体粒子为多个“Fe(OH) 分子”的集合体,因此1 mol Fe3+完全水解得到的Fe(OH) 胶体粒
3 3 3
子少于1 mol。
(4)部分铝盐、铁盐如KAl(SO )·12H O、FeCl ·6H O等溶于水电离出的Al3+、Fe3+水解生成Al(OH) 胶
4 2 2 3 2 3
体、Fe(OH) 胶体,这些胶体能吸附悬浮固体或色素形成沉淀而除杂,因此常用作净水剂。
3
(5)常见的胶体有云、烟、雾、蛋白质溶液、豆浆、牛奶、血浆、土壤胶体、淀粉溶液、有色玻璃等。
【易错提醒】
(1)利用丁达尔效应可以快速鉴别溶液与胶体,但胶体区别于其他分散系的本质特征是胶体粒子的直径
介于1~100 nm之间,而不是丁达尔效应。
(2)胶体微粒一般是离子、分子或难溶物的聚集体,在Fe(OH) 胶体中,Fe(OH) 胶体粒子的数目要远远
3 3
小于原FeCl 溶液中Fe3+的数目。
3
(3)胶体不带电荷,胶体粒子(分散质)带电荷,但淀粉胶体的胶体粒子也不带电荷。
(4)胶粒有很大的比表面积,吸附能力很强。
考向 1 物质的组成与分类
1.[原创题]下列物质中,属于纯净物的是( )
A.纯净空气 B.液氯 C.盐酸 D.软锰矿
【答案】B
【解析】由一种物质组成的是纯净物,由两种或两种以上物质组成的是混合物;空气为混合物,盐酸
为溶液,软锰矿含有多种物质,二者均为混合物;液氯是氯气分子组成的纯净物;故选B。
2.(2025·浙江省名校协作体三开学测试)硫酸铜铵晶体[(NH )Cu(SO )·6H O]属于( )
4 2 4 2 2
A.酸 B.碱 C.盐 D.混合物
【答案】C
【解析】由化学式可知,硫酸铜铵晶体属于复盐,故选C。
3.[新考法](2025·浙江省第二届辛愉杯高三线上模拟考试)下列物质中,不属于配合物的是( )
A.NaAlF B.(NH )C O C.CuSO ·5H O D.[Ag(NH )]OH
3 6 4 2 2 4 4 2 3 2
【答案】B【解析】A项,该物质中,铝离子提供空轨道,氟元素提供孤电子对而形成配位键,所以该物质属于
配合物,故A不选;B项,(NH )C O 属于一般化合物,不含配体,所以不属于配合物,故 B选;C项,
4 2 2 4
CuSO ·5H O以[Cu(HO ]SO ·H O形式存在,四个水分子与铜离子以配位键结合,形成配合物,故C不选;
4 2 2 )4 4 2
D项,该物质中,银离子提供空轨道,NH 中氮原子提供孤电子对而形成配位键,所以该物质属于配合物,
3
故D不选;故选B。
4.[新题型](2025·贵州省贵阳市清华中学月考)近两年,贵阳已然成为全国热门旅游城市,“糯米饭”、
“盐菜脆哨炒饭”、“红糖冰粉”、“酸汤牛肉”、“豆米火锅”等成为游客最为喜爱的美食,下列关于
食品中化学知识说法正确的是( )
A.牛肉中富含的蛋白质属于无机物
B.糯米中富含的微量元素——锌元素存在形式为单质
C.食盐中添加的碘酸钾(KIO )属于无机盐
3
D.红糖水溶液属于混合物,是一种分散系,属于液溶胶
【答案】C
【解析】A项,牛肉中富含的蛋白质属于有机物,A不正确;B项,易被人体吸收的元素通常以易溶
于水的化合物形式存在,糯米中富含的微量元素——锌元素存在形式为化合物,B不正确;C项,食盐中
添加的碘酸钾(KIO )中不含碳元素,属于无机盐,C正确;D项,红糖水溶液属于混合物,是一种分散系,
3
其分散质粒子直径小于1nm,属于溶液,D不正确;故选C。
5.(2025·浙江省强基联盟高三10月联考)下列依据不同角度的分类正确的是( )
A.SiO 既能与氢氟酸反应,又能与氢氧化钠溶液反应,SiO 属于两性氧化物
2 2
B.“长征七号”采用了液氧煤油发动机,煤油是混合物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据物质能否电离,将其分为强电解质和弱电解质
【答案】B
【解析】A项,SiO 能与氢氟酸反应,但并非产生盐和水,A错误;B项,“长征七号”采用了液氧
2
煤油发动机,煤油是石油分分馏产品,是混合物,B正确;C项,根据分散质微粒直径大小,将分散系分
为溶液、胶体和浊液,C错误;D项,根据电解质的电离程度,将其分为强电解质和弱电解质,D错误;
故选B。
考向 2 物质的转化
6.下列变化不能通过一步反应实现的是( )
A.NaCO→NaOH B.Cu→CuCl C.Fe→Fe O D.Fe O→Fe(OH)
2 3 2 3 4 2 3 3
【答案】D
【解析】A项,NaCO +Ba(OH) =BaCO ↓+2NaOH,正确;B项,Cu+Cl====CuCl ,正确;C项,
2 3 2 3 2 23Fe+2O====Fe O ,正确;D项,氧化铁不溶于水,不能一步转化为氢氧化铁,可以通过:Fe O +6HCl
2 3 4 2 3
=2FeCl +3HO、FeCl +3NaOH=FeCl +Fe(OH) ↓,实现转化,错误。
3 2 3 3 3
7.(2025·广东省肇庆市高一统测)下列物质转化(“→”表示一种物质转化为另一种物质),每次转化只通
过一步反应,不可能全部实现的是( )
A.HO→O→CO→HCO B.NaOH→NaNO →NaCO→NaCl
2 2 2 2 2 3 3 2 3
C.CaCO →CaO→Ca(OH) →NaOH D.Mg→MgCl →Mg(OH) →MgSO
3 2 2 2 4
【答案】B
【解析】A项,HO 在MnO 催化下分解产生O,O 与C点燃时反应产生CO,CO 溶于水,与水反
2 2 2 2 2 2 2
应产生HCO,可见在物质转化中,每次转化都是通过一步反应实现,A不符合题意;B项,NaNO 不能
2 3 3
一步反应转化为NaCO,B符合题意;C项,CaCO 高温煅烧分解产生CaO、CO,CaO与水反应产生
2 3 3 2
Ca(OH) ,Ca(OH) 与NaCO 反应产生CaCO 和NaOH,可见在物质转化中,每次转化都是通过一步反应
2 2 2 3 3
实现,C不符合题意;D项,Mg与HCl反应产生MgCl 和H,MgCl 和NaOH反应产生Mg(OH) 和
2 2 2 2
NaCl,Mg(OH) 和硫酸发生中和反应产生MgSO ,可见在物质转化反应中,每次转化都可以通过一步反应
2 4
实现,D不符合题意;故选B。
8.(2025·河南省驻马店市联考)下列物质在给定条件下的转化均能一步实现的是( )
A. B.
C. D.
【答案】A
【解析】A项,Cu与O 反应可生成CuO,CuO溶于HSO 生成CuSO 等,A符合题意;B项,在
2 2 4 4
MnO 的催化作用下,HO 分解生成O,不生成H,B不符合题意;C项,C在O 中不充分燃烧生成
2 2 2 2 2 2
CO,CO与水反应不能生成HCO,C不符合题意;D项,Fe与HCl反应生成FeCl 等,不能直接生成
2 3 2
FeCl ,D不符合题意;故选A。
3
9.[新题型](2025·黑龙江省齐齐哈尔市八中高一月考)下图是单质到盐的转化关系,X为金属单质Na、
A为非金属单质S,C为HSO ,C与Z反应生成 ,下列说法不正确的是( )
2 3
A.D为NaSO B. 与 反应生成盐
2 4
C.Z与B反应生成盐和水 D.W与C可以反应生成盐
【答案】A
【解析】X为金属单质Na,则Y是NaO、Z是NaOH、W是NaCO;A为非金属单质S,C为
2 2 3
HSO ,C与Z反应生成D,则B是SO 、D是NaSO 。A项,C为HSO 、Z是NaOH,C与Z反应生成
2 3 2 2 3 2 3D,D为NaSO ,故A错误;B项,Y是NaO、B是SO ,Y与B反应生成盐NaSO ,故B正确;C项,
2 3 2 2 2 3
Z是NaOH、B是SO ,Z与B反应生成NaSO 和水,故C正确;D项,W是NaCO、C为HSO ,W与
2 2 3 2 3 2 3
C可以反应生成NaSO 、二氧化碳、水,故D正确;故选A。
2 3
10.下表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是( )
选项 甲 乙 丙 丁
A CO CaCO HO O
2 3 2 2
B NaOH NaCl CO NaCO
2 2 3
C HO HO O MgO
2 2 2 2
D CaO Ca(OH) HO CaCl
2 2 2
【答案】A
【解析】二氧化碳与氢氧化钙反应能一步得到碳酸钙,碳酸钙与稀盐酸反应能一步得到水,水通电分
解能一步得到氧气,氧气和碳反应能一步得到二氧化碳,A符合题意;氯化钠不能通过一步反应得到二氧
化碳,B不符合题意;氧化镁不能通过一步反应得到过氧化氢,C不符合题意;水不能通过一步反应得到
氯化钙,氯化钙也不能通过一步反应得到氧化钙,D不符合题意。
题型二 化学用语
1.(2024· 贵州卷,2,3分)下列叙述正确的是( )
A.KBr的电子式:
B.聚乙炔的结构简式:
C.SO 2-的空间结构:平面三角形
3
D.CHCHC(CH)=CH 的名称:2-甲基-2-丁烯
3 2 3 2
【答案】B
【解析】A项,KBr的电子式为 ,A错误;B项,聚乙炔的结构为单双键交替结构,结构简式为 ,B正确;C项,SO 2-中心原子的价层电子对数为4,孤电子对数为1,空
3
间结构为三角锥形,C错误;D项,CHCHC(CH)=CH 的系统命名为2-甲基-1-丁烯,D错误;故选B。
3 2 3 2
2.(2024·甘肃卷,2,3分)下列化学用语表述错误的是( )
A.Ca2+和Cl-的最外层电子排布图均为
B.PH 和HS的电子式分别为 和
3 2
C.CH=CHCHCHCH 的分子结构模型为
2 2 2 3
D.12C、13C和14C互为同位素
6 6 6
【答案】B
【解析】A项,Ca2+和Cl-的核外电子数都是18,最外层电子排布图均为 ,故
A正确;B项,PH 中磷原子和每个氢原子共用一对电子,中心原子P原子价层电子对数为3+ ×(5-
3
3×1)=4,孤电子对数为1,PH 的电子式为 ,故B错误;C项,CH=CHCHCHCH 分子中存在
3 2 2 2 3
1个碳碳双键,位于1号碳原子与2号碳原子之间,存在3个碳碳单键,无支链,且氢原子半径小于碳原子
半径,其分子结构模型表示为 ,故C正确;D项,12C、13C和14C是质子数相
6 6 6
同、中子数不同的碳原子,是碳元素的不同核素,互为同位素,故D正确;故选B。
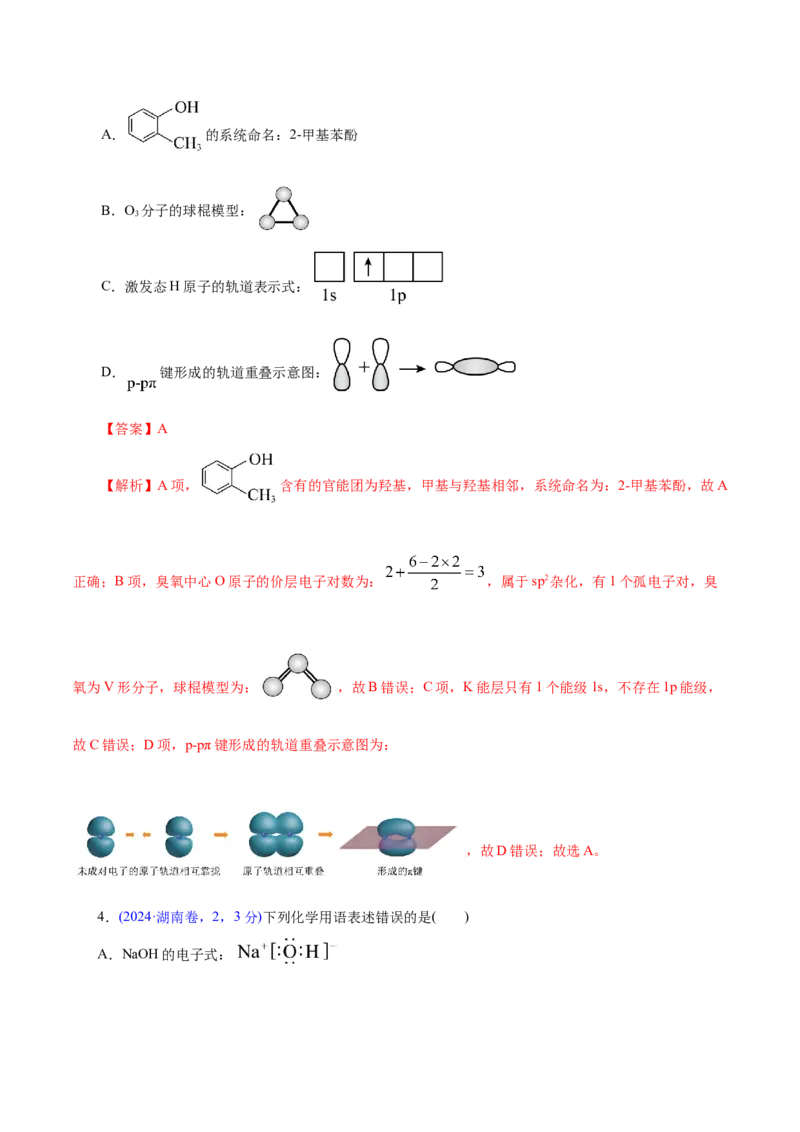
3.(2024·山东卷,3,2分)下列化学用语或图示正确的是( )A. 的系统命名:2-甲基苯酚
B.O 分子的球棍模型:
3
C.激发态H原子的轨道表示式:
D. 键形成的轨道重叠示意图:
【答案】A
【解析】A项, 含有的官能团为羟基,甲基与羟基相邻,系统命名为:2-甲基苯酚,故A
正确;B项,臭氧中心O原子的价层电子对数为: ,属于sp2杂化,有1个孤电子对,臭
氧为V形分子,球棍模型为: ,故B错误;C项,K能层只有1个能级1s,不存在1p能级,
故C错误;D项,p-pπ键形成的轨道重叠示意图为:
,故D错误;故选A。
4.(2024·湖南卷,2,3分)下列化学用语表述错误的是( )
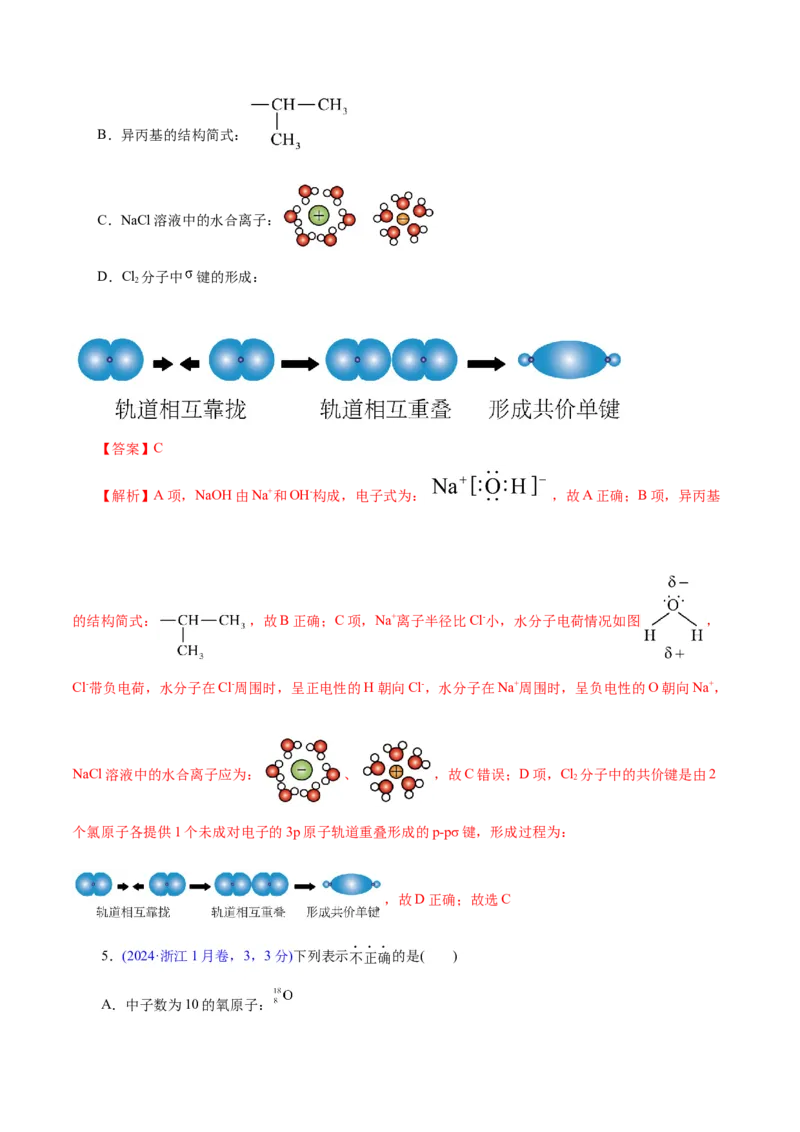
A.NaOH的电子式:B.异丙基的结构简式:
C.NaCl溶液中的水合离子:
D.Cl 分子中 键的形成:
2
【答案】C
【解析】A项,NaOH由Na+和OH-构成,电子式为: ,故A正确;B项,异丙基
的结构简式: ,故B正确;C项,Na+离子半径比Cl-小,水分子电荷情况如图 ,
Cl-带负电荷,水分子在Cl-周围时,呈正电性的H朝向Cl-,水分子在Na+周围时,呈负电性的O朝向Na+,
NaCl溶液中的水合离子应为: 、 ,故C错误;D项,Cl 分子中的共价键是由2
2
个氯原子各提供1个未成对电子的3p原子轨道重叠形成的p-pσ键,形成过程为:
,故D正确;故选C
。
5.(2024·浙江1月卷,3,3分)下列表示不正确的是( )
A.中子数为10的氧原子:B.SO 的价层电子对互斥(VSEPR)模型:
2
C.用电子式表示KCl的形成过程:
D. 的名称: 甲基 乙基戊烷
【答案】D
【解析】A项, 质子数为8,质量数为18,根据质量数=质子数+中子数,可算得中子数为10,A
正确;B项,SO 中心原子S价层电子对数: ,其价层电子对互斥(VSEPR)模型为平面三
2
角形,B正确;C项,KCl为离子化合物,其电子式表示形成过程: ,
C正确;D项,有机物 主链上有6个碳原子,第2、4号碳原子上连有甲基,命名
为:2,4-二甲基己烷,D错误;故选D。
6.(2024·湖北卷,4,3分)化学用语可以表达化学过程,下列化学用语表达错误的是( )
A.用电子式表示 的形成:
B.亚铜氨溶液除去合成氨原料气中的CO:[Cu(NH )]2++CO+NH= [Cu(NH )CO]2+
3 2 3 3 3
C.用电子云轮廓图示意 键的形成:
D.制备芳纶纤维凯芙拉:
【答案】B【解析】A项,氯元素为VIIA族元素,最外层电子数为7,Cl原子与Cl原子共用1对电子形成Cl,
2
电子式表示Cl 的形成过程为: ,A正确;B项,亚铜氨中铜元素的化合价为+1价,
2
而[Cu(NH )]2+中铜元素为+2价,亚铜氨溶液除去合成氨原料气中的CO的原理为:[Cu(NH )]++CO+NH=
3 2 3 2 3
[Cu(NH )CO]+,B错误;C项,π键是由两个原子的p轨道“肩并肩”重叠形成的,用电子云轮廓图表示p-
3 3
pπ键的形成为 ,C正确; D项,
的氨基和 的羧基发生缩聚反应生成高聚物 和水,其
反应的化学方程式为 ,
D正确; 故选B。
1 .电子式:首先要分清书写的对象是离子化合物还是共价化合物,前者存在离子,后者不存在离子 ;
其次对共价型分子,可以先写出结构式,这样可确定分子式中共用电子对的数目,然后再写出电子式,写
完以后,应检查一下每个原子是否达到 8 电子稳定结构 (H 为 2 电子稳定结构 ) ,以防止漏掉一些未成键的电
子对。
2 .球棍模型和比例模型:首先应明确两者的区别,球棍模型存在“棍”而比例模型不存在;其次应
弄清分子的空间构型是否正确;最后应弄清分子中所含几种原子的大小是否正确。
3 .结构式或结构简式:首先应明确两者的区别——结构式必须显示出所有的价键,结构简式一般要
去掉所有的单键,但双键、叁键不能省;其次应根据价键规则 (C—4 键, N—3 键, O 、 S—2 键, H 、 C l 、
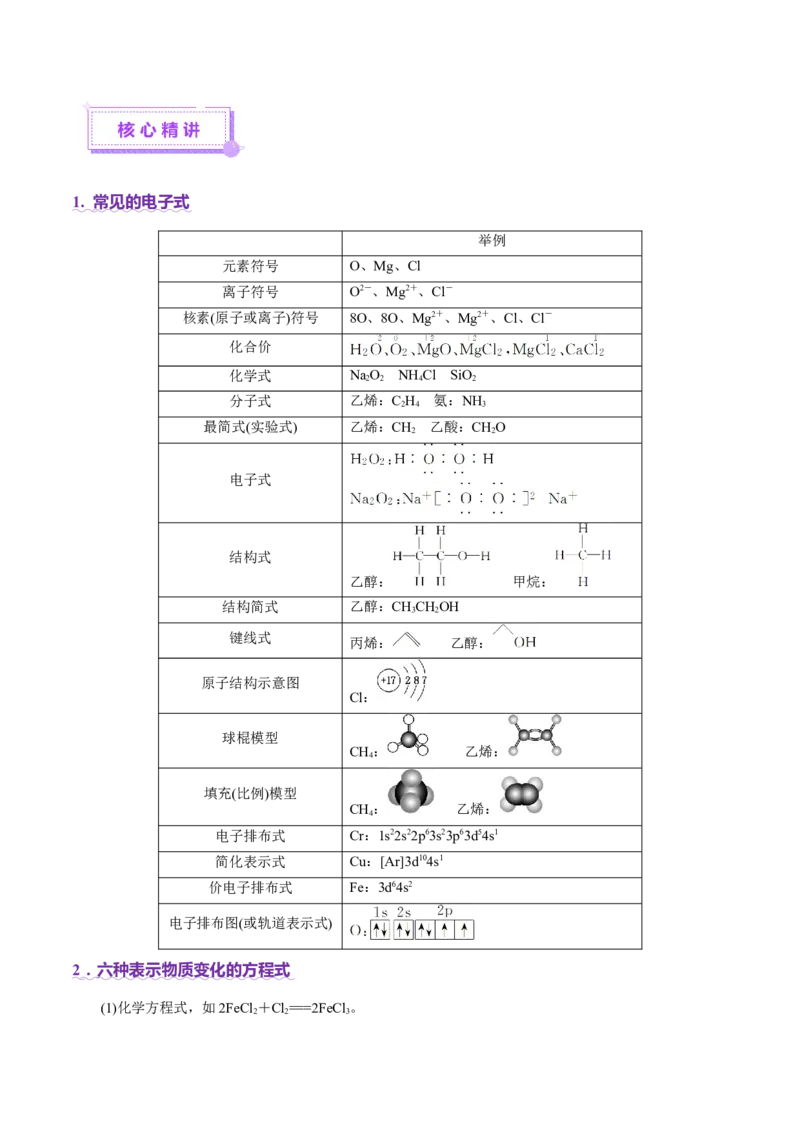
Br—1 键 ) 明确共价键的数目、元素的位置。1. 常见的电子式
举例
元素符号 O、Mg、Cl
离子符号 O2-、Mg2+、Cl-
核素(原子或离子)符号 8O、8O、Mg2+、Mg2+、Cl、Cl-
化合价
化学式 NaO NH Cl SiO
2 2 4 2
分子式 乙烯:C H 氨:NH
2 4 3
最简式(实验式) 乙烯:CH 乙酸:CHO
2 2
电子式
结构式
乙醇: 甲烷:
结构简式 乙醇:CHCHOH
3 2
键线式
丙烯: 乙醇:
原子结构示意图
Cl:
球棍模型
CH: 乙烯:
4
填充(比例)模型
CH: 乙烯:
4
电子排布式 Cr:1s22s22p63s23p63d54s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图(或轨道表示式)
2 . 六种表示物质变化的方程式
(1)化学方程式,如2FeCl +Cl===2FeCl 。
2 2 3(2)离子方程式,如2Fe2++Cl===2Fe3++2Cl-。
2
(3)热化学方程式,如2H(g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1。
2 2 2
(4)电离方程式,如CHCOOHH++CHCOO-。
3 3
(5)电极反应式,如钢铁的吸氧腐蚀,负极:2Fe-4e-===2Fe2+;正极:O+4e-+2HO===4OH-。
2 2
(6)电解方程式,如2NaCl+2HO=====2NaOH+Cl↑+H↑。
2 2 2
【易错提醒】
电子式书写六注意
(1)分清化合物的类型:如HO 的电子式为 ,而不是 。
2 2
(2)确认原子周围的电子数:如CO 的电子式为 ,而不是 。
2
(3)理清原子间的连接顺序:如HClO的电子式为 ,而不是 。
(4)不能因同种微粒而合并:如NaS的电子式为 ,而不是 。
2
(5)不能漏掉未成键电子对:如NH 的电子式为 ,而不是 。
3
(6)区别对待阴离子及复杂阳离子:如 NH Cl 的电子式为 ,而不是
4
或 。
3 .化学用语使用“六”注意
(1)电子式:离子带电荷,原子团不显电性。如OH-为[OH]-,—OH为·OH。
(2)书写化合物的电子式时要切实注意:①明确是离子化合物还是共价化合物;②切勿漏掉未成键电子
对;③理清原子的排列顺序,如HOCl。
(3)结构简式需保留官能团,如CHCH ,不能写成CHCH ,还要注意有机物中原子的连接情况,如
2 2 2 2
(4)各“式”切勿张冠李戴:是名称还是化学式,是分子式还是实验式,是结构式还是结构简式,是原
子结构示意图还是离子结构示意图,是化学方程式还是离子方程式等。
(5)化学方程式或离子方程式要遵守质量守恒,化学计量数要最简,注明反应条件并注意“↑”“↓”
“ ”“===”“―→”符号的使用。
(6)混淆电离方程式和水解方程式而导致错误。如HS-+HO HO++S2-是HS-的电离方程式,HS
2 3-+HO HS+OH-是HS-的水解方程式。
2 2
1.(2025·浙江省新阵地教育联盟高三第一次联考)下列化学用语表示正确的是( )
A.中子数为20的氯离子:
B.Cl 分子中化学键的电子云轮廓图:
2
C.CO2-的价层电子对互斥模型:
3
D.用电子式表示KS的形成过程:
2
【答案】D
【解析】A项,质子数为17、中子数为20的氯离子表示为:37 Cl-,A错误;B项,Cl 分子中化学键
17 2
是p-pσ键,轮廓图为 ,B错误;C项,CO2-的成键电子对是3,孤对电子为0,价
3
层电子对为3,为平面三角形,C错误;D项,KS中K失电子形成K+,S得到电子,形成S2-,K+和S2-通
2
过离子键结合,形成过程为: ,D正确;故选D。
2.(2025·陕西省宝鸡中学高三月考)下列化学用语表示正确的是( )
A.SO 的VSEPR模型:
3
B.顺-2-丁烯的球棍模型:C.一元酸次磷酸(H PO )的结构简式为:
3 2
D.牙膏中添加氟元素的原理:
【答案】D
【解析】A项,SO 的中心原子为S原子,价层电子对为3+ ,VSEPR模型为平面三角形,
3
A错误:B项,顺-2-丁烯的球棍模型中H原子在双键的同一侧,B错误;C项,一元酸次磷酸(H PO )中和
3 2
O原子成键的H原子只有1个,结构简式为: ,B错误;D项,牙膏中添加氟元素使羟基磷酸
钙转化为更难溶的氟磷酸钙,发生沉淀的转化,方程式为:
,D正确;故选D。
3.(2025·河南省豫西北教研联盟高三一模)下列化学用语或图示表达正确的是( )
A.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
B.NaCl溶液中的水合离子:
C.HClO的电子式:
D.聚丙烯的结构简式:
【答案】C
【解析】A项,原子半径:Cl>C>H,因此该模型可表示甲烷,但不能表示四氯化碳,故A错误;B
项,NaCl溶液中存在水合钠离子和水合氯离子,水分子中存在O-H极性键,O带部分负电荷、H带部分正
电荷,氯离子半径大于钠离子,氯离子带负电荷,钠离子带正电荷,则水合钠离子中吸引的是水分子中的
氧原子端、水合氯离子中氯离子吸引的是水分子中的氢原子端,图中显示的错误有:钠离子半径大于氯离
子、钠离子吸引了氢原子、氯离子吸引了氧原子,故B错误;C项,HClO的结构式和电子式依次为H-O-Cl、 ,故C正确;D项,聚丙烯的结构简式: ,故D错误;故选C。
4.(2025·浙江省天域全国名校协作体高三联考)下列说法不正确的是( )
A. 的名称为:3,3-甲基戊烷
B.氨基的电子式:
C.基态碳原子的价电子轨道表示式为:
D.HCl分子σ键电子云轮廓图:
【答案】A
【解析】A项, 的名称为:3,3-二甲基戊烷,A错误;B项,氨基的电子式为 ,B
正确;C项,基态碳原子的价电子排布式为2s22p2,轨道表示式为 ,C正确;D项,
HCl分子中s电子云与p电子云头碰头重叠形成 键,电子云轮廓图为 ,D正确;故选A。
5.[新题型](2025·北京市十一学校高三月考)下列化学用语或图示表达正确的是( )
A.sp2杂化轨道示意图:
B.激发态H原子的轨道表示式:
C.N 的p-pσ键的形成:
2
D.电子式表示MgCl 形成过程:
2
【答案】A【解析】A项,sp2杂化形成的原子轨道为平面三角形,其杂化轨道示意图为 ,A正确;B
项,K层只有s能级,没有p能级,则H原子1s能级上的电子可以跃迁到L能层的s能级或p能级上,B
错误;C项,N 的p-pσ键是头碰头方式重叠形成,电子云图为 ,C错误;D项,MgCl 为
2 2
离子化合物,用电子式表示其形成过程时,应该是Mg失去电子,Cl得到电子:
,D错误;故选A。
6.(2025·辽宁省沈阳市二模)下列化学用语或图示表述正确的是( )
A.激发态H原子的轨道表示式:
B.邻羟基苯甲醛分子内氢键示意图:
C.基态As原子的简化电子排布式为[Ar]4s24p3
D.CN-的电子式为
【答案】D
【解析】A项,K能层只有1个能级1s,不存在1p能级,H原子的1s能级上的电子可以跃迁到L能
层的s能级或p能级上,故A错误;B项,邻羟基苯甲醛分子中羟基和醛基能形成分子内氢键,氢键示意
图为 ,故B错误;C项,砷元素的原子序数为33,位于第四周期第ⅤA族,基态As原子的简
化电子排布式为[Ar]3d104s24p3,故C错误;D项,CN-中C与N共用三对电子,电子式为 ,
故D正确;故选D。
7.(2025·河北省石家庄市高三联考)化学用语可以表达化学过程,下列化学用语表达错误的是( )A.用电子式表示Cl 的形成:
2
B.用电子云轮廓图表示H-Cl的s-pσ键的形成:
C.NaCl溶液中的水合离子:
D.SO 的VSEPR模型为
3
【答案】C
【解析】A项,Cl 形成时两个Cl原子间形成一对共用电子对,电子式表示为:
2
,A不符题意;B项,H原子和Cl原子形成HCl分子时,H原子的1s轨道
与Cl原子的3p轨道通过“头碰头”的形式形成s-pσ键,电子云轮廓图表示为:
,B不符题意;C项,NaCl溶液中Na+周围有5个水分子,Cl-周围
有6个水分子,则氯化钠在水中能形成自由移动的水合氯离子 和水合钠离子 ,C符合
题意;D项,SO 中心原子S价层电子对数: ,无孤电子对,其VSEPR模型为平面三角
3
形,D不符题意;故选C。
8.[原创题]下列表示不正确的是( )
A.HF分子中 键的形成示意图为
B.基态Cr原子的价层电子轨道表示式为C.邻羟基苯甲醛分子内氢键可表示为
D. 的名称:1,3,4-三甲苯
【答案】D
【解析】HF分子中的σ键是H原子的s轨道和F原子的p轨道“头碰头”重叠而成的,HF分子中σ
键的形成示意图为 ,A项正确。基态Cr原子为24号元素,价电子排
布式为3d54s1,价层电子的轨道表示式为 ,B项正确。邻羟基苯甲醛分子内
羟基H原子与醛基中O原子之间形成氢键,结构式为 ,C项正确。 的名
称为1,2,4-三甲苯,D项错误。