文档内容
1.下列反应的离子方程式书写不正确的是( )
A.向氯化铝溶液中加入过量的氨水:Al3++3NH·H O= Al(OH) ↓+3NH+
3 2 3 4
B.用氨水吸收过量的二氧化硫:NH·H O+SO = NH+ +HSO -
3 2 2 4 3
C.向偏铝酸钠溶液中加入过量的稀盐酸:AlO -+H++H O= Al(OH) ↓
2 2 3
D.向次氯酸钠溶液中通入少量二氧化碳:2ClO-+CO +H O=2HClO +CO 2-
2 2 3
【答案】C
2.下列各组粒子在溶液中可以大量共存,且加入或通入试剂X后,发生反应的离子方程式也正确的是
选项 微粒组 加入试剂 发生反应的离子方程式
[来源:学科网ZXXK]
A K+、Na+、HCO -、SiO2- 少量HCl 2H++SiO 2-=H SiO↓
3 3 3 2 3
B NH +、Fe2+、Br-、SO 2- 过量HS Fe2++H S=FeS↓+2H+
4 4 2 2
C HClO、Na+、Fe3+、SO 2- 过量CaCl Ca2++ SO 2-=CaSO ↓
3 2 3 3
D I-、Cl-、H+、SO 2- 适量NaNO 6I-+2NO-+8H+=2NO↑+4HO+3I
4 3 3 2 2
【答案】D
【解析】A.由于酸性HCO ->H SiO,所以在溶液中会发生反应:2HCO -+SiO 2-=H SiO↓+CO 2-,二者不能大量
3 2 3 3 3 2 3 3
共存,A错误;B.因FeS与可与强酸反应,所以不能发生Fe2+与过量HS的反应,B错误;C.HClO、Fe3+都具有
2
强的氧化性,可将SO 2-氧化为SO 2-,不能大量共存,C错误;D.四种离子互不反应,在溶液中可以大量共存,I-
3 4
具有还原性,在酸性条件下,H+ 、I-、NO -发生氧化还原反应,根据电子守恒、电荷守恒及原子守恒,可得方程
3
式为:6I-+2NO-+8H+=2NO↑+4HO+3I ,D正确。
3 2 2
3.常温下,下列各组离子(或在指定条件下)能大量共存的是
A.中性溶液:Na+、Fe3+、Cl-、NO -
3
B.NH +、Na+、NO -、SiO2-
4 3 3C.由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Na+、Mg2+、Cl-、HCO -
3
D.使pH 试纸显蓝色的溶液中:K+、Na+、OH-、SO 2-
4
【答案】D
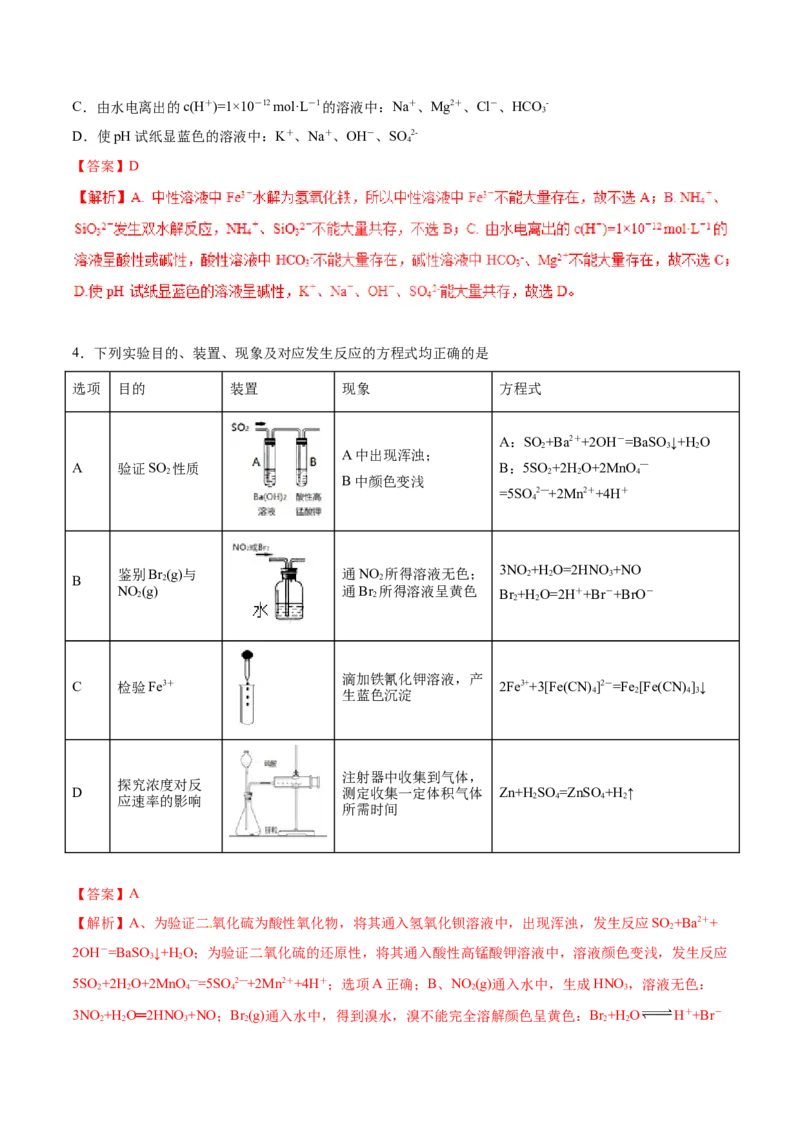
4.下列实验目的、装置、现象及对应发生反应的方程式均正确的是
选项 目的 装置 现象 方程式
A:SO +Ba2++2OH-=BaSO ↓+H O
2 3 2
A中出现浑浊;
A 验证SO 性质 B:5SO +2H O+2MnO —
2 2 2 4
B中颜色变浅
=5SO2—+2Mn2++4H+
4
B 鉴别Br 2 (g)与 通NO 2 所得溶液无色; 3NO 2 +H 2 O=2HNO 3 +NO
[来源:学。科。网
Z。X。X。K] NO 2 (g) 通Br 2 所得溶液呈黄色 Br 2 +H 2 O=2H++Br-+BrO-
滴加铁氰化钾溶液,产
C 检验Fe3+ 2Fe3++3[Fe(CN)]2-=Fe [Fe(CN) ]↓
生蓝色沉淀 4 2 4 3
注射器中收集到气体,
探究浓度对反
D 测定收集一定体积气体 Zn+H SO =ZnSO +H ↑
应速率的影响 2 4 4 2
所需时间
【答案】A
【解析】A、为验证二氧化硫为酸性氧化物,将其通入氢氧化钡溶液中,出现浑浊,发生反应SO +Ba2++
2
2OH-=BaSO ↓+H O;为验证二氧化硫的还原性,将其通入酸性高锰酸钾溶液中,溶液颜色变浅,发生反应
3 2
5SO +2H O+2MnO —=5SO2—+2Mn2++4H+;选项A正确;B、NO (g)通入水中,生成HNO,溶液无色:
2 2 4 4 2 3
3NO +H O═2HNO +NO;Br (g)通入水中,得到溴水,溴不能完全溶解颜色呈黄色:Br +H O H++Br-
2 2 3 2 2 2+HBrO,选项B错误;C、检验Fe3+,应滴加KSCN溶液,溶液变为血红色:Fe3++SCN-=Fe (CCN) ;若检验Fe2
3
+,才是滴加铁氰化钾溶液,产生蓝色沉淀:2Fe3++3[Fe(CN)]2-=Fe [Fe(CN) ]↓;选项C错误;D、实验用长颈
4 2 4 3
漏斗加入稀硫酸与锌粒反应制取氢气,没有液封,实验失败,应改用分液漏斗,且实验中没有计时器和不同浓
度的硫酸溶液,无法探究浓度对反应速率的影响,选项D错误。
5.常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 FeSO 溶液:Na+、K+、Cl-、NO -
4 3
B.滴入酚酞变红色的溶液:K+、Ca2+、HCO -、CO2-
3 3
C.加入铁粉放出氢气的溶液:NH +、Fe3+、ClO-、SO 2-
4 4
D.水电离的c(H+)=1×10-13mol·L-1的溶液:K+、Mg2+、I-、C HO-
6 5
【答案】A
6.下列指定反应的离子方程式正确的是( )
A.电解饱和MgCl 溶液:2Cl-+2HO 2OH-+H↑+Cl↑
2 2 2 2
B.向酸性KMnO 溶液中通入SO :3SO +2MnO -+4OH-===2MnO↓+3SO 2-+2HO
4 2 2 4 2 4 2
C.向Fe(NO ) 稀溶液中滴加足量氢碘酸:3Fe2++NO -+4H+===3Fe3++NO↑+2HO
3 2 3 2
D.向NaClO溶液中通入足量CO:ClO-+CO+HO===HClO+HCO -
2 2 2 3
【答案】D
【解析】A. 电解饱和MgCl 溶液的化学方程式应为:Mg2++2Cl-+2HO Mg(OH) ↓+H↑+Cl↑,故A项错
2 2 2 2 2
误;B. 向酸性KMnO 溶液中通入SO :5SO +2MnO -+2HO ===2Mn2++5SO 2-+4H+,故B项错误;
4 2 2 4 2 4
C. 向Fe(NO ) 稀溶液中滴加足量氢碘酸,除了发生反应3Fe2++NO -+4H+===3Fe3++NO↑+2HO,因氢碘
3 2 3 2
酸足量,其中碘离子继续与氧化性的铁离子发生氧化还原反应,故C项错误;D. 酸性强弱:HCO > HClO >
2 3
HCO -,则向NaClO溶液中通入足量CO:ClO-+CO+HO===HClO+HCO -,故D项正确。
3 2 2 2 3
7.室温下,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变黄的溶液中:NH +、Mg2+、CiO-、NO -
4 3
B.0.1mo/L的NH Al(SO ) 溶液中:K+、Na+、CO2—、Cr-
4 4 2 3C.透明的溶液中:Cu2+、Fe3+、SO 2—、Cr-
4
D.由水电离的c(H+)·c(OH-)=1×10-26溶液:Fe2+、A13+、NO -、SO 2—
3 4
【答案】C
8.下列离子方程式正确的是 ( )
A.HS气体通入FeCl 溶液中: Fe3++H S=Fe2++S↓+2 H+
2 3 2
B.5.6g Fe与200mL2.0mol/L HNO 溶液充分反应:3Fe + 2NO— + 8H+ = 3Fe2+ + 2NO↑ + 4H O
3 3 2
C.往明矾溶液中加入氢氧化钡溶液至Al3+完全沉淀: A13++2SO2-+2Ba2++3OH-=A1(0H) ↓+2BaSO
4 3 4
D.饱和碳酸钠溶液通入二氧化碳后溶液变浑浊: 2Na++CO 2-+CO +H O=2NaHCO ↓
3 2 2 3
【答案】D
【解析】A、硫化氢具有还原性,铁离子具有氧化性,因此二者会发生氧化还原反应:2Fe3++H S=2Fe2+
2
+S↓+2H+,离子反应需遵循电荷守恒,故A项错误;B. 5.6 g Fe的物质的量为0.1 mol,被强氧化性的硝酸氧化
为铁离子,根据电子转移数相等可知需要硝酸的物质的量为0.1 mol,200mL2.0mol/L HNO 溶液的HNO 物
3 3
质的量为0.2 L×2.0 mol/L = 0.4 mol,即硝酸与铁反应时,硝酸过量,产物应为Fe3+,故B项错误;C. 假设
KAl(SO ) 为2 mol,溶液中含有2 mol Al3+,4 mol SO 2-,当Al3+恰好全部沉淀时,需要3mol Ba(OH) ,即加入3
4 2 4 2
mol Ba2+,6 mol OH-,其离子反应方程式为:2Al3++3SO2-+3Ba2++6OH- ═ 2Al(OH) ↓+3BaSO ↓,故C项错误;D.
4 3 4
碳酸钠和水以及二氧化碳反应生成碳酸氢钠,碳酸氢钠的溶解度小于碳酸钠,所以碳酸氢钠会结晶析出,即
2Na++CO 2-+CO +HO=2NaHCO ↓,故D项正确。
3 2 2 3
9.下列解释事实的离子方程式不正确的是
A.铝片放入NaOH溶液中有气体产生:2Al + 2OH-+ 2H O===2AlO -+3H ↑
2 2 2
B.向KCr O 溶液中滴加少量浓HSO ,溶液橙色加深:CrO2-(橙色) + H O 2CrO2-(黄色) + 2H+
2 2 7 2 4 2 7 2 4
C.向NaSiO 溶液中通入过量CO 制备硅酸凝胶:SiO2-+ CO + H O === HSiO(胶体)+ CO2-
2 3 2 3 2 2 2 3 3
D.用NaCO 溶液浸泡锅炉水垢(含CaSO):CaSO + CO 2- CaCO + SO2-
2 3 4 4 3 3 4
【答案】C10.下列化学用语对事实的表述不正确的是( )
A.电解精炼铜的阴极反应:Cu2++2e-===Cu
B.硬脂酸与乙醇的酯化反应:C H COOH+C H18OH C H COOC H+H18O
17 35 2 5 17 35 2 5 2
C.由Na和Cl形成离子键的过程:
D.常温时,0.1 mol·L-1氨水的pH=11.1:NH ·H O NH ++OH-
3 2 4
【答案】B
【解析】A.电解精炼铜时,阴极是电解质溶液中Cu2+得到电子,发生的电极反应为:Cu2++2e-===Cu,不符合
题意;B.羧酸和醇发生酯化反应时,醇脱氢原子,羧酸脱羟基,醇中的氧原子在酯中,正确的方程式为:
C H COOH+C H18OH C H CO18OC H+HO,符合题意;C.由Na和Cl形成离子键的过程是Na
17 35 2 5 17 35 2 5 2
原子失去一个电子,而Cl原子得到一个电子,从而形成离子键,其表述正确,不符合题意;D.常温时,0.1
mol·L-1氨水的pH=11.1,说明氨水是弱电解质,其电离为不完全电离,化学用语表述正确,不符合题意。
11.下列指定反应的离子方程式正确的是
A.向苯酚钠溶液中通入少量CO:2C HO-+CO+HO―→2C HOH+CO2-
2 6 5 2 2 6 5 3
B.向NaNO 溶液中滴加酸性KMnO 溶液:5NO - +2MnO -+3HO===5NO - +2Mn2++6OH-
2 4 2 4 2 3
C.向AlCl 溶液中滴加过量氨水:Al3++3NH ·H O===Al(OH) ↓+3NH +
3 3 2 3 4
D.NaHSO 溶液与Ba(OH) 溶液反应至中性:H++SO 2-+Ba2++OH-===BaSO ↓+HO
4 2 4 4 2
【答案】C
【解析】A.因为酸性强弱关系为HCO>C HOH>HCO -,所以即使通入过量的CO 也不会有CO2-生成:C HO
2 3 6 5 3 2 3 6 5
-+CO+HO―→C HOH+HCO -。A项错误;B.因为是酸性溶液,所以产物中不会有OH-生成,正确的反应
2 2 6 5 3
方程式为5NO - +2MnO -+6H+===5NO - +2Mn2++3HO。B项错误;C.Al(OH) 不能与氨水反应,所以该离
2 4 3 2 3
子方程式是正确的,C项正确;D.离子方程式不符合物质[Ba(OH) ]的组成,正确的离子方程式为2H++SO 2-
2 4+Ba2++2OH-===BaSO ↓+2HO。D项错误。
4 2
12.下列指定反应的离子方程式正确的是( )
A.饱和NaCO 溶液与BaSO 固体反应:CO2-+Ba2+ BaCO
2 3 4 3 3
B.NH HCO 溶液和过量Ca(OH) 溶液混合:Ca2++NH ++HCO -+2OH-===CaCO ↓+HO+ NH ·H O
4 3 2 4 3 3 2 3 2
C.NaClO与HI溶液反应:2ClO-+2HO+2I-===I +Cl↑+4OH-
2 2 2
D.电解氯化镁溶液:2Cl-+Mg2+ Cl↑+Mg
2
【答案】B
13.下列离子方程式书写正确的是
A.氯化铝溶液中加入过量的氨水:Al3+ +3OH- = Al(OH) ↓
3
B.向莫尔盐[(NH )Fe(SO )·6H O]溶液中加入过量氢氧化钠溶液:NH ++Fe2++3OH-
4 2 4 2 2 4
NH ·H O+Fe(OH) ↓
3 2 2 [来源:学§科§网Z§X§X§K]
C.向碳酸氢钠溶液中滴加少量的氢氧化钡溶液:HCO -+Ba2++OH-=BaCO ↓+ H O
3 3 2
D.向AgCl悬浊液中加入NaS溶液,白色沉淀变成黑色:2AgCl+S2- Ag S+2Cl-
2 2
【答案】D
【解析】A、氨水中NH ·H O属于弱碱,书写离子方程式时,不能拆写,正确的是Al3++3NH ·H O=Al(OH) ↓+
3 2 3 2 3
3NH +,故A错误;B、因为加入NaOH为过量,因此反应的离子方程式为2NH ++Fe2++4OH-=2NH·H O+
4 4 3 2
Fe(OH) ↓,故B错误;C、氢氧化钡是少量,发生离子方程式为2HCO -+Ba2++2OH-=BaCO ↓+2HO+CO2
2 3 3 2 3
-,故C错误D、白色变为黑色,说明产生Ag S,反应的离子方程式为2AgCl+S2-=Ag S+2Cl-,故D正确。
2 2
14.一定能在下列溶液中大量共存的离子组是( )
A.水电离产生的c(OH-)=1×10-12 mol·L-1液中:NH +、Na+、Cl-、HCO -
4 3
B.能使pH试纸变深蓝色的溶液中:Na+、AlO-、S2-、CO2-
2 3
C.含有大量Fe3+的溶液:SCN-、I-、K+、Br-
D.澄清透明的无色溶液中:ClO-、MnO -、Al3+、SO 2-
4 4
【答案】B15.解释下列反应原理的离子方程式正确的是
A.用加热的方法降低自来水中钙离子浓度:Ca2++2HCO- CaCO ↓+H O+CO↑
3 3 2 2
B.向CHBrCOOH中加入足量的NaOH溶液并加热:CHBrCOOH+OH-→CHBrCOO-+H O
2 2 2 2
C.向Mg(HCO ) 溶液中加入足量的NaOH溶液:Mg2++2HCO-+2OH-=MgCO↓+CO 2-+H O
3 2 3 3 3 2
D.在强碱溶液中NaClO与Fe(OH) 反应生成NaFeO:3ClO-+2Fe(OH) =2FeO 2-+3Cl-+H O+4H+
3 2 4 3 4 2
【答案】A
[来源:学&科&网Z&X&X&K]
【解析】A.用加热的方法降低自来水中钙离子浓度:Ca2++2HCO- CaCO ↓+H O+CO↑,A正确;
3 3 2 2
B. 向CHBrCOOH中加入足量的NaOH溶液并加热的离子反应为CHBrCOOH+2OH- CH OHCOO-
2 2 2
+Br-+H O,B错误;C.向Mg(HCO ) 溶液中加入足量的NaOH溶液:Mg2++2HCO- +4OH-=Mg(OH) ↓+2CO 2-
2 3 2 3 2 3
+2H O,C错误;D.在强碱溶液中不可能大量存在H+,D错误。
2
16.下列离子方程式表达不正确的是
A.向FeCl 溶液滴加HI溶液:2Fe3++2I-=2Fe2++I
3 2
B.向NaSO 溶液滴加HCl溶液:SO2-+2H+=SO↑+S↓+HO
2 2 3 2 3 2 2
C.向NaAlO 溶液中通入过量CO 制Al(OH) :AlO-+CO +2H O=Al(OH)↓+HCO-
2 2 3 2 2 2 3 3
D.向NH Al(SO ) 溶液中滴加少量Ba(OH) 溶液:2NH ++Ba2++SO2-+2OH—= BaSO↓+2NH·H O
4 4 2 2 4 4 4 3 2
【答案】D
【解析】A项、氯化铁具有氧化性,碘化氢中-1价的碘离子具有还原性,两者发生氧化还原反应生成碘单质和
亚铁离子,反应为:2Fe3++2I-=2Fe2++I ,故A正确;B项、滴加HCl溶液,NaSO 中+2价的元素S能发生歧化
2 2 2 3
反应生成二氧化硫和硫单质,反应的离子方程式为:SO2-+2H+=SO↑+S↓+H O,故B正确;
2 3 2 2
C项、NaAlO 溶液中通入过量的CO,反应生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为AlO-
2 2 2
+CO +2H O=Al(OH)↓+HCO-,故C正确;D项、向NH Al(SO ) 溶液中滴加少量Ba(OH) 溶液,Al3+优于
2 2 3 3 4 4 2 2
NH +先反应,反应的离子方程式为2Al3++3Ba2++3SO2-+6OH—=3BaSO ↓+2Al(OH)↓,故D错误。
4 4 4 3
17.下列反应的离子方程式正确的是A.用氨水吸收少量SO :2NH ·H O+SO =2NH++SO2-+H O
2 3 2 2 4 3 2
B.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO -+H ↑
2 2
C.FeO和稀HNO 的反应:FeO+2H+=Fe2++H O
3 2
D.碳酸钙溶于醋酸中:CaCO +2H+=Ca2++H O+CO↑
3 2 2
【答案】A
18.下列离子方程式正确的是( )
A.BaSO 与稀HNO 反应:3BaSO+2H++ 2NO ˉ = 3BaSO + 2NO↑+H O
3 3 3 3 4 2
B.碳酸钠溶液中滴加少量氯水的离子方程式为:CO2ˉ+Cl +H O = HCO ˉ+Clˉ+HClO
3 2 2 3
C.Fe (SO ) 溶液与Ba(OH) 溶液反应:Fe3++SO2ˉ+Ba2++3OHˉ = Fe(OH) ↓+ BaSO↓
2 4 3 2 4 3 4
D.向FeI 溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl = 2Fe3++2Cl-
2 2
【答案】A
【解析】亚硫酸钡能被硝酸氧化为BaSO,故A正确;酸性HCO> HClO> HCO -,碳酸钠溶液中滴加少量氯水
4 2 3 3
的离子方程式为:2CO2-+Cl+H O=2HCO-+Cl-+ClO-,故B错误;Fe (SO ) 溶液与Ba(OH) 溶液反应:2Fe3+
3 2 2 3 2 4 3 2
+3SO2ˉ+3Ba2++6OHˉ = 2Fe(OH) ↓+ 3BaSO↓,故C错误;还原性I->Fe2+,向FeI 溶液中滴加少量氯水,反应的
4 3 4 2
离子方程式为:2I- +Cl = I+2Cl-,故D错误。
2 2
19.下列离子方程式正确的是
A.硅与氢氟酸的反应:Si+4H++4F-=SiF ↑+2H↑
4 2
B.向NaHCO 溶液中加入少量Ca(OH) 溶液:HCO -+Ca2++OH-=CaCO ↓+H O
3 2 3 3 2
C.向苯酚溶液中滴加NaCO 溶液:2 +CO 2- +CO ↑+H O
2 3 3 2 2
D.向氯化亚铁溶液中滴加稀硝酸:3Fe2++4H++NO-=3Fe3++NO↑+2HO
3 2
【答案】D
【解析】A. 硅与氢氟酸的反应,离子方程式:Si+4HF=SiF ↑+2H ↑,A错误;B.向NaHCO 溶液中加入少量
4 2 3
Ca(OH) ,离子方程式:2HCO -+Ca2++2OH-=CaCO ↓+2H O+CO2-,B错误;C.由于酸性
2 3 3 2 3
HCO>C HOH>HCO -,所以向苯酚溶液中滴加NaCO 溶液,反应产生苯酚和碳酸氢钠,离子方程式为
2 3 6 5 3 2 3+CO 2- +HCO-,C错误;D.稀硝酸具有强氧化性,将Fe2+氧化为Fe3+,它本身被还原
3 3
变为NO,根据电子守恒、电荷守恒及原子守恒可得反应的离子方程式为:3Fe2++4H++NO-=3Fe3++
3
NO↑+2H O,D正确。
2
20.能正确表示下列反应的离子反应方程式为( )
A.Ba(OH) 溶液中加入少量NaHCO 溶液:HCO-+Ba2++OH-=BaCO +H O
2 3 3 3 2
B.向明矾溶液中滴加Ba(OH) 溶液,恰好使SO 2-沉淀完全:3Ba2++3SO2-+2Al3++6OH-═2BaSO ↓+2A(l OH)↓
2 4 4 4 3
C.NH HCO 稀溶液与过量的KOH溶液反应:HCO -+OH-=CO 2-+H O
4 3 3 3 2
D.醋酸除去水垢:2H++CaCO =Ca2++CO ↑+H O
3 2 2
【答案】A
21.能正确表示下列反应离子方程式的是
A.向NaCO 溶液中滴入AgNO 溶液:2Ag++CO 2-=Ag CO↓
2 3 3 3 2 3
B.碳酸氢铵溶液中加入足量氢氧化钡溶液:NH ++HCO-+2OH-=CO 2-+NH·H O+HO
4 3 3 3 2 2
C.Fe(NO ) 溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I
3 3 2
D.用惰性电极电解熔融氯化钠:2Cl-+2H O=Cl +H +2OH-
2 2 2
【答案】A
【解析】A. Na CO 与AgNO 在溶液中发生复分解反应产生Ag CO 沉淀和NaNO ,离子方程式为2Ag++CO 2-
2 3 3 2 3 3 3
=Ag CO↓,A正确;B.碳酸氢铵溶液中加入足量氢氧化钡溶液,反应产生BaCO 沉淀、NH ·H O、HO,反应的
2 3 3 3 2 2
离子方程式为NH ++HCO-+Ba2++2OH-=BaCO ↓+NH·H O+HO,B错误;C.氧化性HNO>Fe3+,所以是NO -获
4 3 3 3 2 2 3 3
得电子变为NO气体,C错误;D.用惰性电极电解熔融氯化钠,Cl-失去电子变为Cl,Na+获得电子变为金属
2
Na,熔融状态中无水,D错误。
22.下列反应中有关原理涉及的离子方程式正确的是
A.NaHCO 溶液中滴入几滴酚酞,溶液变为粉红色:HCO -+H O=HCO+OH-
3 3 2 2 3B.硫酸铝溶液中加入氨水,会生成白色沉淀:Al3++3OH-=Al(OH) ↓
3
C.FeSO 溶液中加入K[Fe(CN) ]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)]3-=Fe [Fe(CN) ]↓
4 3 6 4 3 6 2
D.“84”消毒液中通入二氧化碳,漂白能力增强:2ClO-+CO +H O=CO2-+2HClO
2 2 3
【答案】C
23.下列指定反应的离子方程式正确的是
A.石灰水中加入过量小苏打溶液:Ca2++HCO -+OH-=CaCO ↓+HO
3 3 2
B.次氯酸钠溶液吸收少量二氧化硫气体:SO +HO+ClO-=SO 2-+Cl-+2H+
2 2 4
C.将SO 通入少量氨水中:SO +NH ·H O=HSO -+NH +
2 2 3 2 3 4
D.电解氯化镁溶液:2Cl-+2H O H↑+ Cl↑+2OH-
2 2 2
【答案】C
【解析】A. 石灰水中加入过量小苏打溶液生成碳酸钙、碳酸钠和水:Ca2++2HCO -+2OH-=CaCO ↓+CO2
3 3 3
-+2HO,故A错误;B. 将少量二氧化硫通入次氯酸钠溶液中的离子反应为SO +2OH-+ClO-=SO 2-+Cl-
2 2 4
+HO,故B错误;C. 将SO 通入少量氨水中生成亚硫酸氢铵:SO +NH ·H O=HSO -+NH +,故C正确;D.
2 2 2 3 2 3 4
用惰性电极电解饱和氯化镁溶液的离子反应为Mg2++2Cl-+2H O H ↑+ Cl↑+Mg(OH)↓,故D错误。
2 2 2 2
24.能正确表示下列反应的离子方程式是
A.在硫酸亚铁溶液中通入氧气:4Fe2++O +4H+=4Fe3++2H O
2 2
B.NH HCO 溶液中加入过量的Ba(OH) 溶液:2HCO -+Ba2++2OH-=BaCO ↓+2H O+CO2-
4 3 2 3 3 2 3
C.氢氧化亚铁溶于稀硝酸中:Fe(OH) +2H+=Fe2++2H O
2 2
D.澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO-=CaCO ↓+H O
3 3 2
【答案】A25.下列反应的离子方程式书写正确的是
A.向氯化铁溶液中加入过量的硫化钠:2Fe3++S2- = 2Fe2++S↓
B.氢氧化铁溶于氢碘酸溶液:Fe(OH) + 3H+ = Fe3++ 3H O
3 2
C.硫酸铝溶液中加入过量氨水:Al3++ 4 NH·H O=AlO- +4 NH + 2 H O
3 2 2 2
D.向NaHSO 溶液滴加Ba(OH) 溶液至中性:2H++SO2-+ Ba2++ 2OH-=BaSO ↓+2H O
4 2 4 4 2
【答案】D
【解析】A.向氯化铁溶液中加入过量的硫化钠,反应生成硫化亚铁和硫单质,反应的离子方程式为:
2Fe3++3S2- = 2FeS↓+S↓,选项A错误;B.发生氧化还原反应,生成碘化亚铁、碘、水,离子反应为
2Fe(OH) +2I-+6H+=2Fe2++I +6H O,选项B错误;C.硫酸铝溶液中加入过量氨水的离子反应为Al3+
3 2 2
+3NH·H O═Al(OH) ↓+3NH+,选项C错误;D. 向硫酸氢钠溶液中滴加Ba(OH) 溶液恰好至中性的离子反应
3 2 3 4 2
为2H++SO2-+ Ba2++ 2OH-=BaSO ↓+2H O,所以D选项是正确的。
4 4 2