文档内容
专题 04 氧化还原反应
2020年高考真题
加热
1.【2020年7月浙江选考】反应MnO +4HCl(浓) ¿MnCl +Cl ↑+2H O 中,氧化产物与还原产物的物
2 2 2 2
¿
质的量之比是( )
A.1:2 B.1:1 C.2:1 D.4:1
【答案】B
【解析】由反应方程式可知,反应物MnO 中的Mn元素的化合价为+4价,生成物MnCl 中Mn元素的化
2 2
合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl 中Cl元素的化合价为0价,故MnCl 是还
2 2
原产物,Cl 是氧化产物,由氧化还原反应中得失电子守恒可知,n(Cl ):n(MnCl )=1:1,B符合题意;
2 2 2
答案选B。
2.【2020山东(新高考)】下列叙述不涉及氧化还原反应的是
A.谷物发酵酿造食醋 B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒 D.大气中NO 参与酸雨形成
2
【答案】B
【解析】A.涉及淀粉水解成葡萄糖,葡萄糖氧化成乙醇,乙醇氧化成乙酸,涉及氧化还原反应,A不符
合题意;
B.小苏打即NaHCO ,NaHCO 受热分解产生无毒的CO,因此可用小苏打作食品膨松剂,不涉及氧化还
3 3 2
原反应,B符合题意;
C.利用含氯消毒剂的强氧化性消毒杀菌,涉及氧化还原反应,C不符合题意;
D.NO 与水反应有HNO 产生,因此NO 参与了硝酸型酸雨的形成,涉及氧化还原反应,D不符合题意。
2 3 2
答案选B。
2020届高考模拟试题
3.(浙江省金华十校2020届高三4月模拟考试)下列变化中,气体被还原的是
A.水蒸气使 CuSO 固体变蓝 B.氯气使浅绿色 FeC1 溶液变黄
4 2
C.H 使灼热CuO 固体变红 D.氨气使A1Cl 溶液产生白色沉淀
2 3
【答案】B
【解析】A.水蒸气使 CuSO 固体变蓝,发生了反应:CuSO +5H O= CuSO ∙5H O,不是氧化还原反应,
4 4 2 4 2故A不选;
B.氯气使浅绿色 FeC1 溶液变黄,发生了反应:Cl+2FeCl =2FeCl ,Cl 中0价的Cl反应后降低到了
2 2 2 3 2
FeCl 中的-1价,被还原,故B选;
3
C.H 使灼热CuO 固体变红,发生了反应:H+CuO Cu+H O,H 中H的化合价从0价升高到了水中的
2 2 2 2
+1价,被氧化,故C不选;
D.氨气使A1Cl 溶液产生白色沉淀,发生了反应:AlCl +3NH∙H O=Al(OH) ↓+3NHCl,不是氧化还原反
3 3 3 2 3 4
应,故D不选;
故选B。
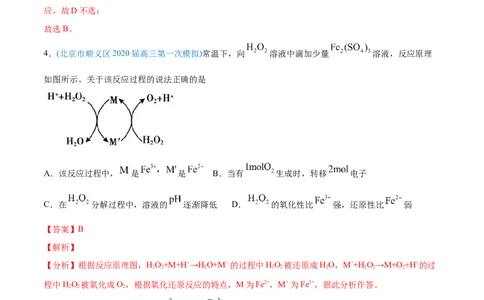
4.(北京市顺义区2020届高三第一次模拟)常温下,向 溶液中滴加少量 溶液,反应原理
如图所示。关于该反应过程的说法正确的是
A.该反应过程中, 是 是 B.当有 生成时,转移 电子
C.在 分解过程中,溶液的 逐渐降低 D. 的氧化性比 强,还原性比 弱
【答案】B
【解析】
【分析】根据反应原理图,HO+M+H+→HO+Mˊ的过程中HO 被还原成HO,Mˊ+HO→M+O+H+的过
2 2 2 2 2 2 2 2 2
程中HO 被氧化成O,根据氧化还原反应的特点,M为Fe2+,Mˊ为Fe3+,据此分析作答。
2 2 2
【详解】A.根据分析, M是 ,Mˊ是 ,故A错误;
B.图示中生成O 的反应为2Fe3++H O=2Fe2++O ↑+2H+,反应过程中O元素的化合价由-1价升至0价,因
2 2 2 2
此当有 生成时,转移 电子,故B正确;
C.图示中的反应为2Fe3++H O=2Fe2++O ↑+2H+、2Fe2++H O+2H+=2Fe3++2H O,则总反应为2HO
2 2 2 2 2 2 2 22HO+O↑,在 分解过程中生成了HO,溶液变稀,则溶液的 会逐渐增大,故C错误;
2 2 2
D.根据2Fe3++H O=2Fe2++O ↑+2H+说明HO 的还原性强于Fe2+,2Fe2++H O+2H+=2Fe3++2H O说明HO 的
2 2 2 2 2 2 2 2 2 2
氧化性强于Fe3+,故D错误;
综上所述,答案为B。
5.(2020届济南市实验中学高三下学期2月份阶段检测)已知酸性 KCr O 溶液可与 FeSO 溶液反应生成
2 2 7 4
Fe3+和 Cr3+。现将硫酸酸化的 KCr O 溶液与 FeSO 溶液混合,充分反应后再向所得溶液中加入KI溶
2 2 7 4
液,混合溶液中Fe3+的物质的量随加入的 KI 的物质的量的变化关系如图所示,下列不正确的是
A.图中AB段的氧化剂为 KCr O
2 2 7
B.开始加入的 KCr O 为 0.25 mol
2 2 7
C.图中 BC 段发生的反应为 2Fe3++2I-=2Fe2++I
2
D.混合之前,KCr O 与 FeSO 的物质的量之比为1∶6
2 2 7 4
【答案】D
【解析】【分析】将硫酸酸化的 KCr O 溶液与 FeSO 溶液混合,发生如下反应:
2 2 7 4
,向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量
随加入的 KI 的物质的量的变化关系如图,可知在AB段发生反应:
,在BC段发生反应:2Fe3++2I-=2Fe2++I。据此解答。
2
【详解】A.在AB段发生反应: ,氧化剂是KCr O,故A正确;
2 2 7
B.根据图像可知,在BC段,消耗I-0.9mol,由反应对应的关系 ,推知在混合时生成了0.9mol Fe3+, ,消耗KCr O 物质的量为0.15mol;又AB段有对应关系:消耗I-
2 2 7
0.6mol, ,消耗KCr O 物质的量为0.1mol;共消耗KCr O 物质的量为
2 2 7 2 2 7
0.15+0.1=0.25mol,故B正确;
C.由分析知,在BC段发生反应:2Fe3++2I-=2Fe2++I,故C正确;
2
D.根据计算可知,在反应前,KCr O 物质的量为0.25mol, FeSO 与Fe3+一样都是0.9mol,二者之比不
2 2 7 4
为1:6,D错误;
答案选D。
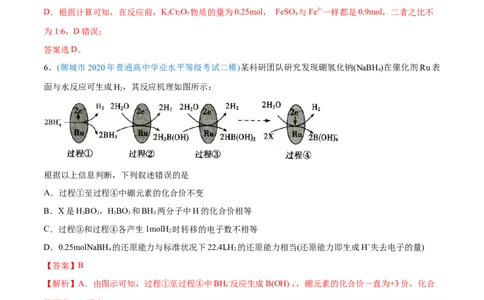
6.(聊城市2020年普通高中学业水平等级考试二模)某科研团队研究发现硼氢化钠(NaBH )在催化剂Ru表
4
面与水反应可生成H,其反应机理如图所示:
2
根据以上信息判断,下列叙述错误的是
A.过程①至过程④中硼元素的化合价不变
B.X是HBO,HBO 和BH 两分子中H的化合价相等
3 3 3 3 3
C.过程③和过程④各产生1molH 时转移的电子数不相等
2
D.0.25molNaBH 的还原能力与标准状况下22.4LH 的还原能力相当(还原能力即生成H+失去电子的量)
4 2
【答案】B
【解析】A.由图示可知,过程①至过程④中BH-反应生成B(OH) -,硼元素的化合价一直为+3价,化合
4 4
价不变,A正确;
B.过程④中2moH O水与2molX反应生成2mol B(OH) -和1molH ,根据元素守恒X为HBO,HBO 中
2 4 2 3 3 3 3
H为+1价,但在BH 分子中H为-1价,B错误;
3
C.由图示可知,过程③中产生1molH 时转移的电子数为N ,过程④产生1molH 时转移的电子数为
2 A 2
2N ,两者不相等,C正确;
A,
D.NaBH 中H为-1价,0.25molNaBH 生成H+失去的电子的量2 0.25mol 4=2mol,标准状况下22.4LH
4 4 2
为1mol,1mol H 生成H+失去的电子的量2 1mol=2mol,故两者还原能力相当,D正确;
2答案选B。
7.(青岛市2020届高三第三次模拟)向含有淀粉的 KIO 酸性溶液滴加 NaHSO 溶液,溶液先变蓝后褪色。
3 3
下列说法错误的是
A.溶液先变蓝的原因:2IO +5HSO =I +5SO +H O+3H+
2 2
B.溶液恰好褪色时 n(KIO ):n(NaHSO)=1:3
3 3
C.还原性 I-> HSO >I
2
D.若向含有淀粉的 NaHSO 溶液中滴加过量 KIO 酸性溶液,则溶液变蓝不褪色
3 3
【答案】C
【解析】A.溶液变成蓝色,说明有单质碘生成,即I元素化合价由+5价降低至0价,被还原,IO 为氧化
剂,S元素的化合价由+4价升高至+6价,被氧化,HSO 为还原剂,反应的离子方程式为2IO +5HSO
=I +5SO +H O+3H+,A选项正确;
2 2
B.溶液褪色,说明碘单质又被亚硫酸氢钠还原,离子方程式为I+HSO =2I-+SO +3H+,结合A选项,
2
可知溶液恰好褪色时n(KIO ):n(NaHSO)=1:3,B选项正确;
3 3
C.由A选项中的反应可知,还原性:HSO >I,由B选项中的反应可知,还原性HSO >I-,又还原性I-
2
>I,则还原性:HSO >I->I,C选项错误;
2 2
D.若向含有淀粉的 NaHSO 溶液中滴加过量KIO 酸性溶液,由于氧化性IO >I,所以不会出现I 被还
3 3 2 2
原的情况,即溶液变蓝不褪色,D选项正确;
答案选C。
6.(天津市南开区2020届高三年级第二次模拟考试)硝酸厂的烟气中含有大量的氮氧化物(NO),将烟气与
x
H 的混合气体通入Ce(SO) 与Ce (SO )[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图
2 4 2 2 4 3
所示。下列说法正确的是A.该转化过程的实质为NO 被H 还原
x 2
B.x=l时,过程II中氧化剂与还原剂的物质的量之比为2:1
C.处理过程中,混合溶液中Ce3+和Ce4+总数减少
D.过程I发生反应的离子方程式:H+Ce4+=2H++Ce3+
2
【答案】A
【解析】
【分析】分析转化过程图,可知在过程I中发生H+2Ce4+=2H++2Ce3+,在过程Ⅱ中发生2NO+4xH++
2 x
4xCe3+=2xHO+N+4xCe4+,据此进行分析。
2 2
【详解】A.由分析可知,总反应可以看作烟气与氢气反应,该转化过程的实质为NO 被H 还原,A项正
x 2
确;
B.x=1时,根据图示,过程II中发生2NO+4H++4Ce3+=2H O+N+4Ce4+,N的化合价降低,NO为氧
2 2
化剂,Ce3+为还原剂,根据得失电子守恒: ,因此氧化剂与还原剂物质的量之比
为1:2,B项错误;
C.过程I发生H+2Ce4+=2H++2Ce3+,过程II发生2NO+4xH++4xCe3+=2xHO+N+4xCe4+,处理过
2 x 2 2
程中,混合液中Ce3+和Ce4+总数不变,C项错误;
D.根据图示,过程I发生H+Ce4+→H++Ce3+,利用化合价升降法进行配平,离子方程式为H+2Ce4+
2 2
=2H++2Ce3+,D项错误;
答案选A。
7.(日照市2020届高三4月模拟考试,不定项)高铁酸钾( )是新型的绿色环保水处理剂。一种制备
的流程如下:下列说法错误的是( )
A.步骤i中反应的离子方程式为
B.步骤ⅱ说明碱性条件下,氧化性:
C.步骤ⅲ的反应为复分解反应,说明溶解度:
D. 作为性能优良的水处理剂,主要是利用了其强氧化性和还原后产生的具有絮凝作用的Fe(Ⅲ)
【答案】BC
【解析】
【分析】根据制备流程分析,FeSO 溶液在酸性条件下与HO 发生氧化还原反应得到Fe (SO ),Fe (SO )
4 2 2 2 4 3 2 4 3
与NaClO在碱性条件下发生氧化还原得到NaFeO,NaFeO 与饱和的KOH溶液得到KFeO 粗品,经洗涤
2 4 2 4 2 4
干燥后得到KFeO 纯品,据此分析解答问题。
2 4
【详解】A.由上述分析可知,步骤ⅰ为FeSO 溶液在酸性条件下与HO 发生氧化还原反应生成HO和
4 2 2 2
Fe (SO ),根据氧化还原反应规律可得反应的离子方程式为:2Fe2++H O+2H+===2Fe3++2H O,A选项正确;
2 4 3 2 2 2
B.步骤ⅱ为Fe (SO ) 与NaClO在碱性条件下发生氧化还原得到NaFeO,氧化剂是NaClO,氧化产物为
2 4 3 2 4
NaFeO,因为氧化剂的氧化性大于氧化产物,故氧化性:NaClO>Na FeO,B选项错误;
2 4 2 4
C.步骤ⅲ为NaFeO 与饱和的KOH溶液发生复分解反应得到KFeO 粗品,溶解度大的物质转化为溶解度
2 4 2 4
小的物质,故溶解度:NaFeO>K FeO,C选项错误;
2 4 2 4
D.由于KFeO 具有强氧化性,因此可用于水的杀菌消毒,且其还原产物产生的Fe3+水解得到Fe(OH) 的
2 4 3
胶体,具有絮凝的作用,故KFeO 是乙中性能优良的水处理剂,D选项正确;
2 4
答案选BC。
8.(2020年山东新高考泰安市第五次模拟,不定项)污水处理厂处理含CN-废水的过程分两步进行:①向含
CN-的废水中加入过量NaC1O将CN-转化为CNO-;②调节①所得溶液为酸性,使CNO-继续被NaC1O转化
为两种无污染的气体。下列关于上述过程的叙述错误的是( )
A.CN-的电子式为B.过程①中,生成CNO-的反应中氧化剂与还原剂的物质的量之比为1:1
C.过程②中,生成的两种无污染的气体为CO 和N
2 2
D.氧化性:CNO->C1O-
【答案】AD
【解析】A.CN-的电子式为 ,故A错误;
B.过程①中,CN-被氧化为CNO-,1mol CN-转移2mol电子,NaC1O被还原为NaC1,1mol NaC1O转移
2mol电子,反应中氧化剂与还原剂的物质的量之比为1:1,故B正确;
C.CO 和N 无污染,过程②中,生成的两种无污染的气体为CO 和N,故C正确;
2 2 2 2
D.CN-被NaC1O氧化为CNO-,所以氧化性:CNO-<C1O-,故D错误;
选AD。
9.(2020年山东新高考烟台市适应性练习一,不定项)《环境科学》刊发了我国科研部门采用零价铁活化过
硫酸钠(Na SO,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示(SO
2 2 8
·、·OH表示自由基)。设阿伏加德罗常数的值为N 。下列叙述错误的是( )
A
A.过硫酸钠中-2价氧与-1价氧的个数比为3:1
B.若56gFe参加反应,共有1.5N 个SO2−被还原
A 2 8
C.碱性条件下硫酸根自由基发生反应的方程式为SO -·+OH-=SO2-+·OH
4 4
D.pH越小,越有利于去除废水中的正五价砷
【答案】BD
【解析】A.过硫酸钠中正负化合价之和为零,S为+6价,Na为+1价,正价之和=(+6)×2+(+1)×2=14,负
价之和为-14,若-2价氧与-1价氧的个数比为3:1,即-2价氧为6个,-1价氧的个数为2个,负价之和为
(-2)×6+(-1)×2=-14,故A正确;
B.56gFe为1mol,根据图示可知,1molS O2−和1molFe反应生成2molSO 2−和1molFe2+,该过程转移2mol
2 8 4电子,但是Fe2+还要与SO2−反应变成Fe3+和自由基,根据图示,形成的沉淀中即含有二价铁离子,又含有
2 8
三价铁离子,即第一步反应中的二价铁没有被完全氧化为三价铁离子,因此1mol铁参加反应消耗小于
1.5mol S O2−,共有少于1.5N 个SO2−被还原,故B错误;
2 8 A 2 8
C.结合图示可知,碱性条件下,SO −发生反应的方程式为:SO −+OH−═SO 2−+OH,故C正确;
4 4 4
D.根据图示可知,最后是碱性条件下⋅,铁离子和亚铁离子转化为⋅氢氧化亚铁和氢⋅ 氧化铁,正五价砷离子
转变为沉淀,二者共同以沉淀形式析出的,则溶液的碱性越强越有利于析出,即pH越大越有利于去除废
水中的正五价砷,故D错误;
答案选BD。
10.(2020年山东新高考烟台市适应性练习一,不定项)用KMnO 酸性溶液处理硫化亚铜(Cu S)和二硫化亚
4 2
铁(FeS )的混合物时,发生的反应Ⅰ: +Cu S+H+→Cu2++ +Mn2++H O(未配平)和反应Ⅱ:
2 2 2
+FeS +H+→Fe3++ +Mn2++H O(未配平)。下列说法正确的是( )
2 2
A.反应Ⅰ中Cu S既是氧化剂又是还原剂
2
B.反应Ⅰ中每生成1mol ,转移电子的物质的量为10mol
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为1:3
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量之
4
比为3:2
【答案】BD
【解析】
【分析】 中Mn元素为+7价,Cu S中Cu和S元素分别为+1、-2价,FeS 中Fe和S元素分别为
2 2
+2、-1价。
【详解】A.反应Ⅰ中Cu S中Cu和S的化合价都升高,发生氧化反应,则Cu S为还原剂,Mn元素的化
2 2
合价降低,发生还原反应, 为氧化剂,A错误;
B.反应Ⅰ中每生成1mol ,参加反应的Cu S为1mol,Cu S化合价共升高2(2-1)+(6+2)=10,反应转
2 2
移电子的物质的量为10mol,B正确;C.反应Ⅱ中氧化剂 化合价降低(7-2)=5,还原剂FeS 化合价共升高1+2(6+1)=15,根据得失电子相
2
等,氧化剂与还原剂的物质的量之比为15:5=3:1,C错误;
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同, 1molKMnO 得到5mol电子,Cu S化合价共升
4 4 2
高2(2-1)+(6+2)=10,应氧化0.5molCu S,FeS 化合价共升高1+2(6+1)=15,应氧化 mol= mol FeS
2 2 2,
则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量之比为0.5mol: mol=3:2,D正确。
答案选BD。
11.(北京市海淀区2020届高三二模)金属铬常用于提升特种合金的性能。工业上以铬铁矿(主要成份为
FeO·Cr O,含有少量Al O)为原料制备金属铬的流程如下图。下列说法不正确的是( )
2 3 2 3
A.①中需持续吹入空气作氧化剂 B.②中需加入过量稀硫酸
C.③中发生了置换反应 D.溶液A为橙色
【答案】B
【解析】A.在铬铁矿中Cr元素化合价为+3价,反应后变为NaCrO 中的+6价,化合价升高,被氧化,因
2 4
此①中需持续吹入空气作氧化剂,A正确;
B.Al(OH) 是两性氢氧化物,能够与硫酸发生反应产生可溶性Al (SO ),因此②中加入的稀硫酸不能过量,
3 2 4 3
B错误;
C.Cr O 与Al在高温下反应产生Cr和Al O,反应物是单质和化合物,生成物也是单质与化合物,因此③
2 3 2 3
中反应类型为置换反应,C正确;
D.NaCrO 在酸性溶液中发生反应: 2CrO2-+2H+ Cr O2-+H O,反应产生Cr O2-使溶液显橙色,D正
2 4 4 2 7 2 2 7
确;故合理选项是B。
12.(山东省实验中学2020届高三下学期打靶模拟考试)高锰酸钾(KMnO)是一种常用的氧化剂。不同条件
4下高锰酸钾可发生如下反应: +5e-+8H+→Mn2++4H O; +3e-+2H O→MnO +4OH-; +e
2 2 2
-→ 。高锰酸钾溶液与硫化亚铁有如下反应:
FeS+KMnO +H SO →KSO +MnSO +Fe (SO )+S+H O(未配平)。下列有关说法正确的是
4 2 4 2 4 4 2 4 3 2
A.由上面的反应可知,高锰酸根离子( )反应后的产物与溶液的酸碱性有关
B.高锰酸钾溶液可代替二氧化锰用来制取Cl,氧化剂和还原剂物质的量之比为1:8
2
C.在高锰酸钾溶液与硫化亚铁的反应中,反应前后固体的质量减少了2.8g,则硫元素与高锰酸钾之间转
移的电子数为0.15N
A
D.高锰酸钾溶液也可与双氧水发生反应,其中双氧水是氧化剂
【答案】A
【解析】A.由不同条件下高锰酸钾发生的反应可知,溶液的酸性越强,反应后锰元素的化合价越低,所
以高锰酸根反应后的产物与溶液的酸碱性有关,A正确;
B.反应2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O,高锰酸钾为氧化剂,盐酸为还原剂,由方程式可知,
4 2 2 2
有2mol高锰酸钾参与反应,则有10mol HCl被氧化,因此,氧化剂和还原剂物质的量之比为1:5,B错误;
C.反应中固体质量变化为:FeS→S,固体质量变化为铁元素的变化,反应前后固体的质量减少了2.8g,
参加反应的亚铁离子的物质的量为 =0.05mol,即被氧化的FeS的物质的量为0.05mol,被高锰酸
根离子氧化的硫离子的物质的量为0.05mol,转移的电子的物质的量为:0.05mol×2=0.1mol,电子数目为
0.1N ,C错误;
A
D.高锰酸钾与双氧水反应,高锰酸钾体现氧化性,双氧水体现还原性,D错误;
故选A。
13.(日照市2020届高三 4月模拟考试) 是一种红色固体,常用作示温涂料。制备反应为:
。下列说法正确的是( )
A.上述反应的产物 中,Hg的化合价为
B.上述反应中Hg元素与Cu元素均被还原C.上述反应中生成 时,转移的电子数为
D.由以上信息可推知:可发生反应
【答案】D
【解析】
【分析】根据制备反应方程式可知,CuSO 中Cu的化合价由+2价降至+1价,作氧化剂,发生还原反应,
4
SO 中S元素的化合价由+4价升至+6价,作还原剂,发生氧化反应,Cu HgI 为还原产物,据此分析解答
2 2 4
问题。
【详解】A.根据上述分析可知,Cu HgI 中Cu的化合价为+1价,则Hg的化合价为+2价,A选项错误;
2 4
B.上述反应中,只有Cu元素被还原,B选项错误;
C.上述反应中,CuSO 中Cu的化合价由+2价降至+1价,生成1mol Cu HgI 时,转移2mol电子,转移的
4 2 4
电子数为2N ,C选项错误;
A
D.根据题干信息,CuSO 可与SO 在盐溶液中发生氧化还原反应,Cu2+被还原为Cu+,SO 被氧化为
4 2 2
SO 2-,则反应2CuSO +NaCl+SO +2H O===2CuCl↓+Na SO +2H SO 可以发生,D选项正确;
4 4 2 2 2 4 2 4
答案选D。
14.(山东师范大学附属中学2020届高三6月份模拟,不定项)氰化物是剧毒物质,传统生产工艺的电镀废
水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl 氧化法处理这
2
种废水,涉及两个反应:反应i,CN- +OH-+Cl OCN- +Cl-+H O(未配平);
2 2
反应ii,OCN- + OH-+ Cl X + Y + Cl-+ H O(未配平)。
2 2
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1: 1
B.X、Y是CO、N,且均为反应ii的氧化产物
2 2
C.该废水处理工艺过程中须采取措施,防止Cl 逸出到空气中
2
D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl 4.48×103L
2
【答案】AC
【解析】A.反应i中氧化剂是Cl,还原剂是CN-,Cl 中的氯元素的化合价降低2,CN-中的碳元素的合
2 2
价升高2(由+2升高到+4),因此i中氧化剂与还原剂的化学计量数之比为1: 1,故A正确;
B.由题中信息可知,X、Y是两种无毒的气体,由反应所涉及的元素可知,X、Y是CO、N,N 为反应
2 2 2
ii的氧化产物,CO 不是反应ii的氧化产物,故B错误;
2
C.氯气有毒,因此该废水处理工艺过程中须采取措施防止Cl 逸出到空气中,故C正确;
2D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,物质的量为0.000 1 mol·L−1×106 L=100mol,则失去电子
100mol×(2+3)=500mol,因此消耗氯气250mol,标况下的Cl 体积为250mol×22.4 L·mol−1=5.6×103L,故D
2
错误。
综上所述,答案为AC。
15.(滨州市2020届高三第三次模拟考试)工业上用发烟HC1O 将潮湿的CrC1 氧化为棕色的烟
4 3
[CrO (C1O)],来除去Cr(Ⅲ),HC1O 中部分氯元素转化为最低价态。下列说法错误的是( )
2 4 2 4
A.CrO(C1O) 中Cr元素显+6价
2 4 2
B.HC1O 属于强酸,该反应还生成了另一种强酸
4
C.该反应中,参加反应的氧化剂与氧化产物的物质的量之比为3:8
D.该反应离子方程式为19ClO +8Cr3++8OH-=8CrO (ClO )+3C1-+4H O
2 4 2 2
【答案】D
【解析】A.CrO(ClO ) 中O为-2价、Cl为+7价,则根据化合物中元素化合价代数和等于0,可知Cr元素
2 4 2
化合价为+6价,A正确;
B.Cl元素非金属性较强,HClO 属于强酸,HC1O 氧化CrC1 为棕色的[CrO (C1O)],部分HClO 被还原
4 4 3 2 4 2 4
生成HCl,HCl也属于强酸,B正确;
C.根据电子守恒、电荷守恒及原子守恒,可得该反应的离子方程式为19ClO -+8Cr3+
4
+4H O=8CrO(ClO )+3C1-+8H+,化合价降低的为氧化剂ClO -,其中有3mol Cl元素发生变化,化合价升高
2 2 4 2 4
的为还原剂,对应的产物为氧化产物,故CrO(ClO ),其中有8mol Cr元素发生变化,故氧化剂与氧化产
2 4 2
物的物质的量之比为3:8,C正确;
D.根据选项B分析可知该反应的离子方程式为19ClO -+8Cr3++4H O=8CrO(ClO )+3C1-+8H+,D错误;
4 2 2 4 2
故合理选项是D。
16.(湖北省2020届高三下学期6月供卷理综化学)我国科技工作者提出的一种OER(氧气析出反应) 机理如
图所示。下列说法错误的是A.物质M不能改变OER反应的趋势
B.每一步反应过程都是氧化还原反应
C.反应过程中只涉及极性键的断裂和形成
D.该总反应方程式为4OH--4e- 2HO+O↑
2 2
【答案】C
【解析】A.OER机理为氧气析出反应,根据图示可知,M为转化过程的催化剂,催化剂能改变反应进程
或改变反应速率,但不能改变OER反应转化率或氧气的产率,故A错误;
B.根据图示,OER(氧气析出反应) 机理每一步反应过程都有电子得失,是氧化还原反应,故B正确;
C.根据图示,反应过程中除了涉及极性键的断裂和形成,由M-O转化为M-OOH含有非极性键的形成,
故C错误;
D.根据图示,可知M为OER(氧气析出反应) 机理的催化剂,四步反应中,每步都有电子失去,反应过程
中生成水和氧气,该总反应方程式为4OH--4e- 2HO+O↑,故D正确;
2 2
答案选C。
17.(2020年山东新高考化学全真模拟卷三,不定项)工业是制取高铁酸钾(K FeO),是先制取高铁酸钠,
2 4
然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备NaFeO 的主要反应为:
2 4
2Fe(OH) +3ClO﹣+4OH﹣=2FeO2﹣+3Cl﹣+5H O;干法备 NaFeO 的主要反应为:2FeSO +6Na O =
3 4 2 2 4 4 2 2
2NaFeO+2Na SO +O ↑。下列有关说法不正确的是( )
2 4 2 4 2
A.湿法和干法制备中,生成1molNa FeO 转移电子数目相同
2 4
B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小
C.干法制备的主要反应中NaO 是氧化剂
2 2
D.KFeO 处理水时,既能杀菌消毒,生成的Fe(OH) 胶体还能吸附水中的悬浮杂质
2 4 3
【答案】AC
【解析】【分析】利用氧化还原基本原理及四组关系分析电子的转移、氧化剂、还原剂;胶体微粒直径介
于 ,可以吸附杂质。
【详解】A.湿法中每生成1molNa FeO,有1molFe(OH) 参加反应,化合价由+3价升高到+6价,转移电
2 4 3
子3mol,干法中每生成1molNa FeO,有1molFeSO 参加反应,化合价由+2价升高到+6价,转移电子
2 4 4
4mol,同时还有0.5mol氧气生成,又转移1mol电子,所以生成1molNa FeO 转移电子数目不相同,故A
2 4错误;
B.在低温下,高铁酸钾容易变成固体析出,所以高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小,故
B正确;
C.反应中NaO 中O元素的化合价既升高又降低,则干法制备的主要反应中NaO 即是氧化剂又是还原剂,
2 2 2 2
故C错误;
D.KFeO 具有强氧化性,利用其强氧化性能杀菌消毒,生成的Fe(OH) 胶体具有吸附性,能吸附悬浮物,
2 4 3
故D正确;答案选AC。
18.(日照市2020届高三校际联合考试化学试题,不定项)由一种阳离子与两种酸根阴离子组成的盐称为混
盐 。 向 混 盐 NaSO 中 加 入 足 量 稀 硫 酸 , 发 生 反 应 :
4 2 3
。下列说法正确的是( )
A.NaSO 的水溶液显碱性
4 2 3
B.1mol Na SO 中共含离子数为5N
4 2 3 A
C.上述反应中,每产生3molS,转移电子的物质的量为6mol
D.CaOCl 也可称为混盐,向CaOCl 中加入足量稀硫酸会有Cl 产生
2 2 2
【答案】AD
【解析】【分析】混盐NaSO 中S元素的平均化合价为+1价,应为NaSO 和NaS的混盐,混盐CaOCl
4 2 3 2 3 2 2
中相当于含有CaCl 和Ca(ClO) 两种盐。
2 2
【详解】A.由分析可知NaSO 为NaSO 和NaS的混盐,NaSO 和NaS都是强碱弱酸盐,溶液呈碱性,
4 2 3 2 3 2 2 3 2
A正确;
B.由分析可知NaSO 为NaSO 和NaS的混盐,所以1molNa SO 中共含离子数为2+1+2+1=6N ,B错
4 2 3 2 3 2 4 2 3 A
误;
C.由 可知,生成单质硫的S元素化合价由+1
变为0,则每产生3molS,转移电子的物质的量为3mol,C错误;
D.在酸性条件下,发生反应:Cl-+ClO-+2H+=Cl↑+H O,即向CaOCl 中加入足量稀硫酸会有Cl 产生,D
2 2 2 2
正确;
答案选AD。
19.(泰安市肥城市2020届高三适应性训练,不定项)铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O 2PbO+2SO ;
2 2③制粗铅:PbO +C Pb +CO↑;PbO+CO Pb+CO。
2
下列说法错误的是( )
A.浮选法富集方铅矿的过程,属于物理变化
B.将lmolPbS冶炼成Pb,理论上至少需要12g碳
C.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO
D.焙烧过程中,每生成lmolPbO转移6mol电子
【答案】BC
【解析】A.浮选法富集方铅矿的过程没有新物质生成,属于物理变化,A正确;
B.将1molPbS冶炼成Pb的过程中,根据方程式得出,2PbS~2PbO~C~2Pb,1molPbS冶炼成Pb理论上至
少需要0.5mol的碳,即需要6g碳,B错误;
C.方铅矿焙烧反应2PbS+3O 2PbO+2SO 中,PbS中S元素化合价升高,是还原剂,氧元素化合价降
2 2
低,还原产物有PbO和SO ,C错误;
2
D.焙烧过程,根据Pb原子守恒,1molPbS转化为1molPbO,Pb化合价没有变化,S转移电子是6mol,D
正确;
故选BC。
20.(山东省2020届普通高中学业水平等级考试模拟卷三,不定项)偏二甲肼[(CH )N—NH]与 NO 是常
3 2 2 2 4
用的火箭推进剂,火箭发射时常出现红棕色气体,发生的化学反应如下:
①(CH)N—NH(1)+2NO(1) = 2CO (g)+3N(g)+4HO(g) H<0
3 2 2 2 4 2 2 2 1
△
②NO(1) 2NO (g) H>0
2 4 2 2
△
下列说法不正确的是 ( )
A.反应①中,NO 为氧化剂
2 4
B.反应①中,生成1mo1CO 时,转移16mo1e-
2
C.由反应②推断:加压、降温是获得液态 NO 的条件
2 4
D.温度升高,反应①的化学反应速率减小、反应②的化学反应速率增大
【答案】BD
【解析】A.反应①中,NO 中N元素的化合价降低,发生还原反应,NO 为氧化剂,故A正确;
2 4 2 4
B.反应中C元素的化合价从-4价升高到+4价,所以反应①中,生成1mol CO 时,转移8 mol e-,故B错
2
误;
C.由反应②:增大压强逆向移动,降低温度向吸热方向移动,降低温度也向逆方向移动,所以加压、降温是获得液态NO 的条件,故C正确;
2 4
D.升高温度增大反应速率,所以温度升高,反应①的化学反应速率增大、反应②的化学反应速率增大,
故D错误。
故选BD。