文档内容
专题 04 氧化还原反应及其应用
考点01 氧化还原反应概念·················································································1
考点02 氧化还原反应的基本规律········································································3
考点03 氧化还原反应方程式的书写与配平····························································8
考点04 氧化还原反应的运用·············································································12
考点 01 氧化还原反应概念
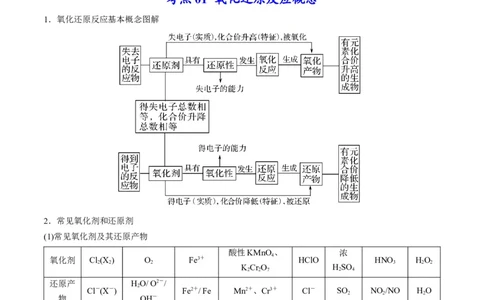
1.氧化还原反应基本概念图解
2.常见氧化剂和还原剂
(1)常见氧化剂及其还原产物
酸性KMnO 、 浓
4
氧化剂 Cl(X ) O Fe3+ HClO HNO HO
2 2 2 3 2 2
KCr O HSO
2 2 7 2 4
还原产 HO/ O2-/
2
Cl-(X-) Fe2+/ Fe Mn2+、Cr3+ Cl- SO NO /NO HO
2 2 2
物 OH-
(2)常见还原剂及其氧化产物
非金属单
还原剂 金属单质 Fe2+ HS/ S2- HI/I- NH CO SO /SO
2 3 2
质
非金属
氧化产物 金属离子 Fe3+ S、SO I N、NO CO SO 、SO
2 2 2 2 3
氧化物
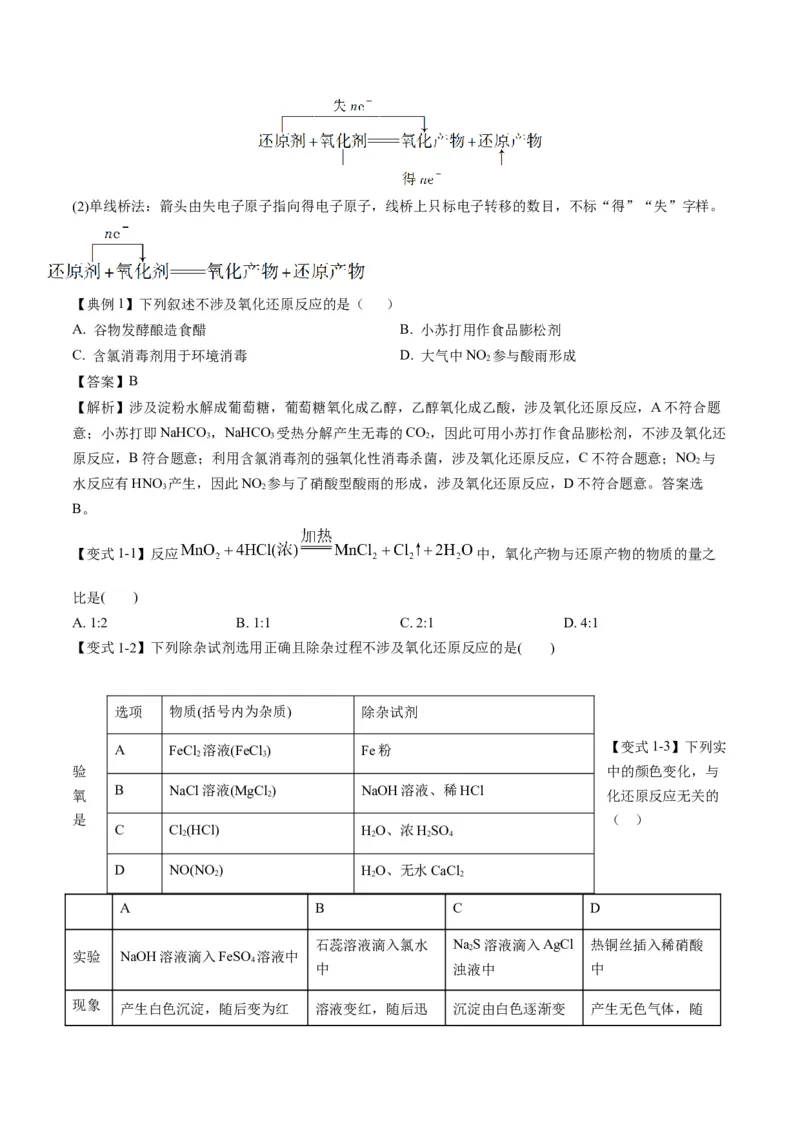
3.电子转移的表示方法
(1)双线桥法:①标变价,②画箭头,③算数目,④说变化。(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字样。
【典例1】下列叙述不涉及氧化还原反应的是( )
A. 谷物发酵酿造食醋 B. 小苏打用作食品膨松剂
C. 含氯消毒剂用于环境消毒 D. 大气中NO 参与酸雨形成
2
【答案】B
【解析】涉及淀粉水解成葡萄糖,葡萄糖氧化成乙醇,乙醇氧化成乙酸,涉及氧化还原反应,A不符合题
意;小苏打即NaHCO ,NaHCO 受热分解产生无毒的CO,因此可用小苏打作食品膨松剂,不涉及氧化还
3 3 2
原反应,B符合题意;利用含氯消毒剂的强氧化性消毒杀菌,涉及氧化还原反应,C不符合题意;NO 与
2
水反应有HNO 产生,因此NO 参与了硝酸型酸雨的形成,涉及氧化还原反应,D不符合题意。答案选
3 2
B。
【变式1-1】反应 中,氧化产物与还原产物的物质的量之
比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1
【变式1-2】下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
选项 物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉 【变式1-3】下列实
2 3
验 中的颜色变化,与
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
氧 2 化还原反应无关的
是 ( )
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
A B C D
石蕊溶液滴入氯水 NaS溶液滴入AgCl 热铜丝插入稀硝酸
2
实验 NaOH溶液滴入FeSO 溶液中
4
中 浊液中 中
现象 产生白色沉淀,随后变为红 溶液变红,随后迅 沉淀由白色逐渐变 产生无色气体,随褐色 速褪色 为黑色 后变为红棕色
考点 02 氧化还原反应的基本规律
1.氧化还原反应的基本规律
化合价升高总数与降低总数相等,实质是反应中失电子总数与得电子总
定义 数相等。即n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原
守恒律 子个数×化合价变化值。
①直接计算参与氧化还原反应物质间的数量关系。
应用
②配平氧化还原反应方程式。
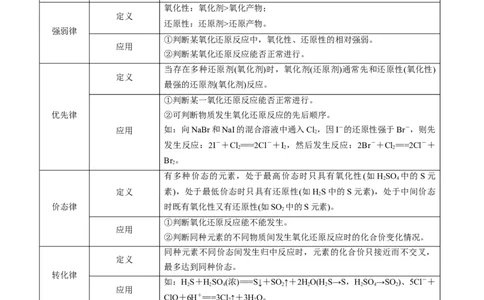
氧化性:氧化剂>氧化产物;
定义
还原性:还原剂>还原产物。
强弱律
①判断某氧化还原反应中,氧化性、还原性的相对强弱。
应用
②判断某氧化还原反应能否正常进行。
当存在多种还原剂(氧化剂)时,氧化剂(还原剂)通常先和还原性(氧化性)
定义
最强的还原剂(氧化剂)反应。
①判断某一氧化还原反应能否正常进行。
优先律 ②可判断物质发生氧化还原反应的先后顺序。
应用 如:向NaBr和NaI的混合溶液中通入Cl,因I-的还原性强于Br-,则先
2
发生反应:2I-+Cl===2Cl-+I ,然后发生反应:2Br-+Cl===2Cl-+
2 2 2
Br 。
2
有多种价态的元素,处于最高价态时只具有氧化性(如HSO 中的S元
2 4
定义 素),处于最低价态时只具有还原性(如HS中的S元素),处于中间价态
2
价态律 时既有氧化性又有还原性(如SO 中的S元素)。
2
①判断氧化还原反应能不能发生。
应用
②判断同种元素的不同物质间发生氧化还原反应时的化合价变化情况。
同种元素不同价态间发生归中反应时,元素的化合价只接近而不交叉,
定义
最多达到同种价态。
转化律
如:HS+HSO (浓)===S↓+SO ↑+2HO(H S→S,HSO→SO)、5Cl-+
2 2 4 2 2 2 2 4 2
应用
ClO+6H+===3Cl↑+3HO。
2 2
2.物质氧化性、还原性强弱的应用
当不同的氧化剂作用于同一还原剂时,若氧化产物价态相同,可依据反
物质氧化
应条件的难易程度来判断氧化剂氧化性的相对强弱,一般来说反应条件
性、还原
(1)依据反应条件 越苛刻,说明反应越难发生(即氧化剂得电子越困难),则对应氧化剂的氧
性强弱判
来判断。 化性越弱,例如:
断的常用
Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
方法
Cu+2HSO (浓) CuSO +SO ↑+2HO
2 4 4 2 2
氧化性:浓硝酸>浓硫酸。①根据元素周期表判断
(2)根据“三表”
②根据金属及非金属的活动性顺序表判断
判断。
①两种不同的金属构成原电池的两极时,负极是电子流出的一极,正极
(3)依据“两池” 是电子流入的极。则两种金属的还原性:正极<负极。
判断。 ②用惰性电极电解混合溶液时,在阴极先得电子的阳离子的氧化性较
强,在阳极先失去电子的阴离子的还原性较强。
一般情况下,浓度越大,温度越高,氧化剂的氧化性(或还原剂的还原性)
(4)依据“三度”
越强;酸碱度是影响氧化性强弱的重要因素。
判断(即:浓
例如:①KMnO 在酸性条件下具有较强的氧化性,常温下即可和浓盐酸
4
度、温度、酸碱
反应制取氯气;②HNO(浓)的氧化性强于HNO(稀)的氧化性;
3 3
度)。
③HNO(热)的氧化性强于HNO(冷)的氧化性。
3 3
【典例2】(2022·安徽池州模拟)将过量HO 溶液加入含(NH )CrO 的氨水中,加热后冷却,生成暗棕
2 2 4 2 4
红色晶体M[化学式为Cr(NH )O],其离子方程式为:CrO+3NH +3HO===M+2HO+2OH-+O↑,测
3 3 4 3 2 2 2 2
得M中有2个过氧键。下列叙述正确的是( )
A.M中Cr的化合价为+3
B.参与反应的HO 全部被氧化
2 2
C.向FeSO 溶液中滴加几滴M的溶液,没有明显现象
4
D.转移0.2 mol电子时,生成M的质量为16.7 g
【答案】D
【解析】本题考查氧化还原反应。由化学方程式可知,反应生成1 mol O ,HO 失去2 mol电子,因反应
2 2 2
生成1 mol M,CrO得(6-a)mol电子,由得失电子数目守恒可知,6-a=2,a=4,故A错;由化学方程
式可知,3 mol H O 参与反应,只有1 mol O 生成说明HO 有一部分没有被氧化,故B错;由题意M中有
2 2 2 2 2
2个过氧键,则向FeSO 溶液中滴加几滴M的溶液,亚铁离子会被M氧化为铁离子,溶液由浅绿色变为黄
4色,故C错;由离子方程式可知,反应转移2 mol电子,生成1 mol M,所以转移0.2 mol电子时,生成M
的质量为0.1 mol×167 g·
mol-1=16.7 g,故D正确。
【变式2-1】(2022·山东聊城模拟)CuS、Cu S用于处理酸性废水中的Cr O,反应如下。
2 2
反应Ⅰ:CuS+Cr O+H+―→Cu2++SO+Cr3++HO(未配平)
2 2
反应Ⅱ:Cu S+Cr O+H+―→Cu2++SO+Cr3++HO(未配平)
2 2 2
下列有关说法正确的是( )
A.反应Ⅰ和Ⅱ中各有2种元素的化合价发生变化
B.处理1 mol Cr O时反应Ⅰ、Ⅱ中消耗H+的物质的量相等
2
C.反应Ⅱ中还原剂与氧化剂的物质的量之比为3∶5
D.质量相同时,Cu S能去除更多的Cr O
2 2
【变式2-2】(2022·陕西榆林模拟)向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质
的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。
下列说法不正确的是( )
A.线段Ⅱ表示Fe2+的变化情况
B.线段Ⅳ发生反应的离子方程式为I+5Cl+12OH-===2IO+10Cl-+6HO
2 2 2
C.根据图像可计算a=6
D.原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
【变式2-3】(2022·内蒙赤峰模拟)为验证还原性SO >Fe2+>Cl-,三组同学分别进行了下图实验,并对
2
溶液1和溶液2中所含离子进行了检验,能证明上述还原性顺序的实验组有( )
溶液1 溶液2
甲 含Fe3+、Fe2+ 含SO
乙 含Fe3+,无Fe2+ 含SO
丙 含Fe3+,无Fe2+ 含Fe2+
A.只有甲 B.甲、乙
C.甲、丙 D.甲、乙、丙
【变式2-4】(2022·四川自贡模拟)已知:2Fe3++2I-===2Fe2++I2Fe2++Br ===2Fe3++2Br-。向含等物
2 2
质的量浓度的FeI、FeBr 混合溶液中通入一定量的氯气后,再滴加少量的KSCN溶液,溶液变为红色,则
2 2
下列离子方程式书写不合理的是( )
A.2Fe2++4I-+3Cl===2Fe3++2I+6Cl-
2 2B.2Br-+2I-+2Fe2++3Cl===I +Br +2Fe3++6Cl-
2 2 2
C.2Br-+4I-+2Fe2++4Cl===2I +Br +2Fe3++8Cl-
2 2 2
D.2I-+2Fe2++2Cl===2Fe3++I+4Cl-
2 2
考点 03 氧化还原反应方程式的书写与配平
1.氧化还原方程式配平的基本原则
2.氧化还原方程式配平的一般步骤
3.书写信息型氧化还原反应的步骤(三步法)
根据氧化还原顺序规律确定氧化性最强的为氧化剂,还原性最强的为还原
剂;根据化合价规律及题给信息和已知元素化合物性质确定相应的还原产物、
第1步
氧化产物;根据氧化还原反应的守恒规律确定氧化剂、还原剂、还原产物、氧
化产物的相应化学计量数。
根据溶液的酸碱性,通过在反应方程式的两端添加H+或OH-的形式使方程式
第2步
两端的电荷守恒。
根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端
2
第3步
的原子守恒。
【典例3】反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比为( )
3 2 2 4 3 2
A.2∶3 B.8∶3 C.6∶3 D.3∶2
【答案】A
【解析】该氧化还原反应用双线桥表示为 ,可知实际升价的N原子为2个,所以
2个NH 被氧化,同时Cl 全部被还原,观察计量数,Cl 为3个,因而被氧化的NH 与被还原的Cl 的物质
3 2 2 3 2
的量之比为2:3。故答案选A。
【变式3-1】(2022·广东韶关模拟)完成下列各小题。(1)将NaBiO 固体(黄色,微溶)加入MnSO 和HSO 的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该
3 4 2 4
反应的离子方程式:
NaBiO+Mn2++________→Na++Bi3++________+________。
3
(2)高铁酸钾(K FeO)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程
2 4
式:
FeO+HO===Fe(OH) (胶体)+O↑+OH-。
2 3 2
(3)以亚氯酸钠和稀盐酸为原料制备ClO ,反应原理为5NaClO+4HCl===5NaCl+4ClO ↑+2HO。该反应
2 2 2 2
中氧化剂和还原剂的物质的量之比为________。
(4)在含VO2+的溶液中加入KClO,可使VO2+转化为VO,则欲使3 mol VO2+变成VO,需要氧化剂KClO
3 3
至少为________mol。
(5)已知MO可与R2-作用,R2-被氧化为R单质,MO的还原产物中M为+3价;又知c(M O)=0.3 mol·L
2 2 2
-1的溶液100 mL可与c(R2-)=0.6 mol·L-1的溶液150 mL恰好完全反应,则n值为________。
【变式3-2】(2022·浙江省山水联盟高三选考模拟)关于反应
CH=CH +KMnO+H SO →MnSO +K SO +CO +H O (没配平),氧化产物和还原产物的物质的量之比是(
2 2 4 2 4 4 2 4 2 2
)
A.5∶6 B.6∶5 C.5∶8 D.8∶5
【变式3-3】(2022·江苏省连云港市高三联考)黄铁矿在潮湿空气中会被缓慢氧化,发生的主要反应如下(未
配平):
a: FeS+ O +H O →SO 2- +Fe2++H+
2 2 2 4
b: Fe2++H++O →Fe3++ H O→
2 2
c: Fe3++FeS + H O→Fe2+ + SO 2-+ H+→
2 2 4
下列说法正确的是( )
A.a反应中氧化产物只有FeSO
4
B.为了验证b反应后溶液中含Fe2+,可选用KSCN溶液和氯水。
C.c反应中每生成1mol Fe2+转移1mol电子
D.长期盛放黄铁矿的纸箱会被腐蚀而发黑
【变式3-4】(2022·宁夏吴忠中学高三月考)高锰酸钾是一种强氧化剂,为紫黑色、细长的棱形结晶或颗
粒,带蓝色的金属光泽,可溶于水。根据所学知识,回答下列问题:
(1)酸性条件下,高锰酸钾可与草酸( )溶液发生反应,其反应为
。
①补上产物,配平化学方程式___________。
②上述反应中HC O 表现的性质有___________。
2 2 4
(2)若将SO 通入硫酸酸化的KMnO 溶液中,溶液褪色,生成Mn2+,此时溶液中仅有一种阴离子。写出发
2 4
生反应的离子方程式:___________,该反应中作还原剂的是___________(填化学式)。
(3)高锰酸钾还可与浓盐酸反应,写出其化学方程式___________,其中浓盐酸表现酸性与还原性的物质的
量之比为:___________。考点 04 氧化还原反应的运用
【典例4】(2022·湖南省长沙市雅礼中学模拟)白银(Ag)是高新技术产业的基础材料之一。在一种光盘金
属层中回收少量白银(金属层中其他金属含量过低,对实验的影响可忽略)的流程如下:
已知:NaC1O溶液在受热或酸性条件下易分解。
下列叙述正确的是
A.“氧化”过程若在加强热和强酸性条件下进行时可提高氧化速率
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、分液漏斗
C.若“还原”过程通过原电池来实现,则N 为正极产物
2
D.“还原”过程中参加反应的n[Ag(NH) ]:n[N H·H O]=4:1
3 2 4 2
【答案】D
【解析】“氧化”过程加入氧化剂NaC1O溶液,NaC1O在受热或酸性条件下易分解,在加强热和强酸性
条件下进行时NaC1O浓度降低氧化速率减慢,A错误;操作1为过滤,所需的玻璃仪器为玻璃棒、烧杯和
普通漏斗,B错误; NH·H O中氮元素化合价升高发生氧化反应生成N,负极发生氧化反应,故N 为负
2 4 2 2 2
极产物,C错误;“还原”过程中Ag(NH) 中银元素化合价降低生成单质银,由+1价变为0价,
3
NH·H O中氮元素化合价升高生成N,由-2价变为0价,根据得失电子守恒,n[Ag(NH) ]:
2 4 2 2 3
n[N H·H O]=4:1,D正确;答案选D。
2 4 2
【变式4-1】(2022·山东青岛模拟)三氯化六氨合钴[Co(NH )]Cl 是橙黄色、微溶于水的配合物,是合成
3 6 3
其他一些含钴配合物的原料。下图是某科研小组以含钴废料(含少量Fe、Al等杂质)制取[Co(NH )]Cl 的工
3 6 3
艺流程:
回答下列问题:
(1)写出加“适量NaClO”发生反应的离子方程式:__________________________________________。
3
(2)“加NaCO 调pH至a”会生成两种沉淀,分别为__________________(填化学式)。
2 3
(3)操作Ⅰ的步骤包括________________________、冷却结晶、减压过滤。
(4)流程中NH Cl除作反应物外,还可防止加氨水时c(OH-)过大,其原理是
4
_____________________________________________________________________________。
(5)“氧化”步骤,甲同学认为应先加入氨水再加入HO,乙同学认为试剂添加顺序对产物无影响。你认为
2 2
______(填“甲”或“乙”)同学观点正确,理由是___________________________________________。
写出该步骤的化学方程式:______________________________________________________。【变式4-2】(2022·湖北荆门一中模拟)在南北朝刘宋·雷敩所著的《雷公炮炙论》中收录了一种矿物类药
材石髓铅,又称自然铜,具有活血化瘀止痛的效果。今用现代分析技术检测一份石髓铅样品,发现其含铜
极少,含有铁元素的质量分数为44.8%,硫元素的质量分数为51.2%。回答下列问题:
(1)石髓铅的主要成分是一种化合物(质量分数为96%),化学式为______________;石髓铅粉末几乎能完全
溶于硫酸酸化的高锰酸钾溶液中,形成多种硫酸盐的混合液,写出主要反应的离子方程式:
______________________。
(2)利用石髓铅、焦炭和氧气在高温下反应可制造硫黄,副产品为Fe O 和CO。Fe O 是________色晶体,
3 4 3 4
可用于制作复印机的墨粉,CO可用于合成在纺织工业中广泛使用的保险粉(Na SO),其流程如下:
2 2 4
合成塔 Ⅰ 中得到的HCOONa溶液溶质质量分数约为5%,从中分离出HCOONa·2H O的主要步骤是
2
________、________、过滤、洗涤、干燥;合成塔Ⅱ中发生主要反应的化学方程式为
___________________。
保险粉暴露在空气中易吸收氧气和水蒸气而变质,当吸收自身物质的量一半的氧气和一定量水蒸气时,变
质形成___________(填化学式)。
1.(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
2.(2022·湖南卷)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的
转化为 进入大气层,反应过程如图所示。
下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
3.(2022·北京·首都师范大学附属中学三模)下列物质在生活中的应用与氧化还原反应无关的是
A.FeSO 补血剂与维生素C配合使用效果更佳
4
B.用明矾处理污水
C.用84消毒液杀灭细菌
D.还原Fe粉用作食品脱氧剂
4.(2022·北京育才学校三模)下列离子检验利用了氧化还原反应的是
选项 待检验离子 检验试剂
A Fe3+ KSCN溶液
2-
B 稀盐酸、氯化钡溶液
SO4
C I- Cl、淀粉溶液
2
D + 浓NaOH溶液、湿润的红色石蕊试纸
NH4
5.(2022·青海西宁·一模)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A Cl(HCl) HO、浓HSO
2 2 2 4
B NaCl溶液(MgCl ) NaOH溶液、过滤、稀HCl
2
C 乙醇(乙酸) NaOH溶液、分液
D NO(NO ) HO、无水CaCl
2 2 2
6.(2022·安徽·淮北市教育科学研究所一模)高铜酸钠(NaCuO )是黑色难溶于水的固体,具有强氧化性,
2
在中性或碱性环境下稳定。一种制备高铜酸钠的原理为:2Cu+3NaClO+2NaOH=2NaCuO +3NaCl+HO。下
2 2
列说法错误的是
A.NaCuO 中铜的化合价为+3价
2
B.1molClO-参加反应转移2mol电子
C.反应中氧化产物和还原产物的物质的量之比为2∶3
D.NaCuO 与稀硫酸反应的离子方程式为:4CuO +12H+=4Cu2++O ↑+6H O
2 2 2
7.(2022·山西吕梁·一模)下列关于反应 (未配平)的说法中
不正确的是
A.被氧化的元素 和S
B.氧化剂与还原剂的物质的量之比为C.生成 (标况下) ,转移电子的物质的量是
D.还原性的强弱关系是:
8.(2022·陕西咸阳·一模) 是一种绿色的饮用水消毒剂。常用下列两种反应原理制备:
反应1:
反应2:
下列说法正确的是
A.两个反应中 都作氧化剂
B.反应1中氧化剂与还原剂的物质的量之比为1∶2
C.反应2中每转移6mol电子,生成气体的物质的量为15mol
D.制备等量的 ,反应1比反应2转移的电子总数多