文档内容
专题 05 化学反应中的能量变化
一、单选题
1.下列反应中属吸热反应的是
A.镁与盐酸反应放出氢气 B.氢氧化钠与盐酸的反应
C.硫在空气或氧气中燃烧 D.Ba(OH) ·8H O与NH Cl反应
2 2 4
2.化学与生活息息相关,下列有关说法不正确的是
A.计算机芯片的主要成分是二氧化硅
B.“温室效应”主要是由空气中CO 的浓度增大引起
2
C.“火树银花”中的焰火实质上是金属元素的焰色反应
D.“冰,水为之,而寒于水”说明相同质量和温度的水和冰,水的能量高
3.人们曾认为的N+3H 2NH 化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不
2 2 3
断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。
从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
合成氨为放热反应,下列说法正确的是
A.断开H—H健放出能量
B.反应物的总能量大于生成物的总能量
C.形成N—H键吸收能量
D.反应物的总能量小于生成物的总能量
4.“嫦娥五号”采用“比能量”达到 的锂离子蓄电池储存由高效太阳能电池产生的电能。太
阳能电池对锂离子蓄电池充电的整个过程中的能量转化形式是
A.太阳能→电能 B.太阳能→电能→化学能
C.化学能→太阳能→电能 D.太阳能→化学能→电能
5.下列有关叙述正确的是
A.“中华有为”华为Mate系列手机采用超大容量高密度电池是一种一次电池
B.根据能量守恒定律,化学反应中反应物的总能量始终等于生成物的总能量
C.等质量的硫蒸气和硫粉分别于氧气反应生成SO 气体,硫蒸气放出的能量更多
2
D.原电池中的两个电极一定是两种不同的金属材料,电解质溶液中阳离子移向正极
6.2010年4月中旬全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题,各式各样电
池的发展是化学对人类的一项重大贡献,下列有关电池的叙述正确的是
A.天然气是一次能源B.锌锰干电池中,锌电极是正极
C.手机上用的锂离子电池属于一次电池
D.太阳能电池的主要材料为二氧化硅
7.肼(H NNH)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量
2 2
(kJ):N≡N为942、O=O为500、N-N为154,则断裂1molN-H所需的能量(kJ)是
A.194 B.391 C.516 D.658
8.下列说法正确的是
A.需要加热才能进行的反应一定是吸热反应
B.2H(g)+O(g)=2HO(g) ΔH>0
2 2 2
C.测定中和热实验中,读取混合溶液不再变化的温度为终止温度
D.已知中和热的热化学方程式为:H+(aq)+OH(aq)=HO(l) △H=-57.4kJ/mol,则含28.0gKOH的稀溶液与
2
稀盐酸完全中和放出28.7kJ的热量
9.下列关于化学键和化学反应的说法中,正确的是
A.非金属元素的原子之间所形成的化学键,一定是共价键
B.化学键的形成一定伴随着电子的转移
C.化学反应中能量变化的主要原因是化学键的断裂与形成
D.物质中的化学键被破坏,一定发生化学变化
10.已知1g氢气完全燃烧生成水蒸气时放出热量121kJ。且氧气中1molO=O键完全断裂时吸收热量
496kJ,水蒸气中1molH—O键形成时放出热量463kJ,则氢气中1molH-H键断裂时吸收热量为
A.920kJ B.557kJ C.436kJ D.188kJ
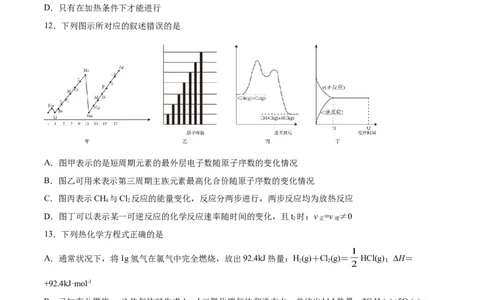
11.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是
2A.该反应是放热反应
B.反应中断开化学键吸收的总能量高于形成化学键放出的总能量
C.反应物的总能量高于生成物的总能量
D.只有在加热条件下才能进行
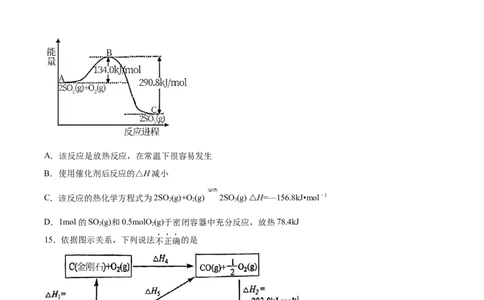
12.下列图示所对应的叙述错误的是
A.图甲表示的是短周期元素的最外层电子数随原子序数的变化情况
B.图乙可用来表示第三周期主族元素最高化合价随原子序数的变化情况
C.图丙表示CH 与Cl 反应的能量变化,反应分两步进行,两步反应均为放热反应
4 2
D.图丁可以表示某一可逆反应的化学反应速率随时间的变化,且t 时:v =v ≠0
2 正 逆
13.下列热化学方程式正确的是
A.通常状况下,将1g氢气在氯气中完全燃烧,放出92.4kJ热量:H(g)+Cl(g)= HCl(g);ΔH=
2 2
+92.4kJ·mol-1
B.已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出bkJ热量:2C H(g)+5O(g)=
2 2 2
4CO(g)+2HO(l);ΔH=-4b kJ·mol-1
2 2
C.1g炭与适量水蒸气反应生成一氧化碳和氢气,需吸收10.94kJ的热量:C+H O=CO+H ΔH=+10.94
2 2
kJ·mol-1
D.已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625kJ∙g-1:CH(g)+2O(g)=CO(g)+2HO(l);
4 2 2 2
ΔH=-55.625 kJ·mol-1
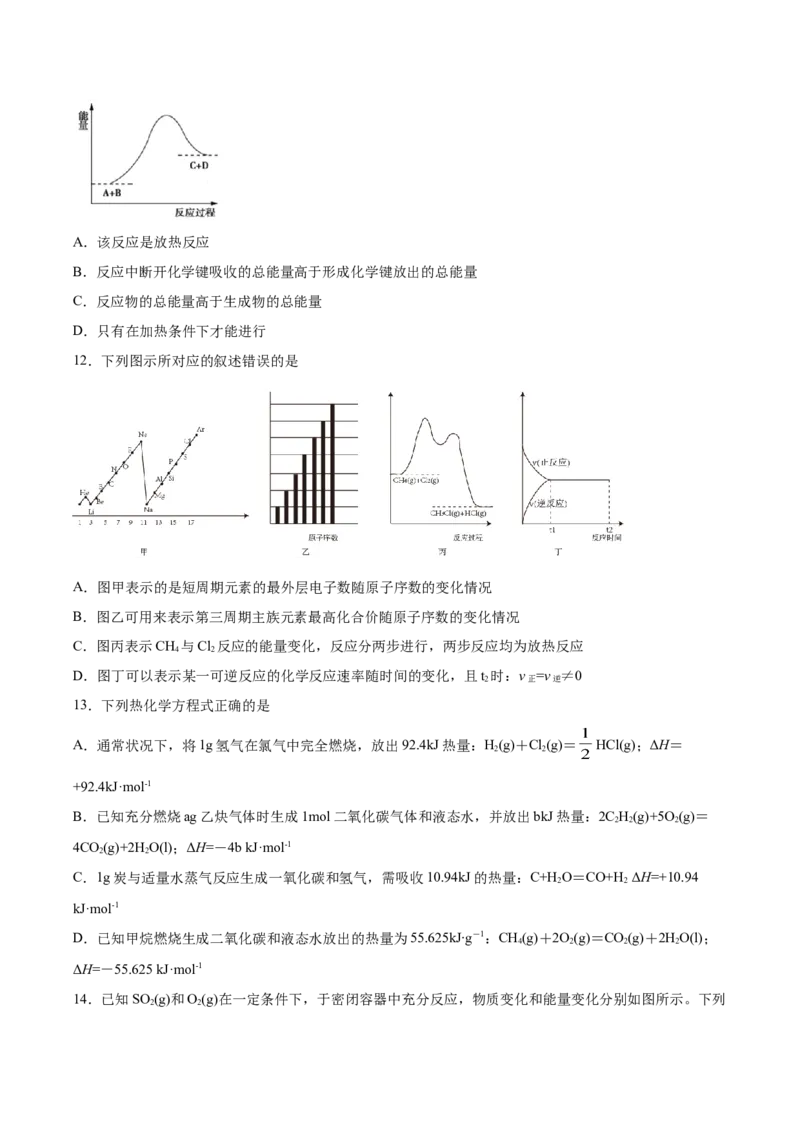
14.已知SO (g)和O(g)在一定条件下,于密闭容器中充分反应,物质变化和能量变化分别如图所示。下列
2 2说法正确的是
A.该反应是放热反应,在常温下很容易发生
B.使用催化剂后反应的△H减小
C.该反应的热化学方程式为2SO (g)+O(g) 2SO (g) △H=—156.8kJ•mol﹣1
2 2 3
D.1mol的SO (g)和0.5molO(g)于密闭容器中充分反应,放热78.4kJ
2 2
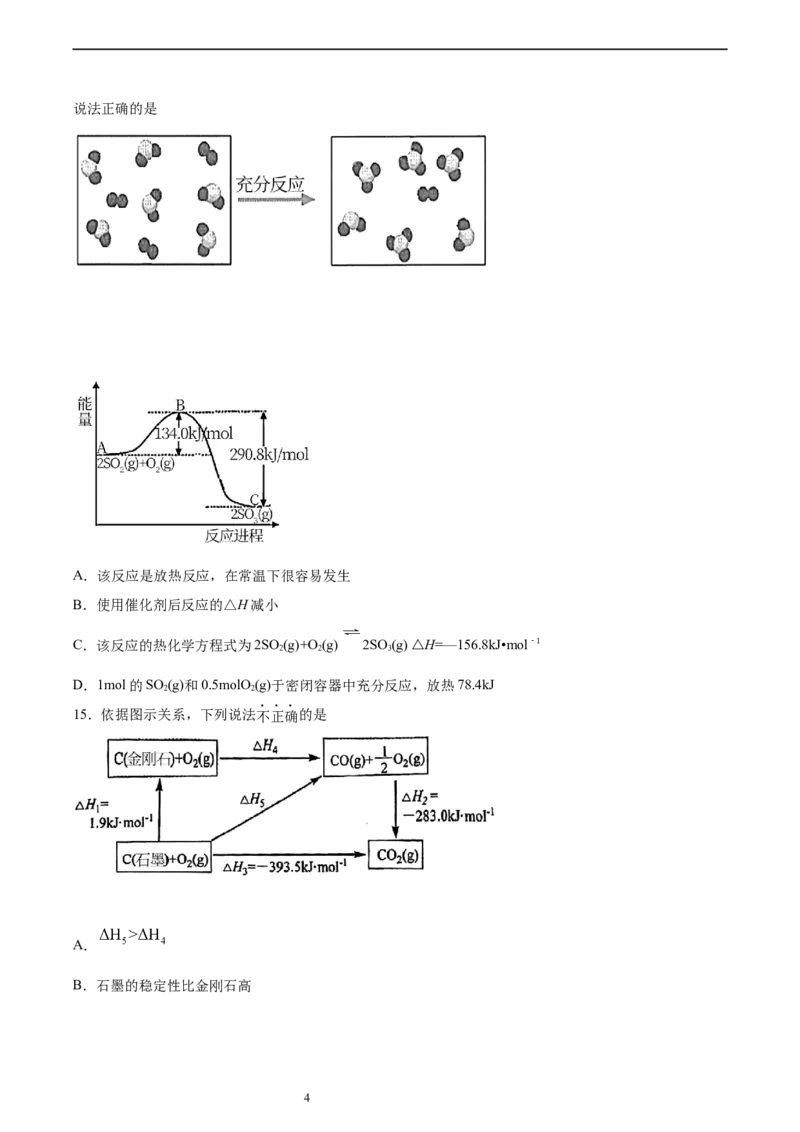
15.依据图示关系,下列说法不正确的是
A.
B.石墨的稳定性比金刚石高
4C.C(石墨,s)
D.1mol石墨或1molCO分别完全燃烧,石墨放出热量多
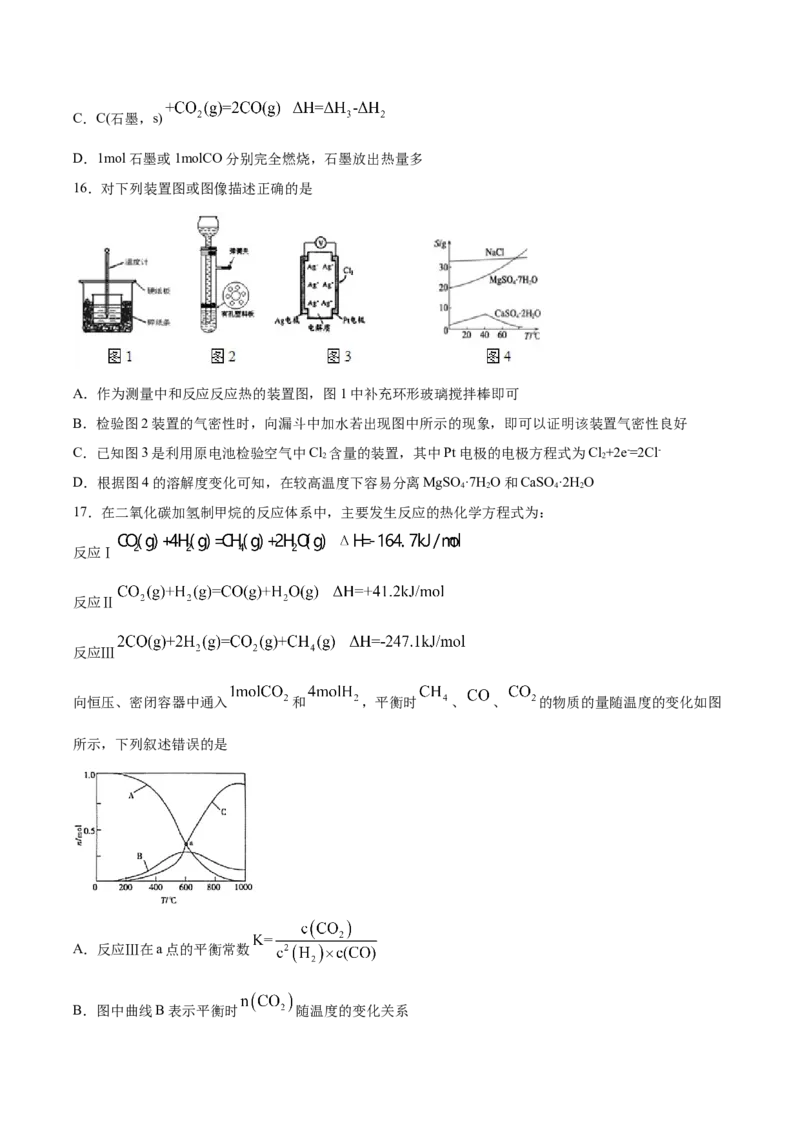
16.对下列装置图或图像描述正确的是
A.作为测量中和反应反应热的装置图,图1中补充环形玻璃搅拌棒即可
B.检验图2装置的气密性时,向漏斗中加水若出现图中所示的现象,即可以证明该装置气密性良好
C.已知图3是利用原电池检验空气中Cl 含量的装置,其中Pt电极的电极方程式为Cl+2e-=2Cl-
2 2
D.根据图4的溶解度变化可知,在较高温度下容易分离MgSO ·7H O和CaSO·2H O
4 2 4 2
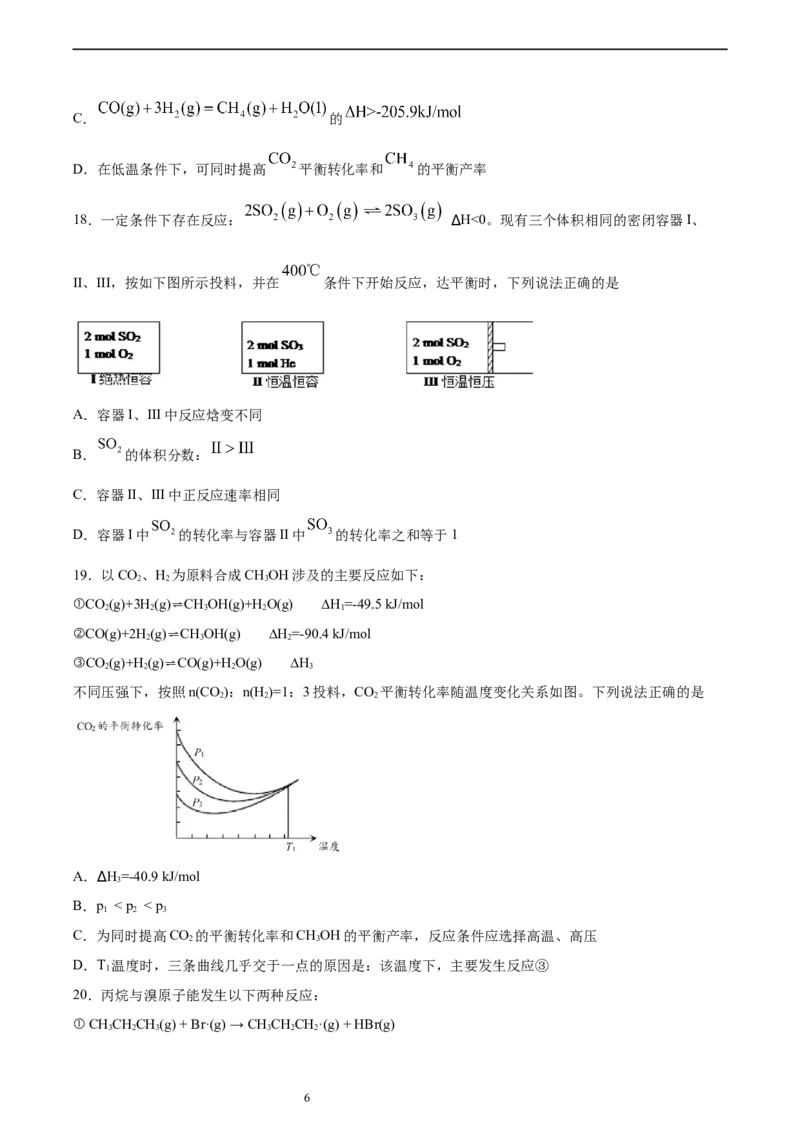
17.在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:
反应Ⅰ
反应Ⅱ
反应Ⅲ
向恒压、密闭容器中通入 和 ,平衡时 、 、 的物质的量随温度的变化如图
所示,下列叙述错误的是
A.反应Ⅲ在a点的平衡常数
B.图中曲线B表示平衡时 随温度的变化关系C. 的
D.在低温条件下,可同时提高 平衡转化率和 的平衡产率
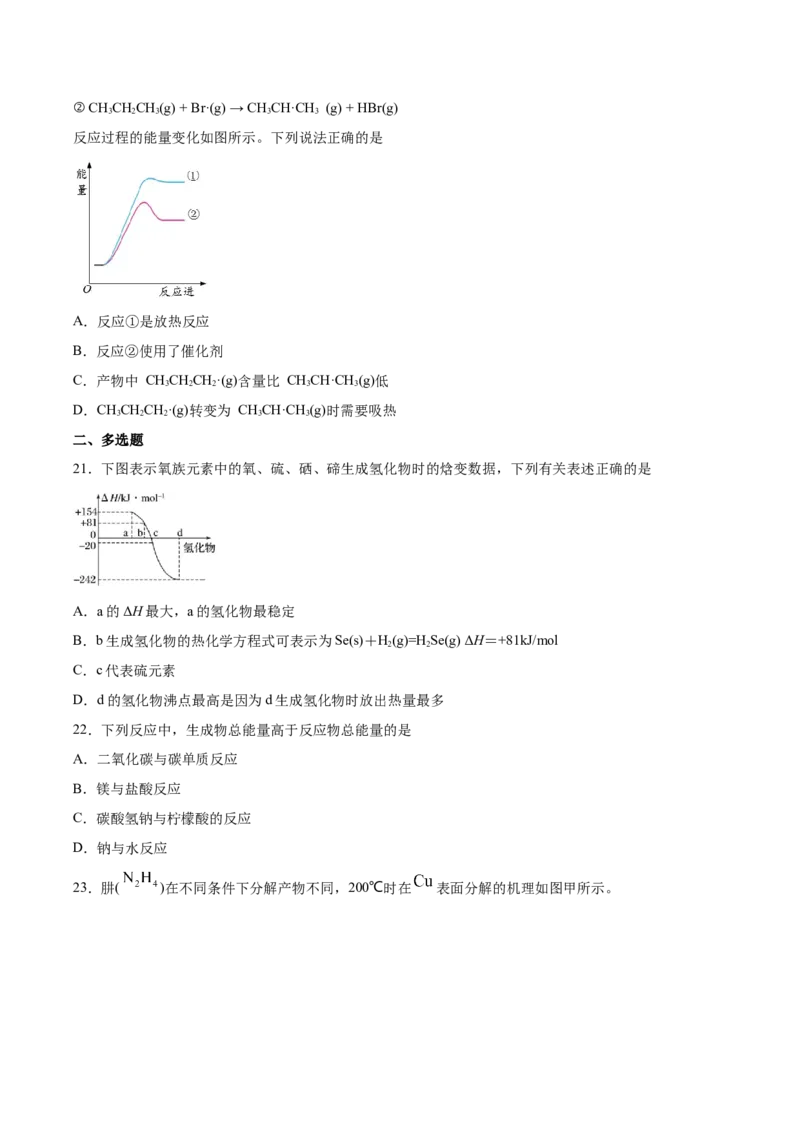
18.一定条件下存在反应: ∆H<0。现有三个体积相同的密闭容器I、
II、III,按如下图所示投料,并在 条件下开始反应,达平衡时,下列说法正确的是
A.容器I、III中反应焓变不同
B. 的体积分数:
C.容器II、III中正反应速率相同
D.容器I中 的转化率与容器II中 的转化率之和等于1
19.以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
①CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) ∆H
1
=-49.5 kJ/mol
②CO(g)+2H
2
(g)⇌CH
3
OH(g) ∆H
2
=-90.4 kJ/mol
③CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ∆H
3
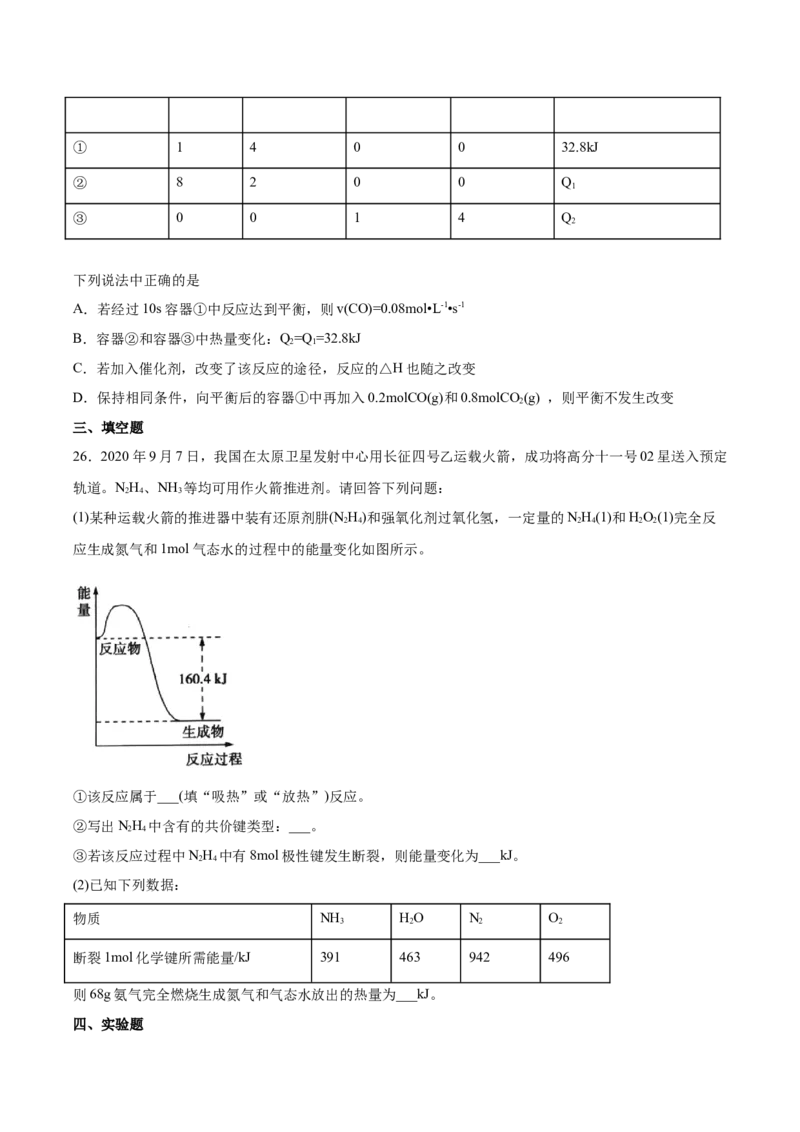
不同压强下,按照n(CO):n(H )=1:3投料,CO 平衡转化率随温度变化关系如图。下列说法正确的是
2 2 2
A.∆H=-40.9 kJ/mol
3
B.p < p < p
1 2 3
C.为同时提高CO 的平衡转化率和CHOH的平衡产率,反应条件应选择高温、高压
2 3
D.T 温度时,三条曲线几乎交于一点的原因是:该温度下,主要发生反应③
1
20.丙烷与溴原子能发生以下两种反应:
① CH CHCH(g) + Br·(g) → CH CHCH·(g) + HBr(g)
3 2 3 3 2 2
6② CH CHCH(g) + Br·(g) → CH CH·CH (g) + HBr(g)
3 2 3 3 3
反应过程的能量变化如图所示。下列说法正确的是
A.反应①是放热反应
B.反应②使用了催化剂
C.产物中 CHCHCH·(g)含量比 CHCH·CH (g)低
3 2 2 3 3
D.CHCHCH·(g)转变为 CHCH·CH (g)时需要吸热
3 2 2 3 3
二、多选题
21.下图表示氧族元素中的氧、硫、硒、碲生成氢化物时的焓变数据,下列有关表述正确的是
A.a的ΔH最大,a的氢化物最稳定
B.b生成氢化物的热化学方程式可表示为Se(s)+H(g)=HSe(g) ΔH=+81kJ/mol
2 2
C.c代表硫元素
D.d的氢化物沸点最高是因为d生成氢化物时放出热量最多
22.下列反应中,生成物总能量高于反应物总能量的是
A.二氧化碳与碳单质反应
B.镁与盐酸反应
C.碳酸氢钠与柠檬酸的反应
D.钠与水反应
23.肼( )在不同条件下分解产物不同,200℃时在 表面分解的机理如图甲所示。已知200℃时,反应I:
反应II:
下列说法正确的是
A.图甲所示过程①为放热反应,过程②为吸热反应
B.反应II的能量过程示意图如图乙所示
C.断裂 中的化学键吸收的能量大于形成 和 中的化学键释放的
能量
D. 时,肼分解生成氮气和氢气的热化学方程式为
24.一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应:2A(g)+B(s)⇌2D(g) △H<0,
测得相关数据如下,分析可知下列说法不正确的是
A.实验Ⅲ的化学平衡常数K>1
B.放出的热量关系为b kJ>2akJ
C.实验Ⅲ在30 min时达到平衡,则30 min内A的平均反应速率v(A)为0.005 mol/(L·min)
D.当容器内气体密度不随时间变化时,表明上述反应已达平衡
25.温度T℃时,在3个1L的恒容密闭容器中发生:C0(g)+H 0(g)= C0 (g) + H(g) △H =-41kJ•mol-1,其起始
2 2 2
时投料的方式、各物质的量及其达平衡过程体系热量的变化入下表所示:
起始各物质物质的量/mol
达平衡过程体系热量的
容器编号
变化(均为正值)
C0 H0(g) C0 H
2 2 2
8① 1 4 0 0 32.8kJ
② 8 2 0 0 Q
1
③ 0 0 1 4 Q
2
下列说法中正确的是
A.若经过10s容器①中反应达到平衡,则v(CO)=0.08mol•L-1•s-1
B.容器②和容器③中热量变化:Q=Q =32.8kJ
2 1
C.若加入催化剂,改变了该反应的途径,反应的△H也随之改变
D.保持相同条件,向平衡后的容器①中再加入0.2molCO(g)和0.8molCO(g) ,则平衡不发生改变
2
三、填空题
26.2020年9月7日,我国在太原卫星发射中心用长征四号乙运载火箭,成功将高分十一号02星送入预定
轨道。NH、NH 等均可用作火箭推进剂。请回答下列问题:
2 4 3
(1)某种运载火箭的推进器中装有还原剂肼(N H)和强氧化剂过氧化氢,一定量的NH(1)和HO(1)完全反
2 4 2 4 2 2
应生成氮气和1mol气态水的过程中的能量变化如图所示。
①该反应属于___(填“吸热”或“放热”)反应。
②写出NH 中含有的共价键类型:___。
2 4
③若该反应过程中NH 中有8mol极性键发生断裂,则能量变化为___kJ。
2 4
(2)已知下列数据:
物质 NH HO N O
3 2 2 2
断裂1mol化学键所需能量/kJ 391 463 942 496
则68g氨气完全燃烧生成氮气和气态水放出的热量为___kJ。
四、实验题27.I.如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管
滴入5mL盐酸于试管中。试回答下列问题:
(1)实验中观察到的现象是___________。
(2)写出有关反应的离子方程式___________。
(3)由实验推知,MgCl 溶液和H 的总能量___________(填“大于”、“小于”、“等于”)镁片和盐酸的总
2 2
能量。
II.(1)若将上述反应设计成原电池,用用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电
池的___________(填“正”或“负”,下同)极。铜片的现象为___________,电解质溶液中H+向
___________极移动。
(2)将铁棒和锌片连接后浸入CuCl 溶液里,当电池中有0.2 mol电子通过时,正极电极反应式:
2
___________,负极质量的变化是___________(填“增加”或“减少”)___________g
(3)氢氧燃料电池是常见的燃料电池,在电解质溶液是KOH溶液的负极反应为___________。
五、计算题
28.甲烷是一种重要的化工原料,广泛应用于民用和工业中。
(1)已知:①CH(g)+HO(g)=CO(g)+3H (g) ∆H
4 2 2 1
②2CO(g)+O (g)=2CO (g) ∆H=-566kJ∙mol−1
2 2 2
③H(g) O(g)=HO(g) ∆H=-242kJ∙mol−1
2 2 2 3
相关化学键的键能数据如下:
共价键 H−O C≡O H−H C−H
键能/(kJ∙mol−1) 463 1076 436 413
由此计算∆H=_______kJ∙mol−1,CH 超干重整CO 技术得到CO和H 的反应的热化学方程式为_______。
1 4 2 2
29.为防止氮的氧化物污染空气,可用活性炭或一氧化碳还原氮氧化物。
已知: ①
10②
③
回答下列问题:
Ⅰ.消除上述气体污染物可用CO与NO反应生成 和 。
(1)请完成热化学方程式: ___________ ,反应的平衡
常数表达式为 ___________。
(2)为提高此反应中NO的转化率,下列措施可行的是___________(填字母代号)。
A.增大压强 B.升高温度
C.使用催化剂 D.增大CO的浓度
Ⅱ.向2 L的密闭容器中加入活性炭(足量)和 ,发生反应:
NO和 的物质的量变化如下表所示:
物质的量浓度/( )
0 5min 10min 15min 20min 25min 30min
NO
0
(1)0~5 min内,以 表示的该反应速率 ___________ ,该条件下的平衡常数
___________。
(2)第15 min后,温度调整到 ,则 ___________ (填“>”“<”或“=”)。
(3)若30 min时,温度保持 不变,向该容器中再加入该四种反应混合物各 ,则此时反应
___________(填“正向”“逆向”或“不”)移动。
六、元素或物质推断题30.A、B、C、D、E、F、G六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子
分子,它与A的单质可形成分子X,X的水溶液呈碱性;A、D同主族,D的焰色反应为黄色;E的简单阳
离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两
个电子,C、G两种元素的原子最外层共有13个电子。则
(1)F在元素周期表中的位置为_______________。
(2)用电子式表示DF的形成过程_____________。
2
(3)在2 L的密闭容器中,充入2 mol B 和3 mol A,在一定条件下发生反应,5 s后测得A 为1.8 mol,则以
2 2 2
B 的表示的反应速率v(B )为__________________________。
2 2
(4)常温下,液态的B A 与气态的BC 两者发生反应生成无毒物质,16g B A 发生反应放热akJ,该反应的
2 4 2 2 4
热化学方程式为_______________。
(5)化学家发现一种化学式为AB 的离子化合物,一定条件下1mol A B 熔融电离生成两种离子各1mol,则
4 4 4 4
该物质熔融时的电离方程式为____________。
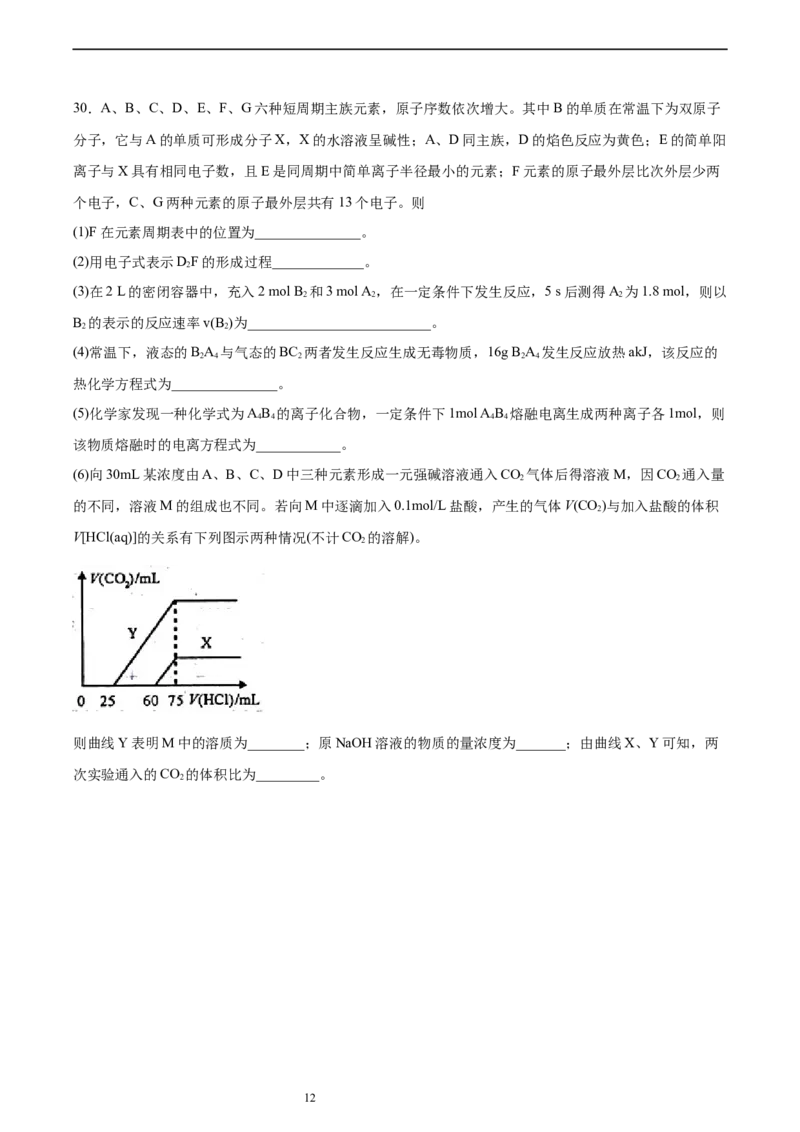
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO 气体后得溶液M,因CO 通入量
2 2
的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO)与加入盐酸的体积
2
V[HCl(aq)]的关系有下列图示两种情况(不计CO 的溶解)。
2
则曲线Y表明M中的溶质为________;原NaOH溶液的物质的量浓度为_______;由曲线X、Y可知,两
次实验通入的CO 的体积比为_________。
2
12参考答案
1.D
【详解】
A.金属和水或酸反应属于放热反应,故A不符题意;
B.酸碱中和反应属于放热反应,故B不符题意;
C.燃烧属于放热反应,故C不符题意;
D.氢氧化钡晶体和氯化铵反应生成氯化钡、氨气和水,同时吸收热量,故D符合题意;
答案为D。
2.A
【详解】
A.计算机芯片的主要成分是硅单质,故A错误;
B.二氧化碳的过度排放导致空气中二氧化碳浓度增大,引发温室效应,故B正确;
C.焰火中出现不同的焰色,是金属在灼烧中出现的焰色反应,故C正确;
D.相同质量和相同温度的液态水的能量高于固体冰的能量,故D正确;
故选:A。
3.B
【详解】
A.形成化学键放出能量,断裂化学键吸收能量,A错误;
B.该反应为放热反应,即从反应物到生成物为放出能量的过程,故反应物的总能量大于生成物的总能量,
B正确;
C.形成化学键放出能量,C错误;
D.根据B选项分析知D错误;
故答案选B。
4.B
【分析】
根据题目信息判断能量转换,充电过程中是电能转换为化学能。
【详解】
太阳能电池将太阳能转化为电能,给蓄电池充电时,电能再转化为化学能,故选答案为B。
5.C
【详解】
A.华为Mate系列手机采用的超大容量高密度电池是可充可放的电池,是二次电池,故A错误;B.根据能量守恒定律知,反应物总能量和生成物总能量不等,反应过程中有能量变化,如果正反应为放
热反应,则反应物总能量大于生成物总能量,如果正反应为吸热反应,则反应物总能量小于生成物总能量,
故B错误;
C.生成物相同,反应物中气态S比固态S能量高,且为放热反应,则硫蒸气反应放出热量多,故C正确;
D.原电池中的电极可能由导电的非金属和金属组成,如Zn、石墨和稀硫酸构成的原电池,故D错误;
故选C。
6.A
【详解】
A.天然气是古代生物的遗骸经复杂变化而形成的化石燃料,是自然界中以现成形式提供的能源,是一次
能源,故A正确;
B.锌锰干电池中锌失去电子发生氧化反应生成Zn2+,所以锌作负极,故B错误;
C.手机上的锂离子电池可以充电、放电,属于二次电池,故C错误;
D.太阳能电池的主要材料为硅,光导纤维的主要材料是二氧化硅,故D错误;
故选A。
7.B
【详解】
根据图中内容,可以看出NH(g)+O(g)=2N(g)+4H(g)+2O(g),∆E=2752J-534kJ=2218kJ,E(N-N)+E(O=O)
2 4 2 1
+4E(N-H)=2218kJ,154kJ+500kJ+4E(N-H) =2218kJ,解得E(N-H)=391kJ,故选B。
8.D
【详解】
A.是否加热为引发反应的外界条件,反应热与是否加热才能进行无关,故A错误;
B.氢气的燃烧是放热反应,ΔH<0,故B错误;
C.中和热的测定实验中,读取混合溶液的最高温度为终止温度,故C错误;
D.中和热的热化学方程式为:H+(aq)+OH(aq)=HO(l) △H=-57.4kJ/mol,表示的是强酸和强碱在稀溶液中
2
反应生成1mol水的热效应,,则含28.0gKOH的稀溶液与稀盐酸完全中和生成0.5molHO,放出的热量为
2
28.7kJ,故D正确;
故选D。
9.C
【详解】
A.非金属元素的原子之间所形成的化学键也可能是离子键,如NH Cl中, 与Cl-之间为离子键,A错
4
2误;
B.非氧化还原反应中化学键的形成没有电子转移,B错误;
C.化学反应中能量变化的主要原因是旧键断裂吸收的能量与新键形成释放的能量不相等,C正确;
D.物质中的化学键被破坏,不一定发生化学变化,如HCl溶于水会破坏共价键,但不是化学反应,D错
误;
故选C。
10.C
【详解】
根据2H+O =2H O反应,1g氢气完全燃烧生成水蒸气时放出热量121kJ,则2mol H 即4g完全燃烧生成水
2 2 2 2
蒸气时放出热量484 kJ,设1mol H—H键断裂时吸收热量为x kJ,根据化学反应放出的热量=新键生成释放
的能量-旧键断裂吸收的能量可得463kJ×4−496kJ−2x=484 kJ,x =436kJ,故答案选C。
11.B
【详解】
A.根据图象,反应物的总能量低于生成物的总能量,该反应是吸热反应,故A错误;
B.该反应是吸热反应,断裂化学键吸收能量,形成化学键放出能量,反应中断开化学键吸收的总能量高
于形成化学键放出的总能量,故B正确;
C.根据图象,反应物的总能量低于生成物的总能量,故C错误;
D.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故D错误;
故选B。
12.C
【详解】
A.短周期元素,最外层电子数:第一周期从1递增到2,二、三周期从1递增到8,周而复始,故A正确;
B.同周期主族元素从左到右,原子的最外层电子数从1递增到7,所以第三周期主族元素的最高化合价随
着原子序数增大而增加,从+1价递增到+7价,故B正确;
C.图中CH 与Cl 的第一步反应中反应物的总能量小于生成物的总能量,为吸热反应,而第二步为放热反
4 2
应,故C错误;
D.可逆反应达到平衡状态时,v(正反应)=v(逆反应)≠0,图中t 为平衡状态,v(正反应)=v(逆反应)≠0,故D
2
正确;
故选C。
13.B
【详解】A.放热反应的ΔH<0,正确的热化学方程式为: H(g)+ Cl(g)=HCl(g) ΔH=-92.4kJ·mol-1,A项
2 2
错误;
B.充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出bkJ热量,则生成4mol CO 和液态
2
水,应放出4bkJ热量,B项正确;
C.1g碳与适量水蒸气反应生成CO和H,需吸收10.94kJ热量,则1mol碳与水蒸气反应,吸收热量为
2
,且热化学方程式需要标注物质的聚集状态。则此反应的热化学方程式为C(s)
+H O(g)=CO(g)+H(g)ΔH=+131.28 kJ·mol-1,C项错误;
2 2
D.题目中给出的数据意义是:燃烧1g的甲烷放出55.625kJ的热量,换算成燃烧1mol甲烷放出的热量为
890kJ。故正确的热化学方程式为:CH(g)+2O(g)=CO(g)+2HO(l);ΔH=-890 kJ·mol-1,D项错误;
4 2 2 2
答案选B。
14.C
【分析】
由左图可知,一定条件下二氧化硫和氧气的反应为可逆反应,由右图可知,该反应为放热反应,反应的热
化学方程式为2SO (g)+O(g) 2SO (g) △H=—156.8kJ•mol﹣1。
2 2 3
【详解】
A.二氧化硫和氧气在常温下不反应,在催化剂作用下,二氧化硫和氧气共热才能反应,故A错误;
B.使用催化剂,可以降低反应的活化能,但不能改变反应的焓变,故B错误;
C.由分析可知,该反应的热化学方程式为2SO (g)+O(g) 2SO (g) △H=—156.8kJ•mol﹣1,故C正确;
2 2 3
D.由分析可知,该反应为可逆反应,1mol的SO (g)和0.5molO(g)于密闭容器中不可能完全反应,则反应
2 2
放出的热量小于78.4kJ,故D错误;
故选C。
15.C
【详解】
A.根据盖斯定律可知, ,故 =(-393.5kJ/mol)-
(-283.0kJ/mol)=-110.5kJ/mol,又 = ,故 =(-110.5kJ/mol)-1.9 kJ/mol
4=-112.4 kJ/mol ,故 ,A正确;
B.由过程1中 可知,石墨转化为金刚石是吸热的,故石墨具有的能量低于金刚石,故石墨的稳定性
比金刚石高,B正确;
C.由图可知,反应①C(石墨,s)+O(g)=CO (g) ,反应②CO(g)+ O(g)=CO (g) ,根据盖
2 2 2 2
斯定律可知,反应C(石墨,s) 由①-2②,故 ,C错误;
D.由图中可知,1mol石墨或1molCO分别完全燃烧,放出的热量分别为:393.5kJ、283.0 kJ,故石墨放出
热量多,D正确;
故答案为:C。
16.D
【详解】
A.大小烧杯口应相平,尽量防止热量散失,故A错误;
B.检验图2装置的气密性时,先关闭止水夹,再向漏斗中加水若出现图中所示的现象,且一段时间液柱
高度不变,则可以证明该气密性良好,故B错误;
C.由2Ag+Cl =2AgCl及装置可知,Ag失去电子作负极,而Pt电极作正极,正极发生还原反应,电极反
2
应式为Cl+2e-+ 2Ag+=2AgCl,故C错误;
2
D.由图可知,温度高于40℃时MgSO •7H O和CaSO•2H O溶解度差异较大,则在较高温度下容易分离
4 2 4 2
MgSO •7H O和CaSO•2H O,要注意温度不易过高,防止结晶水合物分解,故D正确;
4 2 4 2
故选D。
17.C
【分析】
反应I、Ⅲ均为放热反应,升高温度,I、Ⅲ平衡均逆向移动,CH 物质的量减小,因此A代表CH 对应的
4 4
曲线;反应Ⅱ为吸热反应,反应Ⅲ为放热反应,升高温度,反应Ⅱ正向移动,反应Ⅲ逆向移动,CO物质
的量增大,因此C代表CO对应的曲线;则B代表CO 对应的曲线。
2
【详解】
A.反应Ⅲ的平衡常数为 ,在a点 ,所以平衡常数为:,故A正确;
B.由分析可知曲线B为CO 的物质的量变化曲线,故B正确;
2
C.由Ⅱ+Ⅲ得: ,1mol气态水的能量比
1mol液态水的能量高,气态水转化为液态水放热,故
,故C错误;
D.由图可知,温度低于600℃时,随着温度的降低甲烷物质的量增大,二氧化碳低物质的量减小,因此
在低温条件下,可同时提高 平衡转化率和 的平衡产率,故D正确;
故答案为C。
18.B
【详解】
A.焓变仅与物质的状态和系数有关,所以I、III中反应焓变相同,故A错误;
B.容器Ⅱ恒温恒容,III恒温恒压、随着反应进行,容器III的体积小于容器Ⅱ,相当于Ⅱ平衡后增大压强,
平衡右移,SO 的转化率增大,体积分数减小,故B正确;
2
C.容器II、III中压强不同,速率不同,故C错误;
D.若容器Ⅱ恒温恒容,容器Ⅰ也是恒温恒容时,两容器的投料相当,达到相同平衡状态,二氧化硫转化
率和三氧化硫转化率之和为1,但实际容器Ⅰ是绝热恒容,随反应进行温度升高,平衡逆向进行,二氧化
硫转化率减小,因此容器Ⅰ中SO 的转化率与容器Ⅱ中SO 的转化率之和小于1,故D错误;
2 3
故选B。
19.D
【详解】
A.根据盖斯定律可知,反应③可由反应①-反应②,故∆H=∆H -∆H =(-49.5 kJ/mol)-( -90.4 kJ/mol)=+40.9
3 1 2
kJ/mol,A错误;
B.分析反应①正反应为气体体积减小的方向,反应③反应前后气体体积不变,故增大压强,反应①正向
移动,CO 的转化率增大,反应③不移动,故p > p > p,B错误;
2 1 2 3
C.为同时提高CO 的平衡转化率和CHOH的平衡产率,即让反应①尽可能正向移动,而反应①是一个正
2 3
反应为气体体积减小的放热反应,故反应条件应选择低温、高压,C错误;
6D.根据A的分析可知,反应③为吸热反应且反应前后气体的体积不变,故改变压强平衡不移动,升高温
度平衡正向移动,故T 温度时,三条曲线几乎交于一点的原因是:该温度下,主要发生反应③,D正确;
1
故答案为:D。
20.C
【详解】
A.由反应过程的能量变化图可知,反应①和②生成物的能量都高于反应物的能量,属于吸热反应,故A
错误;
B.无法判断反应②是否使用了催化剂,故B错误;
C.反应①的活化能比反应②活化能高,因此反应②更容易进行,反应②产物CHCH·CH (g)含量高,故C
3 3
正确;
D.由反应过程的能量变化图可知,CHCH·CH (g)能量低,CHCHCH·(g)能量高,CHCHCH·(g)转变为
3 3 3 2 2 3 2 2
CHCH·CH (g)时需要放热,故D错误;
3 3
故答案为C。
21.BC
【分析】
根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定;而根据热力
学,能量越低越稳定,依次进行分析;
【详解】
A.根据与氢气化合的难易程度和气态氢化物的稳定性可以判断出a、b、c、d分别代表碲、硒、硫、氧,
a的ΔH最大,a的氢化物最不稳定,A错误;
B.生成HSe的热化学方程式可表示为Se(s)+H(g)==H Se(g) ΔH=+81kJ/mol,B正确;
2 2 2
C.c代表硫元素,C正确;
D.HO的沸点最高是由于水分子间存在氢键,D错误;
2
故选BC。
22.AC
【分析】
生成物总能量高于反应物总能量,说明是吸热反应。
【详解】
A.二氧化碳与碳单质高温反应生成一氧化碳,是吸热反应,故A符合题意;
B.镁与盐酸反应是放热反应,故B不符合题意;
C.碳酸氢钠与柠檬酸的反应生成柠檬酸钠、二氧化碳和水,是吸热反应,故C符合题意;D.钠与水反应生成氢氧化钠和氢气,是放热反应,故D不符合题意。
综上所述,答案为AC。
23.AB
【详解】
A.过程①是NH 分解生成N 和NH ,已知热化学方程式I中△H为负值,所以图示过程①为放热反应,
2 4 2 3
过程②反应为2NH (g)=N(g)+3H(g),由盖斯定理可知该反应的△H=△H-3△H=92.5kJ/mol,为吸热反应,
3 2 2 1 2
故A正确;
B.反应II: ,该反应为放热反应,反应物的能量高
于生成物的能量,过程示意图如图乙所示,故B正确;
C.反应I: ,该反应为放热反应,断裂
中的化学键吸收的能量小于形成 和 中的化学键释放的能量,故
C错误;
D.由盖斯定理可知, 时,肼分解生成氮气和氢气的热化学方程式为
△H-2△H=50.7 kJ/mol,故D错误;
1 2
故选AB。
24.AB
【详解】
A.由于B为固体,该反应的平衡常数为:K= ;实验Ⅲ中,由于反应2A(g)+B(s) 2D(g)
⇌
中,c(A) =0.85mol/L,反应消耗A的浓度为1mol/L-0.85mol/L=0.15mol/L,则生成的D的浓度为
平衡
0.15mol/L,K= = <1,故A错误;
B.在恒容条件下,实验Ⅱ中A的变化浓度是实验Ⅰ中A的变化浓度的2倍,即实验Ⅱ中参加反应的A的
物质的量是实验Ⅰ中参加反应的A的物质的量的2倍,则实验Ⅱ中放出的热量是实验Ⅰ中放出热量的2倍,
即bkJ=2akJ,故B错误;
8C.实验Ⅲ达到平衡时,A的浓度变化是0.15mol/L,A的平均反应速率为
=0.005mol•L-1•min-1,故C正确;
D.由于反应方程式中B是固体,反应两边气体的质量不相等,而容器的容积固定,根据ρ= ,V是定值,
密度不变,说明混合气体的质量不变,此时正逆反应速率相等,达到了平衡状态,故D正确;
故答案为AB。
25.AD
【解析】
【详解】
A.平衡时放出的热量为32.8 kJ,故参加反应的CO的物质的量为 mol=0.8mol,故υ(CO)=
=0.08 mol•L-1•s-1,故A正确;
B.容器①中,
CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)
开始(mol):4 1 0 0
变化(mol):0.8 0.8 0.8 0.8
平衡(mol):0.2 3.2 0.8 0.8
故平衡常数k= = =1;容器①②③温度相同,故平衡常数相同,正逆反应平衡常
数互为倒数;
容器②中的平衡常数为1,令容器②中CO的物质的量变化量为amol,则:
CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)
开始(mol) 8 2 0 0
变化(mol):a a a a
平衡(mol):8-a 2-a a a
平衡常数k= =1,解得a=1.6,
令容器③中CO 的物质的量变化量为bmol,则:
2CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g)
开始(mol):1 4 0 0
变化(mol):b b b b
平衡(mol):1-b 4-b b b
平衡常数k= =1,解得b=0.8,
容器②和容器③中反应物的变化量不等,则能量变化也不等,故B错误;
C.催化剂能改变反应速率,不影响平衡的移动,也不改变反应的△H,故C错误;
D.保持相同条件,向平衡后的容器①中再加入0.2molCO(g)和0.8molCO(g) ,此时Qc= =1=K,
2
仍为平衡状态,即平衡不发生改变,故D正确;
故答案为AD。
【点睛】
判断可逆反应进行的方向:对于可逆反应,在一定的温度的任意时刻,生成物浓度的化学计量数次幂与反
应物的化学计量数次幂的比值叫做反应的浓度商,用Q 表示。Q<K时,向正反应方向进行;Q=K时,
c c c
反应平衡;Q>K时,向逆反应方向进行。
c
26.放热 极性键、非极性键 放热1283.2 1260
【详解】
(1)①由能量图可知反应物的能量高于生成物的能量,为放热反应,故答案为:放热;
②N H 中含有N-N、H-N两种化学键,前者为非极性共价键,后者为极性共价键,故答案为:极性键、非
2 4
极性键;
③由已知可得:NH(1)+2HO(1)=N(g)+4HO(g) ,1molN H 中有4mol极性键,
2 4 2 2 2 2 2 4
若该反应过程中NH 中有8mol极性键发生断裂,则有2molN H 反应,放出的热量为1283.2kJ,故答案为:
2 4 2 4
1283.2;
(2)氨气完全燃烧生成氮气和气态水的热化学方程式为:4NH (g)+3O(1)=2N(g)+6HO(g) ,根据焓变
3 2 2 2
=反应物的键能和-生成物的键能和,可得: =4×391+3×496-2×942-12×463=-1260 ,68g氨气
恰好为4mol,燃烧放出的热量为1260kJ,故答案为:1260。
27.Mg表面有大量气泡产生,Mg逐渐溶解,烧杯中石灰水变浑浊 Mg+2H+=Mg2++H ↑ 小于 正
2
10有气泡产生 正 Cu2++2e-=Cu 减少 6.5 H -2e-+2OH-=2H O
2 2
【分析】
【详解】
I.(1)镁与稀盐酸会发生反应:Mg+2HCl=MgCl +H ↑,该反应为放热反应,因Ca(OH) 溶解度随温度升高
2 2 2
而降低,故实验现象为:镁片上有大量气泡产生,镁片逐渐溶解,烧杯中溶液变浑浊,故答案为:镁片上
有大量气泡产生,镁片逐渐溶解,烧杯中溶液变浑浊;
(2)镁与盐酸反应的离子方程式为:Mg+2H+=Mg2++H↑,故答案为:Mg+2H+=Mg2++H↑;
2 2
(3)该反应为放热反应,即反应物总能量高于生成物总能量,故MgCl 溶液和H 的总能量小于镁片和盐酸
2 2
的总能量,故答案为:小于;
II.(1)由铜、镁和稀盐酸组成的原电池中,镁作负极,则作正极的是Cu;在正极,溶液中的H+得电子生
成氢气,现象为:有气泡产生;原电池中,电解质中的阳离子移向正极,答案为:正;有气泡产生;正;
(2)将铁棒和锌片连接后浸入CuCl 溶液里,形成原电池,负极上是金属锌失电子,设负极上质量减少x,
2
负极上的电极反应式为:Zn-2e- =Zn2+;铁棒为正极,正极电极反应式:Cu2++2e-=Cu;根据电极反应式可
知:1molZn反应会转移2mol电子,则转移0.2mol电子,反应的锌的质量是x=65g×0.2mol÷2mol=6.5g,所
以负极质量减少6.5g,故答案为:Cu2++2e-=Cu;减少;6.5;
(3)氢氧燃料电池总反应为2H+O =2H O(KOH为电解质),构成燃料电池,则负极氢气发生氧化反应,电极
2 2 2
反应为:H+2OH--2e-=2H O,故答案为:H+2OH--2e-=2H O。
2 2 2 2
【点睛】
本题重点Ⅱ,在原电池中,相对活泼的金属电极为负极,相对不活泼的金属电极或非金属电极作正极,且
负极材料能与电解质溶液发生氧化还原反应;设计原电池时,需分析电池反应,失电子的反应物作负极,
得电子的离子来自电解质。
28.+194 CH (g)+CO(g)= 2CO+2H(g) △H=+235 kJ∙mol−1
4 2 2
【详解】
(1)化学反应的△H=旧键断裂吸收的能量-新键形成放出的能量,根据表格数据计算△H=463 kJ∙mol−1×2+
1
413 kJ∙mol−1×4-1076 kJ∙mol−1-436kJ∙mol−1×3=+194kJ∙mol−1,根据盖斯定律,第①个方程式减去第②个方
程式的一半,在加上第③个方程式得到CH 超干重整CO 技术得到 CO 和H 的反应的热化学方程式为
4 2 2
CH(g)+CO(g)= 2CO+2H(g) △H=+235 kJ∙mol−1;故答案为:+194;CH(g)+CO(g)= 2CO+2H(g)
4 2 2 4 2 2
△H=+235 kJ∙mol−1。29. KJ/mol AD > 正向
【详解】
Ⅰ.(1)根据盖斯定律:②×2-①-③得: ;根
据平衡常数的定义,平衡常数表达式 。故答案为: KJ/mol;
(2)由于该反应是气体体积减小的放热反应,
A.增大容器压强平衡正向移动,NO转化率增大,A正确;
B.升高温度平衡逆向移动,NO转化率减小,B错误;
C.使用优质催化剂不改变平衡,C错误;
D.增大CO的浓度,可以提高NO的转化率,D正确。故答案为:AD
Ⅱ.根据盖斯定律:上述已知反应②-③得:
;
(1)利用表格数据:0~5 min内,以 表示的该反应速率
所以以 表示的该反应速率 ;
通过分析知10 min后浓度不再改变,处于平衡状态,分析浓度改变如下:
12平衡常数 。故答案为:0.042;
(2)第15 min后,温度调整到 ,从表格查得NO减少, 增加,平衡正向移动,由于正反应为放热反应,
改变条件为降温,则 。故答案为:>
(3)若30 min时,保持 不变,此时由30min时平衡浓度可得 时平衡常数 ,加入混合
物后反应混合物各物质浓度增加 ,所以此时的浓度熵为 ,则此时反应
正向移动。故答案为:正向。
30.第三周期ⅥA族 0.04mol·L-1·s-1 2N H(l)
2 4
+2NO(g)=3N(g)+4HO(l) △H=-4akJ/mol NH N NH +N NaHCO 和NaCO 0.25mol/L
2 2 2 4 3 3 2 3
3:10
【分析】
A、B、C、D、E、F、G六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,
它与A的单质可形成分子X,X的水溶液呈碱性,X是氨气,因此A是H,B是N;A、D同主族,D的焰
色反应为黄色,D是Na;E的简单阳离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素,
属于E是Al;F元素的原子最外层比次外层少两个电子,F是S,因此G是Cl。C、G两种元素的原子最外
层共有13个电子,因此C的最外层电子数是13-7=6,则C是O;A、B、C、D、E、F、G分别是H、N、
O、Na、Al、S,据此分析。
【详解】
(1) F是S,S在元素周期表中的位置为第三周期ⅥA族;
(2)D F即为NaS,属于离子化合物,两个Na最外层分别失去一个电子,给了硫原子,用电子式表示形成
2 2
过程为: ;
(3)在2 L的密闭容器中,充入2molN 和3molH ,在一定条件下发生反应,5 s后测得H 为1.8 mol,说明
2 2 2消耗氢气是1.2mol,因此消耗氮气是0.4mol,浓度是0.2mol/L,则以B 的表示的反应速率v(B )=
2 2
=0.04mol·L-1·s-1;
(4)常温下,液态的NH 与气态的NO 两者发生反应生成无毒物质,生成物是氮气和HO。16gNH 即
2 4 2 2 2 4
0.5molNH 发生反应放热akJ,该反应的热化学方程式为2NH(l)+2NO(g)=3N(g)+4HO(l)△H=-4akJ/mol;
2 4 2 4 2 2 2
(5)A B 为HN,一定条件下1mol HN 熔融电离生成两种离子各1mol,生成的离子为NH +、N-,则该离
4 4 4 4 4 4 4 3
子化合物为NH N,其电离方程式为NH N NH +N ;
4 3 4 3
(6)由A、B、C、D中三种元素形成一元强碱为NaOH,曲线X、Y,开始没有气体,加入一定体积盐酸后
生成气体,生成气体的反应为:HCO +H+=H O+CO↑,再结合反应OH-+H+=H O、H++CO =HCO 可知,
2 2 2
若X中只有NaCO,开始发生H++CO =HCO ,前后两过程消耗HCl的体积相等,而实际开始阶段消耗
2 3
盐酸体积大于产生二氧化碳消耗的盐酸体积,故X曲线表明M中的溶质为NaOH、NaCO,Y曲线中,前
2 3
后消耗盐酸的体积之比为1:3,则曲线Y表明M中溶质为NaCO、NaHCO ,且二者物质的量之比为1:
2 3 3
2,根据钠元素守恒可知,当加入75mL盐酸时,溶液中的溶质为氯化钠,所以原溶液中的氢氧化钠的物质
的量为0.1mol/L×0.075L=0.0075mol,所以氢氧化钠的物质的量浓度为: ,曲线
X生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线Y生成二氧化碳消耗盐酸体积为(75-
25)mL=50mL,由HCO +H+=H O+CO↑可知,则两次实验通入的CO 的体积之比=15mL:50mL=3:10。
2 2 2
【点睛】
根据曲线,分析每一条曲线代表的化学反应是解本题的关键,若X中只有NaCO,开始发生H++CO
2 3
=HCO ,前后两过程消耗HCl的体积相等,而实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体
积,故X曲线表明M中的溶质为NaOH、NaCO 为难点。
2 3
14