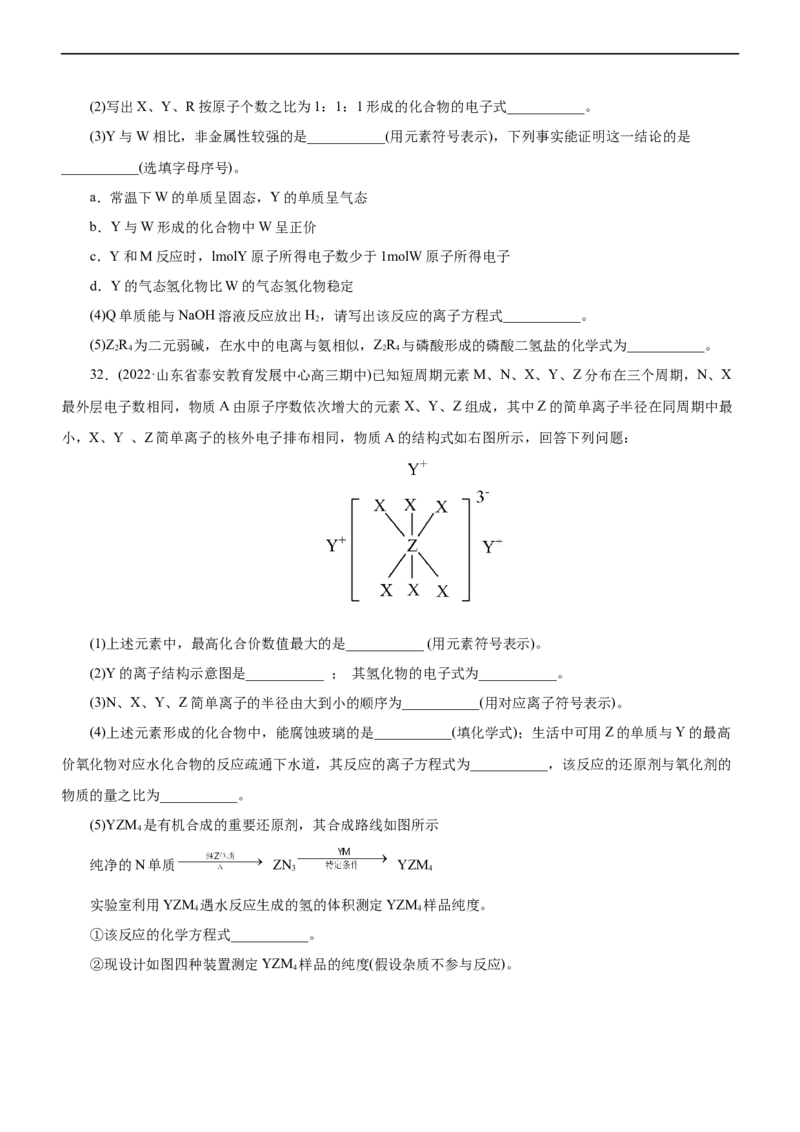文档内容
专题 05 物质结构与元素周期律
一、选择题(每小题只有一个选项符合题意)
1.(2023·北京市北师大实验中学高三期中)碘有多种同位素,其中 是稳定同位素。下列说法不正确的
是( )
A.碘元素位于第六周期ⅦA族 B.碘原子序数为53,是非金属元素
C.可用质谱法区分 和 D.I 易溶于乙醚、乙醇等有机溶剂
2
2.(2022·重庆普通高中学业水平选择性调研考试)下列排列顺序正确的是( )
A.熔点: B.微粒的半径:Cl->Al3+>Mg2+>Na+
C.热稳定性:HF>HCl>HBr>HI D.结合质子能力:F->AlO->CO2-
2 3
3.(2023·山东省泰安市高三期中)下列性质的比较,强弱关系正确且能用元素周期律解释的是( )
A.酸性:HCl>HS>HSe B.碱性:NaOН< Mg (OH) < Al (OH)
2 2 2 3
C.还原性:Cl- <Br- <I- D.沸点: NH <HF<HO
3 2
4.(2022·山西省太原市高三期中)某恒星内部发生的一种核反应为 X+ He Y+ H,X、Y为短周
期元素,X的周期序数是其族序数的3倍。下列说法正确的是( )
A. Y的质量数为24 B.氦气中含有非极性键
C.简单离子半径大小关系:X>Y D.X、Y的氯化物水溶液均呈中性
5.(2022·陕西省汉中市部分高中高三高三联考)下列事实或实验能作为判断依据的是( )
A.盐酸是强酸,氢硫酸是弱酸,判断氯与硫的非金属性强弱
B.热稳定性:HSe<HS<HO,判断氧、硫与硒的非金属性强弱
2 2 2
C.沸点:HO>NH >CH,判断碳、氧与氮的非金属性强弱
2 3 4
D.在MgCl 与AlCl 溶液中分别加入过量的氨水,判断镁与铝的金属性强弱
2 3
6.(2022·陕西省安康市高三期中)黑火药爆炸时发生的反应为:S+2KNO +3C=K S+N↑+3CO ↑。下列说法
3 2 2 2
错误的是( )
A.KNO 是含有共价键的离子化合物
3
B.上述元素的简单离子中,半径最大的是
C.等物质的量浓度的水溶液的酸性:HNO>H SO
2 2 4
D.N、O的最简单气态氢化物分子间均能形成氢键7.(2022·河南省名校联盟高三质量检测)短周期元素W、X、Y、Z的原子序数依次增大,W、Z同主族,
W、Y可形成阴离子YW-,X、Z可形成阴离子XZ-,下列说法错误的是( )
6 2 7
A.X、Y、Z、W的原子半径依次减小 B.气态氯化物Y的稳定性比W的弱
C.W、Z有相同的最高正价 D.X、Z形成的二元化合物的水溶液显酸性
8.(2022·广西省北海市一模)短周期主族元素X、Y、Z、W、Q、R的原子序数依次增大,其中只有Z和
W是金属元素。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z的原子半径是
短周期主族元素中最大的,Q与Y同族。下列说法一定正确的是( )
A.简单离子半径的大小顺序:W>Q>R>Y
B.W的最高价氧化物的水化物是两性氢氧化物
C.X的最简单氢化物沸点低于Y的最简单氢化物沸点
D.ZY 和QY 均具有漂白性,且漂白原理相同
2 2 2
9.(2022·四川省宜宾市高三第一次诊断性检测)X、Y、Z、M为原子序数依次增大的短周期主族元素,在
周期表中互不相邻。X、Z同主族,Y、Z原子序数相差4,Z和M最外层电子数之和为8。下列叙述正确的是(
)
A.原子半径:M>Z>Y>X B.最高价含氧酸酸性:M>Y
C.ZX为共价化合物 D.Z的氧化物只有一种
10.(2022·广东省揭阳市揭东区教育局教研室高三期中)短周期元素X、Y、Z中,其中X、Y位于同一主
族,Y、Z位于同一周期。X是地壳中含量最高的元素,Z原子的核外电子数比Y原子少1个,下列比较正确
的是( )
A.原子半径: B.元素非金属性:
C.气态氢化物的稳定性: D.最高价氧化物水化物的酸性:
11.(2022·陕西省安康市高三期中)X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z为地
壳中含量前三的元素,X、W同主族。下列说法错误的是( )
A.单质的导电性:YW
C.最简单气态氢化物的热稳定性:X>W
D.最高价氧化物对应水化物的酸性:W>Y
12.(2022·陕西省安康市高三期中)VCD光盘的记录材料有很多种,它们都可在激光照射下发生化学或记
忆性能的改变而记录、储存信号。碲(Te)的某种化合物就是常用的VCD光盘记录材料之一、碲元素与氧元素
同族,与碘元素同周期。下列有关说法正确的是( )
A.Te元素位于第六周期VIA族 B.单质碲在常温下是液体C.HTe的稳定性比HI的强 D.HTeO 的酸性比HSO 的弱
2 2 4 2 4
13.(2022·河南省重点中学高三模拟预测)X、Y、Z、W是原子序数递增的短周期主族元素,其中X与Z
同主族,X与Y形成的化合物是光合作用的原料之一,Z、W最高正价相差6.下列说法正确的是( )
A.X、Z两元素间可形成共价键
B.非金属性Y<W
C.简单离子半径:Y<Z<W
D.Y、W形成的某种化合物可用于消毒杀菌
14.(2023·山西省金科大联考高三质量检测)W、X、Y、Z是原子序数依次增大的短周期主族元素,W与
X形成的某种化合物是一种红棕色有刺激性气味的气体,Y的周期数是族序数的3倍,Z核外最外层电子数与
W核外电子总数相同。下列叙述错误的是( )
A.X与其他三种元素均可形成两种或两种以上的二元化合物
B.W、X、Y、Z的最高正化合价分别为+5、+6、+1、+7
C.简单离子半径:Z>W>X>Y
D.单质的熔点:Y>Z
15.(2023·四川省遂宁市高三零诊断考试)X、Y、Z、W是原子序数依次增大的短周期元素,X与W同主
族,且W原子核内质子数是X原子核外电子数的两倍,Y是同周期元素中原子半径最大的,Y、Z、W的最高
价氧化物对应的水化物可两两反应生成盐和水,甲是Z、W两种元素形成的化合物。下列说法错误的是( )
A.X单质的氧化性强于W单质
B.Z的合金在生产生活中用途广泛
C.可以在水溶液中利用复分解反应制备甲
D.离子半径:W>X>Y>Z
16.(2023·海南省部分学校一模)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Z同主族,X的
原子半径在短周期元素中最小,Y原子最外层比内层多3个电子,W原子在同周期主族元素中原子半径最小。
下列判断正确的是( )
A.X与Y、Z、W均能形成共价化合物
B.简单离子的半径:Y>Z>W
C.Z的氧化物对应的水化物含共价键、离子键
D.W的氧化物对应水化物的酸性比Y的强
17.(2022·“四校八校”高三期中质量检测)M、X、Y、Z为原子序数依次增大的短周期主族元素,其中
M、Z位于同一主族,Z的最高价含氧酸为强酸。M、Z的原子序数之和是X的2倍,Y的最外层电子数等于Z
和X的最外层电子数之差。下列叙述正确的是( )A.氢化物沸点:M<Z B.原子半径:M<X<Y<Z
C.工业上用电解法制备单质X D.华为芯片的主要成分为Y的氧化物
18.(2022·广西玉林高三第一次统考)五种短周期元素 X、Y、Z、W、Q 原子序数依次增大,W 在短周
期中原子半径最大,X、W 同族,Z、Q 同族,X、Y 两种元素的最高正价和最低负价代数和均为 0,由上述
五种元素中的某几种元素组成的两种化合物均可在一定条件下洗涤含硫的试管,以下说法正确的是( )
A.酸性:HYO Y>X>W
B.X的最高价氧化物对应水化物为弱碱
C.W与X、Y、Z形成的化合物均有离子键D.Z的单质能与水反应生成氢气
21.(2023·湖南师大附中高三检测)两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依次增大的
五种短周期主族元素。下列说法错误的是( )
A.Q的最高价氧化物对应水化物是弱酸
B.Z的某种同素异形体在大气中的含量与环境污染密切相关
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变深
2
D.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
22.(2023·吉林省长春市高三质量监测)一种外用消炎药主要成分的结构如图所示。分子结构中的苯环和甲
基部分已给出,X、Y、Z、W、M为原子序数依次增大的短周期主族元素、其中X的基态原子核外有3个未
成对电子,W与Y同主族。下列说法错误的是( )
A.简单离子半径: M>Z>X
B.简单氢化物的沸点: Y>X>CH
4
C.WY 分子与Y 分子空间结构相似
2 3
D.最高价氧化物对应水化物的酸性:M>W
23.(2023·江西省南昌市重点校高三第一次联考)中国科学院兰州化物所阎兴斌研究员研究双层电容器中储
能行为时,运用到某种离子化学物结构如图所示。其中X、Y、Z、M、L、Q均为短周期主族元素,且原子序
数依次增大。M、Q同族且两种元素组成的某种阴离子在强酸性溶液环境下可以产生淡黄色沉淀;Y是有机物
的基本骨架元素。下列结论正确的是( )
A.Z的氢化物沸点一定高于Y的氢化物
B.Q的含氧酸不一定属于强酸
C.简单离子半径大小的顺序为:Q>X>M>LD.L的铵盐溶液能存放在玻璃试剂瓶中
24.(2023·湖北省鄂东省级示范高中教育教学改革联盟学校高三联考)卤化金能与亚乙基硫脲形成盐,结构
如图所示。其中X代表卤素原子,W的丰度最大的一种核素原子核无中子,原子半径M>Y>Z,且M的最高
正价与最低负价代数和为4,下列说法不正确的是( )
A.简单氢化物的键角:Y>Z
B.M最外层电子有6种空间运动状态
C.该盐中Y、Z、M均达到8电子稳定结构
D. Au原子中电子填入的最高能级为6s
79
25.(2023·河南省三门峡市高三阶段考试)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。
4 5 8 2
W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21,YZ 分子的总电子数为奇数,常温下为气体。
2
该化合物的热重曲线如图所示,在200℃以下分解时无刺激性气体逸出。下列叙述错误的是( )
A.W与Y可形成既含极性键也含非极性键的化合物
B.最高价氧化物的水化物的酸性:
C.最简单气态氢化物的稳定性顺序为:
D.100~200℃阶段热分解的化学方程式为:YWXZ·4W Z YWXZ+4WZ↑
4 5 8 2 4 5 8 2
二、非选择题
26.(2023·山东省济宁邹城市高三期中联考)已知六种短周期元素 的原子序数依次增大, 的原子核内没有中子, A、D同主族,C、F同主族,A和B可形成5核10电子的阳离子,C与D形成
的离子化合物DC中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物
2
反应,试回答下列问题:
(1)E在元素周期表中的位置是_______。
(2)写出A和B形成4核10电子分子的电子式是_______。
(3)C、D、F的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)根据“对角线规则”,铍( )的性质与上述六种元素中的_______ (填名称)相似,能溶于氢氧化钠溶液,
生成NaBeO 与H。请写出氢氧化铍与氢氧化钠溶液反应的化学方程式_______。
2 2 2
(5)A、C、D可形成多种二元化合物,下列说法不正确的是_______ (填字母)。
A.AC 和DC 中都含共价键
2 2 2 2
B.A、D可形成离子化合物
C.DC>DC 中阴阳离子个数比均为1:2
2 2 2
D.DC和DC 均能溶于ACC,并发生化合反应
2 2 2 2
27.(2023·天津市河北区高三期中质量检测)A、B、D、E、X是原子序数依次增大的五种短周期元素。A
是周期表中相对原子质量最小的元素,A、B能形成两种液态化合物AB和AB 。D是短周期中原子半径最大
2 2 2
的主族元素,E的周期序数和族序数相等,D、X的原子最外层电子数之和为8。回答下列问题:(用化学用语
填空)
(1) A B 的电子式为__________;离子半径D__________B(填“>”或“<”)。
2 2
(2)如图所示,将少量X单质的水溶液分别滴入盛有不同试剂的试管中。
管a中发生反应的化学方程式为__________,该反应可用于制备漂白液。
②试管b中的实验现象为__________,说明X的非金属性强于碘元素,从原子结构的角度解释其原因是
__________。
(3)镓( Ga)与E为同主族元素,氮化镓(GaN)作为第三代半导体材料,具有耐高温、耐高电压等特性。下
31
列相关说法中,正确的是__________ (填字母序号)。
a.Ga位于元素周期表的第四周期
b.GaN中 的化合价为
c.Ga3+的离子半径小于 的离子半径(4)工业上用XB 处理中性废水中的Mn2+,使其转化为MnO 沉淀除去,X被还原至最低价,该反应的离子
2 2
方程式为__________。
28.(2023·江西省稳派高三期中联考)R、W、X、Y、M是原子序数依次增大的五种主族元素。R的最常见
同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX。工业革命以来,人类使用的化
2
石燃料在燃烧过程中将大量WX 排入大气,在一定程度上导致地球表而平均温度升高,Y与X是同一主族的
2
元素,且在元素周期表中与X相邻。
(1)WX 的电子式是_______。
2
(2)R X、R Y中,稳定性较高的是_______(填化学式)。
2 2
(3)Se与Y是同一主族元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是_______(填字母)。
A.Se的最高正化合价为+7 B.HSe的还原性比HY强
2 2
C.HSeO 的酸性比HYO 强 D.SeO 在一定条件下可与NaOH溶液反应
2 3 2 4 2
②室温下向SeO 固体表面吹入NH ,可得到两种单质和HO,该反应的化学方程式为_______。
2 3 2
(4)科研人员从矿石中分离出一种氧化物。化学式可表示为MO。为确定M元素的种类。进行了一系列实
2 3
验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol MO 在碱性溶液中与Zn充分反应可得到M的简单氢化物。反应完全时,被MO 氧化的Zn
2 3 2 3
为0.06 mol。
综合以上信息推断,M可能位于元素周期表第_______族。
29.(2023·河南省洛阳市第一高级中学高三阶段练习)X、Y、Z、W是原子序数依次增大的短周期主族元
素,X、Y同主族且Y的单质可用于制造太阳能电池板,Z的族序数等于X的核外电子数。回答下列问题:
(1)Y、Z、W原子半径由大到小的顺序为_______(用元素符号表示)。
(2) XZ 在工业上可用作溶剂、制作粘胶纤维。500℃~700℃时,以Y的最高价含氧酸作催化剂,用X的
2
简单氢化物和Z单质反应可制备XZ,同时生成Z的简单氢化物,此反应的化学方程式为___。
2
(3)XHW 和YHW 均是重要的化工原料,二者结构相似。
3 3
①XHW 的电子式为_______。
3
②XHW 的沸点为 ,YHW 的沸点为 ,YHW 的沸点更高的原因为_______。
3 3 3
③YHW 遇水时发生反应生成两种酸和H。有研究表明该反应分两步进行:
3 2
第一步:2YHW +3H O=(HYO) O↓+6HW;
3 2 2
第二步:_______请补全第二步反应的化学方程式(用元素符号表示)。
(4)Z和W的简单氢化物中热稳定性更好的是_______(填化学式)。ZW 中各原子最外层均满足8电子结构,
2 2ZW 中含有的共价键类型为_______。
2 2
30.(2022·河北省保定市高三月考)我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品
种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐
剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________;普通玻璃的
主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示
(已知:a为非金属元素)。
①由a、c、d三种元素形成的离子化合物的化学式为___________。
②图中所示元素中金属性最强的是___________(填元素符号),工业上得到该元素的单质的原理为
___________(填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________(用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________(填化学式)。
⑤ad 可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,
2 2
发生反应的离子方程式为___________。
31.(2022·河南省三门峡市高三联考)X、Y、Z、W、M、R、Q是短周期主族元素,部分元素的原子半径
和化合价信息如下表所示:
X Y Z W
原子半径/(nm) 0.074 0.099 0.075 0.102
+7 +5 +6
最高或最低化合价
−2 −1 −3 −2
M的焰色反应为黄色;X、Y、R位于周期表中不同周期;Q的单质为半导体材料。
(1)Y元素在周期表中的位置是___________;构成化合物MX 的化学键类型是___________。
2 2(2)写出X、Y、R按原子个数之比为1:1:1形成的化合物的电子式___________。
(3)Y与W相比,非金属性较强的是___________(用元素符号表示),下列事实能证明这一结论的是
___________(选填字母序号)。
a.常温下W的单质呈固态,Y的单质呈气态
b.Y与W形成的化合物中W呈正价
c.Y和M反应时,lmolY原子所得电子数少于1molW原子所得电子
d.Y的气态氢化物比W的气态氢化物稳定
(4)Q单质能与NaOH溶液反应放出H,请写出该反应的离子方程式___________。
2
(5)Z R 为二元弱碱,在水中的电离与氨相似,ZR 与磷酸形成的磷酸二氢盐的化学式为___________。
2 4 2 4
32.(2022·山东省泰安教育发展中心高三期中)已知短周期元素M、N、X、Y、Z分布在三个周期,N、X
最外层电子数相同,物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最
小,X、Y 、Z简单离子的核外电子排布相同,物质A的结构式如右图所示,回答下列问题:
(1)上述元素中,最高化合价数值最大的是___________ (用元素符号表示)。
(2)Y的离子结构示意图是___________ ; 其氢化物的电子式为___________。
(3)N、X、Y、Z简单离子的半径由大到小的顺序为___________(用对应离子符号表示)。
(4)上述元素形成的化合物中,能腐蚀玻璃的是___________(填化学式);生活中可用Z的单质与Y的最高
价氧化物对应水化合物的反应疏通下水道,其反应的离子方程式为___________,该反应的还原剂与氧化剂的
物质的量之比为___________。
(5)YZM 是有机合成的重要还原剂,其合成路线如图所示
4
纯净的N单质 ZN YZM
3 4
实验室利用YZM 遇水反应生成的氢的体积测定YZM 样品纯度。
4 4
①该反应的化学方程式___________。
②现设计如图四种装置测定YZM 样品的纯度(假设杂质不参与反应)。
4从简约性、准确性考虑,最适宜的方案是___________(填编号)。
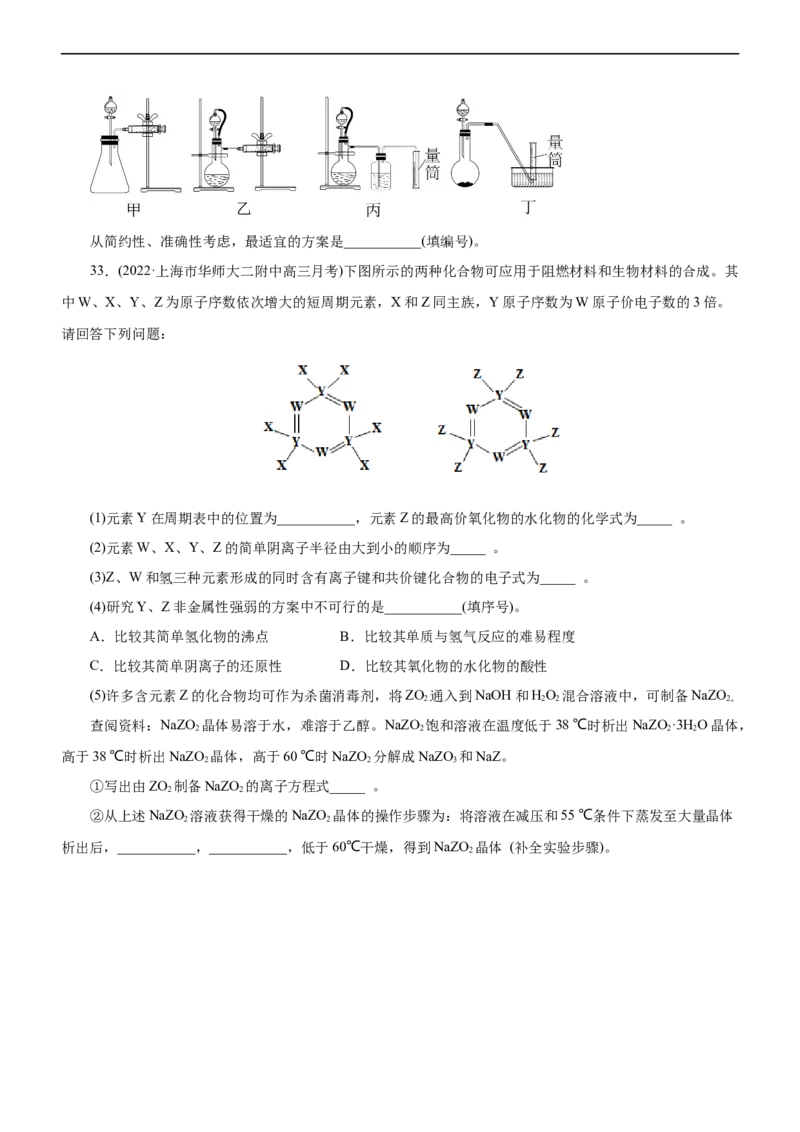
33.(2022·上海市华师大二附中高三月考)下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其
中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。
请回答下列问题:
(1)元素Y在周期表中的位置为___________,元素Z的最高价氧化物的水化物的化学式为_____ 。
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为_____ 。
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为_____ 。
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
A.比较其简单氢化物的沸点 B.比较其单质与氢气反应的难易程度
C.比较其简单阴离子的还原性 D.比较其氧化物的水化物的酸性
(5)许多含元素Z的化合物均可作为杀菌消毒剂,将ZO 通入到NaOH和HO 混合溶液中,可制备NaZO
2 2 2 2。
查阅资料:NaZO 晶体易溶于水,难溶于乙醇。NaZO 饱和溶液在温度低于38 ℃时析出NaZO·3H O晶体,
2 2 2 2
高于38 ℃时析出NaZO 晶体,高于60 ℃时NaZO 分解成NaZO 和NaZ。
2 2 3
①写出由ZO 制备NaZO 的离子方程式_____ 。
2 2
②从上述NaZO 溶液获得干燥的NaZO 晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体
2 2
析出后,___________,___________,低于60℃干燥,得到NaZO 晶体 (补全实验步骤)。
2