文档内容
专题 05 物质结构与元素周期律
1.物质发生下列变化时,需克服的作用力不属于化学键的是( )
A.HCl溶于水 B.I 升华 C.HO电解 D.烧碱熔化
2 2
【答案】B
【解析】HCl溶于水破坏了共价键;I 升华是物质的三态变化,克服的是分子间作用力;HO电解破坏的
2 2
是共价键;烧碱熔化破坏了离子键。
2.对下列物质溶于水时破坏的作用力描述错误的是( )
A.氯化钠,破坏了离子键 B.氯化氢,破坏了共价键
C.蔗糖,破坏了分子间作用力 D.二氧化碳,没有破坏作用力
【答案】D
【解析】CO 溶于水,发生CO+HO HCO,破坏了分子间作用力,也破坏了共价键。
2 2 2 2 3
3.下列各组物质的晶体中,化学键类型相同,熔化时所克服的作用力也完全相同的是
A.CO 和SiO B.NaCl和HCl C.(NH )CO 和CO(NH) D.NaH和KCl
2 2 4 2 3 2 2
【答案】D
【解析】都含有共价键,但CO 为分子晶体,SiO 为原子晶体,熔化时分别克服分子间作用力和共价键,
2 2
A错误; NaCl为离子化合物,含有离子键,HCl为共价化合物,含有共价键,B错误; (NH )CO 为离子化
4 2 3
合物,含有离子键,CO(NH) (尿素)为共价化合物,含有共价键,C错误; NaH和KCl都为离子化合物,熔
2 2
化时都克服离子键,D正确。
4.元素X的原子,其M层与K层电子数相同;元素Y的原子,其L层上有5个电子。X和Y所形成的
稳定化合物的摩尔质量为( )
A.148 g·mol-1 B.100 g·mol-1 C.90 g·mol-1 D.38 g·mol-1
【答案】B
【解析】K层是最里层,有2个电子,M层与K层电子数相同,所以M层有2个电子,所以K、L、M层
电子数分别是2、8、2,所以X是Mg(镁);Y的L层上有5个电子,说明没有全充满,所以K、L层电子数分
别是2、5,所以Y是N(氮),所以Mg和N化合成:MgN,摩尔质量:(3×24+2×14)g·mol-1=100 g·mol-1。
3 2
5.(2022·重庆市高三第四次质量检测)2020年12月17日,“嫦娥五号”顺利将 月壤带回地球。科
学家发现月壤中有地球土壤中没有的3He。3He是一种优良的核反应原料,与氘发生核聚变反应,放出巨大的能量: ,下列有关说法正确的是( )
A.D 和H 互为同位素 B.等质量的3He和2H具有相同的中子数
2 2
C.3He与 发生的核聚变反应属于化学变化 D.3He位于周期表的第1行、第18列
【答案】D
【解析】A项,D和H互为同位素,D 和H 是不同单质,A错误;B项,等质量的3He和2H中子数之比
2 2
为2∶3,B错误;C项,核聚变不是化学反应,C错误;D项,3He属于He元素,是稀有气体,位于周期表的
第1行、第18列,D正确;故选D。
6.从宏观方面看物质是由元素组成的,从微观方面看物质是由粒子构成的。下列有关说法不正确的是(
)
A.元素原子的多样性是由构成原子的质子和中子数目引起的
B.元素的化学性质主要取决于元素原子的最外层电子数
C.只由一种分子构成的物质一定是纯净物
D.质子数等于电子数的微粒,可能是一种分子和一种离子
【答案】D
【解析】A项,原子包含不同元素的不同原子和同种元素的不同原子,原子的多样性是由构成原子的质子
和中子数目引起的,正确;B项,发生化学变化时,一般是原子的最外层电子数发生变化,所以元素的化学性
质主要取决于元素原子的最外层电子数,正确;C项,只由一种分子构成的物质即只含一种物质,一定是纯净
物,正确;D项,分子或原子的质子数等于电子数,离子的质子数不等于电子数,不正确。
7.重水(D O)是重要的核工业原料,下列说法错误的是( )
2
A.氘(D)原子核外有1个电子 B.1H与D互称同位素
C.HO与DO互称同素异形体 D.1HO与DO的相对分子质量相同
2 2
【答案】C
【解析】A项,氘(D)原子为 H,原子核外有1个电子;B项,同位素指同种元素不同种核素间的互称,
1H和D(H)互为同位素,化学性质几乎完全相同;C项,同素异形体指由同一种元素组成的性质不同的单质,
HO和DO均为化合物;D项,1HO和DO的相对分子质量均是20。
2 2
8.(2023·江西省吉安市西路片七校高三联考)北斗导航系统上使用的原子钟是世界上最准确的原子钟——
2000万年相差一秒,该原子钟上使用的核素是 ,已知铯是第ⅠA族元素,下列说法错误的是( )
A.Cs元素的相对原子质量为137 B.CsOH溶液能溶解氧化铝C. 与 核外电子层结构相同 D.酚酞遇CsCO 溶液变红色
2 3
【答案】A
【解析】A项, 的质量数为137,而Cs元素的相对原子质量不是137,A错误;B项,已知铯是第Ⅰ
A族元素,金属性越强,最高价氧化物对应水化物的碱性越强,CsOH为强碱,能溶解氧化铝,B正确;C项,
原子中质子数=电子数, 与 的电子数均为55,核外电子层结构相同,C正确;D项,CsCO 为强碱
2 3
弱酸盐溶液显碱性,故酚酞遇CsCO 溶液变红色,D正确;故选A。
2 3
9.(2023·天津市河北区高三期中质量检测)下列事实不能用元素周期律解释的是( )
A.HSO 的酸性强于HSiO B. 与热水能反应,Al与热水很难反应
2 4 2 3
C.HO的稳定性强于HS D.HI的沸点高于HBr
2 2
【答案】D
【解析】A项,非金属性越强其最高价氧化物对应水化物的酸性就越强,硫的非金属性强于硅,HSO 的
2 4
酸性强于HSiO,A与题意不符;B项,同周期从左到右元素的金属性减弱,单质与水反应由易到难, Mg的
2 3
金属性大于Al,Mg能与热水反应,Al与热水很难反应,B与题意不符;C项,同主族从上到下,元素的非金
属性减弱,氢化物的稳定性减弱,HO的稳定性强于HS,C与题意不符;D项,HI的沸点高于HBr原因是前
2 2
者相对分子质量大于后者相对分子质量,D与题意相符;故选D。
10.(2023·湖北省华中师大一附中高三期中)下列关于物质的结构与性质的叙述正确的是( )
A.Li、Na同主族, Na保存在煤油中,可推断Li也保存在煤油中
B.Be、Mg同主族,MgO不溶于强碱,可推断BeO也不溶于强碱
C.Ge、Pb同主族,Ge可作半导体材料,可推断Pb也可作半导体材料
D.O、S同主族,HO 有氧化性,可推断HS 也有氧化性
2 2 2 2
【答案】D
【解析】A项,Na的密度比煤油大可以保存在煤油中,而Li的密度比煤油小,不能保存在煤油中,故A
错误;B项,BeO属于两性氧化物可溶于强碱,故B错误;C项,Pb的金属性比Ge强,是金属元素, 导体
材料,故C错误;D项,HO 有氧化性,是因-1价O容易得电子转化成-2价,HS 中S也为-1价,也容易得
2 2 2 2
电子生成-2价S,表现氧化性,故D正确;故选D。
11.(2022·湖北省部分学校高三质量检测)下列有关物质性质的比较正确的是( )
A.碱性:Ba(OH) <Ca(OH) <KOH B.离子半径:Mg2+<O2-<F--
2 2
C.还原性:SiH>PH >HCl D.热稳定性:CH>NH >HF
4 3 4 3【答案】C
【解析】A项,金属性Ca>Ba,所以碱性:Ba(OH) >Ca(OH) ,A不符合要求;B项,半径:电子层数相
2 2
同,原子序数越大半径越小,所以O2->F--,B不符合要求;C项,非金属性SiZ>X D.YZX 中Y的化合价可能为+3
3 6
【答案】C
【解析】Z为地壳中含量最高的金属元素,则Z为Al,X、Y、Z原子的最外层电子数之和为11,且最内
层电子数相同,X、Y、Z可以形成一种重要的工业原料YZX,这种原料为冰晶石,则X为F,Y为Na。A
3 6
项,HX为HF,氟化氢是弱酸,在水中不能完全电离,A项错误;B项,钠和铝最高价氧化物对应的水化物分
别是氢氧化钠和氢氧化铝,其中氢氧化铝是难溶物,B项错误;C项,电子层数越多,原子半径越多,同周期
原子半径逐渐减小,因此,Y>Z>X,C项正确;D项,化合物中Y是钠离子,化合价为+1价,D项错误;故
选C。1.核电荷数小于18的某元素X,其原子核外电子层数为a,最外层电子数为(2a+1)。下列有关元素X的
说法中不正确的是( )
A.元素X的原子核内质子数为(2a2-1)
B.元素X的原子半径一定小于钠的原子半径
C.由元素X形成的某些化合物,可能具有杀菌消毒的作用
D.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
【答案】D
【解析】若a=2,则X为N,若a=3,则X为Cl。由原子结构、相关元素及化合物的性质推知A、B、C
项正确;D项氯离子最外层电子数未达到2n2个。
2.(2023届·浙江省浙里卷天下高三开学测试)主族元素X、Y、Z、W的原子序数依次增加,Y、Z、W位
于不同周期,且序数均小于20,X的单质是手机电池重要的材料;常温下,Y的两种气态氧化物之间可发生可
逆反应;X、Y、W最外层电子数之和与Z的最外层电子数相等。下列说法正确的是( )
A.X、W的单质均为活泼金属,通常保存在煤油中
B.常温下,Z的单质与Y的气态氢化物相遇,可能产生白烟
C.Y、Z可形成YZ 化合物,YZ 不能用于进口水果的熏蒸来消杀有害病虫
3 3
D.由X、Z、W三种元素组成的化合物的水溶液显强酸性
【答案】B
【解析】主族元素X、Y、Z、W的原子序数依次增加, X的单质是手机电池重要的电极材料,推知X是
锂元素,Y的两种气态氧化物之间可发生可逆反应,NO 和NO,故Y是氮元素,X、Y、W最外层电子数之
2 2 4
和与Z的最外层电子数相等,故Z的最外层电子数为7,故W最外层1个电子,由此推知Z是氯元素,W是
钾元素。A项,锂比煤油轻,故不能保存在煤油中,而封存在石蜡中,A错误;B项,氨气和氯气反应生成氯
化铵,反应中会有大量白烟产生, B正确;C项,Y、Z可形成YZ 化合物为NCl ,有强氧化性,能用于进
3 3
口水果的熏蒸来消杀有害病虫,C错误;D项,X、Z、W三种元素分别为Li、Cl、K,KCl、LiCl的水溶液均
显中性,D错误;故选B。
3.(2022·福建师大附中高三期中)短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y同主族,W
的简单氢化物与Z的单质混合在光照下反应,气体颜色不断变浅,瓶壁上有油状液滴,X的简单氢化物与Z的
氢化物相遇会产生白烟。下列说法正确的是( )
A.“白烟”晶体中含有离子键和共价键 B.四种元素中,Z的原子半径最大
C.Y的简单氢化物的热稳定性比X的强 D.W的含氧酸的酸性一定比Z的弱
【答案】A
【解析】X的简单氢化物与Z的氢化物相遇会产生白烟,X的原子序数小于Z,则X应为N元素,Z为Cl元素,两种氢化物分别为NH 、HCl;W的简单氢化物与Z的单质,即氯气,混合在光照下反应,气体颜色不
3
断变浅,瓶壁上有油状液滴,则W为C元素,其简单氢化物为CH,W、Y同主族,所以Y为Si元素。A项,
4
“白烟”晶体为HCl和氨气反应生成的氯化铵,含有铵根和氯离子形成的离子键,同时铵根中含有氮原子和
氢原子形成的共价键,A正确;B项,电子层数越多,原子半径越大,电子层数相同时,核电荷数越小半径越
大,所以原子半径最大的是Si,B错误;C项,Si元素的非金属性弱于N元素,所以Y的简单氢化物的热稳定
性比X的弱,C错误;D项,Cl元素有多种含氧酸,例如次氯酸的酸性就比碳酸弱,D错误;故选A。
4.(2022·重庆市八中高三适应性考试)X、Y、Z、R、W是原子序数依次增大的五种短周期元素,Y和R
同主族,R的原子序数是Y的2倍,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时0.01mol/L X
和W形成化合物的水溶液pH为2,下列说法正确的是( )
A.R与Y的单质可以反应,由此可知非金属性Y>R
B.Z、Y形成的两种化合物中阴阳离子的个数比分别为1:2和1:1
C.简单离子半径由大到小排列的是:W>R>Z>Y
D.R与W的最高价含氧酸对水电离的抑制程度WS,因此非金属性O>S,故A正确;B项,NaO
2 2 2
与NaO种阴阳离子个数比均为1:2,故B错误;C项,离子半径大小为R>W>Y>Z,故C错误;D项,项
2
HSO 与HClO 对水电离的抑制程度不是看酸的酸性强弱或酸中所含氢原子的个数,而是看溶液中酸电离的氢
2 4 4
离子浓度大小,由于浓度未知,因此无法判断,故D错误;故选A。
5.(2022·河北省邢台市“五岳联盟”部分重点学校高三联考)W、X、Y、Z、M为原子序数依次增大的短
周期主族元素,W为宇宙中含量最多的元素,X的内层电子数为其最外层的一半,Z与M的最外层电子数相
同,且Z的单质与水反应可以制取Y的单质。下列说法正确的是( )
A.原子半径:M>Y>Z>X B.W与Y形成的化合物种类最多
C.最简单氢化物的沸点:ZX>Y>Z,故A错误;B项,W为H与Y为O形成的化合物有HO、HO 等,而C和H形成
2 2 2
的化合物种类最多,故B错误;C项,元素非金属性越强,最简单氢化物的沸点越高,而非金属性:F>Cl,则
沸点Z>M,故C错误;D项,X、M最高价氧化物对应水化物分别是HCO、HClO,由于碳酸是弱酸,高氯
2 3 4
酸是强酸,则酸性:XC>Si,A
正确;B项,氨气可以形成分子间氢键,使熔沸点升高,所以简单氢化物的沸点:NH >CH ,B正确;C项,
3 4
MgN 为离子化合物,其中只有离子键,没有共价键,C错误;D项,C和SiO 可以发生如下反应:2C+SiO
3 2 2 2
2CO↑+Si,该反应为置换反应,D正确;故选C。
7.(2022·广东省“六校联盟”高三第二次联考)一种矿石(Z XY ·5W Y)的组成元素W、X、Y、Z为原子
2 6 11 2
序数依次增大的1-20号元素,Z是牙齿的主要组成元素,WY分子中含有10个电子,X是一种非金属元素。
2
下列说法正确的是( )
A.Z的最高价氧化物的水化物是弱碱 B.简单离子半径:Y>Z>W
C.X的单质在通常条件下是气体 D.化合物ZY 中含有非极性共价键
2
【答案】D
【解析】Z是牙齿的主要组成元素,推断Z是Ca元素;WY分子中含有10个电子,且是三原子分子,推
2
断WY是HO,则W是H元素,Y是O元素;矿石(Z XY ·5W Y)的组成元素是1-20号元素,从矿石的常见
2 2 2 6 11 2
组成元素推断X是B元素。A项,Z的最高价氧化物的水化物是Ca(OH) ,是强碱,A错误;B项,据分析,
2
Y是O元素,Z是Ca元素,W是H元素,简单离子半径:Ca2+>O2->H+,B错误;C项,X是B元素,其单
质在通常条件下是固体,C错误;D项,化合物ZY 是CaO,其中O2-含有氧氧非极性共价键,D正确;故选
2 2 2
D。8.(2022·广东省湛江市教育局教育研究室高三检测)短周期主族元素X、Y、Z、R的原子序数依次增大,
向空气中大量排放XY 气体会导致温室效应加剧,X与Y的最外层电子数之和为10.Z的最外层电子数等于其
2
电子层数,X的原子最外层电子数和Z的原子核外电子数之和等于R的原子核外电子数。下列说法错误的是(
)
A.原子半径:Z>R>X>Y B.熔点: ZY<ZR
2 3 3
C.最简单氢化物的热稳定性:Y>X D.X与R形成的化合物不止一种
【答案】B
【解析】XY 气体会导致温室效应加剧,即CO,则X是C、Y是O,Z的最外层电子数等于其电子层数,
2 2
且原子序数大于O的,则Z为Al,X的原子最外层电子数是4和Z的原子核外电子数是13之和等于R的原子
核外电子数17,则R是Cl;所以X是C、Y是O、Z为Al、R是Cl。A项,电子层数相同的,核电荷数越大,
原子半径越小,电子层数越大,原子半径越大,则原子半径:Z>R>X>Y,A正确;B项,ZY 是Al O、
2 3 2 3
ZR 是AlCl ,Al O 是离子晶体,AlCl 是共价晶体,离子晶体熔点大于共价晶体,则熔点:ZY>ZR ,B错
3 3 2 3 3 2 3 3
误;C项,X、Y最简单氢化物分别为CH、HO,非金属性越大氢化物的热稳定性越强,非金属性:O>C,则
4 2
稳定性:Y>X,C正确;D项,X与R形成的化合物有四氯化碳CCl 、六氯乙烷C Cl 等,D正确;故选B。
4 2 6
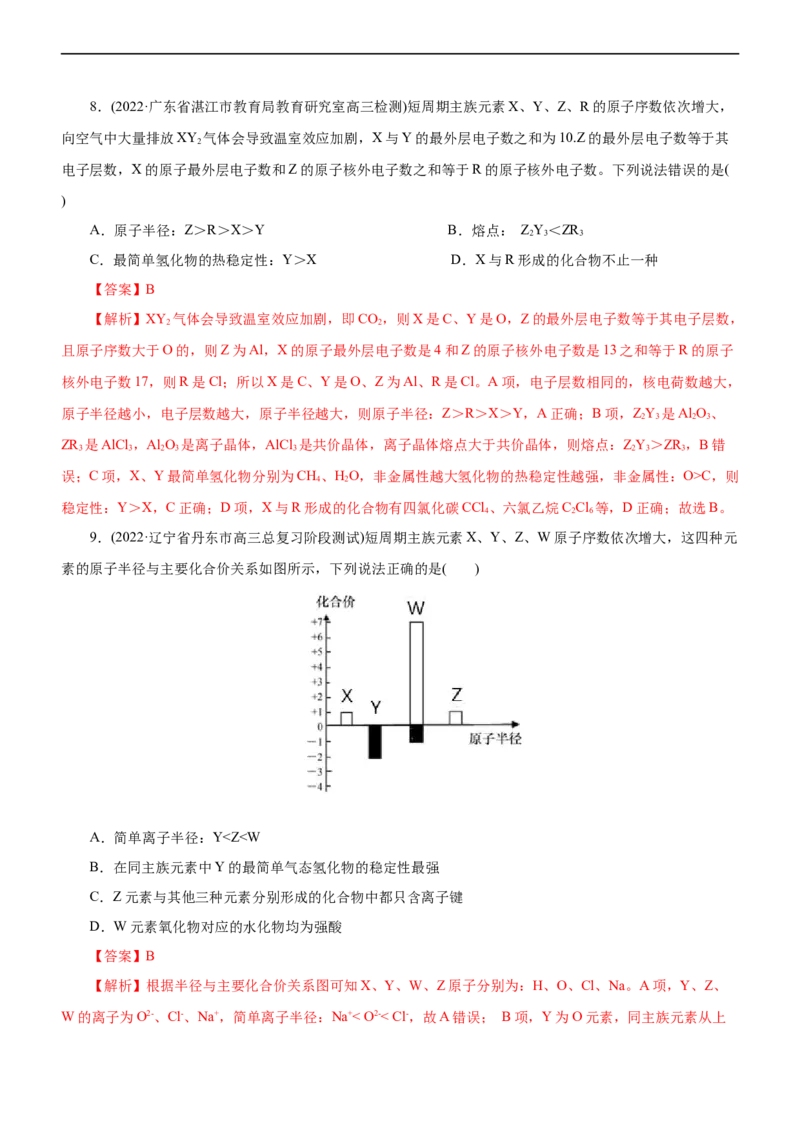
9.(2022·辽宁省丹东市高三总复习阶段测试)短周期主族元素X、Y、Z、W原子序数依次增大,这四种元
素的原子半径与主要化合价关系如图所示,下列说法正确的是( )
A.简单离子半径:YW
C.原子半径:Z>W>Y>X D.火星气体中可能含有XY、
【答案】C
【解析】已知:X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与热水反
应后溶液能使酚酞试液变为浅红色,则Z为Mg;X、W为同一主族元素,Y也是地球地壳中含量最高的元素,
则Y为O元素;火星岩石含有ZWY 则MgWO ,根据化合物中元素化合价代数和为零即+2+ x-6=0可得W的
3 3
化合价为+4价,则W为Si,X为C元素。综上所述X、Y、Z、W分别为C、O、Mg、Si。A项,W为14号
Si元素,位于元素周期表中第三周期第IVA族,故A正确;B项,X、W分别为C、Si的同一主族非金属元素,
由X的非金属性强于W,所以X、W简单氢化物的稳定性:X>W,故B正确;C项,电子层越多,原子半径
越大,同一周期,从左到右,原子半径逐渐减小,X、Y、Z、W分别为C、O、Mg、Si,则原子半径:
Z>W>X>Y,故C错;D项,XY、XY 分别为CO、CO,故D正确;故选C。
2 2
11.(2022·黑龙江省大庆市高三第一次教学质量检测)X、Y、Z、Q、R 是五种短周期主族元素,原子序数
依次增大。X、Y 最高正价与最低负价之和均为0,Q与X同主族,Z的氧化物是大气的主要污染物之一,Z
与R的最外层电子数之和为8,下列说法正确的是( )
A.原子半径大小顺序为:R>Q>Z>Y>X
B.Y的氢化物的沸点一定低于Z的氢化物
C.Z、Q、R的最高价氧化物对应的水化物两两之间可以相互反应
D.元素Q、R分别与氯元素形成的化合物均为离子化合物
【答案】C
【解析】X、Y、Z、Q、R是五种短周期主族元素,原子序数依次增大。X、Y两元素最高正价与最低负
价之和均为0,则X是H,Y为C,Q与X同主族,则Q为Na,Z的氧化物是大气的主要污染物之一,Z是
N,Z与R的最外层电子数之和为8,则R是P,X、Y、Z、Q、R分别是:H,C,N,Na,Al。A项,—般而言,电子层数越多,半径越大,电子层数相同,质子数越小,半径越大,所以原子半径大小顺序为:Na >Al >
C > N > H,A错误;B项,Y的氢化物碳原子数可能比较多,常温的时候可能为固态,沸点较大,B错误;C
项,Z、Q、R的最高价氧化物对应的水化物分别为硝酸,氢氧化钠,氢氧化铝,这些物质两两之间可以相互
反应,C正确;D项,AlCl 为共价化合物,不是离子化合物,D错误;故选C。
3
12.(2022·吉林省长春外国语学校阶段测试)W、X、Y、Z是四种原子序数依次增大的短周期主族元素,
W的单质是密度最小的非金属单质;X的单质是空气中含量第二位的物质;Y和Z同周期,其化合物为离子化
合物且水溶液呈中性,下列说法错误的是( )
A.原子半径:W<X<Z<Y
B.制备Y和Z的单质均可用电解法
C.W与X或者Y形成的化合物中,W的化合价相同
D.X和Y形成的化合物中,X和Y均达到了8e-稳定结构
【答案】C
【解析】W、X、Y、Z是四种原子序数依次增大的短周期主族元素,W的单质是密度最小的非金属单质,
则W为H;X的单质是空气中含量第二位的物质,则X为O;Y和Z同周期,其化合物为离子化合物且水溶
液呈中性,Y、Z的原子序数均大于O,应该位于第三周期,该离子化合物为NaCl,则Y为Na,Z为Cl元素,
结合分析可知,W为H,X为O,Y为Na,Z为Cl元素。A项,电子层越多离子半径越大,电子层结构相同
时,核电荷数越大离子半径越小,则简单离子半径:W<Y<X<Z,故A正确;B项,通过电解熔融氯化钠可
获得金属钠和氯气,故B正确;C项,W与X形成的化合物为水和双氧水,水和双氧水分子中H的化合价为
+1,W与Y形成的化合物为NaH,NaH中H的化合价为-1,H的化合价不同,故C错误;D项,X和Y形成
的化合物为氧化钠和过氧化钠,氧化钠和过氧化钠中钠离子和氧离子、过氧根离子均满足8e-稳定结构,故D
正确;故选C。
13.(2022·重庆市高三第四次质量检测)m、n、p、q为原子序数依次增大的前四周期主族元素,p元素的
原子最外层电子数是周期数的三倍。W是上述元素中的两种组成的常见化合物,常温下呈液态,法拉第称其
为“氢的重碳化合物”;X、Y、Z是m、p、q对应的常见单质,常温下Z是深红棕色的液体。下列说法正确
的是( )
A.四种元素的原子半径大小顺序为q>p>n>m
B.m和n形成的化合物一定含有非极性共价键
C.W在Y中燃烧时有明亮并带有浓烟的火焰
D.W与Z在一定条件下反应得到的有机物密度比水小
【答案】C
【解析】p元素的原子最外层电子数是周期数的三倍,则p为O元素,Y为O;常温下Z是深红棕色的液
2体,则Z应为Br ,q为Br元素;W是上述元素中的两种组成的常见化合物,常温下呈液态,法拉第称其为
2
“氢的重碳化合物”,m的原子序数小于n,所以m为H元素,n为C元素,W为C H,X为H。A项,电
6 6 2
子层数越多,原子半径越大,电子层数相同核电荷数越小,半径越大,所以原子半径Br>C>O>H,即
q>n>p>m,A错误;B项,甲烷为C、H元素形成的化合物,但甲烷中不存在非极性共价键,B错误;C项,
苯中含碳量较高,在氧气中燃烧有明亮并带有浓烟的火焰,C正确;D项,苯和液溴在催化剂催化作用下可以
生成溴苯,溴苯的密度比水大,D错误;故选C。
14.(2022·湖南省五市十校教研教改共同体高三第二次大联考)近来,科学家发现一种高能盐,该盐由 、
、 、 四种原子序数依次增大的短周期元素组成,其化学式为(Y )(X Z)(YX )M。该盐的两种阳离子均
5 6 3 3 4 4
为10电子离子,分别是由 与 、 与 组成。化合物 是18电子分子。下列说法错误的是( )
A. 与 可形成10电子和18电子的分子
B.该盐中存在离子键、极性共价键和非极性共价键
C.该盐的阴离子均可破坏水的电离平衡
D. 原子和 原子半径关系为:
【答案】C
【解析】盐(Y )(X Z)(YX )M由X、Y、Z、M四种原子序数依次增大的短周期元素组成,该盐的两种阳
5 6 3 3 4 4
离子均为10电子离子,分别是由X与Y、X与Z组成,两种阳离子分别为HO+、NH +,X的原子序数最小,
3 4
则X为H,化合物HM是18电子分子,则M原子的核外电子总数为17,为Cl元素,则Y为N,Z为O元素,
由题意可知X、Y、Z、M分别为H、N、O、Cl。A项,H与O形成的10电子为HO,18电子为HO,故A
2 2 2
正确;B项,(Y )(X Z)(YX )M为(N )(H O) (NH )Cl,该盐中含有阴阳离子之间形成的离子键,还存在H-
5 6 3 3 4 4 5 6 3 3 4 4
O、N-H等极性键及N-N非极性键,故B正确;C项,该盐中的阴离子有Cl-,其中Cl-不水解,不会破坏水的
电离平衡,故C错误;D项,电子层越多原子半径越大,则原子半径关系为:Cl>N,故D正确;故选C。
15.(2022·天津市河西市高三期中)部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法不
正确的是( )
A.惰性电极电解a的溶液时,阳极可得b气体B.c可作自来水消毒剂,其化学式为
C.d的酸性较HBrO 的酸性弱
4
D.溶液e具有强氧化性
【答案】C
【解析】由题中价类二维图可知,a为HCl、b为Cl、c为ClO 、d为HClO、e为次氯酸盐,含ClO-。A
2 2 4
项,惰性电极电解HCl溶液,阳极是氯离子失去电子发生氧化反应,生成氯气,电极反应式为2Cl--2e-=Cl↑,
2
故A正确;B项,c为ClO ,具有强氧化性,可以作自来水消毒剂,故B正确;C项,d为HClO,Cl和Br属
2 4
于同主族元素,从上而下,非金属性依次减弱,原子序数Cl<Br,非金属性Cl>Br,非金属性越强,其最高
价氧化物对应水合物酸性越强,即酸性HClO>HBrO ,故C错误;D项,溶液e含ClO-,ClO-具有强氧化性,
4 4
故D正确;故选C。
16.(2022·辽宁省沈阳市重点高中高中联合体高三联考)2019年诺贝尔化学奖颁给研究锂电池的科学家,
一种用作锂电池电解液的锂盐结构如图所示。其中,X位于第三周期,X原子的电子数为Z原子的两倍,W、
Z、Y位于同一周期。下列叙述正确的是( )
A.非金属性:X>Z>W
B.原子半径:X>W>Z
C.电负性:W>Z>Y
D.X的氧化物对应的水化物均为强酸
【答案】B
【解析】从结构图中可以看出,X能形成6个共价键,则其原子的最外层有6个电子,X位于第三周期,
从而得出X为硫元素;X原子的电子数为Z原子的两倍,则Z为氧元素;从结构图中可以看出,Y能形成1个
共价键,W、Z、Y位于同一周期,则Y为氟元素;阴离子所得电子应填充在W的最外层上,所以W的最外
层应有5个电子,从而确定W为氮元素。W、X、Y、Z分别为N、S、F、O元素。A项,X、Z、W分别为
S、O、N元素,非金属性:Z(O)>W(N)>X(S),A不正确;B项,X、Z、W分别为S、O、N元素,原子半径:
X(S)>W(N)>Z(O),B正确;C项,W、Y、Z分别为N、F、O元素,非金属性Y(F)>Z(O)>W(N),则电负性:
Y(F)>Z(O)>W(N),C不正确;D项,X为S元素,X的氧化物对应的水化物HSO 为弱酸,D不正确;故选
2 3
B。17.(2022·安徽师范大学附属中学高三检测)某化合物结构如图所示,其中X、Y、W、Z是原子序数依次
增大的短周期元素,且四种元素分布在三个周期,W的最外层电子数是Y的最外层电子数的2倍,Z和X同
主族。下列说法不正确的是( )
A.W与Z形成的化合物中可能既有离子键,又有共价键
B.该化合物中除X原子外,其他原子都满足8电子稳定结构
C.原子半径:Z>Y>W>X
D.Y的最高价氧化物对应水化物是一种一元弱酸
【答案】B
【解析】X、Y、W、Z是原子序数依次增大的短周期元素,且四种元素分布在三个周期,则X为H元素;
根据该化合物的结构示意图,Z为+1价阳离子,Z和X同主族,则Z为Na元素;W形成2个共价键,则W为
ⅥA元素,为O元素;W的最外层电子数是Y的最外层电子数的2倍,则Y为B元素,根据上述分析,X为
H元素,Y为B元素,W为O元素,Z为Na元素。A项,W与Z形成的化合物为氧化钠和过氧化钠,其中过
氧化钠中既有离子键,又有共价键,故A正确;B项,根据该化合物的结构示意图,B原子部分满足8电子稳
定结构,部分不满足8电子稳定结构,故B错误;C项,一般而言,电子层数越多,半径越大,电子层数相同,
原子序数越大,半径越小,原子半径:Z>Y>W>X,故C正确;D项,Y的最高价氧化物对应水化物为
HBO,是一种一元弱酸,故D正确;故选B。
3 3
18.(2022·安徽省六安一中高三月考)科学家合成出了一种用于分离铜系金属的化合物A(如下图所示),短
周期元素X、Y、Z原子序数依次增大,其中Z位于第三周期。Z与Y 可以形成分子ZY,该分子常用作高压
2 6
电气设备的绝缘介质。下列关于X、Y,Z的叙述,正确的是( )
A.化合物A中,X、Y、Z最外层都达到8电子稳定结构
B.离子半径:
C.最简单氢化物的沸点:D.最高价氧化物对应水化物的酸性:
【答案】A
【解析】短周期元素X、Y、Z原子序数依次增大,其中Z位于第三周期,根据结构式可知,Z可形成3
个共价键,带1个单位正电荷,所以Z的最外层电子数应为6,推知Z为S元素,又Z与Y 可以形成分子
2
ZY,该分子常用作高压电气设备的绝缘介质,说明该分子为SF ,即Y为F元素,X形成4个共价键后还有
6 6
一个孤电子用来得1个单位负电荷,则X的最外层电子数为3,所以推知X为B,根据上述分析可知,X、
Y,Z分别为B、F和S。A项,化合物A中,各元素原子均达到满8电子结构,其中B与F存在一个配位键,
A正确;B项,电子层数越多,简单离子半径越大,则离子半径: ,B错误;C项,HF分子
间存在氢键,沸点较高,所以最简单氢化物的沸点: ,C错误;D项,F无正价,没有最高
价氧化物对应水化物的酸性,D错误;故选A。
19.(2023届•浙江省舟山市普陀中学高三返校考试)常温下,化合物M为无色晶体,易溶于水,可用于除
去墨水渍点,洁净金属、木材等,其组成元素X、Y、Z、W均为主族元素且原子序数依次增大,Z原子的最
外层电子数是其电子层数的3倍,四种元素原子序数关系满足:X+W=2Y+Z,M的结构如图所示,下列说法
正确的是( )
A.原子半径由小到大的顺序为X<Y<Z<W
B.Z的简单氢化物的沸点大于Y的简单氢化物的沸点
C.M的水溶液呈碱性
D.W分别与X、Z形成的二元化合物均为只含离子键的离子化合物
【答案】B
【解析】Z原子的最外层电子数是其电子层数的3倍,则Z为O;化合物M的结构中,Y原子周围有2个
单键和1个双键,且Y的原子序数小于Z,则Y为C;四种元素中,X的原子序数最小,且化合物M中,X原
子周围有1个单键,则X为H;四种元素原子序数关系满足:X+W=2Y+Z,则W的原子序数为19,即W为
K;综上所述,X为H,Y为C,Z为O,W为K,M为KHC O。A项,X为H,Y为C,Z为O,W为K,
2 4
原子半径由小到大的顺序为:H<O<C<K,A错误;B项,Y为C,Z为O,C的简单氢化物是CH,O的简
4单氢化物是HO,HO分子间可以形成分子间氢键,CH 分子间不能形成氢键,故HO的沸点大于CH 的沸点,
2 2 4 2 4
B正确;C项,M为KHC O,KHC O 溶液中,HC O-的电离程度大于其水解程度,则KHC O 溶液呈酸性,
2 4 2 4 2 4 2 4
C错误;D项,X为H,Z为O,W为K;K与H形成的二元化合物KH是只含离子键的离子化合物,而K与
O形成的二元化合物中,KO 是含离子键和共价键的离子化合物,D错误;故选B。
2 2
20.(2022·河北省唐山一中高三期中)化合物A(结构式如下图)是重要的药物中间体和分析试剂,化合物A
由原子序数依次增大的短周期元素X、Y、Z、W可组成,W是地壳中分布最广的元素,下列说法正确的是(
)
A.Y的氢化物的沸点一定低于W的氢化物的沸点 B.原子半径大小顺序为:W>Z>Y>X
C.非金属性强弱顺序为:X>W>Y>Z D.X、Y、Z、W四种元素可形成离子化合物
【答案】D
【解析】化合物A由原子序数依次增大的短周期元素X、Y、Z、W可组成,W是地壳中分布最广的元素,
则W为O元素,由化合物A的结构式 可知,X只形成一根共价键,原子序数小于O,且
在这几种元素中原子序数最小,则X为H元素,Y形成四根共价键,且原子序数小于O,则Y为C元素,Z
形成三根共价键,且原子序数小于O,则Z为N元素。A项,Y为C元素,W为O元素,C的氢化物有可能
是分子量很大的烃,沸点有可能比HO或HO 高,故A错误;B.项,X为H元素,Y为C元素,Z为N元
2 2 2
素,W为O元素,根据电子层数越多,半径越大,同周期元素随着原子序数的递增,半径减小,则H只有一
个电子层,半径最小,C、N、O均有二个电子层,属于同周期元素,原子序数C<N<O,半径C>N>O>
H,即Y>Z>W>X,故B错误;C项,X为H元素,Y为C元素,Z为N元素,W为O元素,根据同周期元
素从左至右非金属性依次增强,则原子序数C<N<O,非金属性O>N>C,在CH 中H呈现正价,非金属性
4
C>H,所以非金属性O>N>C>H,即W>Z>Y>X,故C错误;D项,X为H元素,Y为C元素,Z为N元素,W为O元素,这四种元素可形成(NH )CO 或NH HCO 离子化合物,故D正确;故选D。
4 2 3 4 3
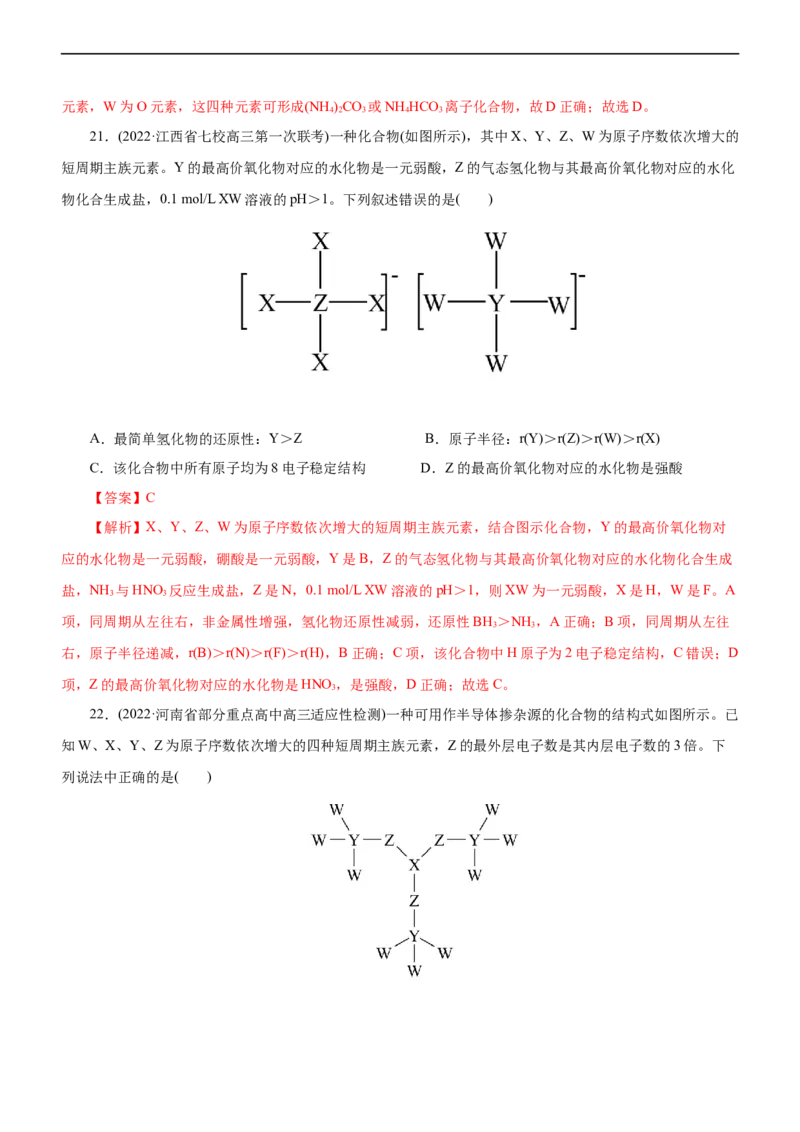
21.(2022·江西省七校高三第一次联考)一种化合物(如图所示),其中X、Y、Z、W为原子序数依次增大的
短周期主族元素。Y的最高价氧化物对应的水化物是一元弱酸,Z的气态氢化物与其最高价氧化物对应的水化
物化合生成盐,0.1 mol/L XW溶液的pH>1。下列叙述错误的是( )
A.最简单氢化物的还原性:Y>Z B.原子半径:r(Y)>r(Z)>r(W)>r(X)
C.该化合物中所有原子均为8电子稳定结构 D.Z的最高价氧化物对应的水化物是强酸
【答案】C
【解析】X、Y、Z、W为原子序数依次增大的短周期主族元素,结合图示化合物,Y的最高价氧化物对
应的水化物是一元弱酸,硼酸是一元弱酸,Y是B,Z的气态氢化物与其最高价氧化物对应的水化物化合生成
盐,NH 与HNO 反应生成盐,Z是N,0.1 mol/L XW溶液的pH>1,则XW为一元弱酸,X是H,W是F。A
3 3
项,同周期从左往右,非金属性增强,氢化物还原性减弱,还原性BH>NH ,A正确;B项,同周期从左往
3 3
右,原子半径递减,r(B)>r(N)>r(F)>r(H),B正确;C项,该化合物中H原子为2电子稳定结构,C错误;D
项,Z的最高价氧化物对应的水化物是HNO,是强酸,D正确;故选C。
3
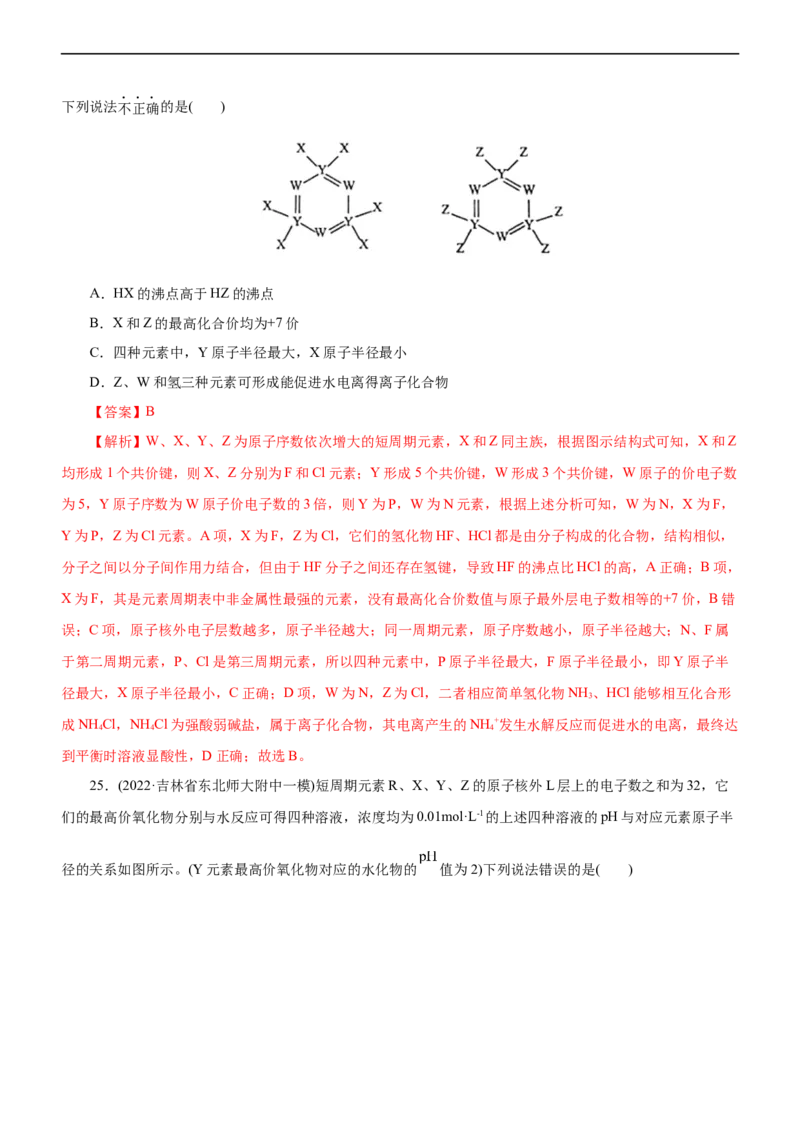
22.(2022·河南省部分重点高中高三适应性检测)一种可用作半导体掺杂源的化合物的结构式如图所示。已
知W、X、Y、Z为原子序数依次增大的四种短周期主族元素,Z的最外层电子数是其内层电子数的3倍。下
列说法中正确的是( )A.原子半径:Z>Y>X>W
B.X、Y的最高价含氧酸均为强酸
C.W和Y能形成多种原子个数比为1∶1的化合物
D.除W原子外,分子中的其他原子均满足8电子稳定结构
【答案】C
【解析】根据Z的最外层电子数是其内层电子数的3倍可知,Z为O,又W、X、Y、Z为原子序数依次增
大的四种短周期主族元素和根据所形成物质的结构可得W、Ⅹ、Y分别为H、B、C。A项,原子半径:
B>C>O>H,A项错误;B项,硼酸和碳酸均为弱酸,B项错误;C项,乙炔、苯、苯乙烯中的H原子与C原
子的个数比均为1∶1,C项正确;D项,H原子形成1个共价键,最外层电子数为2,B原子形成3个共价键,
最外层电子数为6,二者均不满足8电子稳定结构,D项错误;故选C。
23.(2022·河北省石家庄市高三教学质量检测)一种低毒杀虫剂的结构如图所示,其组成元素W、X、Y、
Z、M、Q为原子序数依次增大的短周期主族元素,其中W的原子核内只有1个质子,原子核外电子的数目Q
比Z多8个。下列说法正确的是( )
A.WMZ 是一种强酸 B.简单氢化物沸点:
3 4
C.简单离子半径:Q>M>Y>Z D.QZ2-和XZ2-均能使酸性高锰酸钾溶液褪色
2 3 2 4
【答案】D
【解析】元素W、X、Y、Z、M、Q为原子序数依次增大的短周期主族元素,W的原子核内只有1个质子,
W为H元素;根据该杀虫剂的结构可知,X形成4个共价键,X为C元素;Z形成2个共价键,Z为O元素;
则Y为N元素;原子核外电子的数目Q比Z多8个,Q的原子核外电子数为8+8=16个,Q为S元素;M为+5
价,原子序数小于16,大于8,则M为P元素,根据上述分析,W为H元素,X为C元素,Y为N元素,Z
为O元素,M为P元素,Q为S元素。A项,WMZ 为HPO ,是一种中强酸,故A错误;B项,水分子和氨
3 4 3 4
气分子间能够形成氢键,硫化氢不能,则硫化氢的沸点最低,故B错误;C项,一般而言,电子层数越多,半
径越大,电子层数相同,原子序数越大,半径越小。Q、M离子的电子层数比Y、Z离子多,因此简单离子半
径:M>Q> Y>Z,故C错误;D项,QZ2-和XZ2-分别为SO2-、C O2-,亚硫酸根和草酸根均具有还原性,都
2 3 2 4 2 3 2 4
能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,故D正确;故选D。
24.(2022·吉林省东北师大附中一模)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中
W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子最外层电子数的3倍。下列说法不正确的是( )
A.HX的沸点高于HZ的沸点
B.X和Z的最高化合价均为+7价
C.四种元素中,Y原子半径最大,X原子半径最小
D.Z、W和氢三种元素可形成能促进水电离得离子化合物
【答案】B
【解析】W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,根据图示结构式可知,X和Z
均形成1个共价键,则X、Z分别为F和Cl元素;Y形成5个共价键,W形成3个共价键,W原子的价电子数
为5,Y原子序数为W原子价电子数的3倍,则Y为P,W为N元素,根据上述分析可知,W为N,X为F,
Y为P,Z为Cl元素。A项,X为F,Z为Cl,它们的氢化物HF、HCl都是由分子构成的化合物,结构相似,
分子之间以分子间作用力结合,但由于HF分子之间还存在氢键,导致HF的沸点比HCl的高,A正确;B项,
X为F,其是元素周期表中非金属性最强的元素,没有最高化合价数值与原子最外层电子数相等的+7价,B错
误;C项,原子核外电子层数越多,原子半径越大;同一周期元素,原子序数越小,原子半径越大;N、F属
于第二周期元素,P、Cl是第三周期元素,所以四种元素中,P原子半径最大,F原子半径最小,即Y原子半
径最大,X原子半径最小,C正确;D项,W为N,Z为Cl,二者相应简单氢化物NH 、HCl能够相互化合形
3
成NH Cl,NH Cl为强酸弱碱盐,属于离子化合物,其电离产生的NH +发生水解反应而促进水的电离,最终达
4 4 4
到平衡时溶液显酸性,D正确;故选B。
25.(2022·吉林省东北师大附中一模)短周期元素R、X、Y、Z的原子核外L层上的电子数之和为32,它
们的最高价氧化物分别与水反应可得四种溶液,浓度均为0.01mol·L-1的上述四种溶液的pH与对应元素原子半
径的关系如图所示。(Y元素最高价氧化物对应的水化物的 值为2)下列说法错误的是( )A.X、Y形成的化合物均满足8电子结构
B.R元素与氢元素形成的化合物具有强还原性
C.Z、R组成的化合物R Z 中,含有离子键和非极性共价键
2 8
D.简单气态氢化物的热稳定性:Y>Z>X
【答案】A
【解析】短周期元素R、X、Y、Z的原子核外L层上的电子数之和为32,L层电子数最多不超过8个,推
断这四种元素均在第三周期;结合图示它们的最高价氧化物分别与水反应可得四种溶液的pH与对应元素原子
半径的关系,0.01mol·L-1的R溶液pH是12,判断R是Na元素,对应溶液是NaOH溶液;0.01mol·L-1的Y对
应溶液pH是2,Y的半径最小,判断Y是Cl元素,对应溶液是HClO 溶液;相同物质的量浓度的Z对应溶液
4
的酸性比HClO 溶液强,Z的半径比Cl大,判断Z是S元素,对应溶液是HSO 溶液;X的半径比S大,
4 2 4
0.01mol·L-1的X对应溶液pH值大于2,说明其是弱酸,判断X是P元素,对应溶液是HPO 溶液。A项,X、
3 4
Y形成的化合物PCl 满足8电子结构,PCl 的P则不是8电子结构,A错误;B项,R元素与氢元素形成的化
3 5
合物NaH具有强还原性,B正确;C项,Z、R组成的化合物R Z,即中NaS,Na+与S2-存在离子键,S2-中
2 8 2 8 8 8
S原子间存在非极性共价键,C正确;D项,X、Y、Z简单气态氢化物分别是PH 、HCl、HS,原子半径:
3 2
P>S>Cl,故气态氢化物热稳定性:HCl > H S > PH ,D正确;故选A。
2 3
26.(2022·广东省高三联考)短周期主族元素R、X、Y、Z、W的原子序数依次增大,由这五种元素组成
的一种化合物M常用作食品的增味剂,M的结构式如图所示。下列说法正确的是( )
A.原子半径:X>Y B.由R、Y、Z三种元素形成的化合物均为共价化合物
C.熔点:WZ<R Z D.工业上采用电解熔融的WZ制备W单质
2 2 2
【答案】A【解析】根据结构简式中各原子的成键数可知,阴离子所带负电荷位于最左侧的Z原子,W带1个单位
正电荷,结合W为短周期主族元素和原子序数最大可知,W为Na,X形成4个共价键,Y形成3个共价键,
Z形成2个共价键,三者的原子序数均小于Na,因此X为C,Y为N,Z为O,R形成1个共价键,且原子序
数小于C,因此R为H。A项,同一周期从左至右,主族元素的原子半径逐渐减小,因此原子半径:C>N,故
A正确;B项,H、N、O形成的化合物中,NH NO 、NH NO 都是离子化合物,故B错误;C项,NaO为离
4 3 4 2 2
子化合物,HO为分子化合物,因此熔点:NaO>HO,故C错误;D项,工业上采用电解熔融的NaCl制备
2 2 2
Na单质,故D错误;故选A。
27.(2022·上海市复旦附中高三期中)科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一
短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.WZ的水溶液呈碱性 B.元素非金属性强弱的顺序为
C.Y的最高价氧化物的水化物是弱电解质 D.该新化合物中Y不满足8电子稳定结构
【答案】C
【解析】W、X、Y、Z为同一短周期元素,则不可能为第一周期元素,由化合物结构可知Z形成1个共
价单键,最外层电子数为7,X形成4个共价单键,最外层电子数为4,Z的核外最外层电子数是X核外电子
数的一半可知,Z为Cl、X为Si,则W为Na,由结构可知Y原子最外层电子数为8-2-1=5,为P。A项,WZ
即NaCl,NaCl为强酸强碱正盐,水溶液呈中性,故A错误;B项,X为Si,Y为P,Z为Cl,同周期元素从
左到右,非金属性依次增强,则非金属性的强弱顺序为Z(Cl)>Y(P)>X(Si),故B错误;C项,Y为P,P元素
的最高价氧化物对应水化物为磷酸,磷酸是三元中强酸,只能部分电离,属于弱电解质,故C正确;D项,新
化合物中P元素最外层电子数为5+2+1=8,满足8电子稳定结构,故D错误;故选C。
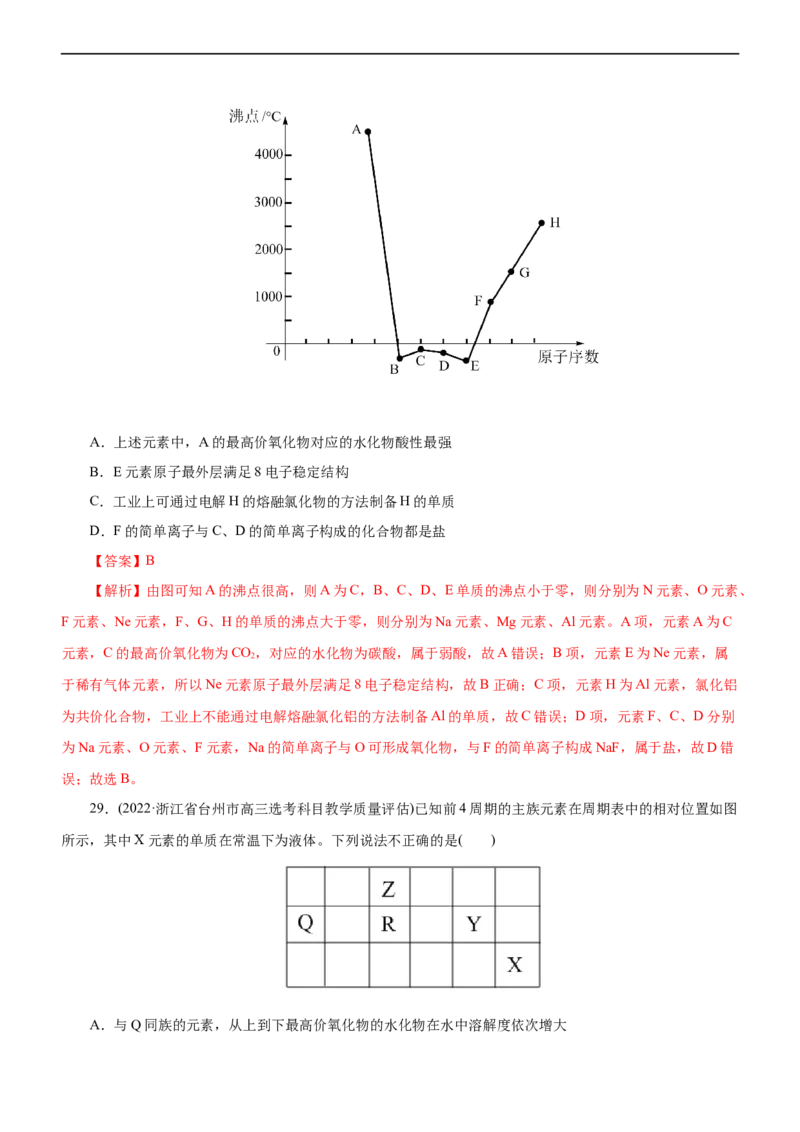
28.(2022·天津市部分区高三期中)短周期内连续八种元素单质的沸点与原子序数的关系如图,下列说法正
确的是( )A.上述元素中,A的最高价氧化物对应的水化物酸性最强
B.E元素原子最外层满足8电子稳定结构
C.工业上可通过电解H的熔融氯化物的方法制备H的单质
D.F的简单离子与C、D的简单离子构成的化合物都是盐
【答案】B
【解析】由图可知A的沸点很高,则A为C,B、C、D、E单质的沸点小于零,则分别为N元素、O元素、
F元素、Ne元素,F、G、H的单质的沸点大于零,则分别为Na元素、Mg元素、Al元素。A项,元素A为C
元素,C的最高价氧化物为CO,对应的水化物为碳酸,属于弱酸,故A错误;B项,元素E为Ne元素,属
2
于稀有气体元素,所以Ne元素原子最外层满足8电子稳定结构,故B正确;C项,元素H为Al元素,氯化铝
为共价化合物,工业上不能通过电解熔融氯化铝的方法制备Al的单质,故C错误;D项,元素F、C、D分别
为Na元素、O元素、F元素,Na的简单离子与O可形成氧化物,与F的简单离子构成NaF,属于盐,故D错
误;故选B。
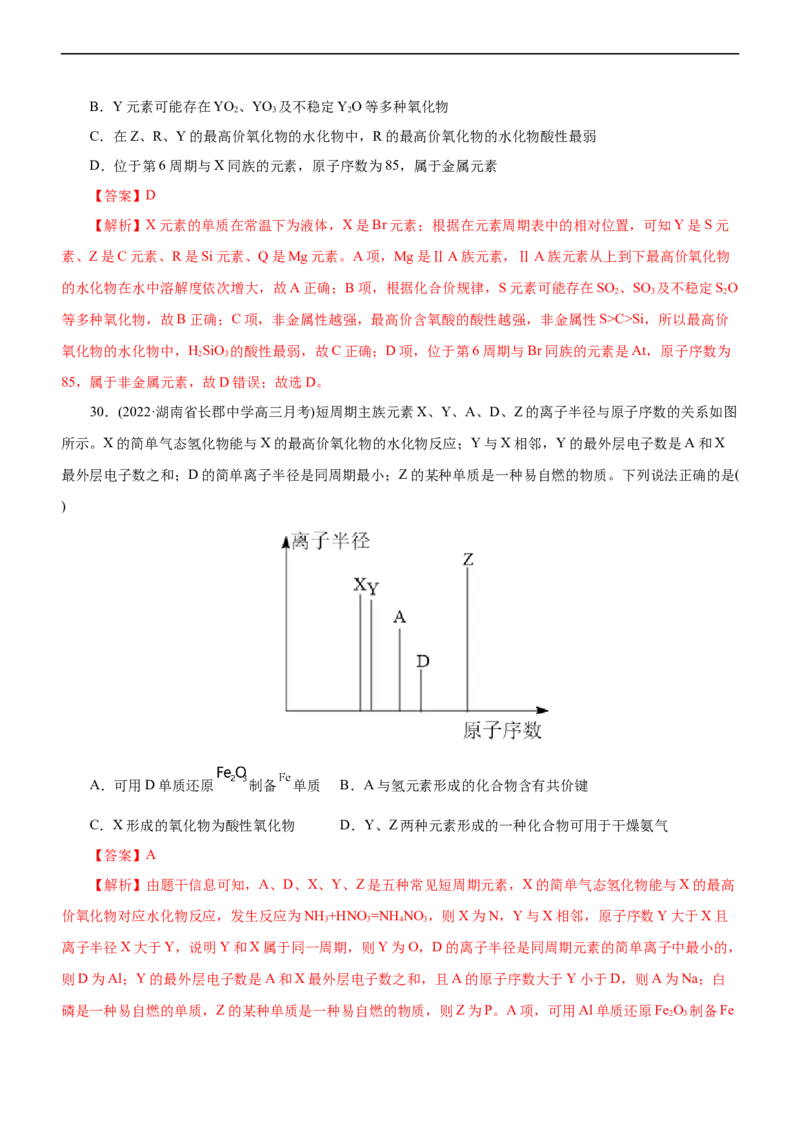
29.(2022·浙江省台州市高三选考科目教学质量评估)已知前4周期的主族元素在周期表中的相对位置如图
所示,其中X元素的单质在常温下为液体。下列说法不正确的是( )
A.与Q同族的元素,从上到下最高价氧化物的水化物在水中溶解度依次增大B.Y元素可能存在YO 、YO 及不稳定YO等多种氧化物
2 3 2
C.在Z、R、Y的最高价氧化物的水化物中,R的最高价氧化物的水化物酸性最弱
D.位于第6周期与X同族的元素,原子序数为85,属于金属元素
【答案】D
【解析】X元素的单质在常温下为液体,X是Br元素;根据在元素周期表中的相对位置,可知Y是S元
素、Z是C元素、R是Si元素、Q是Mg元素。A项,Mg是ⅡA族元素,ⅡA族元素从上到下最高价氧化物
的水化物在水中溶解度依次增大,故A正确;B项,根据化合价规律,S元素可能存在SO 、SO 及不稳定SO
2 3 2
等多种氧化物,故B正确;C项,非金属性越强,最高价含氧酸的酸性越强,非金属性S>C>Si,所以最高价
氧化物的水化物中,HSiO 的酸性最弱,故C正确;D项,位于第6周期与Br同族的元素是At,原子序数为
2 3
85,属于非金属元素,故D错误;故选D。
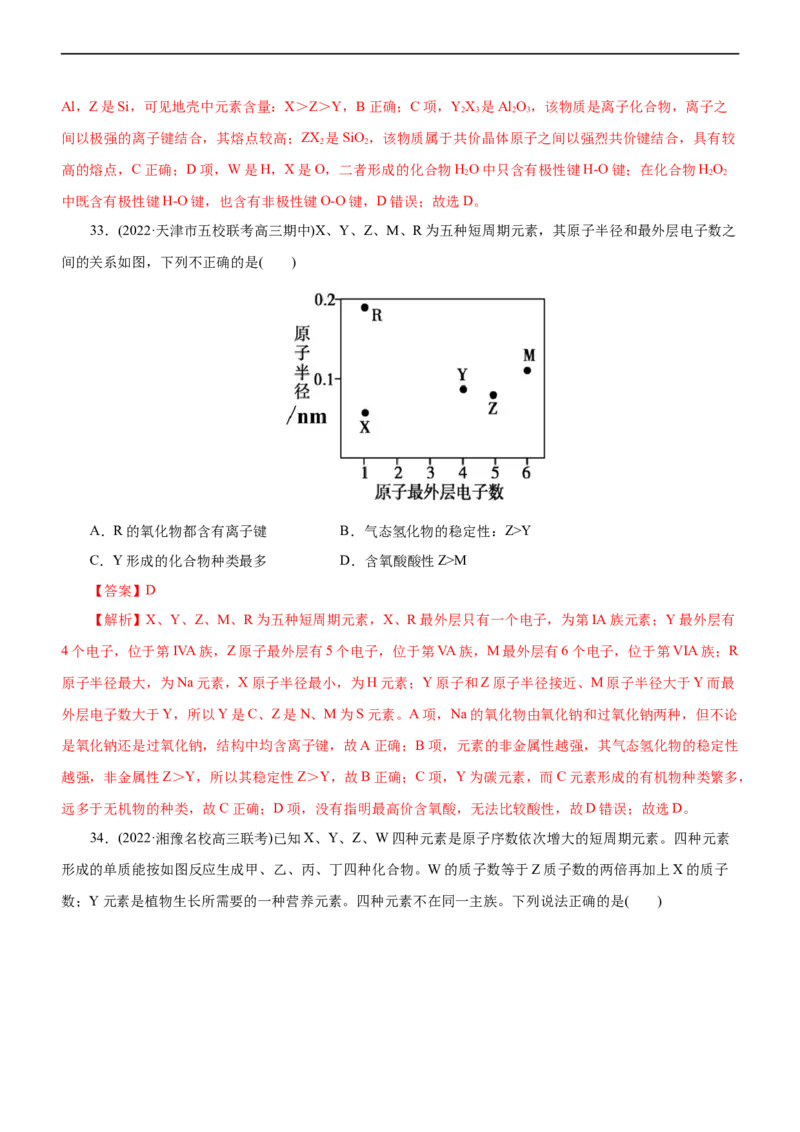
30.(2022·湖南省长郡中学高三月考)短周期主族元素X、Y、A、D、Z的离子半径与原子序数的关系如图
所示。X的简单气态氢化物能与X的最高价氧化物的水化物反应;Y与X相邻,Y的最外层电子数是A和X
最外层电子数之和;D的简单离子半径是同周期最小;Z的某种单质是一种易自燃的物质。下列说法正确的是(
)
A.可用D单质还原 制备 单质 B.A与氢元素形成的化合物含有共价键
C.X形成的氧化物为酸性氧化物 D.Y、Z两种元素形成的一种化合物可用于干燥氨气
【答案】A
【解析】由题干信息可知,A、D、X、Y、Z是五种常见短周期元素,X的简单气态氢化物能与X的最高
价氧化物对应水化物反应,发生反应为NH +HNO =NHNO ,则X为N,Y与X相邻,原子序数Y大于X且
3 3 4 3
离子半径X大于Y,说明Y和X属于同一周期,则Y为O,D的离子半径是同周期元素的简单离子中最小的,
则D为Al;Y的最外层电子数是A和X最外层电子数之和,且A的原子序数大于Y小于D,则A为Na;白
磷是一种易自燃的单质,Z的某种单质是一种易自燃的物质,则Z为P。A项,可用Al单质还原Fe O 制备Fe
2 3单质即铝热反应制备铁,A正确;B项,Na与氢元素形成的化合物为离子化合物,只含有离子键,B错误;C
项,氮的氧化物有很多种,如NO、NO 均不是酸性氧化物,C错误;D项,PO 为酸性氧化物,会与氨气反
2 2 5
应,不可用于干燥氨气,D错误;故选A。
31.(2022·广东省化州市高三质量调研)已知X、Y、Z、W四种短周期主族元素的原子序数依次增大,X
原子的最外层电子数与电子层数相等,Y与X同主族,且最高价化物对应的水化物是一种强碱,Z的一种氧化
物溶在雨水中,可形成酸雨。下列说法正确的是( )
A.原子半径大小: B.X与Y、Z、W三种元素都可形成共价化合物
C.非金属性 D.W的单质常用于自来水的杀菌消毒
【答案】D
【解析】X原子的最外层电子数与电子层数相等,Y与X同主族,且最高价化物对应的水化物是一种强碱,
则X是H元素、Y是Na元素;Z的一种氧化物溶在雨水中,可形成酸雨,Z是S元素,X、Y、Z、W四种短
周期主族元素的原子序数依次增大,W是Cl元素。A项,电子层数越多半径越大,电子层数相同,质子数越
多半径越小,原子半径大小: ,故A错误;B项,H与Na形成离子化合物NaH,故B错
误;C项,同周期元素从左到右,非金属性增强,非金属性Cl>S,故C错误;D项,Cl 常用于自来水的杀菌
2
消毒,故D正确;故选D。
32.(2022·河南省南阳市高三期中)短周期元素W、X、Y、Z的原子序数依次增大,浙江大学研究团队以
aYX·bZX (固态物质,a、b为系数)为载体,利用 纳米颗粒催化气态单质W、X 合成WX,其原理
2 3 2 2 2 2 2
如下图所示。下列说法错误的是( )
A.元素主要化合价(最高正价):Z>Y B.地壳中元素含量:X>Z>Y
C.YX、ZX 均具有较高熔点 D.W与X形成的化合物只含极性键
2 3 2
【答案】D
【解析】根据四种元素形成的化合物结构aYX·bZX 的特点,该物质是盐,表示成氧化物形式,应该为
2 3 2
硅酸盐。结合元素原子序数大小关系及气态单质W、X 合成WX,可知:W是H,X是O,Y是Al,Z是Si
2 2 2 2
元素。A项,Z是Si元素,最高是+4价,Y是Al元素,最高是+3价,所以元素主要化合价(最高正价):Z>
Y,A正确;B项,在地壳中各种元素的含量由多到少的顺序为:O、Si、Al、Fe、Ca、Na等,X是O,Y是Al,Z是Si,可见地壳中元素含量:X>Z>Y,B正确;C项,YX 是Al O,该物质是离子化合物,离子之
2 3 2 3
间以极强的离子键结合,其熔点较高;ZX 是SiO,该物质属于共价晶体原子之间以强烈共价键结合,具有较
2 2
高的熔点,C正确;D项,W是H,X是O,二者形成的化合物HO中只含有极性键H-O键;在化合物HO
2 2 2
中既含有极性键H-O键,也含有非极性键O-O键,D错误;故选D。
33.(2022·天津市五校联考高三期中)X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之
间的关系如图,下列不正确的是( )
A.R的氧化物都含有离子键 B.气态氢化物的稳定性:Z>Y
C.Y形成的化合物种类最多 D.含氧酸酸性Z>M
【答案】D
【解析】X、Y、Z、M、R为五种短周期元素,X、R最外层只有一个电子,为第IA族元素;Y最外层有
4个电子,位于第IVA族,Z原子最外层有5个电子,位于第VA族,M最外层有6个电子,位于第VIA族;R
原子半径最大,为Na元素,X原子半径最小,为H元素;Y原子和Z原子半径接近、M原子半径大于Y而最
外层电子数大于Y,所以Y是C、Z是N、M为S元素。A项,Na的氧化物由氧化钠和过氧化钠两种,但不论
是氧化钠还是过氧化钠,结构中均含离子键,故A正确;B项,元素的非金属性越强,其气态氢化物的稳定性
越强,非金属性Z>Y,所以其稳定性Z>Y,故B正确;C项,Y为碳元素,而C元素形成的有机物种类繁多,
远多于无机物的种类,故C正确;D项,没有指明最高价含氧酸,无法比较酸性,故D错误;故选D。
34.(2022·湘豫名校高三联考)已知X、Y、Z、W四种元素是原子序数依次增大的短周期元素。四种元素
形成的单质能按如图反应生成甲、乙、丙、丁四种化合物。W的质子数等于Z质子数的两倍再加上X的质子
数;Y元素是植物生长所需要的一种营养元素。四种元素不在同一主族。下列说法正确的是( )A.Y的氧化物形成的水化物是强酸 B.化合物甲可以与化合物乙反应
C.化合物丙的比例模型: D.化合物甲的沸点高于化合物丁
【答案】D
【解析】X、Y、Z、W四种元素是原子序数依次增大的短周期元素,Y元素是植物生长所需要的一种营
养元素,则Y为N,W的质子数等于Z质子数的两倍再加上X的质子数;则Z只能是O,W为Cl,X为H,
则甲为HO,乙为NO,丙为NCl ,丁为NH 。A项,Y的氧化物形成的水化物不一定是强酸,比如亚硝酸,
2 3 3
故A错误;B项,化合物甲(H O)可以与化合物乙(NO)不反应,故B错误;C项, 不是化合物丙的
2
比例模型,氮原子比Cl原子半径小,故C错误;D项,化合物甲(H O)的沸点高于化合物丁(NH ),故D正确。
2 3
故选D。
35.(2023·山东省泰安市高三期中)化合物(WYZ·X Z)中的四种元素X、Y、Z、W为前20号元素,且原
2 4 2
子序数依次增大,Y和Z位于同周期的不同主族,W最高价氧化物对应的水化物的溶液是检验YZ 气体的常用
2
试剂,该化合物的热重分析曲线如图所示。下列说法正确的是( )A.X、Y、Z、W四种元素只能形成一种离子化合物W(XYZ )
3 2
B.200~400℃阶段热分解将失去1个XZ
2
C.400~600℃热分解后生成的固体化合物是XYZ ,且该反应为非氧化还原反应
3
D.该反应过程最终分解得到的固体产物属于碱性氧化物
【答案】D
【解析】Y和Z位于同周期的不同主族,W最高价氧化物对应的水化物的溶液是检验YZ 气体的常用试剂,
2
故W为Ca,其最高价氧化物对应的水化物的溶液是Ca(OH) ,YZ 是CO,即Y为C,Z为O;根据该化合物
2 2 2
的化学式可知XZ为结晶水,X为H,该化合物为CaC O·H O,相对分子质量为146。A项,H、C、O、Ca
2 2 4 2
四种元素可以形成离子化合物:Ca(HC O) 和Ca(HCO ),A错误;B项,00~400℃阶段该化合物的质量保留
2 4 2 3 2
百分数不变,不发生质量减少,B错误;C项,当温度为400℃时,质量保留百分比为87.67%,相对分子质量
为 ,失去了一个结晶水,此时剩余固体为CaC O;当温度为600℃时,质量保留百分比为
2 4
68.49%,相对分子质量为 ,剩余固体为CaCO ,对比可知失去了CO,碳元素化合价发生了
3
变化,是氧化还原反应,C错误;D项,当温度接近1000℃时,质量保留百分比为38.36%,相对分子质量为
,剩余固体为CaO,是碱性氧化物,D正确;故选D。
36.(2022·北京市首都师范大学附属中学高三月考)R、W、X、Y、M是原子序数依次增大的五种主族元
素。R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX。工业革命以来,
2
人类使用的化石燃料在燃烧过程中将大量WX 排入大气,导致地球表面平均温度升高。Y与X是同一主族的
2
元素,且在元素周期表中与X相邻。
(1)W的原子结构示意图是 _______。(2)WX 的电子式是 _______。
2
(3)R X、R Y中,稳定性较高的是 _______(填化学式),沸点较高的是 _______。(填化学式)
2 2
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是 _______。(填字母序号)
a.Se的最高正化合价为+7价 b.HSe的还原性比HY强
2 2
c.HSeO 的酸性比HYO 强 d.SeO 在一定条件下可与NaOH溶液反应
2 3 2 4 2
②室温下向SeO 固体表面吹入NH ,可得到两种单质和HO,该反应的化学方程式为 _______。
2 3 2
(5)科研人员从矿石中分离出一种氧化物,化学式可表示为AO。为确定A元素的种类,进行了一系列实
2 3
验,结果如下:①A的相对原子质量介于K和Rb(铷)之间;②0.01mol AO 在碱性溶液中与Zn充分反应可得
2 3
到A的简单氢化物,反应完全时,被AO 氧化的Zn为0.06mol;综合以上信息推断,A可能位于元素周期表
2 3
第 _______族。
【答案】(1) (2) (3)H O H O
2 2
(4)bd 3SeO +4NH═3Se+2N+6H O (5)VA
2 3 2 2
【解析】R、W、X、Y、M是原子序数依次增大的五种主族元素,R最常见同位素的原子核中不含中子,
则R为H;W与X可形成两种稳定的化合物WX和WX,工业革命以来,人类使用的化石燃料在燃烧过程中
2
将大量WX 排入大气,在一定程度导致地球表面平均温度升高,W为C、X为O;Y与X是同一主族的元素,
2
且在元素周期表中与X相邻,则Y为S;M的原子序数大于S,则M为Cl。(1)由上述分析可知,W为C元素,
原子序数为6,其原子结构示意图是 ;(2)由分析可知,W为C,X为O,则WX 为CO,CO 属于
2 2 2
共价化合物,其电子式是 ;(3)R X、R Y中分别为HO、HS,O与S为同主族元素,O的电子层数
2 2 2 2
小于S,O的原子半径小于S,O的原子核对核外电子吸引能力大于S原子,O的非金属性强于S,故HO的
2
稳定性大于HS;由于HO分子间存在氢键,导致HO的沸点较高;(4)①a项,Se的最外层电子数为6,最高
2 2 2
正化合价为+6价,a错误;b项,非金属性S大于Se,则HSe的还原性比HY强,b正确;c项,HSeO 的酸
2 2 2 3
性比HYO 弱,前者为弱酸,后者为强酸,c错误;d项,SeO 在一定条件下可与NaOH溶液反应生成盐和水,
2 4 2
d正确;故选bd;②室温下向SeO 固体表面吹入NH ,可得到两种单质和HO,结合化合价变化可知,生成
2 3 2
两种单质为Se、N,该反应的化学方程式为:3SeO+4NH═3Se+2N+6H O;(5)0.01 mol AO 在碱性溶液中与
2 2 3 2 2 2 3
Zn充分反应可得到A的简单氢化物,反应完全时,被AO 氧化的Zn为0.06 mol,设氢化物中A元素的化合
2 3价为x,由电子守恒可知0.01mol×2×(3-x)=0.06mol×(2-0),解得:x=-3,则A元素的最高价为+5价,A位于元
素周期表第VA族。
37.(2022·重庆八中高三期中)短周期元素A、B、C、D、E在周期表中相对位置如图所示。已知:D原子
的原子序数等于其最外层电子数的3倍。
请回答下列问题:
(1)B在周期表中位于第___________周期___________族。
(2)E B分子的电子式为___________,该分子所含化学键类型是___________。
2
(3)在B、D、E的气态氢化物中,热稳定性最弱的是___________(填化学式)。
(4)工业上,制备C单质的化学方程式为___________。
(5)在A的氢化物中,能与溴水、酸性KMnO 溶液发生化学反应的有___________(填一种物质的结构简式)。
4
(6)D的单质在氯气中燃烧生成两种产物X和Y,其中X分子中每个原子最外层都达到8电子结构。Y与
足量的NaOH溶液反应生成两种盐和水,写出该反应的化学方程式:___________。
【答案】(1) 二 ⅥA (2) 共价键(或极性共价键)
(3)PH (4)2AlO(熔融) 4Al+3O ↑
3 2 3 2
(5)CH =CH (6)PCl +8NaOH=Na PO +5NaCl+4HO
2 2 5 3 4 2
【解析】D应处于第三周期,且D原子的原子序数等于其最外层电子数的3倍,则D为P,由元素在周期
表中的位置,则A为C、B为O、C为Al、E为Cl。(1)B为O,在周期表中位于第二周期第VIA族;(2)E B是
2
ClO,由O和2个Cl原子各共用1对电子对,电子式为 ,化学键类型是共价键;(3)在B、D、E分
2
别为O、P、S,非金属性越强,其气态氢化物越稳定,由非金属性:O>S>P,则热稳定性最弱的是PH ;(4)工
3
业上,制备Al单质是电解熔融的氧化铝,反应的化学方程式为2Al O(熔融) 4Al+3O ↑;(5)A是C,
2 3 2
能与溴水、酸性KMnO 溶液发生化学反应的有乙烯,结构简式是CH=CH ;(6)D的单质P在氯气中燃烧生成
4 2 2
两种产物X和Y,其中X分子中每个原子最外层都达到8电子结构说明X为PCl ,则Y为PCl ,PCl 与足量
3 5 5的NaOH溶液反应生成两种盐为NaPO 、NaCl和水,该反应的化学方程式:
3 4
PCl +8NaOH=Na PO +5NaCl+4HO。
5 3 4 2
1.(2021•浙江1月选考)下列含有共价键的盐是( )
A.CaCl B.HSO C.Ba(OH) D.NaCO
2 2 4 2 2 3
【答案】D
【解析】A项,CaCl 由Ca2+和Cl-构成,只含有离子键不含有共价键,A不符合题意;
2
B项,HSO 由分子构成,只含有共价键不含有离子键,B不符合题意;C项,Ba(OH) 由Ba2+和OH-构成,
2 4 2
属于碱,不属于盐,C不符合题意;D项,NaCO 有Na+和CO2-构成,含有离子键,CO2-内部C与O原子之
2 3 3 3
间还含有共价键,D符合题意;故选D。
2.(2021•北京卷)下列化学用语不正确的是( )
A.溴乙烷比例模型: B.Na+的原子结构示意图:
C.N 的结构式:N≡N D.CO 的电子式:
2 2
【答案】D
【解析】A项,溴乙烷比例模型: ,A正确;B项,Na+的原子结构示意图: ,B正确;
C项,N 分子中N原子间是三键,结构式:N≡N,C正确;D项,CO 的电子式: ,D错误。
2 2
3.(2022•江苏卷)少量NaO 与HO反应生成HO 和NaOH。下列说法正确的是( )
2 2 2 2 2
A.NaO 的电子式为 B.HO的空间构型为直线形
2 2 2
C.HO 中O元素的化合价为-1 D.NaOH仅含离子键
2 2
【答案】C
【解析】A项,过氧化钠是离子化合物,电子式是 ,A错误;B项,HO中氧原
2
子的成键电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其空间构型为V形,B
错误;C项,HO 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;D项,NaOH中O
2 2和H之间是共价键,D错误;故选C。
4.(2022·浙江省1月选考)下列说法不正确的是( )
A.32S和34S互为同位素 B.C 和纳米碳管互为同素异形体
70
C.CHClCH Cl和CHCHCl 互为同分异构体D.C H 和C H 一定互为同系物
2 2 3 2 3 6 4 8
【答案】D
【解析】A项,32S和34S是质子数相同、中子数不同的原子,互为同位素,故A正确;B项,C 和纳米
70
碳管是由碳元素组成的不同单质,互为同素异形体,故B正确;C项,CHClCH Cl和CHCHCl 的分子式相同、
2 2 3 2
结构不同,互为同分异构体,故C正确;D项,C H 和C H 可能为烯烃或环烷烃,所以不一定是同系物,故
3 6 4 8
D错误;故选D。
5.(2022·浙江省6月选考)下列说法不正确的是( )
A.乙醇和丙三醇互为同系物
B. 和 互为同位素
C. 和 互为同素异形体
D.丙酮( )和环氧丙烷( )互为同分异构体
【答案】A
【解析】A项,结构相似,组成上相差若干个CH 原子团的有机化合物为同系物,乙醇(CHCHOH)是饱
2 3 2
和一元醇,丙三醇是饱和三元醇,两者所含官能团数目不同,不互为同系物,A错误;B项,质子数相同、中
子数不同的同种元素互为同位素,35Cl的质子数为17,中子数为18,37Cl的质子数为17,中子数为20,两者
质子数相同、中子数不同,互为同位素,B正确;C项,由同种元素组成的不同的单质互为同素异形体,O 和
2
O 是由氧元素组成的不同的单质,两者互为同素异形体,C正确;D项,分子式相同、结构不同的化合物互为
3
同分异构体,丙酮和环氧丙烷的分子式相同、结构不同,两者互为同分异构体,D正确;故选A。
6.(2022•全国乙卷)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元
4 5 8 2
素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热重曲线如图所
2
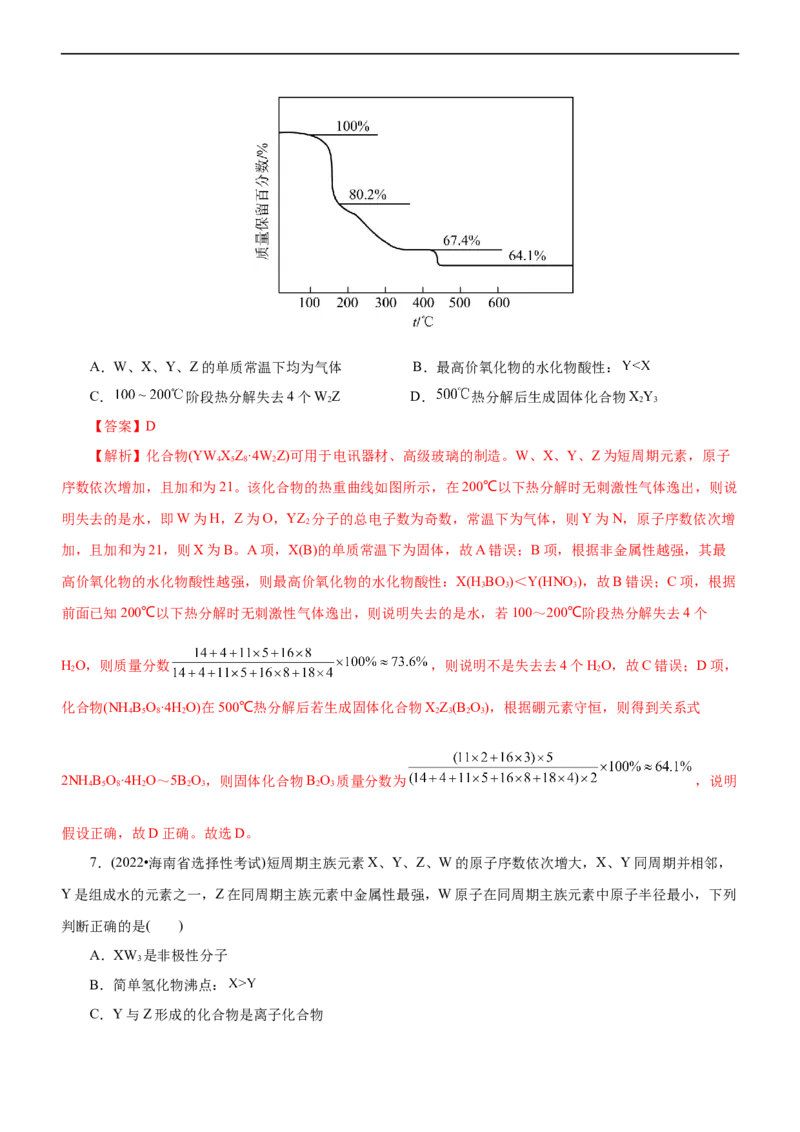
示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是( )A.W、X、Y、Z的单质常温下均为气体 B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个WZ D. 热分解后生成固体化合物XY
2 2 3
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子
4 5 8 2
序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则说
明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序数依次增
2
加,且加和为21,则X为B。A项,X(B)的单质常温下为固体,故A错误;B项,根据非金属性越强,其最
高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错误;C项,根据
3 3 3
前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热分解失去4个
HO,则质量分数 ,则说明不是失去去4个HO,故C错误;D项,
2 2
化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到关系式
4 5 8 2 2 3 2 3
2NH B O·4H O~5B O,则固体化合物B O 质量分数为 ,说明
4 5 8 2 2 3 2 3
假设正确,故D正确。故选D。
7.(2022•海南省选择性考试)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,
Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列
判断正确的是( )
A.XW 是非极性分子
3
B.简单氢化物沸点:
C.Y与Z形成的化合物是离子化合物D.X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【解析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且Y是组成水的元
素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,则Z为Na元素,W原子在同周期
主族元素中原子半径最小,则W为Cl元素。A项,X为N元素,W为Cl元素,NCl 分子的空间构型为三角
3
锥形,其正负电荷的中心不重合,属于极性分子,A错误;B项,HO和NH 均含有氢键,但HO分子形成的
2 3 2
氢键更多,故沸点HO>NH ,B错误;C项,Y为O元素,Z为Na元素,两者形成的化合物为NaO、NaO
2 3 2 2 2
均为离子化合物,C正确;D项,N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
3 2
故选C。
8.(2022·浙江省6月选考)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数
等于其周期数,YX 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周
3
期中非金属性最强的元素。下列说法正确的是( )
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C.MZ与MQ的晶体类型不同
2
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【解析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于
3
X、Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q为
Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl。A项,X为H,Z为O,则其形成的10电子微粒
有HO、OH-、HO+,A错误;B项,Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;
2 3 2
C项,Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,为离子晶体,晶体类型相同,
2 2
C错误;D项,X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,D错误;故选B。
9.(2022·浙江省1月选考)W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y同族,Y的原子
序数是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是( )
A.非金属性:Y>W B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸 D.X与Y可形成化合物XY
2 3
【答案】D
【解析】X是地壳中含量最多的金属元素,X为Al元素,W和Y同族,Y的原子序数是W的2倍,W为
O元素,Y为S元素,Z为Cl元素。A项,非金属性同主族从上至下逐渐减弱:Y<W,A错误;B项,氯化
铝是共价化合物,B错误;C项,Y、Z的最高价氧化物对应的水化物分别硫酸和高氯酸,两者均为强酸,次氯酸也是氯的氧化物对应的水化合物,但次氯酸为弱酸,C错误;D项,根据化合物的化合价代数和为0可知,
铝与硫元素形成的化合物化学式为Al S,D正确;故选D。
2 3
10.(2021•全国甲卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X
的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是(
)
A.原子半径:
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【解析】根据题意,W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X
的最外层电子数之和,也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X的单质
常温下均为气体,则推知W和X为非金属元素,所以可判断W为H元素,X为N元素,Z的最外层电子数为
1+5=6,Y的最外层电子数为 =3,则Y为Al元素,Z为S元素。根据上述分析可知,W为H元素,X为N
元素,Y为Al元素,Z为S元素。A项,电子层数越多的元素原子半径越大,同周期元素原子半径依次减弱,
则原子半径:Y(Al)>Z(S)>X(N)>W(H),A错误;B项,W为H元素,X为N元素,两者可形成NH 和
3
NH,B错误;C项,Y为Al元素,其氧化物为两性氧化物,可与强酸、强碱反应,C错误;D项,W、X和
2 4
Z可形成(NH )S、NH HS,两者既含有离子键又含有共价键,D正确。故选D。
4 2 4
11.(2021•全国乙卷)我国蠕娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球士壤类似土
壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、Y、Z为同周期相邻
元素,且均不与W同族,下列结论正确的是( )
A.原子半径大小顺序为 B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的 D.Z的氧化物的水化物的酸性强于碳酸
【答案】B
【解析】由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、Y、Z为同周
期相邻元素,可知W所在主族可能为第ⅢA族或第ⅥA族元素,又因X、Y、Z为同周期相邻元素,且均不与
W同族,故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已知可推知W、X、Y、Z依
次为O、Mg、Al、Si。A项,O原子有两层,Mg、Al、Si均有三层且原子序数依次增大,故原子半径大小顺序为Mg>Al>Si>O,即X>Y>Z>W,A错误;B项,化合物XW即MgO为离子化合物,其中的化学键为
离子键,B正确;C项,Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性
介于导体和绝缘体之间,故Y单质的导电性能强于Z单质的,C错误;D项,Z的氧化物的水化物为硅酸,硅
酸酸性弱于碳酸,D错误;故选B。
12.(2021•浙江1月选考)现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一
周期。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为零
Z 单质为淡黃色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是( )
A.常温时,X单质能与水发生剧烈反应
B.Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C.Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D.第五周期且与Q同主族元素的单质在常温常压下呈液态
【答案】B
【解析】X原子的最外层电子数是核外电子总数的一半,由于最外层电子数不超过8个,因此X只能是第
二周期的Be;Y元素的最高化合价和最低化合价之和为零,位于第ⅣA族,Y是C或Si;Z单质为淡黄色固
体,常存在于火山喷口附近,因此Z是S;Q是同周期元素中原子半径最小,且Z和Q位于同一周期,因此Q
是Cl。根据以上分析可知X是Be,Y是C或Si,Z是S,Q是Cl。则:A项,Be的金属性弱于Mg,常温时镁
和冷水不反应,因此Be单质不能与水发生剧烈反应,A错误;B项,Y与Q元素组成的CCl 或SiCl 分子,空
4 4
间构型均为正四面体,B正确;C项,Y、Z、Q三种元素的非金属性逐渐增强,非金属性越强,最高价含氧酸
的酸性越强,则最高价氧化物对应水化物的酸性依次增强,C错误;D项,第五周期且与Cl同主族元素的单
质是碘,在常温常压下呈固态,D错误;故选B。
13.(2021•浙江6月选考)已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如下所示,其中Y
的最高化合价为+3。下列说法不正确的是( )A.还原性:ZQ<ZR B.X能从ZQ 中置换出Z
2 4 2
C.Y能与Fe O 反应得到Fe D.M最高价氧化物的水化物能与其最低价氢化物反应
2 3
【答案】A
【解析】根据短周期元素X、Y、Z、M、Q和R在周期表中的相对位置,以及Y的最高化合价为+3,可
推知,X为:Mg,Y为:Al,Z为:C,M为:N,Q为:S,R为:Cl。A项,ZQ 为CS,ZR 为CCl ,CS
2 2 4 4 2
中硫的还原性强于CCl 中的氯元素,A错误;B项,Mg和CO 发生下述反应:2Mg+CO 2MgO+O,B正
4 2 2
确;C项,Al和Fe O 发生铝热反应如下:2Al+Fe O Al O +2Fe,C正确;D项,M为:N,N的最高
2 3 2 3 2 3
价氧化物的水化物为HNO,最低价氢化物为NH ,二者发生如下反应:HNO+NH=NHNO ,D正确;故选
3 3 3 3 4 3
A。
14.(2022·浙江省1月选考)回答下列问题:
(1)两种有机物的相关数据如表:
物质 HCON(CH ) HCONH
3 2 2
相对分子质量 73 45
沸点/℃ 153 220
HCON(CH ) 的相对分子质量比HCONH 的大,但其沸点反而比HCONH 的低,主要原因是
3 2 2 2
____________________________________。
(2)四种晶体的熔点数据如表:
物质 CF SiF BF AlF
4 4 3 3
熔点/℃ -183 -90 -127 >1000
CF 和SiF 熔点相差较小,BF 和AlF 熔点相差较大,原因是________________。
4 4 3 3
【答案】(1)HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分子间
3 2 2
作用力更容易,所以沸点低。
(2)CF 和SiF 都是分子晶体,结构相似,分子间作用力相差较小,所以熔点相差较小;BF 通过分子间作
4 4 3
用力形成分子晶体,AlF 通过离子键形成离子晶体,破坏离子键需要能量多得多,所以熔点相差较大。
3
【解析】(1)HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分子间
3 2 2
作用力更容易,所以沸点低;(2)CF 和SiF 都是分子晶体,结构相似,分子间作用力相差较小,所以熔点相差
4 4
较小;BF 通过分子间作用力形成分子晶体,AlF 通过离子键形成离子晶体,破坏离子键需要能量多得多,所
3 3
以熔点相差较大。
15.(2021年1月浙江选考)(1)用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰,原因是______。
(2)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF GaCl GaBr
3 3 3
熔点/℃ > 1000 77. 75 122. 3
【答案】(1)两个乙酸分子通过氢键形成二聚体( )
(2)GaF 是离子晶体,GaCl 是分子晶体;离子键强于分子间作用力 GaF 熔点比GaCl 熔点高很多的原因
3 3 3 3
是______。
【解析】(1)质谱检测乙酸时,出现质荷比为120的峰,说明可能为两分子的乙酸结合在一起,由于乙酸
分子中存在可以形成氢键的O原子,故这种结合为以氢键形式结合的二聚体( ),故答案为:
两个乙酸分子通过氢键形成二聚体( );(2)F的非金属性比Cl强,比较GaF 和GaCl 的熔点
3 3
可知,GaF 为离子晶体,GaCl 为分子晶体,离子晶体中主要的作用为离子键,分子晶体中主要的作用为分子
3 3
间作用力,离子键强于分子间作用力,故GaF 的熔点高于GaCl ,故答案为:GaF 是离子晶体,GaCl 是分子
3 3 3 3
晶体;离子键强于分子间作用力。