文档内容
专题 07 元素周期律与元素周期表
内容 原子结构与化学键 元素周期表与元素周期律
1.了解原子的构成及原子序数、核电
1.了解元素周期表(长式)的结构(周期、族)及其应用
荷数、质子数、中子数、核外电子
课 数之间的关系 2.掌握元素周期律的实质
标 2.了解原子核外电子排布规律 3.以第3周期为例,掌握同一周期内元素性质的递变规
律与原子结构的关系
解 解读 3.了解元素、核素和同位素的含义
4.以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变
读
4.了解化学键的定义
规律与原子结构的关系
5.了解离子键、共价键的形成
5.了解金属、非金属元素性质的递变规律以及在周期表
6.掌握电子式的书写方法 中的位置
本专题知识在高考中的命题形式通常有两种:一种是通过观察、比较图表中数据的变化趋
考情分析 势,总结出有关规律,再运用于解题;另一种是以文字形式给出信息,先进行元素的推断,
再以所得元素为载体进行考查。
试题往往以原子结构或元素化合物性质为突破口进行元素推断,然后综合考查元素周期律、
备考策略
化学键、常见物质的性质等。
核心素养 宏观辨识与微观探析
高频考点一 原子结构、化学用语与化学键
1.微粒中“各数”间的定量关系
(1)原子或离子:质量数(A)=质子数(Z)+中子数(N)。
(2)原子:核电荷数=质子数=原子序数=核外电子数。
(3)阴离子:核外电子数=质子数+离子电荷数。
(4)阳离子:核外电子数=质子数-离子电荷数。
2.“四同”比较
同位素 同素异形体 同分异构体 同系物
“同”含义 质子数相同 元素相同 分子式相同 结构相似
“异”含义 中子数不同 性质、结构、组成不同 结构不同 相差“CH”
2
研究对象 核素、原子 单质 化合物 有机物
3.表示物质组成和结构的两种模型、四种符号、六种图示(2)四种符号
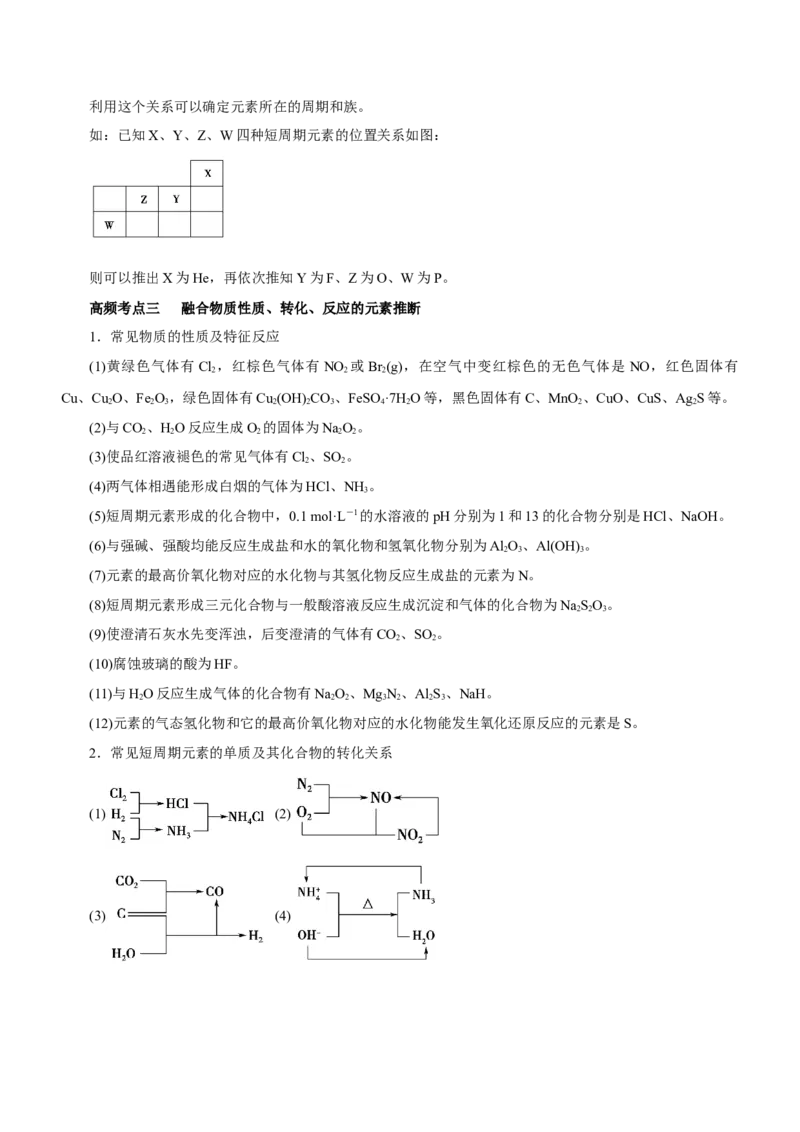
4.化学键与化合物的关系
高频考点二 “位—构—性”的关系及其应用
1.原子序数与元素位置的“序数差值”规律
(1)同周期相邻主族元素的“序数差值”规律。
①除第ⅡA族和第ⅢA族外,其余同周期相邻元素序数差为1。
②同周期第ⅡA族和第ⅢA族元素,其原子序数差分别是:第二、三周期相差 1,第四、五周期相差
11,第六、七周期相差25。
(2)同主族相邻元素的“序数差值”规律。
①第二、三周期的同族元素原子序数相差8。②第三、四周期的同族元素原子序数相差有两种情况:第ⅠA族、ⅡA族相差8,其他族相差18。
③第四、五周期的同族元素原子序数相差18。
④第五、六周期的同族元素原子序数镧系之前的相差18,镧系之后的相差32。
⑤第六、七周期的同族元素原子序数相差32。
2.元素金属性、非金属性强弱的实验比较法
(1)元素金属性强弱的实验比较法。
①单质与水或非氧化性酸反应越剧烈,金属性越强。
②单质还原性越强或离子氧化性越弱,金属性越强。
③最高价氧化物对应水化物的碱性越强,金属性越强。
④若Xn++Y―→X+Ym+,则Y金属性比X强。
(2)元素非金属性强弱的实验比较法。
①与H 化合越容易,气态氢化物越稳定,非金属性越强。
2
②单质氧化性越强,阴离子还原性越弱,非金属性越强。
③最高价氧化物对应水化物的酸性越强,非金属性越强。
④An-+B―→Bm-+A,则B非金属性比A强。
3.元素性质递变规律
(1)同周期,从左到右,主族元素的金属性减弱,非金属性增强。
(2)同主族,从上到下,元素的金属性增强,非金属性减弱。
4.“四看”突破粒子半径大小比较
(1)“一看”电子层数:当最外层电子数相同,电子层数不同时,电子层数越多,半径越大。(同主族)
(2)“二看”核电荷数:当电子层数相同时,核电荷数越大,半径越小。(同周期)
(3)“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。(同元素)
(4)“四看”原子序数:当核外电子数相同时,原子序数越高,离子半径越小。(同结构)
5.建立“位—构—性”关系模型
这类题目往往将元素化合物知识、物质结构理论、化学基本理论等知识串联起来,综合性较强,难度较
大,解题的关键是正确推断元素,常用的主要方法有:
(1)原子或离子结构示意图。
(2)元素主要化合价的特征关系。
(3)原子半径的递变规律。
(4)元素周期表中短周期的特殊结构。
如:①元素周期表中第一周期只有两种元素H和He,H元素所在的第ⅠA族左侧无元素分布;
②He为0族元素,0族元素为元素周期表的右侧边界,0族元素右侧没有元素分布。利用这个关系可以确定元素所在的周期和族。
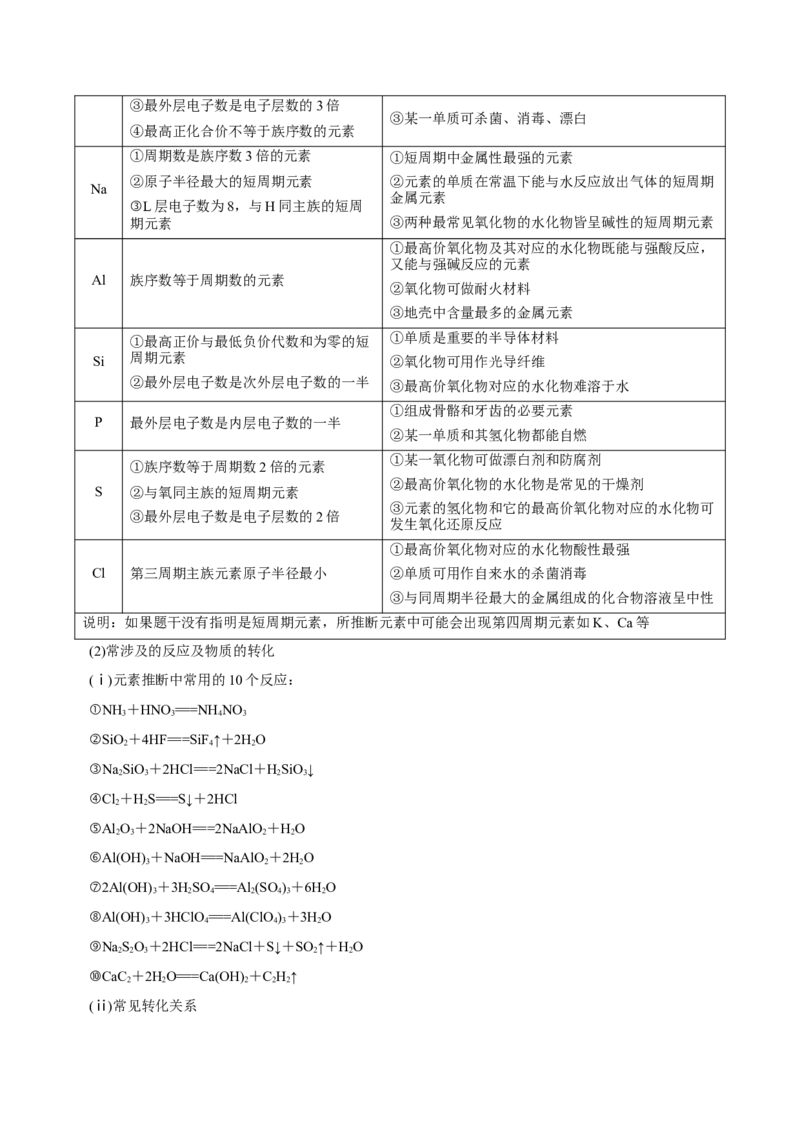
如:已知X、Y、Z、W四种短周期元素的位置关系如图:
则可以推出X为He,再依次推知Y为F、Z为O、W为P。
高频考点三 融合物质性质、转化、反应的元素推断
1.常见物质的性质及特征反应
(1)黄绿色气体有Cl ,红棕色气体有NO 或Br (g),在空气中变红棕色的无色气体是 NO,红色固体有
2 2 2
Cu、Cu O、Fe O,绿色固体有Cu (OH) CO、FeSO ·7H O等,黑色固体有C、MnO 、CuO、CuS、Ag S等。
2 2 3 2 2 3 4 2 2 2
(2)与CO、HO反应生成O 的固体为NaO。
2 2 2 2 2
(3)使品红溶液褪色的常见气体有Cl、SO 。
2 2
(4)两气体相遇能形成白烟的气体为HCl、NH 。
3
(5)短周期元素形成的化合物中,0.1 mol·L-1的水溶液的pH分别为1和13的化合物分别是HCl、NaOH。
(6)与强碱、强酸均能反应生成盐和水的氧化物和氢氧化物分别为Al O、Al(OH) 。
2 3 3
(7)元素的最高价氧化物对应的水化物与其氢化物反应生成盐的元素为N。
(8)短周期元素形成三元化合物与一般酸溶液反应生成沉淀和气体的化合物为NaSO。
2 2 3
(9)使澄清石灰水先变浑浊,后变澄清的气体有CO、SO 。
2 2
(10)腐蚀玻璃的酸为HF。
(11)与HO反应生成气体的化合物有NaO、MgN、Al S、NaH。
2 2 2 3 2 2 3
(12)元素的气态氢化物和它的最高价氧化物对应的水化物能发生氧化还原反应的元素是S。
2.常见短周期元素的单质及其化合物的转化关系
(1) (2)
(3) (4)(5)
(6)
(7)NH ―→NO―→NO ―→HNO
3 2 3
(8)S(H S)―→SO ―→SO ―→HSO
2 2 3 2 4
3.常见短周期元素组成的物质主要反应
(1)SiO+4HF===SiF ↑+2HO
2 4 2
(2)C+4HNO(浓)=====CO↑+4NO ↑+2HO
3 2 2 2
(3)2Cl +2Ca(OH) ===CaCl +Ca(ClO) +2HO
2 2 2 2 2
(4)SO +2HS===3S↓+2HO
2 2 2
(5)2NaCl+2HO=====2NaOH+Cl↑+H↑
2 2 2
4.元素及化合物性质推断
(1)常考11种元素推断
元素 排布特点(结构特征) 性质特征
①最外层只有一个电子
②族序数等于周期数 ①密度最小的单质
H
③无中子 ②宇宙含量最多的元素
④半径最小
①周期数是族序数2倍的元素
Li 电极材料
②最外层电子数是内层电子数的一半
①族序数等于周期数2倍的元素 ①形成化合物种类最多的元素
C ②单质是自然界中硬度最大的物质
②最高正价与最低负价代数和为零的短
周期元素 ③元素的气态氢化物中氢的质量分数最高的元素
①空气中含量最多的元素
②气态氢化物的水溶液呈碱性的元素
③元素的气态氢化物和它的最高价氧化物对应的水化
N
物能起化合反应
④某一氢化物可做液态燃料
⑤常见氢化物可做制冷剂
①族序数等于周期数3倍的元素 ①地壳中含量最多的元素
O
②最外层电子数是最内层电子数的3倍 ②氢化物在通常情况下呈液态的元素③最外层电子数是电子层数的3倍
③某一单质可杀菌、消毒、漂白
④最高正化合价不等于族序数的元素
①周期数是族序数3倍的元素 ①短周期中金属性最强的元素
②原子半径最大的短周期元素 ②元素的单质在常温下能与水反应放出气体的短周期
Na
金属元素
③L层电子数为8,与H同主族的短周
期元素 ③两种最常见氧化物的水化物皆呈碱性的短周期元素
①最高价氧化物及其对应的水化物既能与强酸反应,
又能与强碱反应的元素
Al 族序数等于周期数的元素
②氧化物可做耐火材料
③地壳中含量最多的金属元素
①最高正价与最低负价代数和为零的短 ①单质是重要的半导体材料
Si 周期元素 ②氧化物可用作光导纤维
②最外层电子数是次外层电子数的一半 ③最高价氧化物对应的水化物难溶于水
①组成骨骼和牙齿的必要元素
P 最外层电子数是内层电子数的一半
②某一单质和其氢化物都能自燃
①某一氧化物可做漂白剂和防腐剂
①族序数等于周期数2倍的元素
②最高价氧化物的水化物是常见的干燥剂
S ②与氧同主族的短周期元素
③元素的氢化物和它的最高价氧化物对应的水化物可
③最外层电子数是电子层数的2倍
发生氧化还原反应
①最高价氧化物对应的水化物酸性最强
Cl 第三周期主族元素原子半径最小 ②单质可用作自来水的杀菌消毒
③与同周期半径最大的金属组成的化合物溶液呈中性
说明:如果题干没有指明是短周期元素,所推断元素中可能会出现第四周期元素如K、Ca等
(2)常涉及的反应及物质的转化
(ⅰ)元素推断中常用的10个反应:
①NH +HNO===NHNO
3 3 4 3
②SiO +4HF===SiF ↑+2HO
2 4 2
③Na SiO+2HCl===2NaCl+HSiO↓
2 3 2 3
④Cl +HS===S↓+2HCl
2 2
⑤Al O+2NaOH===2NaAlO+HO
2 3 2 2
⑥Al(OH) +NaOH===NaAlO+2HO
3 2 2
⑦2Al(OH) +3HSO ===Al(SO )+6HO
3 2 4 2 4 3 2
⑧Al(OH) +3HClO===Al(ClO )+3HO
3 4 4 3 2
⑨Na SO+2HCl===2NaCl+S↓+SO ↑+HO
2 2 3 2 2
⑩CaC +2HO===Ca(OH) +C H↑
2 2 2 2 2
(ⅱ)常见转化关系③化合物A――→B――→C――→酸满足此条件的有CH、NH 、HS。
4 3 2
④X、Y、Z、W四种物质在一定条件下具有如图所示的转化关系,列举出符合此转化关系 X、Y、Z、W
的三组物质化学式
【题型突破】
题型一 考查同位素、同素异形体
例1.(2022·浙江卷)下列说法不正确的是
A.乙醇和丙三醇互为同系物
B. 和 互为同位素
C. 和 互为同素异形体
D.丙酮( )和环氧丙烷( )互为同分异构体
【答案】A
【解析】结构相似,组成上相差若干个CH 原子团的有机化合物为同系物,乙醇(CHCHOH)是饱和一元
2 3 2
醇,丙三醇是饱和三元醇,两者所含官能团数目不同,不互为同系物,A错误;质子数相同、中子数不同的同
种元素互为同位素,35Cl的质子数为17,中子数为18,37Cl的质子数为17,中子数为20,两者质子数相同、
中子数不同,互为同位素,B正确;由同种元素组成的不同的单质互为同素异形体,O 和O 是由氧元素组成
2 3
的不同的单质,两者互为同素异形体,C正确;分子式相同、结构不同的化合物互为同分异构体,丙酮和环氧
丙烷的分子式相同、结构不同,两者互为同分异构体,D正确;故选A。【变式探究】(2022·浙江卷)下列说法不正确的是
A.32S和34S互为同位素 B.C 和纳米碳管互为同素异形体
70
C.CHClCH Cl和CHCHCl 互为同分异构体 D.C H 和C H 一定互为同系物
2 2 3 2 3 6 4 8
【答案】D
【解析】32S和34S是质子数相同、中子数不同的原子,互为同位素,故A正确;C 和纳米碳管是由碳元
70
素组成的不同单质,互为同素异形体,故B正确;CHClCH Cl和CHCHCl 的分子式相同、结构不同,互为
2 2 3 2
同分异构体,故C正确;C H 和C H 可能为烯烃或环烷烃,所以不一定是同系物,故D错误;故选D。
3 6 4 8
【变式探究】(2021·浙江卷)下列说法正确的是
A. 14N 和15N 互为同位素 B. 间二甲苯和苯互为同系物
2 2
C. Fe C和Fe C互为同素异形体 D. 乙醚和乙醇互为同分异构体
2 3
【答案】B
【解析】14N 和15N 均为氮气分子,不能互称同位素,同位素指的是同一种元素的不同原子,A不正确;
2 2
间二甲苯和苯结构相似,分子中均含有1个苯环,两者在分子组成上相关2个“CH”原子团,因此,两者互为
2
同系物,B正确;Fe C和Fe C均为化合物,不能互称同素异形体,同素异形体的研究对象是单质,C不正
2 3
确;乙醚的分子式为C H O,乙醇的分子式为C HO,两者分子式不同,因此,两者不能互称同分异构体,D
4 10 2 6
不正确。综上所述,本题选B。
题型二 化学用语与化学键
例2.(2022·浙江卷)下列表示不正确的是
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
【答案】C
【解析】乙炔中碳碳之间为三键,故结构简式HC≡CH,选项A正确;KOH为离子化合物,故电子式为
,选项B正确; 为乙烷的比例模型,不是球棍模型,选项C错误;氯离子的核电荷数是
17,电子数为18,氯离子的结构示意图为 ,选项D正确;故选C。
【变式探究】(2022·浙江卷)下列表示正确的是A.乙醛的结构简式: B. 丁烯的键线式:
C. 的结构示意图: D.过氧化钠的电子式:
【答案】D
【解析】乙醛含醛基,其结构简式为:CHCHO,A错误;2-丁烯的结构简式为CHCH=CHCH ,键线式
3 3 3
为: ,B错误;硫的原子序数为16,硫原子最外层有6个电子,得2个电子形成硫离子,硫离子的结
构示意图为: ,C错误;过氧化钠为离子化合物,含离子键和氧氧非极性共价键,其电子式为:
,D正确;故选D。
【变式探究】(2021·辽宁卷)下列化学用语使用正确的是
A.基态C原子价电子排布图: B. 结构示意图:
C. 形成过程: D.质量数为2的氢核素:
【答案】D
【解析】基态C原子价电子排布图为: ,A错误; 结构示意图为: ,B错误; 形成
过程为: ,C错误;质量数为2的氢核素为: ,D正确;故选D。
题型三 结构、性质叙述式“位、构、性”关系的应用
例3.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次
增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A. 原子半径: B. 非金属性:C. Z的单质具有较强的还原性 D. 原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、
Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、Y
为O元素、Z为F元素、W为Si元素。同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大
小顺序为C>O>F,故A正确;同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元
素的非金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;位于元素周期表右上角
的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;原子序数为82的元素为铅元素,与硅元素都
位于元素周期表ⅣA族,故D正确;故选C。
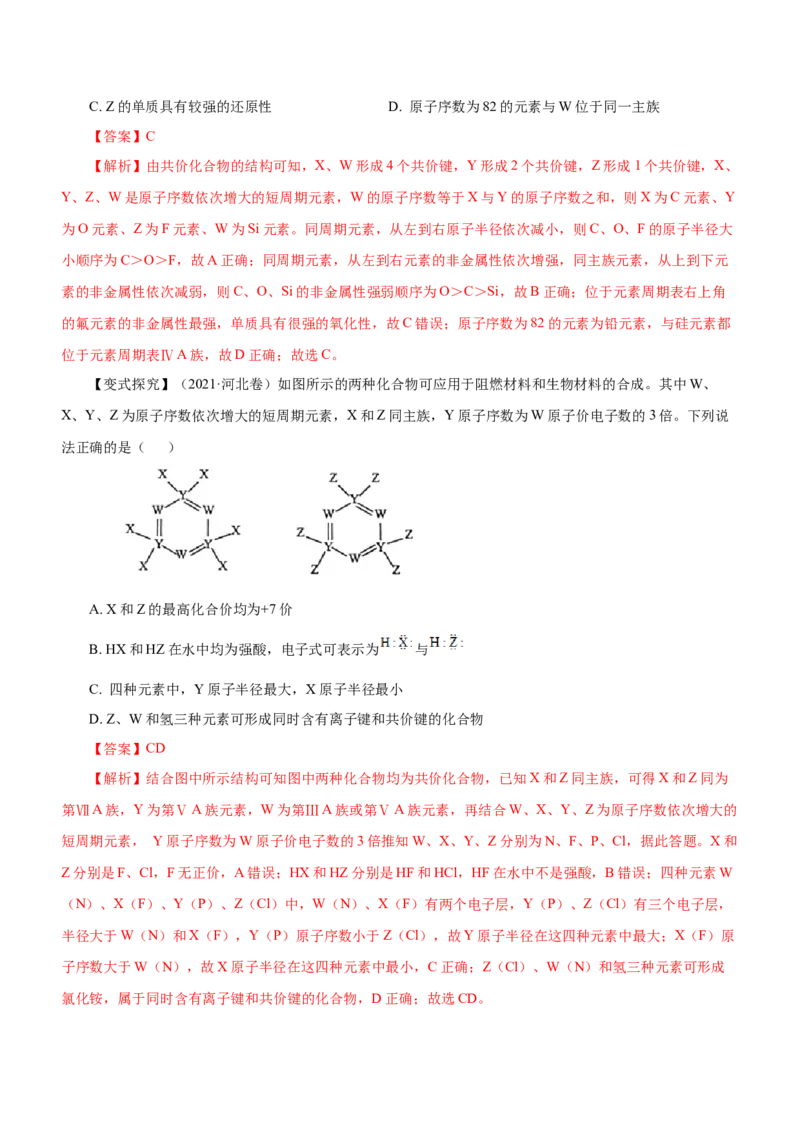
【变式探究】(2021·河北卷)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、
X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列说
法正确的是( )
A. X和Z的最高化合价均为+7价
B. HX和HZ在水中均为强酸,电子式可表示为 与
C. 四种元素中,Y原子半径最大,X原子半径最小
D. Z、W和氢三种元素可形成同时含有离子键和共价键的化合物
【答案】CD
【解析】结合图中所示结构可知图中两种化合物均为共价化合物,已知X和Z同主族,可得X和Z同为
第ⅦA族,Y为第ⅤA族元素,W为第ⅢA族或第ⅤA族元素,再结合W、X、Y、Z为原子序数依次增大的
短周期元素, Y原子序数为W原子价电子数的3倍推知W、X、Y、Z分别为N、F、P、Cl,据此答题。X和
Z分别是F、Cl,F无正价,A错误;HX和HZ分别是HF和HCl,HF在水中不是强酸,B错误;四种元素W
(N)、X(F)、Y(P)、Z(Cl)中,W(N)、X(F)有两个电子层,Y(P)、Z(Cl)有三个电子层,
半径大于W(N)和X(F),Y(P)原子序数小于Z(Cl),故Y原子半径在这四种元素中最大;X(F)原
子序数大于W(N),故X原子半径在这四种元素中最小,C正确;Z(Cl)、W(N)和氢三种元素可形成
氯化铵,属于同时含有离子键和共价键的化合物,D正确;故选CD。题型四 表格片段式“位、构、性”关系的应用
例4.(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物
对应的水化物为强酸。下列说法不正确的是
A. 原子半径:丁>戊>乙
B. 非金属性:戊>丁>丙
C. 甲的氢化物遇氯化氢一定有白烟产生
的
D. 丙 最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁为
P。根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;根据同周期从左到右
非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;甲的氢化物可能为氨气,可能为甲烷、乙烷等,
若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故C错
误;丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。综上所
述,答案为C。
的
【变式探究】(2021·广东卷)一种麻醉剂 分子结构式如图所示。其中, 的原子核只有1个质子;元
素 、 、 原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列说法
不正确的是
A. 是一种强酸 B. 非金属性:
C. 原子半径: D. 中,Z的化合价为+2价
【答案】C
【解析】题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。X的原子核只有1个质子,则X为H元素;元素Y、Z、W原子序数依次增大,且均位于X的下一周期,即第二周期
元素,则Y为C元素,Z为O元素,W为F元素;元素E的原子比W原子多8个电子,则E为Cl元素,综合
以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。据此分析解答。氯元素非金属性较强,其最
高价氧化物的水化物HClO 是一种强酸,故A正确;同一周期元素从左到右非金属性逐渐增强,所以非金属
4
性:F>O>C,故B正确;同一周期从左到右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,电子
层越多半径越大,所以原子半径:Cl>C>F,故C错误; OF 中,F为-1价,则O的化合价为+2价,故D正
2
确;答案选C。
【变式探究】(2021·浙江卷)现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q
在同一周期。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为零
Z 单质为淡黃色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是
A. 常温时,X单质能与水发生剧烈反应
B. Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C. Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D. 第五周期且与Q同主族元素的单质在常温常压下呈液态
【答案】B
【解析】X原子的最外层电子数是核外电子总数的一半,由于最外层电子数不超过8个,因此X只能是第
二周期的Be;Y元素的最高化合价和最低化合价之和为零,位于第ⅣA族,Y是C或Si;Z单质为淡黄色固
体,常存在于火山喷口附近,因此Z是S;Q是同周期元素中原子半径最小,且Z和Q位于同一周期,因此Q
是Cl,据此解答。根据以上分析可知X是Be,Y是C或Si,Z是S,Q是Cl。则Be的金属性弱于Mg,常温
时镁和冷水不反应,因此Be单质不能与水发生剧烈反应,A错误;Y与Q元素组成的CCl 或SiCl 分子,空间
4 4
构型均为正四面体,B正确;Y、Z、Q三种元素的非金属性逐渐增强,非金属性越强,最高价含氧酸的酸性
越强,则最高价氧化物对应水化物的酸性依次增强,C错误;第五周期且与Cl同主族元素的单质是碘,在常
温常压下呈固态,D错误;答案选B。
题型五 离子化合物和共价化合物
例5.(2022·海南卷)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正
确的是
A. 是非极性分子 B. 简单氢化物沸点:
C. Y与Z形成的化合物是离子化合物 D. X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【解析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且Y是组成水的元
素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,则Z为Na元素,W原子在同周期
主族元素中原子半径最小,则W为Cl元素,据此分析解答。由分析,X为N元素,W为Cl元素,NCl 分子
3
的空间构型为三角锥形,其正负电荷的中心不重合,属于极性分子,A错误;HO和NH 均含有氢键,但HO
2 3 2
分子形成的氢键更多,故沸点HO>NH ,B错误;Y为O元素,Z为Na元素,两者形成的化合物为NaO、
2 3 2
NaO 均为离子化合物,C正确;N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
2 2 3 2
故选C。
【变式探究】(2022·浙江卷)W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y同族,Y的
原子序数是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是
A.非金属性:Y>W B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸 D.X与Y可形成化合物XY
2 3
【答案】D
【解析】X是地壳中含量最多的金属元素,X为Al元素,W和Y同族,Y的原子序数是W的2倍,W为
O元素,Y为S元素,Z为Cl元素,据此分析解题。非金属性同主族从上至下逐渐减弱:Y<W,A错误;氯
化铝是共价化合物,B错误;Y、Z的最高价氧化物对应的水化物分别硫酸和高氯酸,两者均为强酸,次氯酸
也是氯的氧化物对应的水化合物,但次氯酸为弱酸,C错误;根据化合物的化合价代数和为0可知,铝与硫元
素形成的化合物化学式为Al S,D正确;故选D。
2 3
题型六 化学键
例6.(2022·湖南卷)下列说法错误的是
A. 氢键,离子键和共价键都属于化学键
B. 化学家门捷列夫编制了第一张元素周期表
C. 药剂师和营养师必须具备化学相关专业知识
D. 石灰石是制造玻璃和水泥的主要原料之一
【答案】A
【解析】离子键和共价键都属于化学键,氢键属于分子间作用力,A说法错误;第一张元素周期表是俄国化学家门捷列夫编制的,B说法正确;药剂师和营养师的工作分别与药剂和营养物质有关,因此必须具备相关
的化学专业知识才能胜任相关工作,C说法正确;制造玻璃的主要原料是石灰石、石英和纯碱,制造水泥的主
要原料是石灰石和黏土,D说法正确;综上所述,本题选A。
【变式探究】(2021·全国甲卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子
数是W和X的最外层电子数之 和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙
述正确的是( )
A.原子半径:Z>Y>X>W
B. W与X只能形成一种化合物
C. Y的氧化物为碱性氧化物,不与强碱反应
D. W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【解析】W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电
子数之和,同时也是Y的最外层电子数的2倍,可知Z应该位于第三周期且最外层电子数为偶数,推测Z为S
元素,W和X的单质常温下均为气态,推测W为H元素,X为N元素,则Y为Al元素。H元素、N元素和S
元素能够形成物质(NH )S,该物质中同时含有离子键和共价键,故D正确;原子核外电子层数不同时,电子
4 2
层数越多,原子半径越大,原子核外电子层数相同时,原子对应元素的原子序数越小,则原子半径越大,四种
元素的原子半径由大到小依次为Al>S>N>H,故A错误;B项,H元素和N元素能够形成NH 、NH 等多种化
3 2 4
合物,故B错误;Al元素的氧化物为Al O,属于两性氧化物,既能和酸反应,又能和碱反应,故C错误。综
2 3
上所述,本题选D。
【变式探究】(2021·海南卷)短周期主族元素 、 、 、 的原子序数依次增大, 离子与 分子
均含有14个电子;习惯上把电解饱和 水溶液的工业生产称为氯碱工业。下列判断正确的是
A.原子半径: B.最高价氧化物对应的水化物的酸性:
C.化合物 的水溶液呈中性 D. 分子中既有 键又有 键
【答案】BD
【解析】 离子与 分子均含有14个电子,则X为C,Y为N;习惯上把电解饱和ZW水溶液的工业
生产称为氯碱工业,则Z为Na,W为Cl。同周期元素原子半径随核电荷数的增大半径逐渐减小,故Na>Cl,
故A错误;同周期元素随核电荷数的增大非金属性逐渐增强,其最高价氧化物对应的水化物的酸性越强,故
HNO>HCO,故B正确;NaCN为强碱弱酸盐,显碱性,故C错误;(CN) 的结构简式为 ,分子
3 2 3 2中单键为 键,三键中含有1个 键和2个 键,故D正确;故选BD。
题型七 金属性和非金属性
例7.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次
增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A. 原子半径: B. 非金属性:
C. Z的单质具有较强的还原性 D. 原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、
Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、Y
为O元素、Z为F元素、W为Si元素。同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大
小顺序为C>O>F,故A正确;同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元
素的非金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;位于元素周期表右上角
的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;原子序数为82的元素为铅元素,与硅元素都
位于元素周期表ⅣA族,故D正确;故选C。
【变式探究】(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数
之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下
列说法正确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的佛点: D.最高价含氧酸的酸性:
【答案】D
【解析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子最
外层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最外层电
子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、Y、Z的最外层电
子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的最外
层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,则Z的
最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解题。X为Al,Q为N或O或F,同
一周期从左往右元素非金属性依次增强,同一主族从上往下依次减弱,故非金属性:Q>X,A错误;由分析可
知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X,B错误;含有氢
键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为Cl或S或P,其简
2 3
单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在,故沸点Q>Z,C错
2 3
误;元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧酸
酸性:Z>Y,D正确;故答案为D。
题型八 综合考查
例8.(2022·全国乙卷)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z
为短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数常温下为气体。该化合物的热
重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
A. W、X、Y、Z的单质常温下均为气体 B. 最高价氧化物的水化物酸性:
C. 阶段热分解失去4个 D. 热分解后生成固体化合物
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子
4 5 8 2
序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则说
明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序数依次增
2
加,且加和为21,则X为B。X(B)的单质常温下为固体,故A错误;根据非金属性越强,其最高价氧化物的
水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错误;根据前面已知200℃以下
3 3 3
热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热分解失去4个HO,则质量分数
2
,则说明不是失去去4个HO,故C错误;化合物(NH B O·4H O)在
2 4 5 8 2500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到关系式2NH B O·4H O~5B O,则固
2 3 2 3 4 5 8 2 2 3
体化合物B O 质量分数为 ,说明假设正确,故D正确。答案为D。
2 3
【变式探究】(2022·浙江卷)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电
子数等于其周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q
是同周期中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【解析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于
3
X、Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q为
Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl,以此解题。由分析可知X为H,Z为O,则其形
成的10电子微粒有HO、OH-、HO+,A错误;由分析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用
2 3 2
于自来水消毒,B正确;由分析可知Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,
2 2
为离子晶体,晶体类型相同,C错误;由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,
其溶液显碱性,D错误;故选B。