文档内容
专题 07 非金属及其化合物
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·河北省邯郸市部分学校高三联考)在给定条件下,下列选项所示的物质间转化均能实现的是
( )
A.
B.
C.
D.
2.(2022·辽宁省六校高三期中联考)工业上制备下列物质的生产流程合理的是( )
A.N(g) NO(g) HNO(aq)
2 3
B.石英砂 粗硅 SiHCl 纯硅
3
C.饱和食盐水 漂白粉
D.NH (g) NaCO(s) NaHCO (s)
3 2 3 3
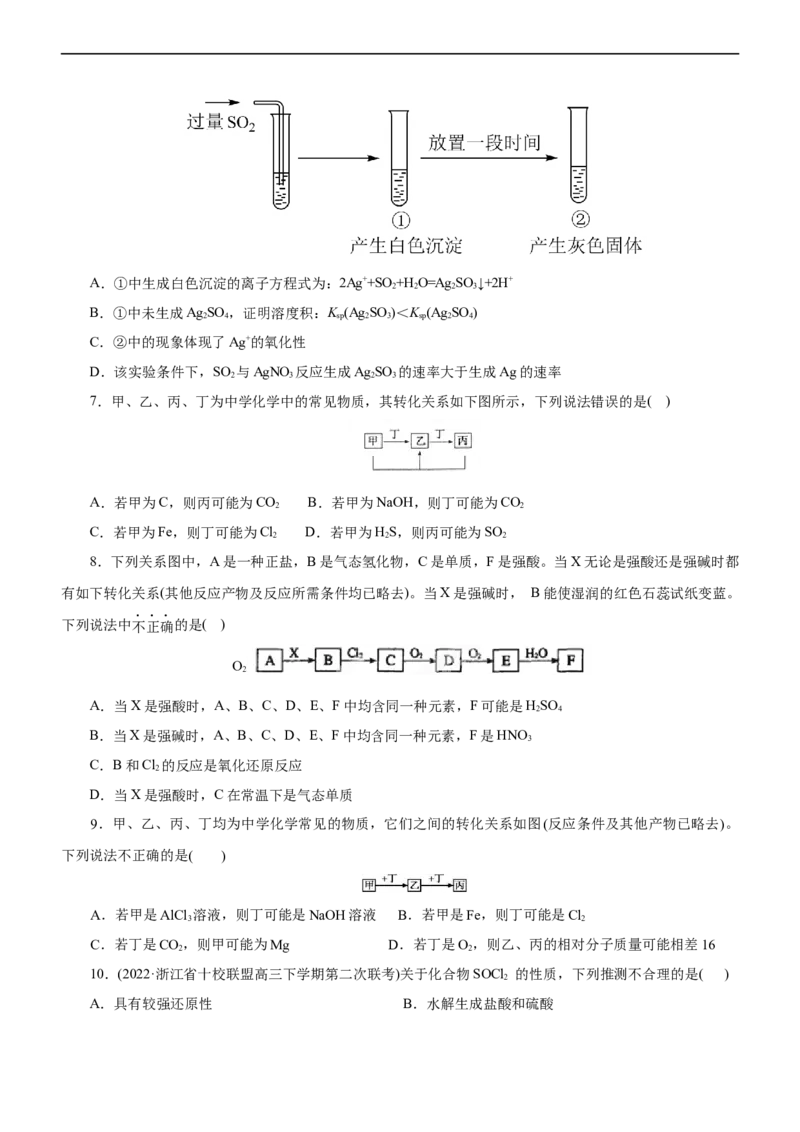
3.(2022·广东珠海市高三一模)部分含氯物质的分类与相应氯元素的化合价关系下图所示。下列说法错误
的是( )
A.a 与d,a与e在酸性情况下反应,均可以得到b
B.c 为一种新型自来水消毒剂,代替 b的原因是:c的毒性更小C.b 的水溶里加入 CaCO ,可以增加d的产量
3
D.消毒液可用于环境消毒,主要是因为含有d,e的固体可用于实验室制O
2
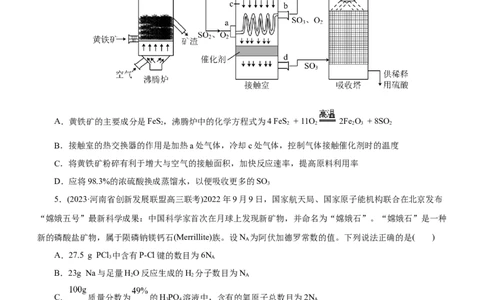
4.(2023·黑龙江省绥化市第一中学高三期中)图为接触法制硫酸的示意图,已知2SO (g)+CO(g)
2 2
2SO (g) ΔH<0,下列说法不正确的是( )
3
A.黄铁矿的主要成分是FeS,沸腾炉中的化学方程式为4 FeS + 11O 2Fe O + 8SO
2 2 2 2 3 2
B.接触室的热交换器的作用是加热a处气体,冷却c处气体,控制气体接触催化剂时的温度
C.将黄铁矿粉碎有利于增大与空气的接触面积,加快反应速率,提高原料利用率
D.应将98.3%的浓硫酸换成蒸馏水,以便吸收更多的SO
3
5.(2023·河南省创新发展联盟高三联考)2022年9月9日,国家航天局、国家原子能机构联合在北京发布
“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种
新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族。设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.27.5 g PCl 中含有P-Cl键的数目为6N
3 A
B.23g Na与足量HO反应生成的H 分子数目为N
2 2 A
C. 质量分数为 的HPO 溶液中,含有的氧原子总数目为2N
3 4 A
D.在25°C时,1L pH=12的Ca(OH) 溶液中含有OH-数目为0.01N
2 A
6.(2023·江苏省南通市如东县高三期中学情检测)SO 和NOx在生产、生活和科学研究中有着广泛的应用,
2
也是大气主要污染物。硫酸盐(含SO 2-、HSO -)气溶胶是PM 的成分之一,SO 在VO 催化作用下与空气中的
4 4 2.5 2 2 5
O 在接触室中发生可逆反应,反应的热化学方程式表示为:2SO (g)+ O(g) 2SO (g) ΔH=-196.6
2 2 3
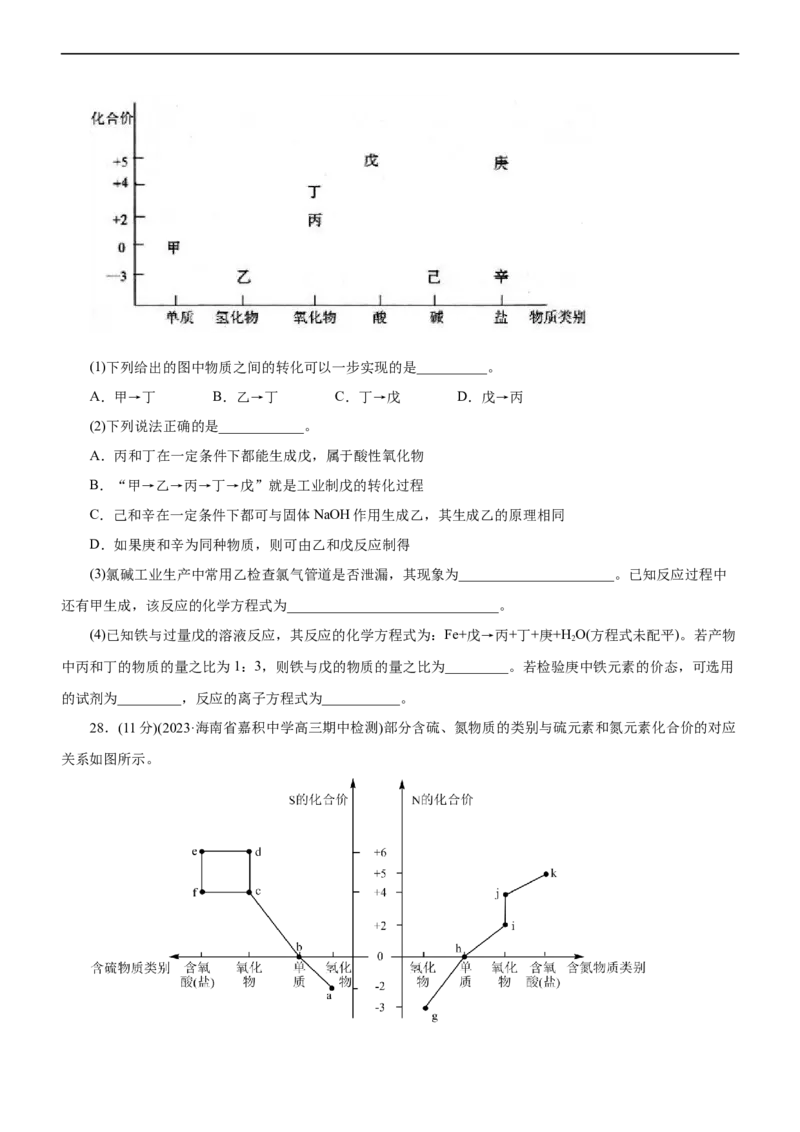
kJ·mol-1 。向AgNO 溶液中通入过量SO ,过程和现象如下图。经检验,白色沉淀为AgSO ;灰色固体中含
3 2 2 3
有Ag。下列说法不正确的是( )A.①中生成白色沉淀的离子方程式为:2Ag++SO+H O=AgSO ↓+2H+
2 2 2 3
B.①中未生成AgSO ,证明溶度积:K (AgSO )<K (AgSO )
2 4 sp 2 3 sp 2 4
C.②中的现象体现了Ag+的氧化性
D.该实验条件下,SO 与AgNO 反应生成AgSO 的速率大于生成Ag的速率
2 3 2 3
7.甲、乙、丙、丁为中学化学中的常见物质,其转化关系如下图所示,下列说法错误的是( )
A.若甲为C,则丙可能为CO B.若甲为NaOH,则丁可能为CO
2 2
C.若甲为Fe,则丁可能为Cl D.若甲为HS,则丙可能为SO
2 2 2
8.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都
有如下转化关系(其他反应产物及反应所需条件均已略去)。当X是强碱时, B能使湿润的红色石蕊试纸变蓝。
下列说法中不正确的是( )
O
2
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是HSO
2 4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO
3
C.B和Cl 的反应是氧化还原反应
2
D.当X是强酸时,C在常温下是气态单质
9.甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其他产物已略去)。
下列说法不正确的是( )
A.若甲是AlCl 溶液,则丁可能是NaOH溶液 B.若甲是Fe,则丁可能是Cl
3 2
C.若丁是CO,则甲可能为Mg D.若丁是O,则乙、丙的相对分子质量可能相差16
2 2
10.(2022·浙江省十校联盟高三下学期第二次联考)关于化合物SOCl 的性质,下列推测不合理的是( )
2
A.具有较强还原性 B.水解生成盐酸和硫酸C.与乙酸作用能产生CHCOCl D.与NaOH溶液反应可生成三种钠盐
3
11.(2022·浙江省浙南名校高三联考)关于化合物KICl 的性质,下列推测不合理的是( )
2
A.与KOH反应可生成两种盐 B.受热分解生成KI和Cl
2
C.具有强氧化性 D.与KI反应可生成I 和KCl
2
12.(2022•浙江省稽阳联谊学校高三联考)下列“类比”合理的是( )
A.SiH 的沸点高于CH 的沸点,则PH 的沸点高于NH 的沸点
4 4 2 4 2 4
B.CO 与Ba(NO ) 溶液不反应,则SO 与Ba(NO ) 溶液也不反应
2 3 2 2 3 2
C.Fe与Cl 反应生成FeCl ,则Fe与I 反应生成FeI
2 3 2 3
D.NaCl与浓HSO 加热可制HCl,则NaBr与浓HPO 加热可制HBr
2 4 3 4
13.(2022•浙江省绍兴市高三选考诊断性考试)下列“类比”结果正确的是( )
A.乙炔的分子构型为直线形,则 的分子构型也为直线形
B.单质的熔点Br <I,则单质的熔点Na<K
2 2
C.CO、SO 是酸性氧化物,则NO 也是酸性氧化物
2 2 2
D.SO 通入BaCl 溶液不产生沉淀,则SO 通入Ba(NO ) 溶液也不产生沉淀
2 2 2 3 2
14.学习化学不是靠一味背诵的,要学会运用合适的方法,如“类推”,这样才能事半功倍。下列“类
推”结果正确的是( )
A.CO、SO 是酸性氧化物,则NO 也是酸性氧化物
2 2 2
B.Ba(HCO ) 的溶解度比BaCO 的大,则NaHCO 的溶解度也比NaCO 的大
3 2 3 3 2 3
C.pH=1的盐酸稀释100倍后pH=3,则pH=6的CHCOOH稀释100倍后pH=8
3
D.将丙三醇加入新制Cu(OH) 中溶液呈绛蓝色,则将葡萄糖溶液加入新制Cu(OH) 中溶液也呈绛蓝色
2 2
15. (2022•浙南名校联盟高三第一次联考)下列“类比”合理的是( )
A.由O+2H S=S+2H O,说明非金属性O>S,推测:高温下2C+ SiO = Si+2CO,非金属性C>Si
2 2 2 2
B.由CO+Ca(ClO) +H O=CaCO ↓+2HClO推测:SO +Ca(ClO) +H O=CaSO↓+2HClO
2 2 2 3 2 2 2 3
C.Fe与S在加热条件下反应生成FeS,推测:Cu与S在加热条件下生成CuS
D.由NaSO +2HCl=2NaCl+H O+SO ↑,推测:NaSO +H SO =Na SO +H O+SO ↑
2 3 2 2 2 3 2 4 2 4 2 2
16.(2022•浙江省9 +1高中联盟高三联考)H O、HO 和HO (超氧化氢)等都属于氢氧化合物,其中HO 又
2 2 2 2 2
叫超氧酸,与HO 化学性质相似,又有某些性质与HX(X=Cl、Br、I)相似。下列说法不正确的是( )
2 2
A.HO 在碱性条件下比酸性条件更易分解产生O
2 2
B.向品红溶液中加入足量HO ,红色褪去,加热后又恢复红色
2
C.HO 可与硝酸银溶液发生如下反应:HO +AgNO =AgO↓+HNO
2 2 3 2 3
D.KO 与冰水反应理论上可得到HO
2 217.剧毒品氰化钠(NaCN)在天津爆炸的事故中给大家带来恐惧,含NaCN超标的废水可用两段氧化法处
理:(1)NaCN与NaClO反应,生成NaOCN和NaCl;(2)NaOCN与NaClO反应,生成NaCO 、CO 、NaCl和
2 3 2
N;
2
已知:HCN为弱酸,且有剧毒;HCN、HOCN中N元素的化合价相同;达到排放标准NaCN含量应低于
0.5mg/L
下列说法不正确的是( )
A.HClO的电子式为 ,可用作漂白剂
B.第一次氧化时,溶液的pH应调节为酸性
C.第二次氧化时发生反应的离子方程式为2OCN-+3ClO-=CO 2-+CO ↑+3Cl-+N ↑
3 2 2
D.处理100m3含NaCN 10.3mg/L的废水,实际至少需3.725kg NaClO
18.(2022·浙江省金华十校高三下学期4月模拟)某些化合物类别往往会随着状态改变而改变。例如气态
PCl 为共价化合物,固态PCl 却是离子化合物,阳离子为正四面体结构,阴离子为正八面体结构。下列说法不
5 5
正确的是( )
A.固态PCl 中的阳离子为[ PCl ]+
5 4
B.固态PCl 是离子晶体,能导电
5
C.PCl 部分氟化可得PCl F,其化学式可表述为[ PCl ]+ [ PF ]-
5 2 3 4 6
D.固态P Br 中不存在正八面体阴离子的原因是Br-的离子半径过大
5
19.(2023·浙江省十校联盟高三10月月考)魔酸是五氟化锑和氟磺酸的混合物,化学式为SbF ∙HSO F,是
5 3
一种酸性比普通无机酸强106~1010倍的超强酸,能将HClO 质子化:SbF ∙HSO F+HClO=[SbF∙SO F]-+
4 5 3 4 5 3
[H ClO ]+。下列推测不合理的是( )
2 4
A.魔酸没有固定的沸点 B.SbF ∙HF是超强酸
5
C.魔酸具有强氧化性 D.魔酸与NaClO 溶液反应可生成[H ClO ]+
4 2 4
20.(2023·浙江省名校协作体高三开学考试)已知氯磺酸(ClSOH)是极易水解的一元强酸,下列推测不合理
3
的是( )
A.ClSOH与足量氢氧化钠溶液反应能生成两种盐
3
B.相同条件下,ClSOH比FSO H更容易水解
3 3
C.ClSOH的制备可以用HCl与SO 反应,也可用浓盐酸和浓HSO 反应制得
3 3 2 4
D.相同条件下,等物质的量的ClSOH和HCl分别溶于水制成1L溶液,两者pH不同
3
21.(2023·浙江省Z20名校新高考研究联盟高三第一次联考)下列“类比”结果正确的是( )
A.Cl、Br 、I 的沸点逐渐升高,则H、N、O 的沸点也逐渐升高
2 2 2 2 2 2B.CHCHO与H 可发生加成反应,则相同条件下CHCOOH也可以与H 发生加成反应
3 2 3 2
C.向NaCO 中加入少量水,伴随放热现象,则向NaHCO 中加入少量水,也伴随放热现象
2 3 3
D.乙醇与足量酸性高锰酸钾溶液反应生成乙酸,则乙二醇与足量酸性高锰酸钾溶液反应生成乙二酸
22.(2023·浙江省强基联盟高三上学期10月统测)类比推理是化学中常用的思维方法。下列推理正确的是(
)
A.NH 的熔沸点高于PH ,则CH 的熔沸点也高于SiH
3 3 4 4
B.PCl 水解生成HPO 和 ,则NCl 水解生成HNO 和
3 3 3 3 2
C.CO 是直线形分子,则SiO 也是直线形分子
2 2
D.NH 能与HCl反应生成NH Cl,则HN-NH 也可以与HCl反应生成NHCl
3 4 2 2 2 6 2
23.(2023·浙江省强基联盟高三上学期10月统测)硫的四种含氧酸根离子的结构如图所示,下列有关说法
正确的是( )
A.①②③④中都含有极性键和非极性键
B.①④中硫原子的化合价不同
C.能在酸性溶液中将Mn2+转化为MnO-的只有④
4
D.只考虑硫元素的价态,②只有氧化性
24.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧化
3
B Cu能与浓HNO 反应 性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
25.根据下列实验和现象,所得实验结论正确的是( )
选项 实验 现象 实验结论原溶液中含有 SO 2-、
向某溶液中先滴加适量稀硝酸,再滴加 4
A 出现白色沉淀 SO 2-、HSO -中的一种或
少量BaCl 溶液 3 3
2 几种
向装有Fe(NO ) 溶液的试管中加入稀硫 在管口观察到
B 3 2 HNO 分解成了NO
酸 红棕色气体 3 2
左边棉球变为
C 橙色,右边棉 氧化性:Cl>Br >I
2 2 2
球变为蓝色
D SO 和SO 混合气体通入Ba(NO ) 溶液 出现白色沉淀 得到的沉淀只有BaSO
2 3 3 2 4
二、非选择题(本题包括5小题,共50分)
26.(8分)(2022·海南省高三学业水平诊断考试)氮、氧、硫、氯是四种重要的非金属元素,研究它们的性
质及用途对生产,生活、科研具有重要意义。
(1)一氯胺(NH Cl)是一种长效缓释水消毒剂,工业上可利用反应NHI (g)+Cl (g)=NH Cl(g)+HCl(g)制备。
2 3 2 2
①一氯胺(NH Cl)在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质,该物质的电
2
子式为___________。
②氨气也是工业上制备硝酸的主要原料,制备硝酸的过程中涉及NO 与水的反应。该反应中氧化剂与还
2
原剂的物质的量之比为___________。
(2)SO 、NO 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收SO 能得到含
2 2 2
(NH )SO 和NH HSO 的吸收液,写出生成(NH )SO 的离子方程式:___________。若向吸收液中通入过量
4 2 3 4 3 4 2 3
NO ,NH HSO 能与NO 发生反应生成N 和(NH )SO ,写出该反应的离子方程式:___________。
2 4 3 2 2 4 2 4
(3)Cl 与NaOH溶液反应可制取“84”消毒液。用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含
2
NaClO,),此时ClO-的浓度为c mol/L;加热时NaClO能转化为NaClO,测得t时刻溶液中ClO-的浓度为c
3 0 3 1
mol/L (不考虑加热前后溶液体积的变化)。
①写出溶液中NaClO分解生成NaClO 的化学方程式:___________。
3
②t时刻溶液中c(Cl-)=___________mol/L(用含c、c 的代数式表示)。
0 1
27.(10分)利用下图可以从不同角度研究含氮物质的性质及其转化关系。图中甲~辛均含氮元素。回答下
列问题:(1)下列给出的图中物质之间的转化可以一步实现的是__________。
A.甲→丁 B.乙→丁 C.丁→戊 D.戊→丙
(2)下列说法正确的是____________。
A.丙和丁在一定条件下都能生成戊,属于酸性氧化物
B.“甲→乙→丙→丁→戊”就是工业制戊的转化过程
C.己和辛在一定条件下都可与固体NaOH作用生成乙,其生成乙的原理相同
D.如果庚和辛为同种物质,则可由乙和戊反应制得
(3)氯碱工业生产中常用乙检查氯气管道是否泄漏,其现象为______________________。已知反应过程中
还有甲生成,该反应的化学方程式为______________________________。
(4)已知铁与过量戊的溶液反应,其反应的化学方程式为:Fe+戊→丙+丁+庚+H O(方程式未配平)。若产物
2
中丙和丁的物质的量之比为1:3,则铁与戊的物质的量之比为_________。若检验庚中铁元素的价态,可选用
的试剂为_________,反应的离子方程式为___________。
28.(11分)(2023·海南省嘉积中学高三期中检测)部分含硫、氮物质的类别与硫元素和氮元素化合价的对应
关系如图所示。回答下列问题:
(1)h的电子式为_______。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是_______(填序号)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将 的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是_______。
(4)S N(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入SCl
4 4 2 2
的CCl 浓液中,可制得该物质:6 S Cl+16NH=S N+S +12NHCl (已知S 是硫单质中最稳定的)。
4 2 2 3 4 4 8 4 8
①上述制备反应中被氧化的元素是_______(填元素符号),物质g体现的性质有_______。
②SN 在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方
4 4
程式是_______。
29.(10分)(2022·浙江省杭州地区及周边重点中学高一期中联考)Cl O为国际公认高效安全灭菌消毒剂之一,
2
实验室可用潮湿的Cl 与NaCO 反应制取反应装置如图所示(夹持装置已略)。
2 2 3
已知:ClO熔点为-116℃,沸点为3.8℃,浓度过高或加热时易发生分解并爆炸。Cl 沸点为-34.6℃,液氨
2 2
沸点为-33.5℃。
(1)实验室可利用MnO 和浓盐酸制备氯气,下列哪组物质也可用于实验室制备氯气_____________。
2
A.KClO 固体和浓盐酸 B.KMnO 固体和浓盐酸 C.NaCl固体和浓硫酸
3 4
(2)检查虚框中装置气密性的方法为:用止水夹夹住装置A两端的橡胶管,打开分液漏斗旋塞加水,若
____________________________________,则装置的气密性良好。
(3)下列有关该实验的说法中,不正确的是_____________。
A.实验过程中,若MnO 过量,浓盐酸能被完全反应
2
B.B中试剂是浓硫酸,目的是干燥氯气
C.氮气的作用之一是稀释生成的ClO,减少实验爆炸危险
2D.从装置D中逸出气体的主要成分是ClO
2
(4)①装置C中潮湿的Cl 与NaCO 以等物质的量反应,生成NaHCO 、气体ClO和另一种盐X,试写出
2 2 3 3 2
该反应化学方程式_______________________________________。
②液氨的作用是_______________________________________。
(5)该实验装置存在一处明显的不足,其改进措施为_____________________。
30.(11分)(2022·陕西省泾阳县教育局教学研究室高三期中)随着现代工业发展,SO 烟气排放量急剧增加。
2
将SO 还原为硫磺是目前烟气脱硫研究的热点。根据SO 的反应状态,将SO 还原法分为气相还原法和液相还
2 2 2
原法。
Ⅰ.气相还原法-固体还原剂直接还原法
固体还原剂直接还原法是指在一定温度下(200℃~300℃)将SO 烟气通过固体还原剂,使SO 中的氧原子转
2 2
移到固体还原剂上,从而实现SO 的还原,其流程如图:
2
(1)再生塔中生成的物质_______(填化学式)可在流程中循环使用。
(2)脱硫塔中发生反应的化学方程式为_______。
(3)脱硫过程中,当产生48g单质S 时,转移电子的物质的量为_______mol。
2
Ⅱ.液相还原法-液相催化歧化制硫法
Petrusevski等人用 作为催化剂,在常温下,将NaHSO 进行液相催化回收硫磺的工艺如图:
3
(4)仪器中,“操作”时不需要用到的是_______(填字母)。A. B. C. D.
(5) 催化NaHSO 的反应过程为:第一步:_______(用离子方程式表示),第二步:I+ HSO -+ H O=2I-+
3 2 3 2
SO 2-+3H+。
4
(6)液相催化歧化制硫法具有反应条件温和、运行费用低等优点,然而其缺点是硫磺的回收率不会高于
_______%(保留1位小数)。