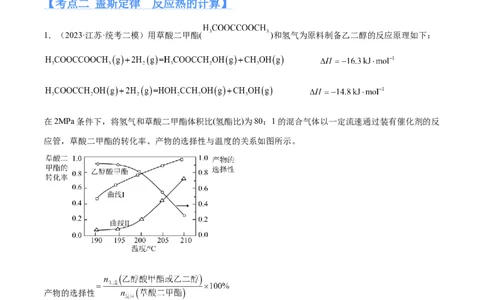
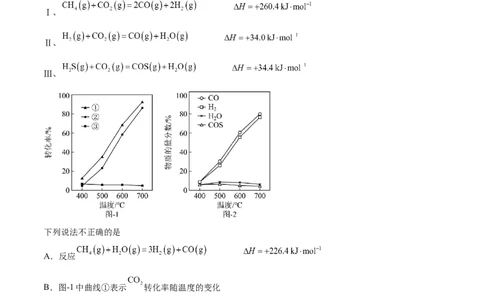
文档内容
专题验收评价
专题 08 化学反应与能量变化
内容概览
A·常考题不丢分
【考点一 反应热及其表示方法】
【考点二 盖斯定律 反应热的计算】
【微专题 化学反应历程图像分析】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 反应热及其表示方法】
1.(2023·上海崇明·统考一模)反应A(g)+B(g)→C(g)-Q (Q >0)分两步进行:①A(g)+B(g)→X(g)
1 1
+Q (Q >0);②X(g)→C(g)-Q (Q >0)。下列图中,能正确表示总反应过程中能量变化的是
2 2 3 3
A. B. C. D.
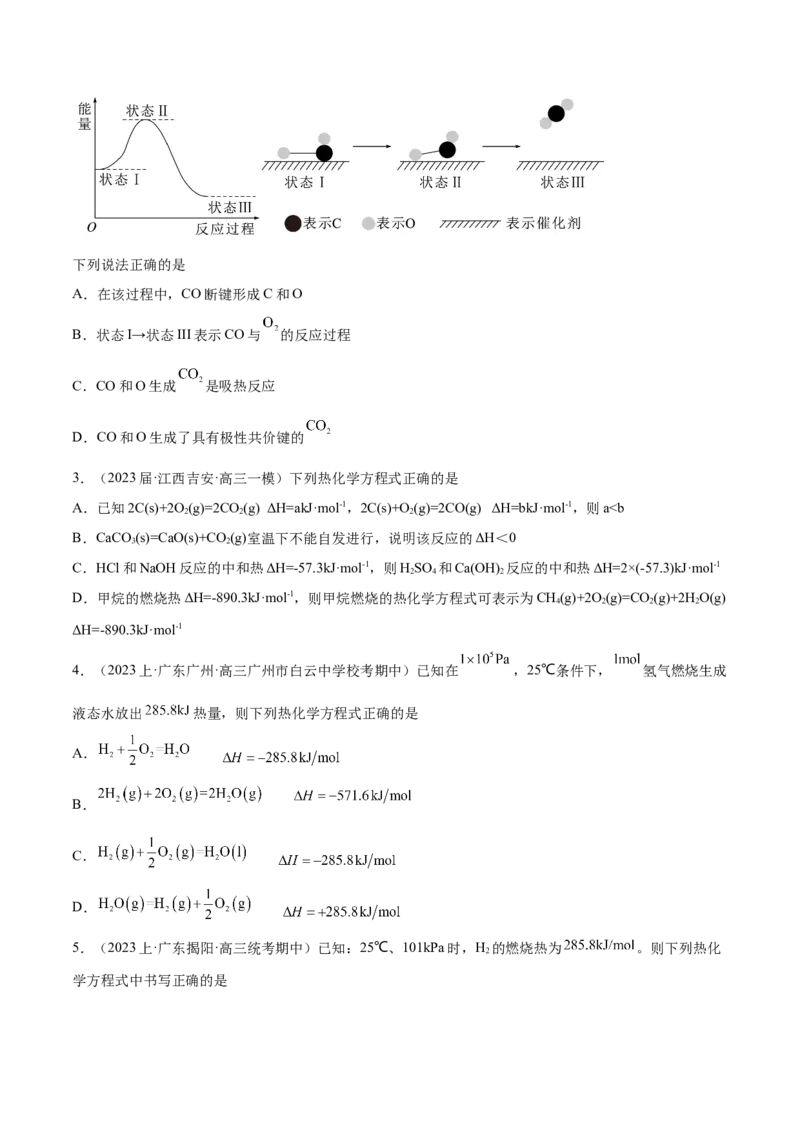
2.(2023·河南安阳·安阳一中校考模拟预测)最新报道:科学家首次用X射线激光技术观察到CO与O在
催化剂表面形成化学键的过程。反应过程的示意图如图:下列说法正确的是
A.在该过程中,CO断键形成C和O
B.状态I→状态III表示CO与 的反应过程
C.CO和O生成 是吸热反应
D.CO和O生成了具有极性共价键的
3.(2023届·江西吉安·高三一模)下列热化学方程式正确的是
A.已知2C(s)+2O(g)=2CO (g) ΔH=akJ·mol-1,2C(s)+O(g)=2CO(g) ΔH=bkJ·mol-1,则aK(700℃)
3.(2023·山东德州·德州市第一中学校联考模拟预测)下列说法正确的是
A. ,则
B. 的摩尔燃烧焓为 ,则C. ,则完全破坏等质量的 和 中的化学键,需要的能量 大
D. ,则 与足量 反应放热
4.(2023上·黑龙江齐齐哈尔·高三校联考期末)以CO和 为原料合成甲醇是工业上的成熟方法,直接
以 为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就是将 转化为
甲醇。
已知:①
②
③
下列说法正确的是
A.若温度不变,反应①中生成 时,放出的热量小于45.25kJ
B.对于反应②③,选用高效催化剂,可分别降低反应的焓变
C. 与 合成甲醇的热化学方程式为
D.以 和 为原料合成甲醇,同时生成 ,该反应放出能量
5.(2023下·浙江·高三校联考)乙烯氢化的热化学方程式为C H(g) + H(g) = C H(g) H= akJ·mol-1,使
2 4 2 2 6
用不同含Au催化剂的反应历程如图所示,下列说法正确的是 △A.1 mol C H(g)的能量大于 1 mol C H(g)与1 mol H (g)具有的能量之和
2 6 2 4 2
B.该反应的焓变:△H = -129.6 kJ·mol-1
C.过渡态物质的稳定性:过渡态1大于过渡态2
D.相应的活化能:催化剂AuF小于催化剂AuPF
【微专题 化学反应历程图像分析】
1.(2023·山东济宁·统考三模)我国科学家以Bi为电极在酸性水溶液中可实现电催化还原 ,两种途
径的反应机理如下图所示,其中TS表示过渡态、数字表示微粒的相对总能量。
下列说法错误的是
A.HCOOH分解生成CO和 的反应为吸热反应
B.电催化还原 生成HCOOH的选择性高于生成CO的选择性
C.HCOOH是阴极产物
D.途径二的电极反应式为
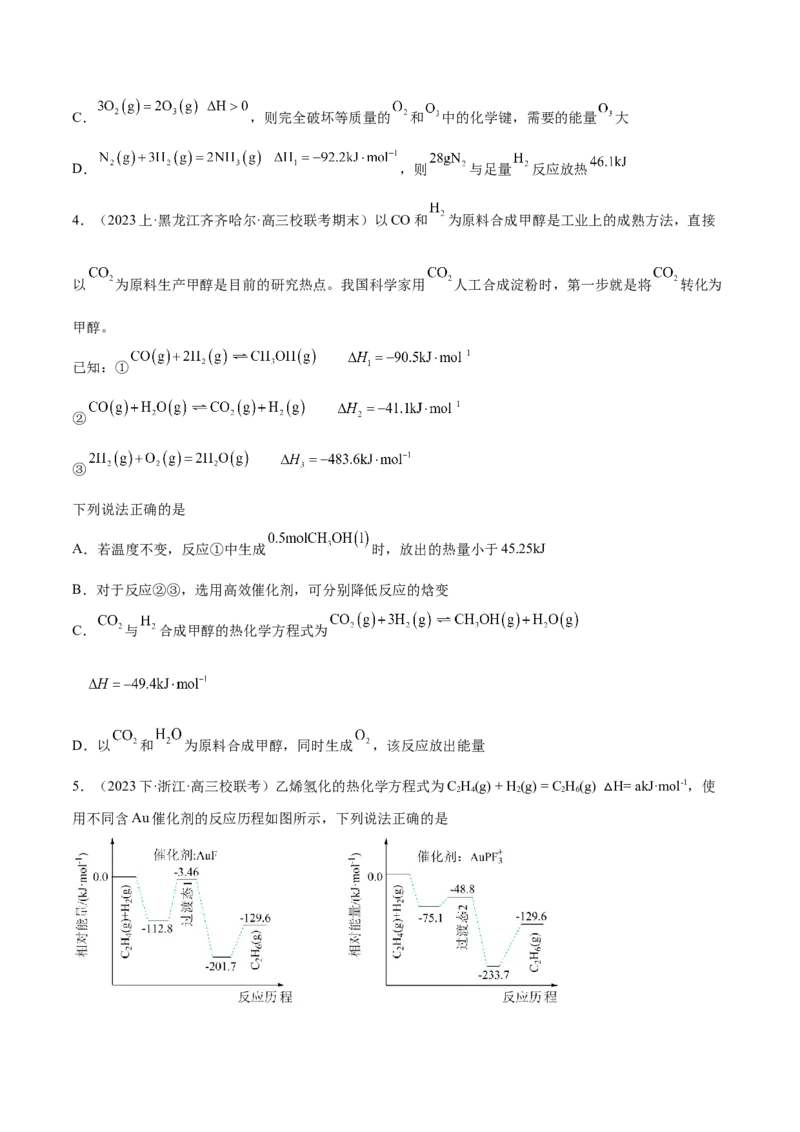
2.(2023·北京海淀·清华附中校考三模)汽车尾气中CO与NO转化的三段反应历程及各物质的相对能量
如图所示,其中TS代表过渡态,IM表示反应过程中的复杂中间产物,每段历程的反应物相对总能量定义
为0.下列说法不正确的是A.反应①决定尾气转化的快慢
B.反应①为吸热反应,反应②、③为放热反应
C.由上图可判断过渡态的相对能量:TS1>TS3>TS2
D.采用对反应③选择性高的催化剂可以避免尾气中出现
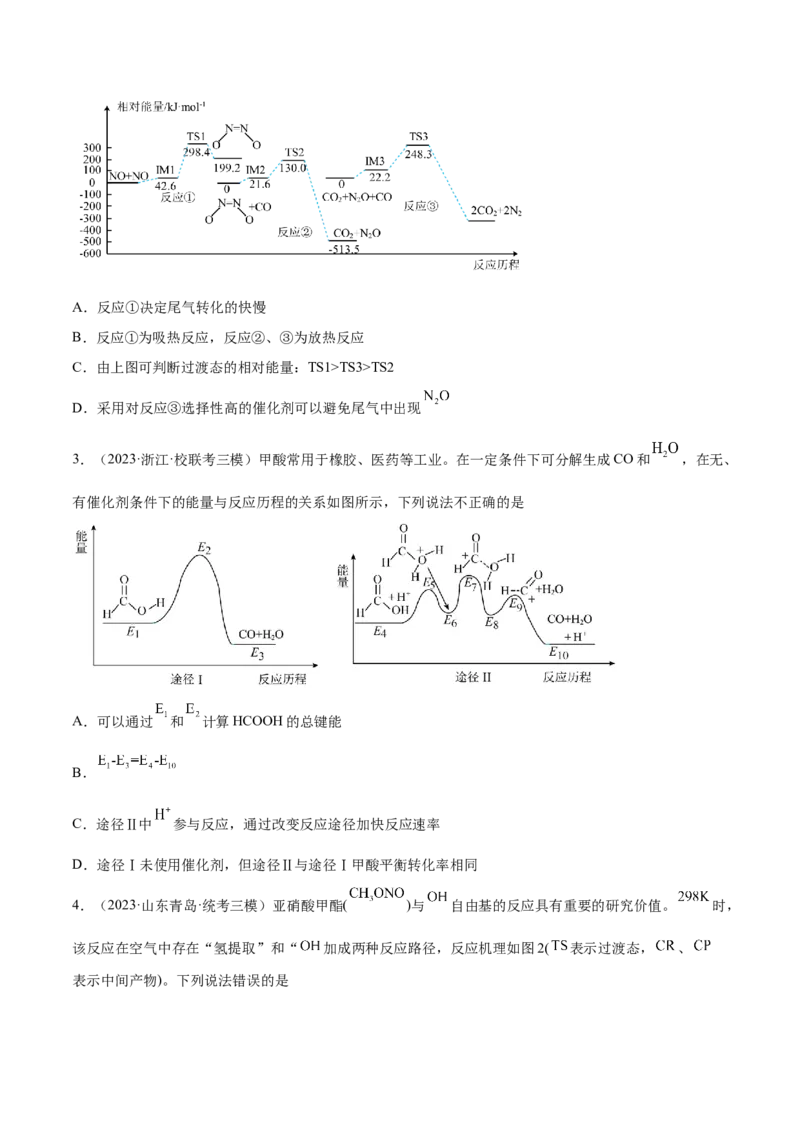
3.(2023·浙江·校联考三模)甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和 ,在无、
有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
A.可以通过 和 计算HCOOH的总键能
B.
C.途径Ⅱ中 参与反应,通过改变反应途径加快反应速率
D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同
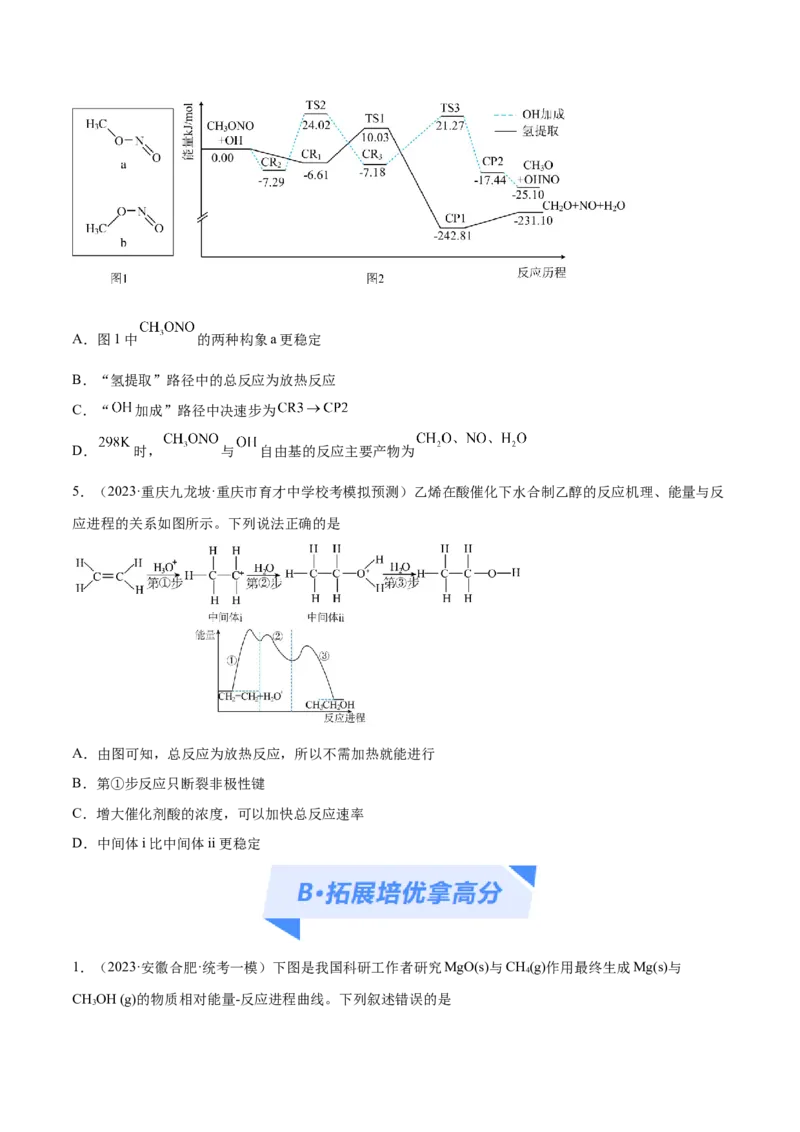
4.(2023·山东青岛·统考三模)亚硝酸甲酯( )与 自由基的反应具有重要的研究价值。 时,
该反应在空气中存在“氢提取”和“ 加成两种反应路径,反应机理如图2( 表示过渡态, 、
表示中间产物)。下列说法错误的是A.图1中 的两种构象a更稳定
B.“氢提取”路径中的总反应为放热反应
C.“ 加成”路径中决速步为
D. 时, 与 自由基的反应主要产物为
5.(2023·重庆九龙坡·重庆市育才中学校考模拟预测)乙烯在酸催化下水合制乙醇的反应机理、能量与反
应进程的关系如图所示。下列说法正确的是
A.由图可知,总反应为放热反应,所以不需加热就能进行
B.第①步反应只断裂非极性键
C.增大催化剂酸的浓度,可以加快总反应速率
D.中间体i比中间体ii更稳定
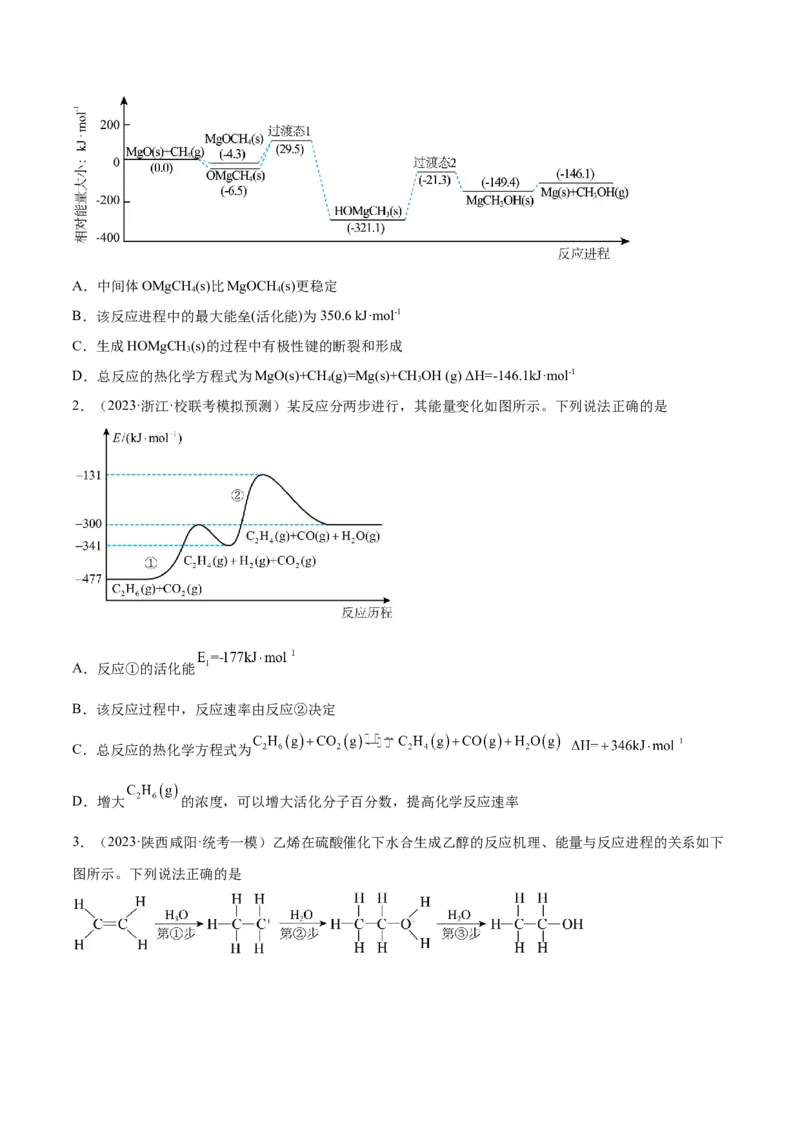
1.(2023·安徽合肥·统考一模)下图是我国科研工作者研究MgO(s)与CH(g)作用最终生成Mg(s)与
4
CHOH (g)的物质相对能量-反应进程曲线。下列叙述错误的是
3A.中间体OMgCH (s)比MgOCH (s)更稳定
4 4
B.该反应进程中的最大能垒(活化能)为350.6 kJ·mol-1
C.生成HOMgCH (s)的过程中有极性键的断裂和形成
3
D.总反应的热化学方程式为MgO(s)+CH (g)=Mg(s)+CH OH (g) ΔH=-146.1kJ·mol-1
4 3
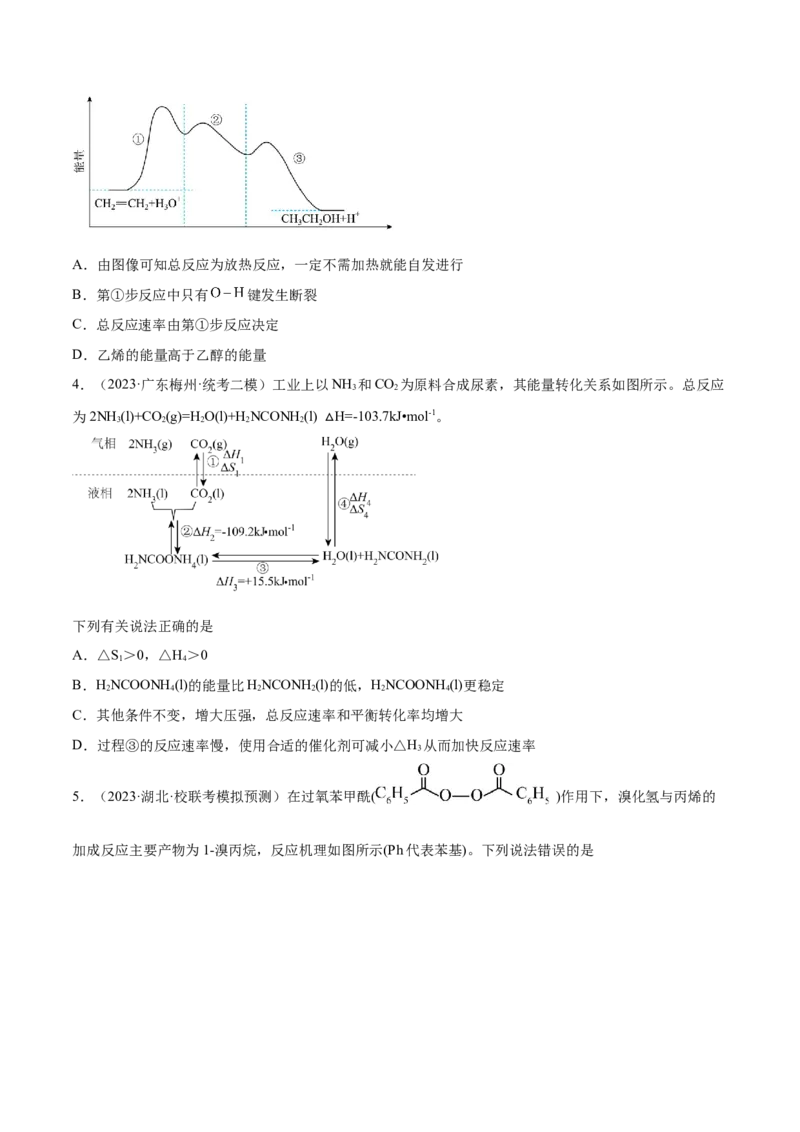
2.(2023·浙江·校联考模拟预测)某反应分两步进行,其能量变化如图所示。下列说法正确的是
A.反应①的活化能
B.该反应过程中,反应速率由反应②决定
C.总反应的热化学方程式为
D.增大 的浓度,可以增大活化分子百分数,提高化学反应速率
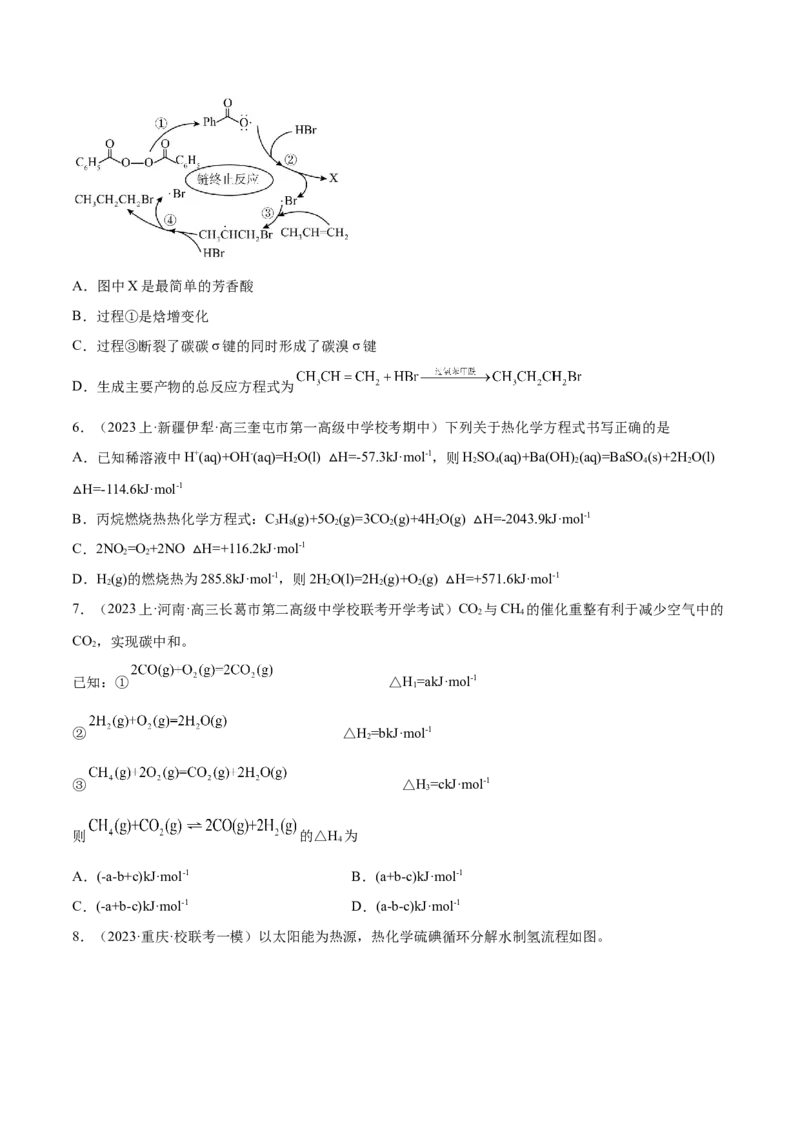
3.(2023·陕西咸阳·统考一模)乙烯在硫酸催化下水合生成乙醇的反应机理、能量与反应进程的关系如下
图所示。下列说法正确的是A.由图像可知总反应为放热反应,一定不需加热就能自发进行
B.第①步反应中只有 键发生断裂
C.总反应速率由第①步反应决定
D.乙烯的能量高于乙醇的能量
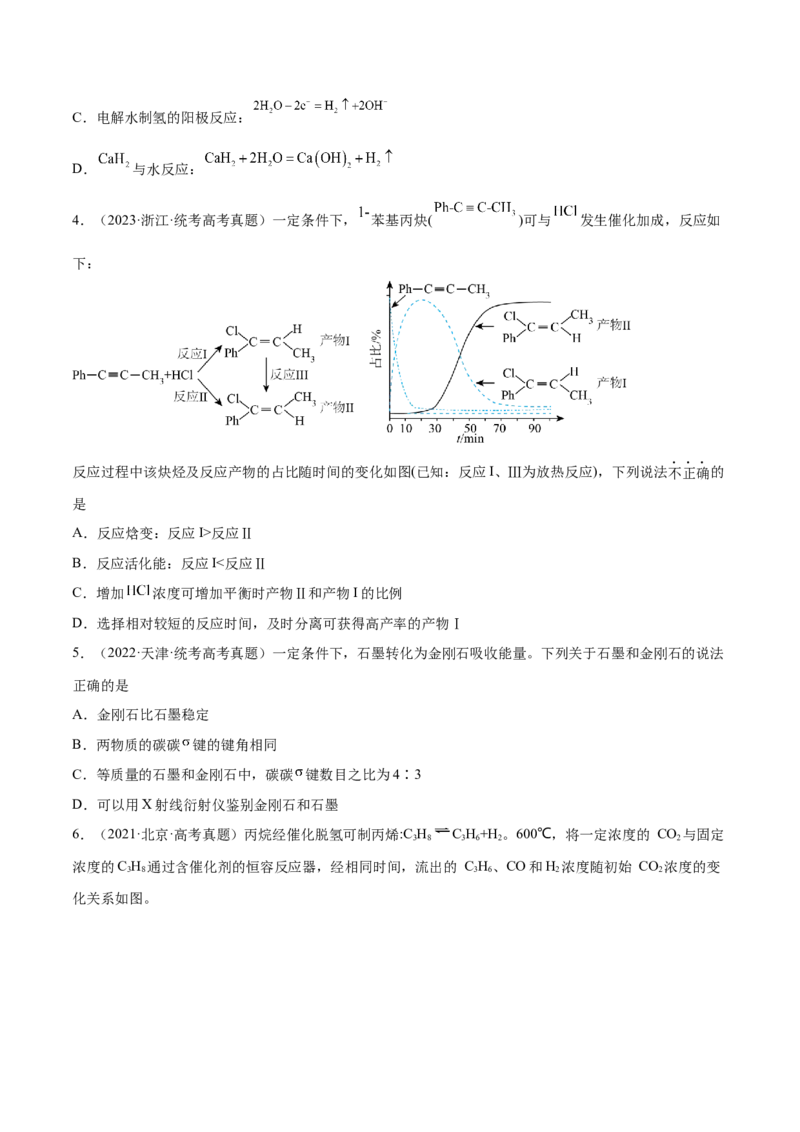
4.(2023·广东梅州·统考二模)工业上以NH 和CO 为原料合成尿素,其能量转化关系如图所示。总反应
3 2
为2NH (l)+CO (g)=HO(l)+HNCONH(l) H=-103.7kJ•mol-1。
3 2 2 2 2
△
下列有关说法正确的是
A.△S>0,△H>0
1 4
B.HNCOONH (l)的能量比HNCONH(l)的低,HNCOONH (l)更稳定
2 4 2 2 2 4
C.其他条件不变,增大压强,总反应速率和平衡转化率均增大
D.过程③的反应速率慢,使用合适的催化剂可减小△H 从而加快反应速率
3
5.(2023·湖北·校联考模拟预测)在过氧苯甲酰( )作用下,溴化氢与丙烯的
加成反应主要产物为1-溴丙烷,反应机理如图所示(Ph代表苯基)。下列说法错误的是A.图中X是最简单的芳香酸
B.过程①是焓增变化
C.过程③断裂了碳碳σ键的同时形成了碳溴σ键
D.生成主要产物的总反应方程式为
6.(2023上·新疆伊犁·高三奎屯市第一高级中学校考期中)下列关于热化学方程式书写正确的是
A.已知稀溶液中H+(aq)+OH-(aq)=H O(l) H=-57.3kJ·mol-1,则HSO (aq)+Ba(OH)(aq)=BaSO (s)+2HO(l)
2 2 4 2 4 2
H=-114.6kJ·mol-1 △
△B.丙烷燃烧热热化学方程式:C
3
H
8
(g)+5O
2
(g)=3CO
2
(g)+4H
2
O(g) H=-2043.9kJ·mol-1
C.2NO =O +2NO H=+116.2kJ·mol-1 △
2 2
D.H(g)的燃烧热为△285.8kJ·mol-1,则2HO(l)=2H(g)+O(g) H=+571.6kJ·mol-1
2 2 2 2
7.(2023上·河南·高三长葛市第二高级中学校联考开学考试)△CO 与CH 的催化重整有利于减少空气中的
2 4
CO,实现碳中和。
2
已知:① △H=akJ·mol-1
1
② △H=bkJ·mol-1
2
③ △H=ckJ·mol-1
3
则 的△H 为
4
A.(-a-b+c)kJ·mol-1 B.(a+b-c)kJ·mol-1
C.(-a+b-c)kJ·mol-1 D.(a-b-c)kJ·mol-1
8.(2023·重庆·校联考一模)以太阳能为热源,热化学硫碘循环分解水制氢流程如图。已知氢气燃烧热△H=-286kJ/mol,△H 为
3
A.+172kJ/mol B.+400kJ/mol C.+29kJ/mol D.+254kJ/mol
9.(2023·北京石景山·统考模拟预测)CO 催化加氢制CH 的反应为:
2 4
。催化剂上反应过程示意如图1所示。其他条件不变时,CO
2
的转化率和CH 的选择性(CO 转化为甲烷的量/ CO 转化的总量)随温度变化如图2所示。下列说法不正确
4 2 2
的是
A.催化剂改变了 中O—C—O键的键角
B.150℃到350℃时,基本没有发生副反应
C. 催化加氢制 是一个吸热反应
D.结合下列热化学方程式,可以通过盖斯定律计算 加氢制 的反应热
、
10.(2023·江苏南通·统考一模)工业上常用浓氯水检验输送氧气的营道是否泄漏,泄漏处有白烟生成,
工业合成氨的反应为 。对于工业合成氨的反应,下列说法正确的是
A.使用高效催化剂可减小△H
B.适当降温或加压,反应的平衡常数都增大
C.及时将体系中的 液化分离有利于平衡正向移动
D.用E表示键能,则:
1.(2021·重庆·统考高考真题)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物NO
2
和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热∆H = -283 kJ·mol-1,则
2NO(g)=2N (g) + O(g)的反应热∆H (kJ·mol-1)为
2 2 2
A.-152 B.-76 C.+76 D.+152
2.(2023·江苏·统考高考真题)二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是A.反应 的焓变
B. 的平衡选择性随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
3.(2023·江苏·统考高考真题)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是氢
元素的3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、
、 、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法
制氢反应中, 与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶炼、
新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国科学
家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
A.水煤气法制氢:
B. 催化加氢生成 的反应:C.电解水制氢的阳极反应:
D. 与水反应:
4.(2023·浙江·统考高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如
下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
5.(2022·天津·统考高考真题)一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法
正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
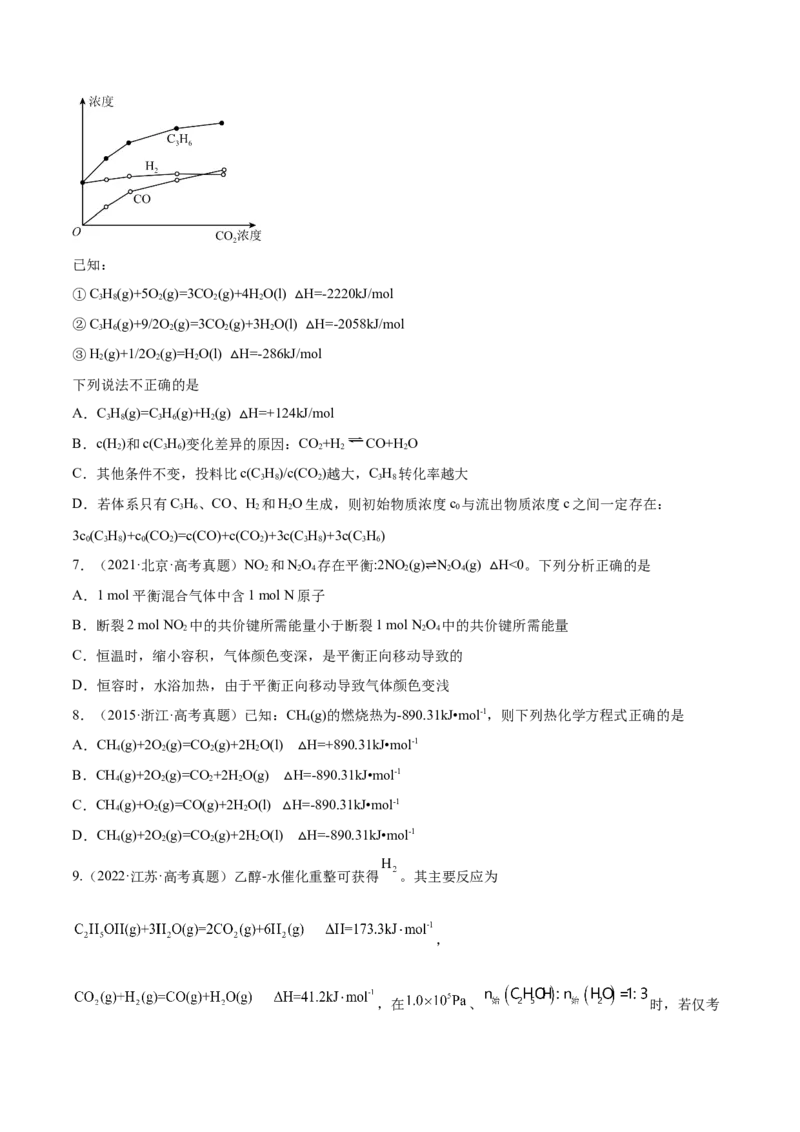
6.(2021·北京·高考真题)丙烷经催化脱氢可制丙烯:C H C H+H 。600℃,将一定浓度的 CO 与固定
3 8 3 6 2 2
浓度的C H 通过含催化剂的恒容反应器,经相同时间,流出的 C H、CO和H 浓度随初始 CO 浓度的变
3 8 3 6 2 2
化关系如图。已知:
①C H(g)+5O(g)=3CO (g)+4HO(l) H=-2220kJ/mol
3 8 2 2 2
②C H(g)+9/2O (g)=3CO (g)+3HO(l)△ H=-2058kJ/mol
3 6 2 2 2
③H(g)+1/2O (g)=HO(l) H=-286kJ/m△ol
2 2 2
下列说法不正确的是 △
A.C H(g)=C H(g)+H(g) H=+124kJ/mol
3 8 3 6 2
B.c(H)和c(C H)变化差异△的原因:CO+H CO+HO
2 3 6 2 2 2
C.其他条件不变,投料比c(C H)/c(CO )越大,C H 转化率越大
3 8 2 3 8
D.若体系只有C H、CO、H 和HO生成,则初始物质浓度c 与流出物质浓度c之间一定存在:
3 6 2 2 0
3c(C H)+c (CO)=c(CO)+c(CO )+3c(C H)+3c(C H)
0 3 8 0 2 2 3 8 3 6
7.(2021·北京·高考真题)NO 和NO 存在平衡:2NO(g) NO(g) H<0。下列分析正确的是
2 2 4 2 2 4
A.1 mol平衡混合气体中含1 mol N原子 ⇌ △
B.断裂2 mol NO 中的共价键所需能量小于断裂1 mol N O 中的共价键所需能量
2 2 4
C.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的
D.恒容时,水浴加热,由于平衡正向移动导致气体颜色变浅
8.(2015·浙江·高考真题)已知:CH(g)的燃烧热为-890.31kJ•mol-1,则下列热化学方程式正确的是
4
A.CH(g)+2O(g)=CO (g)+2HO(l) H=+890.31kJ•mol-1
4 2 2 2
B.CH(g)+2O(g)=CO +2H O(g) H△=-890.31kJ•mol-1
4 2 2 2
C.CH(g)+O(g)=CO(g)+2HO(l) △H=-890.31kJ•mol-1
4 2 2
D.CH(g)+2O(g)=CO (g)+2HO(l)△ H=-890.31kJ•mol-1
4 2 2 2
△
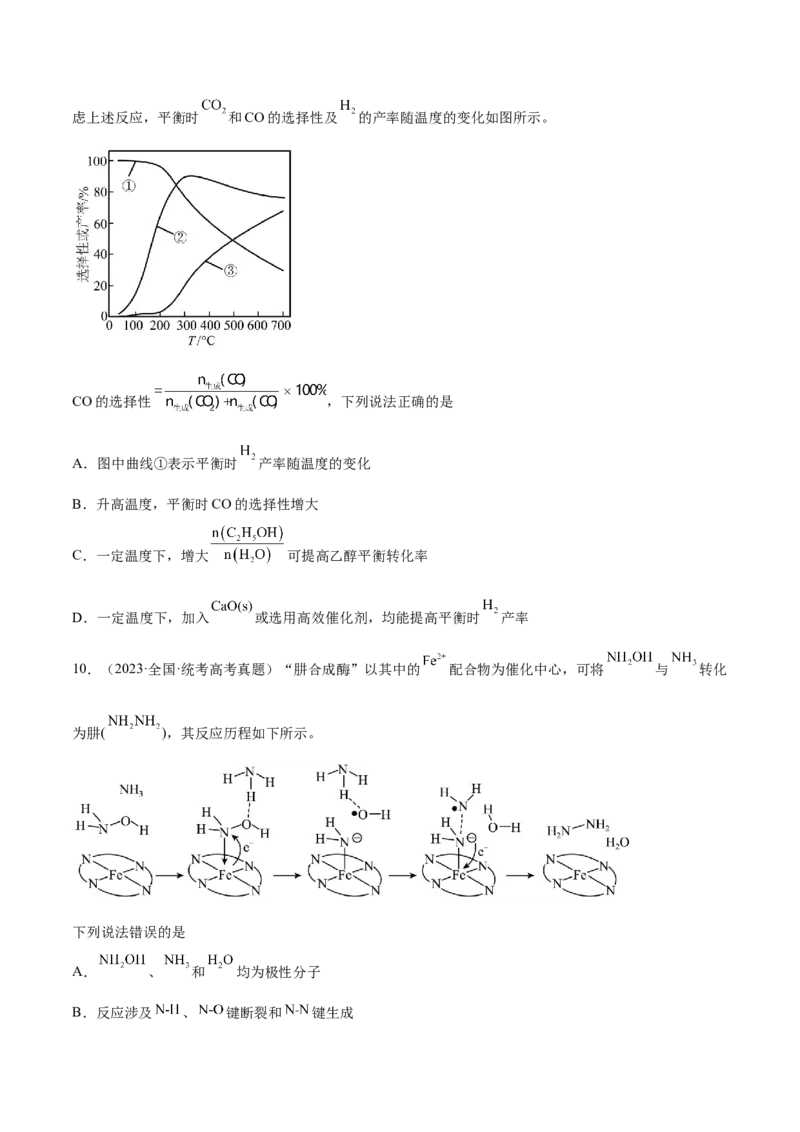
9.(2022·江苏·高考真题)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
10.(2023·全国·统考高考真题)“肼合成酶”以其中的 配合物为催化中心,可将 与 转化
为肼( ),其反应历程如下所示。
下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得