文档内容
专题 12 大题突破——物质结构与性质综合
目录
01考情透视·目标导航............................................................................................................................
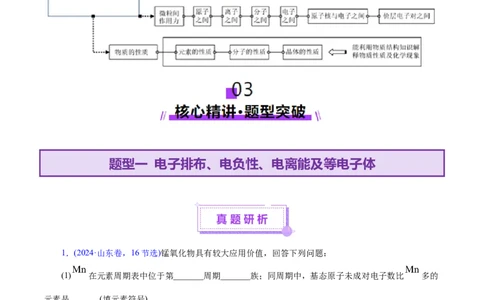
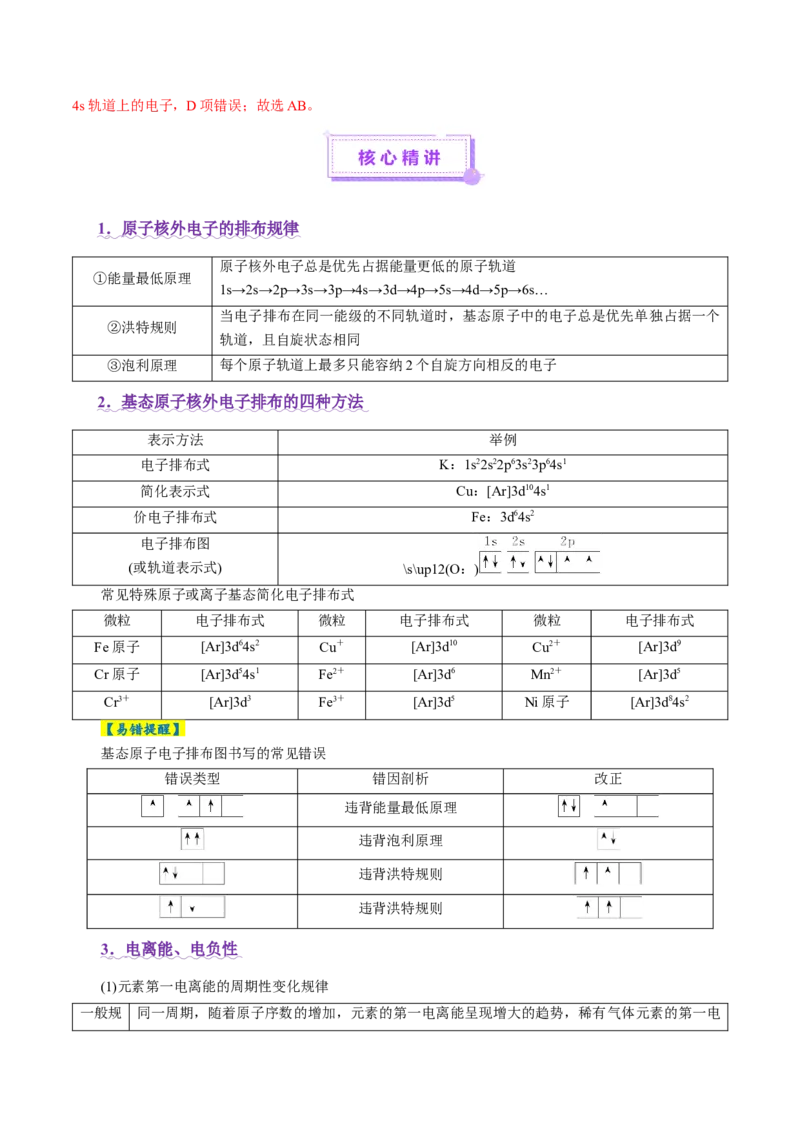
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 电子排布、电负性、电离能及等电子体.............................................................................
【真题研析】.............................................................................
【核心精讲】.............................................................................
1.原子核外电子的排布规律................................................................
2.基态原子核外电子排布的四种方法........................................................
3.电离能、电负性........................................................................
4.常见等电子体..........................................................................
【命题预测】.............................................................................
考向1 核外电子的排布....................................................................
考向2电离能、电负性.....................................................................
题型二 立体构型、杂化类型、晶体类型的判断及原因解释.....................................................
【真题研析】.............................................................................
【核心精讲】.............................................................................
1.中心原子杂化类型和分子空间构型的相互判断..............................................
2.常见结构与性质问题的原因解释..........................................................
【命题预测】.............................................................................
题型三 晶体化学式及粒子数的确定.............................................................................................
【真题研析】.............................................................................
【核心精讲】.............................................................................
1.晶胞中微粒数的计算方法——均摊法......................................................
2.晶胞中粒子配位数的计算................................................................
【命题预测】.............................................................................
考向1晶体化学式及粒子数的确定...........................................................
考向2配位数的计算.......................................................................
题型四 晶胞参数的计算.................................................................................................................【真题研析】.............................................................................
【核心精讲】.............................................................................
1.晶胞参数..............................................................................
2.宏观晶体密度与微观晶胞参数的关系......................................................
3.空间利用率............................................................................
【命题预测】.............................................................................
考点要求 考题统计 考情分析
2024·山东卷,16(1);2024·北京卷,
15(1);2024·浙江1月卷,17(2);2024·浙
江6月卷,17(2);2023全国乙卷35(1) 随着改革的深入,《物质结构与性
题,15分;2023浙江1月选考17(2)题, 质》已列入各省市必考题,题目一
般是以元素推断或某主族元素为背
原子结构 10分;2023北京卷,15(1)(2)题;2022全
景,以“拼盘”形式呈现,各小题
与性质 国甲卷,35(1)(2)题;2022河北卷,17(1)
之间相对独立,主要考查原子结构
(2);2022湖南卷,18(1)(2);2022全国乙
与性质、分子结构与性质、晶体结
卷,35(1);2022重庆卷,18(1)(2);2022
构与性质。试题背景新颖,注重体
北京卷,15(1)(2)(3);2022海南卷,19(1)
现科学新成果或新发现,更注重
(2);2022广东卷,20(1)题;
“结构决定性质”思想的树立,考
查空间想象能力。在原子结构部分
2024·山东卷,16(3);2024·北京卷,
主要命题点有电子排布式或排布图
15(2);2024·浙江1月卷,17(3);2024·浙
的书写,电离能、电负性大小的比
江6月卷,17(3);2024· 海南卷,19(1)(2)
较与判断;在分子结构部分主要命
(3)(4)(5);2023浙江6月选考,17(2);
题点有化学键类型的判断,分子构
分子结构 2023全国乙卷,35(2);2023山东卷,
型的判断,中心原子杂化方式的判
与性质 16(2);2023浙江1月选考,17(1);2023
断;在晶体结构部分主要命题点有
北京卷,15(3);2022河北卷,17(3);
晶体类型的判断,晶体结构的计算
2022湖南卷,18(3);2022广东卷,20(2) 等。预测2025年试题背景新颖,注
(4)(5);2022全国乙卷,35(2);2022全国 重体现科学新成果或新发现,更注
甲卷,35(3);2022海南卷,19(3); 重“结构决定性质”思想的树立,
考查空间想象能力。从题型上看,
2024·山东卷,16(2);2024·福建卷,
一般给出一定的知识背景,然后设
11(5);2024·北京卷,15(3);2024·浙江1
置3~4个小问题,每一个小题考查
月卷,17(1);2024·浙江6月卷,17(1);
相应的知识要点仍是今后命题的基
2024·广西卷,15(6);2024· 贵州卷, 本模式。在原子结构部分主要命题
16(5);2024·甘肃卷,15(5);2024· 海南 点有电子排布式或排布图的书写,
卷,19(6);2024·广东卷,18(6);2023全 电离能、电负性大小的比较与判
晶体结构 国乙卷,35(3);2023全国甲卷,35;2023 断;在分子结构部分主要命题点有
与性质 浙江1月选考,17(3);2023浙江6月选 化学键类型的判断,分子构型的判
考,17(3);2023山东卷,16(1)(3);2023 断,中心原子杂化方式的判断;在
北京卷,15(5)(6);2022全国甲卷,3(5); 晶体结构部分主要命题点有晶体类
2022全国乙卷,35(3)(4);2022重庆卷, 型的判断,晶体结构的计算等。
18(3)(4);2022北京卷,15(4)(5);2022湖
南卷,18(4)(5)(6);2022广东卷,20(6);
2022江苏卷,17(2);题型一 电子排布、电负性、电离能及等电子体
1.(2024·山东卷,16节选)锰氧化物具有较大应用价值,回答下列问题:
(1) 在元素周期表中位于第_______周期_______族;同周期中,基态原子未成对电子数比 多的
元素是_______(填元素符号)。
【答案】(1)①四 ②ⅦB ③Cr
【解析】(1)Mn的原子序数为25,位于元素周期表第四周期Ⅶ B族;基态Mn的电子排布式为:
[Ar]3d54s2,未成对电子数有5个,同周期中,基态原子未成对电子数比Mn多的元素是Cr,基态Cr的电
子排布式为[Ar]3d54s1,有6个未成对电子。
2.(2024·北京卷,15节选)锡(Sn)是现代“五金”之一,广泛应用于合金、半导体工业等。
(1) Sn位于元素周期表的第5周期第IVA族。将Sn的基态原子最外层轨道表示式补充完整: 。【答案】(1)
【解析】(1)Sn位于元素周期表的第5周期ⅣA族,基态Sn原子的最外层电子排布式为5s25p2,Sn的
基态原子最外层轨道表示式为 。
3.(2024·浙江1月卷,17节选)氮和氧是构建化合物的常见元素。
(2)下列说法正确的是_______。
A.电负性:B>N>O B.离子半径:P3-<S2-<Cl-
C.第一电离能:Ge<Se<As D.基态 2+的简化电子排布式:[Ar]3d4
【答案】(2)CD
(2)A项,同一周期,从左到右,电负性依次增强,故顺序为O>N>B,A错误;B项,核外电子排布
相同,核电荷数越大,半径越小,故顺序为P3->S2->Cl-,B错误;C项,同一周期,从左到右,电离能增
大的趋势,VA族和ⅥA族相反,故顺序为Ge<Se<As,C正确;D项,基态Cr的简化电子排布式:
[Ar]3d54s1,Cr2+的简化电子排布式为[Ar]3d4,D正确;故选CD。
4.(2024·浙江6月卷,17节选)氧是构建化合物的重要元素。请回答:
(2)下列有关单核微粒的描述正确的是_______。
A.Ar的基态原子电子排布方式只有一种
B.Na的第二电离能 的第一电离能
C.Ge的基态原子简化电子排布式为[Ar]4s24p2
D.Fe原子变成Fe+,优先失去 轨道上的电子
【答案】(2)AB
【解析】(2)A项,根据原子核外电子排布规律,基态Ar原子的电子排布方式只有1s22s22p63s23p6一种,
A项正确;B项,Na的第二电离能指气态基态Na+失去一个电子转化为气态基态正离子所需的最低能量,
Na+和Ne具有相同的电子层结构,Na+的核电荷数大于Ne,Na+的原子核对外层电子的引力大于Ne的,故
Na的第二电离能>Ne的第一电离能,B项正确;C项,Ge的原子序数为32,基态Ge原子的简化电子排
布式为[Ar]3d104s24p2,C项错误;D项,基态Fe原子的价电子排布式为3d64s2,Fe原子变成Fe+,优先失去4s轨道上的电子,D项错误;故选AB。
1 . 原子核外电子的排布规律
原子核外电子总是优先占据能量更低的原子轨道
①能量最低原理
1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s…
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个
②洪特规则
轨道,且自旋状态相同
③泡利原理 每个原子轨道上最多只能容纳2个自旋方向相反的电子
2 . 基态原子核外电子排布的四种方法
表示方法 举例
电子排布式 K:1s22s22p63s23p64s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图
(或轨道表示式) \s\up12(O:)
常见特殊原子或离子基态简化电子排布式
微粒 电子排布式 微粒 电子排布式 微粒 电子排布式
Fe原子 [Ar]3d64s2 Cu+ [Ar]3d10 Cu2+ [Ar]3d9
Cr原子 [Ar]3d54s1 Fe2+ [Ar]3d6 Mn2+ [Ar]3d5
Cr3+ [Ar]3d3 Fe3+ [Ar]3d5 Ni原子 [Ar]3d84s2
【易错提醒】
基态原子电子排布图书写的常见错误
错误类型 错因剖析 改正
违背能量最低原理
违背泡利原理
违背洪特规则
违背洪特规则
3 . 电离能、电负性
(1)元素第一电离能的周期性变化规律
一般规 同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的第一电离能最大,碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元素的第一电离
律
能逐渐减小
第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布在能量
特殊情
相等的轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、d10、f14)结构时,原子的能量较
况
低,该元素具有较大的第一电离能
(2)电离能、电负性大小判断
规律 在周期表中,电离能、电负性从左到右逐渐增大,从上往下逐渐减小
同周期主族元素,第ⅡA族(ns2)全充满、第ⅤA族(np3)半充满,比较稳定,所以其第一电离能
特性
大于同周期相邻的第ⅢA族和第ⅥA族元素
常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比较:①HClO中Cl为+
方法 1价、O为-2价,可知O的电负性大于Cl;②Al O 是离子化合物、AlCl 是共价化合物,可
2 3 3
知O的电负性大于Cl
4 .常见等电子体
粒子 通式 价电子总数 立体构型
CO、SCN-、NO、N、NO、COS、CS AX 16e- 直线形
2 2 2 2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N、C AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
考向 1 核外电子排布
1.(2025·北京市海淀区高三模拟,节选)锡(Sn)是现代“五金”之一,广泛应用于合金、半导体工业等。
(1)Sn位于元素周期表的第5周期第ⅣA族,属于 区。
【答案】(1)p
【解析】(1)Sn位于元素周期表的第五周期第ⅣA族,其价电子排布为5s25p2,属于p区元素。
2.(2025·浙江省金华第一中学高三选考模拟,17节选)铑(Rh)和铱(Ir)形成的材料在生产生活中应用广
泛,如铑(Rh)膦络合物常用作催化剂,二氧化铱(IrO )可用作电生理学研究中的微电极。请回答:
2
(1)铱(Ir)的原子序数为77,其价电子排布式为 ,位于元素周期表的 区。
【答案】(1) 5d76s2 d
【解析】(1)铱(Ir)的原子序数为77,根据稀有气体原子序数依次为2、10、18、36、54、86、118,可推出铱(Ir)的其价电子排布式为5d76s2,其属于过渡区金属元素,位于元素周期表d区。
3.(2025·广东省广东实验中学高三模拟,节选)锂电池的电解液是目前研究的热点。
(1)锂电池的电解液可采用溶有LiPF 的碳酸酯类有机溶液。
6
①基态Li+的电子云轮廓图的形状为 。
②基态 原子的价层电子轨道表示式为 。
【答案】(1)球形
【解析】(1)①基态Li+的核外电子排布式为1s2,电子云轮廓图的形状为球形。②元素P是15号元素,
最外层电子数为5,P元素位于周期表P区,基态P原子的价层电子轨道表示式为 。
4.(2025·江西省九校联考高三期中,节选)硼及其化合物在材料制造、有机合成等方面用途非常广泛,
其在化合物中常显+3价。回答下列问题:
(1)有机中常用BCl 做催化剂。形成BCl 时,基态B原子价电子层上的电子先激发再杂化,激发过程
3 3
形成的原子光谱为 光谱(填“吸收”或“发射”),激发后B 原子的价电子轨道表示式最可能为
(填标号)。
【答案】(1)吸收 C
【解析】(1)B的价层电子排布式为2s22p1,形成BCl 时,基态B原子2s上的电子先激发到2p能级上
3
再杂化,电子由2s跃迁到2p能级上形成的原子光谱为吸收光谱,且激发后B 原子的价电子排布式为
2s12p2,价电子轨道表示式最可能为 ,故答案为C。
5.(2025·辽宁省沈阳市高中联合体高三模拟,节选)第ⅢA族元素及其化合物应用广泛。回答下列问
题:
(1)基态Ga原子的价层电子排布式为 。
(2)下列不同状态的硼中,失去一个电子需要吸收能量最多的是_______(填标号)。
A. B.C. D.
【答案】(1)4s24p1 (2)C
【解析】(1)Ga为31号元素,基态Ga原子的价层电子排布式为:4s24p1;(2)B的原子序数是5,基态
B原子电子排布式1s22s22p1,其失去第二个电子更难,吸收能量更大, 为2s填满的较稳定结构,
失去电子较 更难,故选C。
6.(2025·湖南省多校高三联考,节选)氮气的活化与转化是现代化学领域极具挑战的课题之一。
(1)基态15N核外有 个运动状态不同的电子;某学生将基态硅原子核外电子轨道表示式画为
,该轨道表示式违反了 。
(2)Li原子的核外电子由 状态变化为 状态所得原
子光谱为 (填“发射”或“吸收”)光谱。
(3)从原子结构角度解释电负性Si<Cl的原因: 。
【答案】(1) 7 洪特规则 (2)吸收
(3)Cl的原子半径小于Si的,且Cl元素的核电荷数大于Si元素的,Cl原子对键合电子吸引能力更强,
电负性更大
【解析】(1)基态15N核外电子排布式为1s22s22p3,有7个电子,每个电子的运动状态都不同,则基态
15N核外有7个运动状态不同的电子;某学生将基态硅原子核外电子轨道表示式画为
,洪特规则是指在能量相等的轨道上,电子尽可能分占在
不同的轨道上,并且自旋方向相同,该轨道表示式违反了洪特规则。(2)Li原子的核外电子由
状态变化为 状态,电子由低能级跃迁到高能级,需
要吸收能量,所得原子光谱为吸收光谱。(3)Cl的原子半径小于Si的,且Cl元素的核电荷数大于Si元素的,Cl原子对键合电子吸引能力更强,电负性更大。
7.(2025·上海市复旦附中分校高三期中,节选)(1)基态铁原子核外电子排布式为 ,其核外电子
的空间运动状态有 种,价层电子的运动状态有 种。
(2)基态Fe3+较基态Fe2+稳定的原因是 。
(7)Cd为第48号元素,Cd在元素周期表中的位置为 ,电子占据的最高能级的原子轨道的电子
云轮廓图的形状为 。
【答案】(1)[Ar]3d64s2 15 8
(2)基态Fe2+的价层电子排布为3d6,基态Fe3+的价层电子排布为3d5,基态Fe3+的3d轨道为半充满状态,
比较稳定
(7)第五周期ⅡB族 球形
【解析】(1)铁为26号元素,基态铁原子的核外电子排布式为:1s22s22p63s23p63d64s2或[Ar]3d64s2;核外
电子的空间运动状态数等于原子轨道数,则基态铁原子核外电子的空间运动状态有1+1+3+1+3+5+1=15种;
价层电子排布式为3d64s2,有8个电子,每个电子的运动状态均不同,则价层电子的运动状态有8种;(2)
基态Fe3+较基态Fe2+稳定的原因是:基态Fe2+的价层电子排布为3d6,基态Fe3+的价层电子排布为3d5,基
态Fe3+的3d轨道为半充满状态,比较稳定;(7)Cd为第48号元素,Cd在元素周期表中位于第五周期第12
列,即第五周期ⅡB族,电子占据的最高能级为5s,原子轨道的电子云轮廓图为球形。
考向 2 电负性、电离能
8.(2025·海南省一模,节选)(4)含铜废液可以利用双缩脲[HN(CONH )]进行萃取,实现铜离子的富集、
2 2
进行回收。HN(CONH ) 中除氢外的非金属元素第一电离能由大到小的顺序是 (用元素符号表示)。
2 2
【答案】(4)N>O>C
【解析】(4)HN(CONH ) 除H外,所含元素为C、N、O三种,同周期元素从左到右第一电离能呈逐渐
2 2
增大趋势,根据N原子2p轨道为半满状态,第一电离能大于同周期相邻元素,电离能递变规律为N>O>
C。
9.(2025·山东省济南市高三联考,节选)镍及其化合物应用广泛。回答下列问题:
(1)基态Ni原子的价电子排布式为 。已知第四电离能:I(Fe)>I(Ni),从原子结构的角度
4 4
分析原因 。
【答案】(1)3d84s2 Fe失去的是半满状态3d5上的一个电子
【解析】(1)Ni的原子序数为28,价层电子排布式为:3d84s2;Ni失去3个电子后价电子变为3d7,故
再失去的是3d7上的一个电子,Fe失去3个电子后是3d5,再失去的是3d5上的一个电子,而3d5是半满结构,
较稳定,故I(Fe)>I(Ni)。
4 4
10.[真题改编] (1)(2021·全国乙卷,35节选)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产
和国防建设中有着广泛应用。对于基态Cr原子,下列叙述正确的是( )。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)(2020·全国Ⅰ卷,35节选)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方
面的卓越贡献而获得 2019 年诺贝尔化学奖。Li 及其周期表中相邻元素的第一电离能(I)如表所示。
1
I(Li)>I(Na) , 原 因 是 ______________________________ 。 I(Be)>I(B)>I(Li) , 原 因 是
1 1 1 1 1
_____________________。
I/(kJ·mol-1)
1
Li Be B
520 900 801
Na Mg Al
496 738 578
(3)(2020·全国Ⅱ卷,35节选)钙钛矿(CaTiO )型化合物是一类可用于生产太阳能电池、传感器、固体电
3
阻器等的功能材料。CaTiO 的组成元素的电负性大小顺序是________________。
3
【答案】(1)AC
(2)Na与Li同族,Na的电子层数多,原子半径大,易失电子 Li、Be、B同周期,核电荷数依次增加,
Be为1s22s2全满稳定结构,第一电离能最大,与Li相比,B的核电荷数大,原子半径小,较难失去电子,
故第一电离能较大
(3)O>Ti>Ca
【解析】(1)电负性为原子对键合电子的吸引力,同周期除0族外,原子序数越大电负性越强,钾与铬
位于同周期,铬原子序数大于钾,故铬的电负性比钾高,原子对键合电子的吸引力比钾大,C项正确。(2)
同主族元素,从上至下,原子半径逐渐增大,第一电离能逐渐减小,所以I(Li)>I(Na);同周期元素,从左
1 1
至右,第一电离能呈现增大的趋势,但由于第ⅡA族元素基态原子s能级轨道处于全充满的状态,能量更
低更稳定,所以其第一电离能大于同一周期的第ⅢA族元素,因此I(Be)>I(B)>I(Li)。(3)CaTiO 晶体中含
1 1 1 3
有Ca、Ti、O三种元素,Ca、Ti是同为第四周期的金属元素,Ca在Ti的左边,根据同一周期元素的电负
性从左往右依次增大,故电负性Ti>Ca,O为非金属元素,故其电负性最强,故三者电负性由大到小的顺
序是O>Ti>Ca。
11.(2025·上海市复旦附中分校高三期中,节选)(3)在NH HPO 中的N、P、O三种元素的电负性由大
4 2 4
到小的顺序是 ;N的第一电离能大于O,原因是 。
(6)已知Ga与B同主族,基态Ga原子的原子结构示意图为 。Ga失去电子的逐级电离能(单位:
kJ·mol−1)的数值依次为577、1984.5、2961.8、6192.由此可推知镓的主要化合价为 和+3。
【答案】(3) O>N>P 基态N原子的价层电子排布为2s22p3,2p轨道为半充满状态,比较稳定,
不易失电子;而基态O原子的价层电子排布为2s22p4,2p轨道若失去一个电子,则比较稳定的半充满状态,
因此O更容易失去1个电子。因此N的第一电离能大于O(6) +1
【解析】(3)同一周期从左到右,元素电负性依次增大,即电负性:O>N;同一主族从上到下,元素电
负性依次减弱,即电负性:N>P,则在NH HPO 中的N、P、O三种元素的电负性由大到小的顺序是:O
4 2 4
>N>P;同一周期元素从左到右,第一电离能呈增大趋势,但第ⅡA、第ⅤA族的第一电离能大于其右边
相邻元素的第一电离能,即N的第一电离能大于O,其原因是:基态N原子的价层电子排布为2s22p3,2p
轨道为半充满状态,比较稳定,不易失电子;而基态O原子的价层电子排布为2s22p4,2p轨道若失去一个
电子,则比较稳定的半充满状态,因此O更容易失去1个电子。因此N的第一电离能大于O;(6)已知Ga
与B同主族,其原子序数为31,则基态Ga原子的原子结构示意图为 。最外层有3个电
子,又知Ga失去电子的逐级电离能(单位:kJ·mol−1)的数值依次为577、1984.5、2961.8、6192,第一电离
能和第二电离能之差为1407.5 kJ·mol−1,第二电离能和第三电离能之差为977.3 kJ·mol−1,第三电离能和第
四电离能之差为3230.2 kJ·mol−1,说明失去第2个电子和第4个电子比较困难,由此可推知镓的主要化合价
为+1和+3。
12.(2025·浙江省天域全国名校协作体高三联考,17节选)含铜铟镓硒元素的化合物作为太阳能吸收层
薄膜材料,可用于生产第三代太阳能电池。已知镓(Ga)、铟(In)、铊(Tl)是原子序数依次增大的ⅢA族元素,
请回答:
(1)三乙基铝Al(C H) 常温下为无色液体,是烯烃定向聚合的催化剂,可与醚、胺类等形成相当稳定的
2 5 2
配合物。
①基态Al原子的核外电子空间运动状态有 种。三乙基铝的晶体类型为 。
②三乙基铝能与乙醚形成配合物A[(C H)AlO(C H)]。比较键角 的大小:三乙基铝
2 5 3 2 5 2
配合物A(填“>”“<”或“=”)。
③三乙基铝还能与N,N-二甲基环己胺( )形成配合物B,已知A的稳定性小于B,解释原因:
。(2)下列说法不正确的是___________。
A.第一电离能:Se>Ga
B.金属Ga的熔点比Al低
C.Al(OH) 具有两性,故Tl(OH) 具有两性
3 3
D.基态In原子简化的电子排布式为 [Kr] 5s25p1
【答案】(1) 7 分子晶体 > N元素的电负性小于O,更易给出孤电子对
(2)CD (3) InCuSe 6
2
【解析】(1)①基态Al原子的核外电子排布式为1s22s22p63s23p1,s为1种,2p有3种,3p有1种,空间
运动状态有7种,三乙基铝常温下为无色液体,所以推测晶体类型为分子晶体;②三乙基铝能与乙醚形成
配合物A[(C H)AlO(C H)],氧原子提供孤对电子,对C-Al斥力增大,所以键角 的大小:三
2 5 3 2 5 2
乙基铝>配合物A;③三乙基铝还能与N,N-二甲基环己胺( )形成配合物B,已知A的稳定性
小于B,是因为N元素的电负性小于O,更易给出孤电子对;(2)A项,同一周期第一电离能从左至右呈增
大趋势,所以第一电离能:Se>Ga,正确;B项,Ga、Al为同主族的金属晶体,同主族从上到下金属晶体
的金属键逐渐减弱,熔点降低,金属Ga的熔点为29.93℃,比Al低,正确;C项,同主族从上到下最高价
氧化物对应水化物的碱性逐渐增强,Al(OH) 具有两性,Tl(OH) 不具有两性,错误;D项,基态In原子简
3 3
化的电子排布式为[Kr]4d105s25p1,错误;故选CD。
题型二 立体构型、杂化类型、晶体类型的判断及原因解释
1.(2024·山东卷,16节选)锰氧化物具有较大应用价值,回答下列问题:
(3)[BMIM]+BF- (见图)是MnO 晶型转变的诱导剂。BF-的空间构型为_______;[BMIM]+中咪唑环存
4 x 4
在 大 键,则N原子采取的轨道杂化方式为_______。
(4) MnO 可作 转化为FDCA的催化剂(见下图)。FDCA的熔点远大于HMF,除相对分子质量存
x在差异外,另一重要原因是_______。
【答案】(3)①正四面体形 ②sp2
(4)FDCA形成的分子间氢键更多
【解析】(3)BF -中B形成4个σ键(其中有1个配位键),为sp3杂化,空间构型为正四面体形;咪唑环
4
存在 大 键,N原子形成3个σ键,杂化方式为sp2;(4)由HMF和FDCA的结构可知,HMF和FDCA
均能形成分子间氢键,但FDCA形成的分子间氢键更多,使得FDCA的熔点远大于HMF。
2.(2024·北京卷,15节选)锡(Sn)是现代“五金”之一,广泛应用于合金、半导体工业等。
(2) SnCl 和SnCl 是锡的常见氯化物,SnCl 可被氧化得到。
2 4 2
①SnCl 分子的 模型名称是 。
2
②SnCl 的Sn-Cl键是由锡的 轨道与氯的 轨道重叠形成σ键。
4
【答案】 (2)平面三角形 sp3杂化
【解析】(2)①SnCl 中Sn的价层电子对数为2+ ×(4-2×1)=3,故SnCl 分子的VSEPR模型名称是平面
2 2
三角形;②SnCl 中Sn的价层电子对数为4+ ×(4-4×1)=4,有4个σ键、无孤电子对,故Sn采取sp3杂化,
4
则SnCl 的Sn—Cl键是由锡的sp3杂化轨道与氯的3p轨道重叠形成σ键。
4
3.(2024·浙江1月卷,17节选)氮和氧是构建化合物的常见元素。
(3)①HN-NH+H+→HN-NH+,其中-NH 的N原子杂化方式为 ;比较键角 中
2 2 2 3 2
的-NH HN-NH+中的-NH + (填“>”、“<”或“=”),请说明理由 。
2 2 3 3
②将HNO 与SO 按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是
3 3
NO +。比较氧化性强弱:NO + HNO (填“>”、“<”或“=”);写出A中阴离子的结构式 。
2 2 3
【答案】(3) ①sp3 < -NH 有孤电子对,孤电子对对成键电子排斥力大,键角变小
2②>
【解析】(3)①-NH 的价层电子对数 ,故杂化方式为sp3;-NH 价层电子对数为4,有一
2 2
对孤电子对,-NH +价层电子对数 ,无孤对电子,又因为孤电子对对成键电子的排斥力大
3
于成键电子对成键电子的排斥力,故键角 中的-NH <HN-NH+中的-NH +;②将HNO 与
2 2 3 3 3
SO 按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是NO +,则A为
3 2
NO HS O,NO +为硝酸失去一个OH-,得电子能力更强,氧化性更强,故氧化性强弱:NO + >HNO;阴
2 2 7 2 2 3
离子为HS O-根据已知可知其结构式为 。
2 7
4.(2024·浙江6月卷,17节选)氧是构建化合物的重要元素。请回答:
(3)化合物 和 的结构如图2。
① 和 中羟基与水均可形成氢键( ),按照氢键由强到弱对三种酸排序 ,
请说明理由 。
②已知 、 钠盐的碱性NaC>NaD,请从结构角度说明理由 。
【答案】(3) ①HC>HB>HA O、S、Se的电负性逐渐减小,键的极性:C=O>C=S>C=Se,使得
HA、HB、HC中羟基的极性逐渐增大,其中羟基与HO形成的氢键逐渐增强
2
②S的原子半径大于O的原子半径,S—H键的键长大于O—H键,S—H键的键能小于O—H键,同时
HC可形成分子间氢键,使得HD比HC更易电离出H+,酸性HD>HC,C-的水解能力大于D-,碱性NaC
>NaD
【解析】(3)①O、S、Se的电负性逐渐减小,键的极性:C=O>C=S>C=Se,使得HA、HB、HC中羟
基的极性逐渐增大,从而其中羟基与水形成的氢键由强到弱的顺序为HC>HB>HA;②HC、HD钠盐的碱性NaC>NaD,说明酸性HC<HD,原因是:S的原子半径大于O的原子半径,S—H键的键长大于O—H
键,S—H键的键能小于O—H键,同时HC可形成分子间氢键,使得HD比HC更易电离出H+,酸性HD
>HC,C-的水解能力大于D-,钠盐的碱性NaC>NaD。
5.(2024· 海南卷,19节选)锂电池是新型储能系统中的核心部件。作为锂电池中用到的电解质材料之
一,Li-bfsi (阴离子bfsi结构见下图。A)深受关注。
回答问题:
(1) Li-bfsi的制备前体Li-bfsi (B),可由C的氟化反应得到,C中第三周期元素有 (填元素符号)。
(2)C分子中,两个H-N-S键角均为117°,S-N-S键角为126°,N的原子轨道杂化类型为 。
(3)B溶于某溶剂发生自耦电离(2B A+F),阳离子F的结构式为 。
(4)B和D水溶液均呈酸性,相同温度下,K 值大小关系:B D(填“>”或“<”);沸点大小关系:
a
B(170℃)>E(60.8℃),其原因是 。
(5)研究表明,某有机溶剂中,相同浓度的G溶液和H溶液,前者电导率显著低于后者,原因是
。
【答案】(1)Cl、S (2) sp2
(3) 或
(4) > B分子间存在氢键
(5)G中正、负电荷距离更近,G中N原子的配位能力强于H中磺酰基上的O原子,G溶液中阴阳离子
浓度小于H溶液
【解析】(1)由图可知,C中第三周期元素为氯元素和硫元素;(2)由键角可知,C中氮原子的价层电子
对数为3,原子的杂化方式为sp2杂化;(3)由原子个数和电荷总数守恒可知,阳离子 F的结构式可能为或 ;(4)氟原子是吸电子基,会使氮氢键的极性增强,电离出氢离子的能力增大,
乙基是供电子基,会使氮氢键的极性减弱,电离出氢离子的能力减弱,则b的酸性强于D;由图可知,B
分子能形成分子间氢键,E分子不能形成分子间氢键,所以B的分子间作用力强于B,沸点强于B;(5)由
图可知,G中正、负电荷距离更近,G中N原子的配位能力强于H中磺酰基上的O原子,G溶液中阴阳离
子浓度小于H溶液,所以有机溶剂中,相同浓度的G溶液和H溶液,前者电导率显著低于后者。
键角大小比较思维模型
1 . 中心原子杂化类型和分子空间构型的相互判断
分子(A为 中心原子 中心原子孤
分子构型 示例
中心原子) 杂化方式 电子对数
sp 0 直线形 BeCl
2
AB sp2 1 V形 SO
2 2
sp3 2 V形 HO
2
sp2 0 平面三角形 BF
3
AB
3
sp3 1 三角锥形 NH
3
AB sp3 0 正四面体形 CH
4 4
2 .常见结构与性质问题的 原因解释
(1)物质稳定性比较
①CuO在1 273 K时分解为Cu O和O ,请从铜的原子结构来说明在高温下Cu O比CuO更稳定的原因:
2 2 2最外层电子排布 C u O 中 Cu + 为 3d 10 ,而 CuO 中 Cu 2+ 为 3d 9 ,最外层电子排布达到全充满时更稳定 。
2
②稳定性HS>HSe的原因: 硫原子半径比硒小, S—H 的键能比 Se—H 的键能大 。
2 2
③SiH 的稳定性小于CH ,更易生成氧化物,原因是 C—H 的键能大于 C—O , C—H 比 C—O 稳定,而
4 4
Si—H 的键能却远小于 Si—O ,所以 Si—H 不稳定而倾向于形成更稳定的 Si—O 。
(2)配位键的形成
①CN-作配体时,提供孤电子对的通常是碳原子,而不是氮原子,原因是碳元素的电负性小于氮元素的
电负性,对孤电子对的吸引能力弱,给出电子对更容易。
②已知NF 与NH 的空间结构相同,但NF 不易与Cu2+形成配离子,原因是 F 的电负性比 N 大, N—F
3 3 3
成键电子对偏向氟原子,偏离氮原子,使得氮原子核对其孤电子对的吸引能力增强,难与 C u 2 + 形成配位键 。
(3)键角的大小
CH、NH 、HO的键角由大到小的顺序为CH>NH>H O,原因:三种氢化物的中心原子价层电子对数
4 3 2 4 3 2
均为 4 , VSEPR 模型均为四面体,但中心原子的孤电子对数依次增多,对成键电子对的排斥作用增大,故
键角依次减小。
(4)氢键
①水由液体形成固体后密度却减小,原因是水在形成晶体时,由于氢键的作用使分子间距离增大,空
间利用率降低,密度减小。
②测定化合物HF的相对分子质量时,发现实验值一般高于理论值,其主要原因是 HF 分子间存在氢键 ,
易形成缔合分子 (HF ) 。
n
③HO沸点高于HS的原因:H O 分子间存在氢键,且比范德华力强 。
2 2 2
(5)晶体导电的原因
①Fe O 晶体能导电的原因:电子可在两种不同价态的铁离子间迅速发生转移。
3 4
②金属镍导电的原因:镍单质是金属晶体,由金属阳离子和自由电子构成,自由电子在外加电场的作
用下可发生定向移动。
(6)晶体熔、沸点比较
①氯化铝的熔点为190 ℃,而氟化铝的熔点为 1 290 ℃,导致这种差异的原因:AlCl 是分子晶体,而
3
AlF 是离子晶体,离子键比分子间作用力强得多。
3
②氮化硼(BN)和磷化硼(BP)都是耐磨涂料,它们的结构相似,但是氮化硼晶体的熔点要比磷化硼晶体
的熔点高,原因是 氮化硼 (BN ) 和磷化硼 (BP ) 都属于共价晶体,而氮原子的半径比磷原子小, B—N 的键长
比 B—P 短,键能更大,熔化时破坏化学键需要的能量更多,所以氮化硼晶体的熔点要比磷化硼晶体的熔
点高。
③K和Cr属于同一周期,且核外最外层电子构型相同,但金属钾的熔、沸点等都比金属铬低,原因是
由于钾原子的半径比铬原子大而且价层电子数较少,其金属键比 C r 弱,所以其熔、沸点较低 。1.(2025·广东省广东实验中学高三模拟,节选)锂电池的电解液是目前研究的热点。
(2)为提高锂电池的安全性,科研人员采用离子液体作电解液。某种离子液体的阳离子的结构简式如下,
阴离子为PF -。
6
① 、 、 三种元素的电负性由大到小的顺序为 。
②该阳离子中,带“*”的 原子的杂化轨道类型为 杂化。
③根据 模型,PF -的中心原子上的价层电子对数为 ,空间结构为正八面体形。
6
【答案】(2) F>N>P sp2 6
【解析】(2)①一般,周期表从左到右,元素的电负性逐渐变大,从上到下,逐渐变小。根据元素周期
表位置可知,电负性由大到小的是F>N>P;②该阳离子结构中, ,带
“*”的C原子含有3个σ键,没有孤电子对,则价电子对数是n=3,为sp2杂化;③阴离子为PF -,其中心
6
原子P的价层电子对数是 。
2.(2025·湖南省多校高三联考,节选)氮气的活化与转化是现代化学领域极具挑战的课题之一、我国
学者以氮气为氮源高效合成了活性氮物质LiCN,以LiCN 为合成子,能用于多种高附加值含氮化合物的
2 2 2 2
合成。如有机物甲的合成路径如图所示:
(4) (CH )SiCl分子中碳、硅原子的杂化类型分别为 、 。
3 3
(5)1mol甲分子中 键数目为 。
【答案】(4) sp3 sp3 (5) 28N 或28×6.02×1023
A
【解析】(4)(CH )SiCl中C原子和Si原子均形成4个σ键且没有孤电子对,杂化类型均为sp3。(5)单键
3 3
是σ键,双键中含有1个σ键和1个π键,甲分子中含有2×(3×3+4+1)=28,则1mol甲分子中σ键数目为28N 或28×6.02×1023。
A
3.(2025·浙江部分高中高三联考,17节选)C、 元素是构成物质世界的基本元素。
(2)C 在超导、强磁性、耐高压等方面有优异的性能,其晶体采用面心立方堆积方式。下列说法正确的
60
是 。
A.C 晶体特征符合分子密堆积
60
B.C 中的碳原子的杂化方式有sp2、sp3
60
C.能量最低的激发态C原子的电子排布式:1s22s22p12p1
x z
D.C 能与杯酚通过共价键相结合,经过尺寸匹配实现“分子识别”
60
E.C 晶体中分子的配位数为12
60
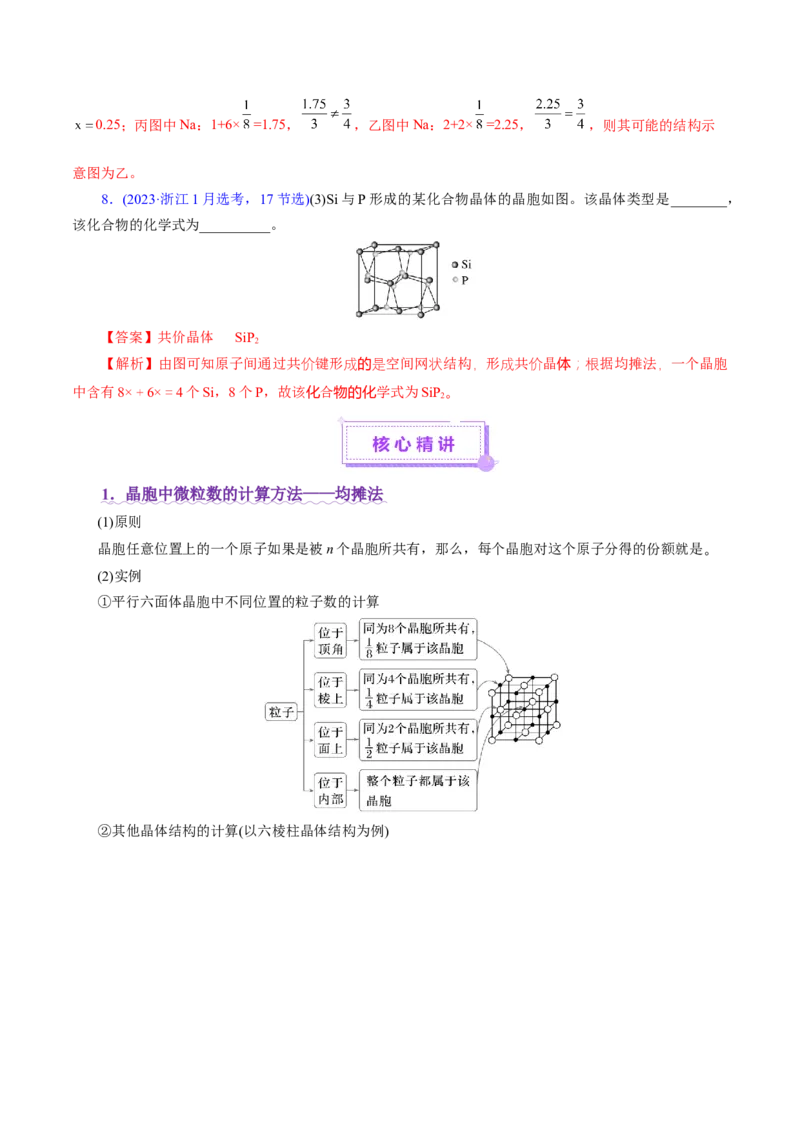
(3)已知:乙二酸分子内脱水可生成C O。芳香族化合物C O 也可用于类似原理生成,核磁共振谱显
2 3 12 9
示该分子中仅存在两种化学环境不同的碳原子,则C O 的结构简式为 。
12 9
(4)物质的微观结构决定其宏观性质,进而影响其用途。
①氢氟酸( 的水溶液)能与二氧化硅反应,工业常常通过此方法来生成磨砂玻璃。其反应能进行的原
因除了氟的电负性比氧大,能够更强烈地吸引电子对,导致 键易断裂以外,请从化学反应的进行角
度解释能够发生的原因 。
②白磷(P )为正四面体构型(如图),其中每个P均以sp3杂化,请从物质结构角度解释白磷易自燃的原因
4
。
【答案】(2)AE (3)
(4)①反应属于熵增效应(或该反应生成气体离开体系,平衡向右边移动,更易进行) ②白磷分子呈
正四面体结构(或磷原子采用sp3杂化形式),其中键角为60°,而正四面体结构键角倾向于 ,使得P-P
键弯曲而具有较大张力,其键能较小,易断裂(或由于P的原子半径较大,使得原子重叠程度较小,其键能
较小,易断裂)
【解析】(2)A项,C 是分子晶体,符合分子密堆积方式,故A正确;B项,C 分子中C原子形成3
60 60
个 键,且不含有孤对电子,其杂化方式为sp2,故B错误;C项,1s22s22p12p1是基态C原子的电子排布
x z
式,能量最低的激发态C原子的电子排布式1s22s22p13s1,故C错误;D项,C 能与杯酚通过范德华力相结
60合成超分子,经过尺寸匹配实现“分子识别”,故C错误;E项,晶体采用面心立方堆积方式,以顶点的
C 为对象,其距离最近的C 位于与之相邻的三个面心上,顶点的C 被8个晶胞共用,面心的C 被两个
60 60 60 60
晶胞共用,则其配位数为 个,故E正确;故选AE;(3)乙二酸分子内脱水可生成C O,其原理
2 3
为: ,则芳香族化合物C O 也可用于类似原理生成,核磁共
12 9
振谱显示该分子中仅存在两种化学环境不同的碳原子,其结构简式为 。(4)①反应化
学方程式为4HF+SiO =SiF ↑+H O,该反应生成气体离开体系,平衡向右边移动,更易进行;②白磷分子呈
2 4 2
正四面体结构,磷原子采用sp3杂化形式,其中键角为60°,而正四面体结构键角倾向于 ,使得P-P
键弯曲而具有较大张力,其键能较小,易断裂(或由于P的原子半径较大,使得原子重叠程度较小,其键能
较小,易断裂)。
4.[真题改编] (2021·广东卷,20改编)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例
如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
①化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有__________________。
A.在Ⅰ中S原子采取sp3杂化 B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C—C—C键角是180° D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的
是___________。
【答案】①AD ②化合物Ⅲ6-2×1
【解析】①化合物Ⅰ中S原子的价层电子对数=2+ =4,因此S原子采取sp3杂化,A项正确;
2
化合物Ⅱ中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元素从
上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,B项错误;化合物Ⅲ中C原子成
键均为单键,因此C原子采取sp3杂化,所以C—C—C键角接近109.5°,C项错误;化合物Ⅲ中存在C—
H、C—C、C—S、S=O、S—O、S—H共价键和离子键,D项正确。②化合物Ⅰ中羟基能与水分子之间形
成分子间氢键,化合物Ⅲ为易溶于水的钠盐,溶于水后电离出的 中O原子均能与水分子之间
形成氢键,相同物质的量两种物质溶于水后, 形成的氢键更多,因此化合物Ⅲ更易溶于水。
5.(2025·浙江省金华第一中学高三选考模拟,17节选)铑(Rh)和铱(Ir)形成的材料在生产生活中应用广
泛。
(2)固体铑(Rh)膦缘金催化剂(Ph为苯基)的结构如图所示,分子中P原子的杂化方式为 ,
1mol该物质中含有的σ键的数目为 。
(4)均为平面结构的吡咯( )和吡啶( )在盐酸中溶解度较大的为 ,原因是
。
【答案】(2) sp3 114N
A
(4) 吡咯 吡咯和吡啶相比,吡咯是一个五元杂环化合物,其中氮原子与两个碳原子相连,形成一
个环状结构,在吡咯中,氮原子的孤对电子参与了环的芳香性,这使得氮原子上的电子云密度降低,从而
减弱了其碱性,即吡啶更容易与盐酸电离出的H+结合,即吡咯再盐酸中的溶解性比吡啶的更大
【解析】(2)根据固体铑(Rh)膦络合催化剂(Ph为苯基)的结构图,可知P原子的价电子对数为4,其杂
化方式为sp3;PPH 中σ键的数目36,1个CO分子中含有1个σ键,Rh周围有5个单键,因此1mol该物
3
质中含有的σ键的数目为(36×4+1+5)mol=114mol,即1mol该物质中含有的σ键的数目为114N 。(4)吡咯和
A
吡啶相比,吡咯是一个五元杂环化合物,其中氮原子与两个碳原子相连,形成一个环状结构,在吡咯中,
氮原子的孤对电子参与了环的芳香性,这使得氮原子上的电子云密度降低,从而减弱了其碱性,即吡啶更容易与盐酸电离出的H+结合,即吡咯在盐酸中的溶解性比吡啶的更大。
6.(2025·辽宁省沈阳市高中联合体高三模拟,节选)(5)六方氮化硼晶体也被称为“白石墨”,具有和
石墨晶体相似的层状结构(如下图所示)。
①比较B和N的电负性大小,并从原子结构角度说明理由: 。
②分析六方氮化硼晶体层间是否存在化学键并说明依据: 。
【答案】(5) B和N电子层数相同,核电核数BN,原子核对键合电子的吸引作用
BN,原子核对键合电子的吸引作用
B N元素的电负性小于O,更易给出孤电子对
(2)CD (3) InCuSe 6
2
【解析】(3)①由晶胞可知In位于顶点、面上和体心,所以个数为 ,Cu位于棱上和面
上,所以个数为 ,Se位于体内,所以个数为8,该化合物的化学式为InCuSe ;②该晶胞中,
2
通过观察可以看出1号Se原子左边都连接In、右边连接Cu,除此之外只有6号原子连接方式相同,所以
通过平移能与1号Se原子完全重合的原子为6号。
6.[新考法](2025·山东省Eternal7社区高三模拟预测,节选)(5)已知钇(Y)的另外一种二元化合物X具
有金属般的导电性能,晶体结构如图所示,其间可捕获自由电子(e-),且碳以C 2-单元存在,据此猜想X的
2
微粒组成可表示为 。
【答案】(5) Y(C 2-)(e-)
2
【解析】(5)根据“均摊法”,晶胞中含 个 、 个C,也就是2个C 2-,其间还可
2
捕获自由电子(e-),结合电中性可知,X的微粒组成可表示为Y(C 2-)(e-)。
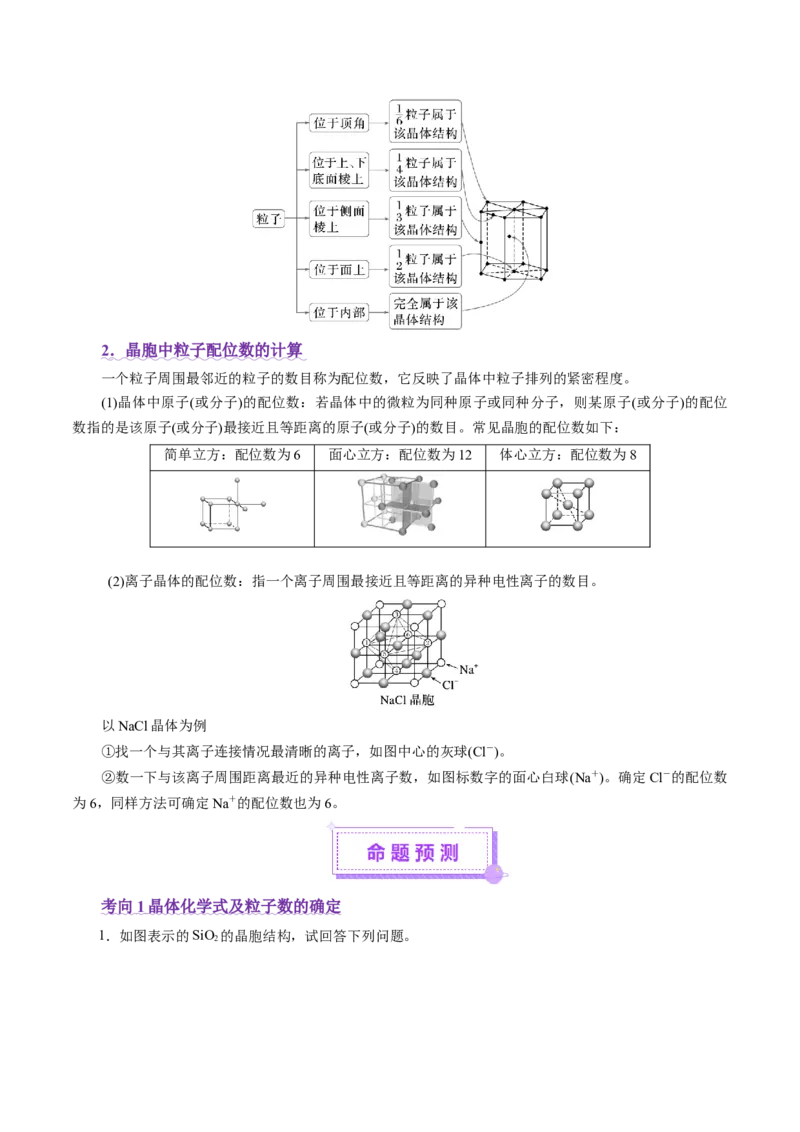
2考向 2 配位数的计算
7.Cu O的晶胞结构如图所示,则Cu+的配位数为 。
2
【答案】2
【解析】晶胞中白色原子的个数为 ,黑色原子个数为4,则白色的原子表示O,黑色的表
示Cu,根据晶胞结构可知O2-与周围4个Cu+构成正四面体,则O2-的配位数为4,根据化学式可知,Cu+的
配位数为2。
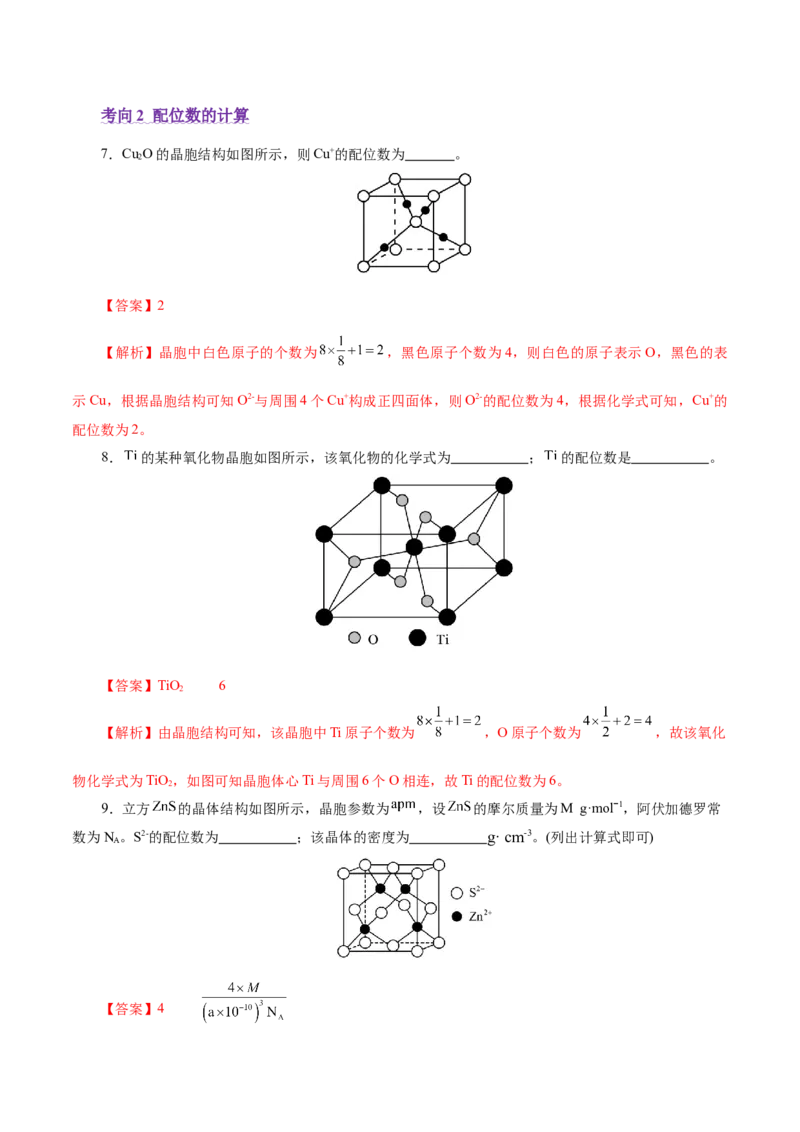
8. 的某种氧化物晶胞如图所示,该氧化物的化学式为 ; 的配位数是 。
【答案】TiO 6
2
【解析】由晶胞结构可知,该晶胞中Ti原子个数为 ,O原子个数为 ,故该氧化
物化学式为TiO,如图可知晶胞体心Ti与周围6个O相连,故Ti的配位数为6。
2
9.立方 的晶体结构如图所示,晶胞参数为 ,设 的摩尔质量为M g·molˉ1,阿伏加德罗常
数为N 。S2-的配位数为 ;该晶体的密度为 g· cm-3。(列出计算式即可)
A
【答案】4【解析】根据晶胞结构分析,S2-位于晶胞的顶点和面心,1个S2-周围有4个与之等距且最近的Zn2+,
所以S2-的配位数为4;一个晶胞中含有S2-的个数为 ,含有Zn2+的个数为4个,晶胞的体积为
,所以晶体的密度为 。
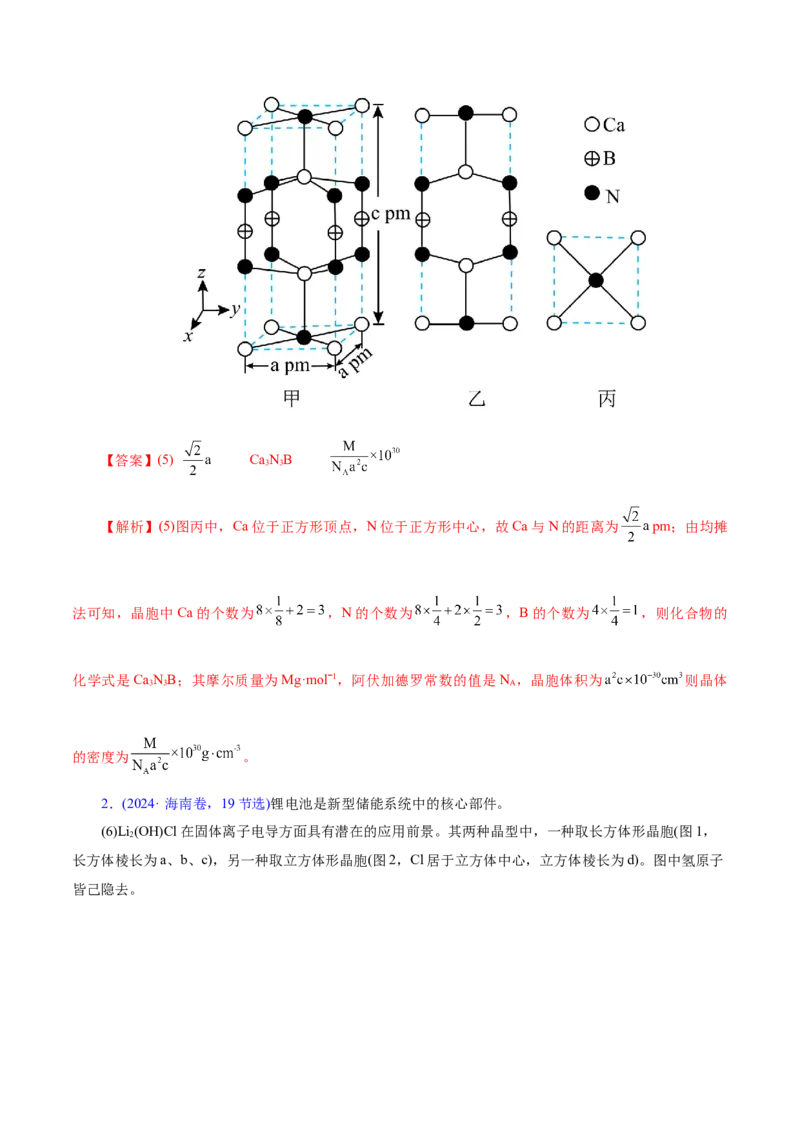
10.某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电
解质材料(图2)。
图1中O原子的配位数为 ,图2表示的化学式为 (设该晶胞中Cl的个数为 )
【答案】6
【解析】图1中以面心O原子为例,最近原子同层4个、上下层各1个,则配位数为6;据“均摊
法”,晶胞中含氯和溴共为 个,同时含 个O、1个Li,结合化合价则含有1个镁,则化学
式为 。
11. 和 可以组成多种氧化物,其中一种氧化物的晶胞如图所示。
①该晶体中 的配位数为 。
②已知阿伏加德罗常数的值为 ,该晶体的密度 (用含 、 的代数式表示)。【答案】4
【解析】晶胞结构中体心位置的Mn与4个O原子相连,故配位数为4;晶胞中有2个Mn,4个O,
故化学式为MnO , 。
2
12.Mn和O可以组成多种氧化物,其中一种氧化物的晶胞如图所示。
①该晶体中Mn的配位数为 。
②已知阿伏加德罗常数的值为 ,该晶体的密度 (用含a、b的代数式表示)。
【答案】6
【解析】①由晶胞结构可知,每个锰原子被6个氧原子包围,因此Mn的配位数为6;②锰离子的个数
为: ,氧离子的个数为: ,该锰氧化物的化学式为MnO ,阿伏加德罗常数为 ,
2
每个晶胞中含有2个MnO ,则该晶体的密度为 。
2
13.某新型超导材料晶体中含有镍、镁、碳3种元素,镁原子和镍原子形成立方晶胞如图所示(碳原子
位于体心)。①该晶体的化学式为 。
②若取碳原子为晶胞顶点,则镍原子位于晶胞的 位置。
③Mg的C配位数为 。
【答案】MgNiC 棱心 8
3
【解析】①在晶体中,镍原子位于面心,个数为 ;镁原子位于顶点,个数为 ;碳原子
位于体心,个数为1,该晶体的化学式为Mg Ni C;②若取碳原子为晶胞顶点,以xyz轴方向进行棱的延
3
伸,则棱边恰好经过镍原子,得到镍原子位于此晶胞的棱心位置;③在此晶胞中,以Mg原子体心,则C
原子位于顶点位置,则C配位数为8。
题型四 晶胞参数的计算
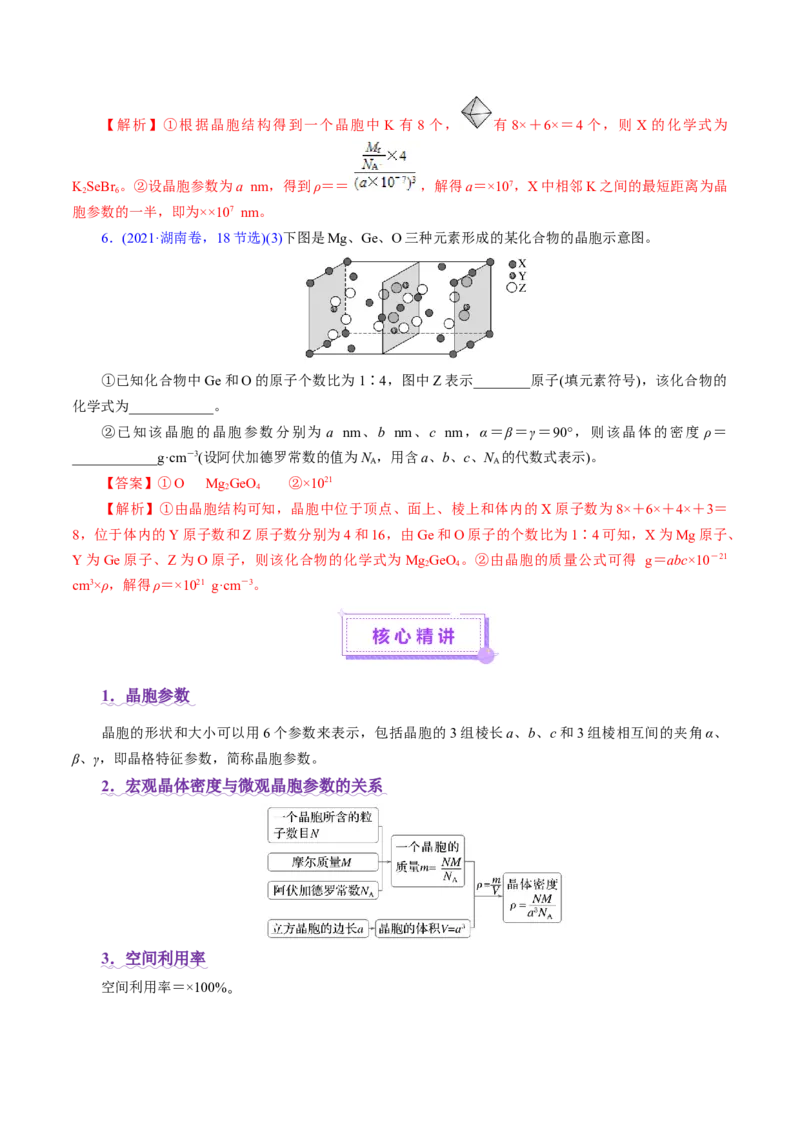
1.(2024·甘肃卷,15节选)(5)某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞
底面显示为图丙,晶胞参数 。图丙中 与N的距离为 ;化合物的化学式是
,其摩尔质量为Mg·molˉ1,阿伏加德罗常数的值是N ,则晶体的密度为 g· cm-3 (列出计算表达式)。
A【答案】(5) Ca NB
3 3
【解析】(5)图丙中,Ca位于正方形顶点,N位于正方形中心,故Ca与N的距离为 pm;由均摊
法可知,晶胞中Ca的个数为 ,N的个数为 ,B的个数为 ,则化合物的
化学式是Ca NB;其摩尔质量为Mg·molˉ1,阿伏加德罗常数的值是N ,晶胞体积为 则晶体
3 3 A
的密度为 。
2.(2024· 海南卷,19节选)锂电池是新型储能系统中的核心部件。
(6)Li(OH)Cl在固体离子电导方面具有潜在的应用前景。其两种晶型中,一种取长方体形晶胞(图1,
2
长方体棱长为a、b、c),另一种取立方体形晶胞(图2,Cl居于立方体中心,立方体棱长为d)。图中氢原子
皆己隐去。①立方体形晶胞所代表的晶体中部分锂离子(●Li)位置上存在缺位现象,锂离子的总缺位率为 ;
该晶型中氯离子周围紧邻的锂离子平均数目为 。
②两种晶型的密度近似相等,则c= 。(以含a、b和d的代数式表达)
【答案】(6) 8
【解析】(6)①由晶胞结构可知,晶胞中位于体心的氯离子个数为1,位于顶点的氧离子个数为8×
=1,位于棱上的锂离子个数为12× =3,由化合价代数和为0可知,晶胞中锂离子的个数为2,则锂离子的
总缺位率为 = ;晶胞中位于体心的氯离子与位于棱上的锂离子距离最近,其中上下棱上的锂离子为两
个立方体所共有,则氯离子周围紧邻的锂离子平均数目为4+8× =8;②设Li(OH)Cl的相对分子质量为
2
M,由晶胞结构可知,长方体形晶胞的密度为 ,立方体形晶胞 ,由两种晶型的密度近似相等
可知,c= 。
3.(2024·广东卷,18节选) 镓( )在半导体、记忆合金等高精尖材料领域有重要应用。
(6)一种含Ga、Ni、Co元素的记忆合金的晶体结构可描述为 与Ni交替填充在Co构成的立方体体心,
形成如图所示的结构单元。该合金的晶胞中,粒子个数最简比Co:Ga:Ni= ,其立方晶胞的体积为 nm3。
【答案】(6) 2:1:1 8a3
【解析】(6)合金的晶体结构可描述为Ga与Ni交替填充在Co构成的立方体体心,形成如图所示的结
构单元,取Ga为晶胞顶点,晶胞面心也是Ga,Ni处于晶胞棱心和体心,Ga和Ni形成类似氯化钠晶胞的
结构,晶胞中Ga和Ni形成的8个小正方体体心为Co,故晶胞中Ga、Ni个数为4,Co个数为8,粒子个
数最简比Co:Ga:Ni=2:1:1,晶胞棱长为两个最近的Ga之间(或最近的Ni之间)的距离,为2a nm,故
晶胞的体积为8a3nm3。
4.(2023·北京卷,15节选)(5)MgS O·6H O的晶胞形状为长方体,边长分别为a nm、b nm、c nm,
2 3 2
结构如图所示。
晶胞中的[Mg(H O) ]2+个数为____________。已知MgS O·6H O的摩尔质量是M g·mol-1,阿伏加德
2 6 2 3 2
罗常数的值为N ,该晶体的密度为____________g·cm-3。(1 nm=10-7 cm)
A
【答案】4 ×1021
【解析】由晶胞结构可知,1个晶胞中含有8×+4×+2×+1=4个[Mg(H O) ]2+,含有4个SO;该晶
2 6 2
体的密度ρ= g·cm-3=×1021 g·cm-3。
5.(2022·广东卷,20节选)(6)化合物X是筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z
轴方向的投影均为图2。
①X的化学式为________。
②设 X 的最简式的式量为 M ,晶体密度为 ρ g·cm-3,则 X 中相邻 K 之间的最短距离为
r
________________nm(列出计算式,N 为阿伏加德罗常数的值)。
A
【答案】①KSeBr ②××107
2 6【解析】①根据晶胞结构得到一个晶胞中 K 有 8 个, 有 8×+6×=4 个,则 X 的化学式为
KSeBr 。②设晶胞参数为a nm,得到ρ== ,解得a=×107,X中相邻K之间的最短距离为晶
2 6
胞参数的一半,即为××107 nm。
6.(2021·湖南卷,18节选)(3)下图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。
①已知化合物中Ge和O的原子个数比为1∶4,图中Z表示________原子(填元素符号),该化合物的
化学式为____________。
②已知该晶胞的晶胞参数分别为 a nm、b nm、c nm,α=β=γ=90°,则该晶体的密度 ρ=
____________g·cm-3(设阿伏加德罗常数的值为N ,用含a、b、c、N 的代数式表示)。
A A
【答案】①O Mg GeO ②×1021
2 4
【解析】①由晶胞结构可知,晶胞中位于顶点、面上、棱上和体内的X原子数为8×+6×+4×+3=
8,位于体内的Y原子数和Z原子数分别为4和16,由Ge和O原子的个数比为1∶4可知,X为Mg原子、
Y为Ge原子、Z为O原子,则该化合物的化学式为 MgGeO 。②由晶胞的质量公式可得 g=abc×10-21
2 4
cm3×ρ,解得ρ=×1021 g·cm-3。
1 .晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的夹角α、
β、γ,即晶格特征参数,简称晶胞参数。
2 .宏观晶体密度与微观晶胞参数的关系
3 .空间利用率
空间利用率=×100%。1.(2025·浙江部分高中高三联考,17节选)C、 元素是构成物质世界的基本元素。
(1)尿素[CO(NH)]是无色或白色针状晶体,该晶体属于四方晶系,晶胞参数
2 2
,晶胞结构如图所示,其中所有分子均在棱上。
①按照第一电离能由大到小对组成元素排序 。
②该晶体的密度为 g· cm-3。
【答案】(1) N>O>C>H
【解析】(1)①同周期元素从左到右第一电离能呈增大趋势,N元素2p能级为半满结构,第一电离能大
于同周期相邻元素,H元素只有一个电子,很容器失去电子,第一电离能最小,则第一电离能N>O>C>
H;②根据均摊法,晶胞中含有[CO(NH)]的个数为 ,则晶胞的密度为
2 2
。
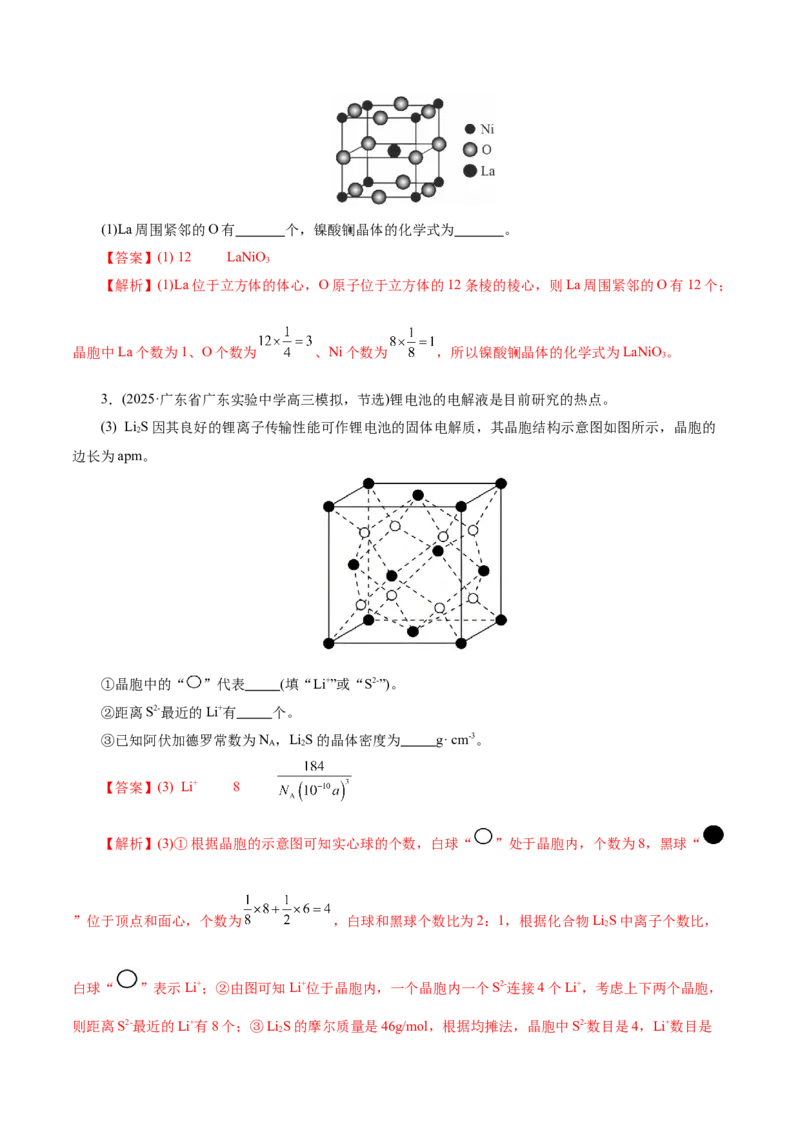
2.(2025· 浙江省杭州市浙南联盟高三联考,17节选)镍酸镧具有良好的电化学性能,可用于光电化学
领域。镍酸镧电催化剂立方晶胞如图所示:(1)La周围紧邻的O有 个,镍酸镧晶体的化学式为 。
【答案】(1) 12 LaNiO
3
【解析】(1)La位于立方体的体心,O原子位于立方体的12条棱的棱心,则La周围紧邻的O有12个;
晶胞中La个数为1、O个数为 、Ni个数为 ,所以镍酸镧晶体的化学式为LaNiO 。
3
3.(2025·广东省广东实验中学高三模拟,节选)锂电池的电解液是目前研究的热点。
(3) LiS因其良好的锂离子传输性能可作锂电池的固体电解质,其晶胞结构示意图如图所示,晶胞的
2
边长为apm。
①晶胞中的“ ”代表 (填“Li+”或“S2-”)。
②距离S2-最近的Li+有 个。
③已知阿伏加德罗常数为N ,LiS的晶体密度为 g· cm-3。
A 2
【答案】(3) Li+ 8
【解析】(3)①根据晶胞的示意图可知实心球的个数,白球“ ”处于晶胞内,个数为8,黑球“
”位于顶点和面心,个数为 ,白球和黑球个数比为2:1,根据化合物LiS中离子个数比,
2
白球“ ”表示Li+;②由图可知Li+位于晶胞内,一个晶胞内一个S2-连接4个Li+,考虑上下两个晶胞,
则距离S2-最近的Li+有8个;③LiS的摩尔质量是46g/mol,根据均摊法,晶胞中S2-数目是4,Li+数目是
28。则晶胞质量为 ,体积是(10-10a)3cm3,晶胞密度 = 。
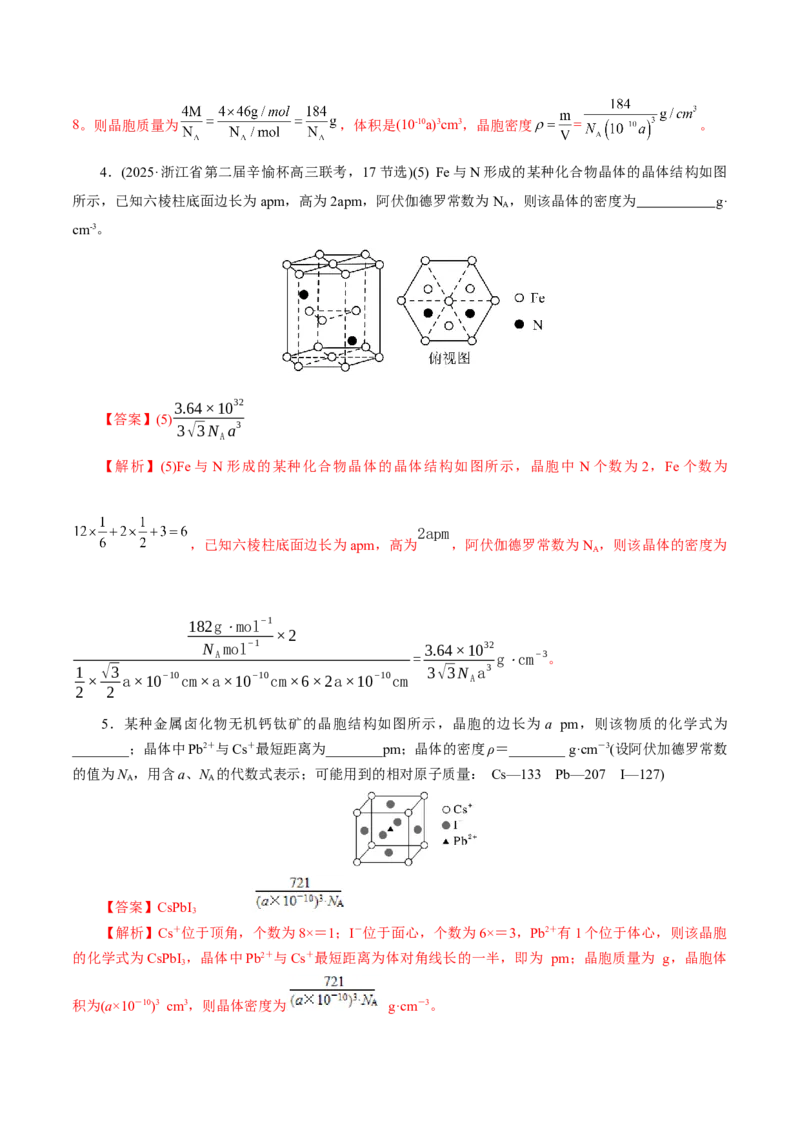
4.(2025·浙江省第二届辛愉杯高三联考,17节选)(5) Fe与N形成的某种化合物晶体的晶体结构如图
所示,已知六棱柱底面边长为apm,高为2apm,阿伏伽德罗常数为N ,则该晶体的密度为 g·
A
cm-3。
3.64×1032
【答案】(5)
3√3N a3
A
【解析】(5)Fe与N形成的某种化合物晶体的晶体结构如图所示,晶胞中 N个数为2,Fe个数为
2apm
,已知六棱柱底面边长为apm,高为 ,阿伏伽德罗常数为N ,则该晶体的密度为
A
182g⋅mol−1
×2
N mol−1 3.64×1032
A = g⋅cm−3。
1 √3 3√3N a3
× a×10−10cm×a×10−10cm×6×2a×10−10cm A
2 2
5.某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长为 a pm,则该物质的化学式为
________;晶体中Pb2+与Cs+最短距离为________pm;晶体的密度ρ=________ g·cm-3(设阿伏加德罗常数
的值为N ,用含a、N 的代数式表示;可能用到的相对原子质量: Cs—133 Pb—207 I—127)
A A
【答案】CsPbI
3
【解析】Cs+位于顶角,个数为8×=1;I-位于面心,个数为6×=3,Pb2+有1个位于体心,则该晶胞
的化学式为CsPbI ,晶体中Pb2+与Cs+最短距离为体对角线长的一半,即为 pm;晶胞质量为 g,晶胞体
3
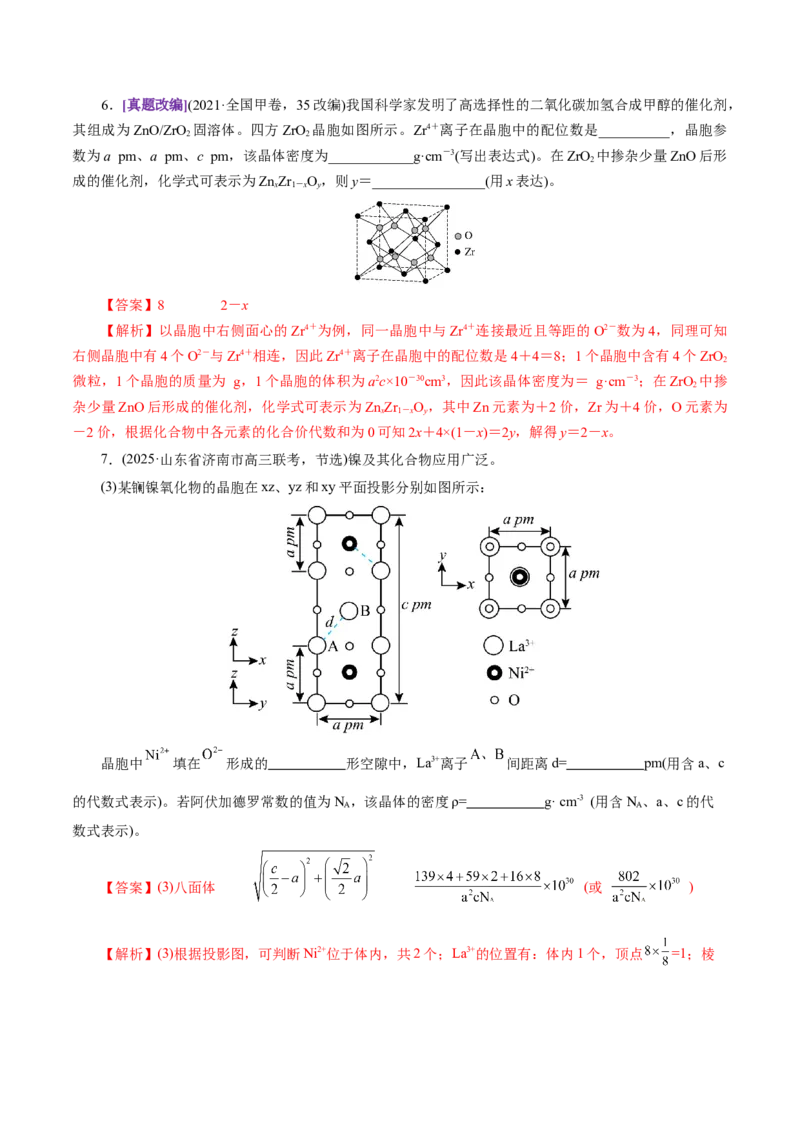
积为(a×10-10)3 cm3,则晶体密度为 g·cm-3。6.[真题改编](2021·全国甲卷,35改编)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,
其组成为ZnO/ZrO 固溶体。四方ZrO 晶胞如图所示。Zr4+离子在晶胞中的配位数是__________,晶胞参
2 2
数为a pm、a pm、c pm,该晶体密度为____________g·cm-3(写出表达式)。在ZrO 中掺杂少量ZnO后形
2
成的催化剂,化学式可表示为ZnZr O,则y=________________(用x表达)。
x 1-x y
【答案】8 2-x
【解析】以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+连接最近且等距的O2-数为4,同理可知
右侧晶胞中有4个O2-与Zr4+相连,因此Zr4+离子在晶胞中的配位数是4+4=8;1个晶胞中含有4个ZrO
2
微粒,1个晶胞的质量为 g,1个晶胞的体积为a2c×10-30cm3,因此该晶体密度为= g·cm-3;在ZrO 中掺
2
杂少量ZnO后形成的催化剂,化学式可表示为ZnZr O,其中Zn元素为+2价,Zr为+4价,O元素为
x 1-x y
-2价,根据化合物中各元素的化合价代数和为0可知2x+4×(1-x)=2y,解得y=2-x。
7.(2025·山东省济南市高三联考,节选)镍及其化合物应用广泛。
(3)某镧镍氧化物的晶胞在xz、yz和xy平面投影分别如图所示:
晶胞中 填在 形成的 形空隙中,La3+离子 间距离d= pm(用含a、c
的代数式表示)。若阿伏加德罗常数的值为N ,该晶体的密度ρ= g· cm-3 (用含N 、a、c的代
A A
数式表示)。
【答案】(3)八面体 (或 )
【解析】(3)根据投影图,可判断Ni2+位于体内,共2个;La3+的位置有:体内1个,顶点 =1;棱上 =2,共4个;O2-的位置有:体内2个,面上 ,棱上 ,共8个;因此1个Ni2+周围
距离相等且最近的O2-形成的空间结构为正八面体形;由上述分析可知,底面面对角线长度的一半,A到棱
心的长度,以及要计算得d三者构成直角三角形,d为斜边的长度,底面面对角线长度的一半= apm;A
到棱心的长度为( )pm;故d= ;根据上述计算,晶胞的质量为
,晶胞的体积为 cm3,故晶体的密度
(或 g· cm-3)。