文档内容
专题 12 铁及其重要化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 铁及其化合物的结构、性质及应用
考点二 铁及其化合物制备的工艺流程
考点三 铁及其化合物的有关计算
考点一 铁及其化合物的结构、性质及应用
1.(2023·浙江·模拟预测) 是一种高效水处理剂,下列说法中不正确的是
A. 溶液属于强电解质
B. 有强氧化性
C.该物质中Fe元素被还原后的产物可能发生水解
D.Fe元素位于元素周期表VIII族
【答案】A
【解析】A. 溶液属于混合物不属于强电解质,A错误;B. 中铁元素的化合价是+6价
具有强氧化性,B正确;C.该物质中Fe元素被还原后的产物是+3价,可能发生水解,C正确;D.Fe元
素位于元素周期表VIII族,D正确;故选A。
2.(2023·浙江杭州·校联考模拟预测) 是铁锈的主要成分,下列说法正确的是
A. 在纯氧中受热可以生成
B. 的检验,可用 溶液,生成蓝色溶液
C.铁元素位于周期表中第四周期,第ⅧB族
D.钢铁发生吸氧腐蚀可形成铁锈( ),负极反应式为
【答案】A
【解析】A.Fe O 中铁的化合价有+2价,也有+3价,+3价的在纯氧中不发生变化,+2价的在纯氧中被氧
3 4
化为+3价,即在纯氧中受热可以生成,故A正确;B. Fe3+遇到 K[Fe(CN) ]溶液会生成蓝色沉淀,不是
4 6
蓝色溶液,故B错误;C.铁元素位于周期表中第四周期第Ⅷ族,铁不是主族元素也不是副族元素,故C
错误;D.钢铁发生吸氧腐蚀可形成铁锈,但负极反应式为Fe-2e-=Fe2+,故D错误;故本题选A。
3.(2023·上海徐汇·统考二模)可用于检验 溶液是否少量变质的试剂
A.NaOH B.Fe C. D.KSCN
【答案】D
1
原创精品资源学科网独家享有版权,侵权必究!【解析】 易被氧化为Fe (SO ),只需检验是否含有Fe3+即可说明 溶液是否变质,Fe3+能和
2 4 3
SCN-生成络合物硫氰化铁,使溶液呈现血红色,因此可用KSCN检验 溶液是否少量变质;故答案选
D。
4.(2023·广东广州·统考二模)下列关于铁及其化合物之间转化反应的方程式书写正确的是
A. (g)通过灼热铁粉:
B.过量铁粉加入稀硝酸中:
C.氢氧化铁中加入氢碘酸:
D. 溶液中加入酸性 溶液:
【答案】D
【解析】A.Fe与HO(g)高温反应生成Fe O 和H,A错误;B.稀硝酸有强氧化性,能把Fe氧化成
2 3 4 2
Fe3+,过量铁粉与Fe反应生成Fe2+,总反应产物应是Fe2+而不是Fe3+,B错误;C.Fe3+具有强氧化性,I-具
有强还原性,两者能发生氧化还原反应,分别生成Fe2+和I,C错误;D.酸性KMnO 具有强氧化性,可
2 4
把Fe2+氧化成Fe3+,本身被还原生成Mn2+,D正确;故选D。
5.(2023·上海嘉定·统考二模)将过氧化钠粉末投入到氯化亚铁溶液中,可观察到的现象是
A.最终生成红褐色沉淀 B.没有气体产生
C.最终生成白色沉淀 D.最终生成血红色溶液
【答案】A
【解析】将NaO 投入FeCl 溶液中,发生的反应为2NaO+2H O=4NaOH+O ↑,氧气和NaO 具有强氧化
2 2 2 2 2 2 2 2 2
性,可以把Fe2+氧化为Fe3+,Fe3+与氢氧化钠反应3OH-+Fe3+=Fe(OH) ↓,立即生成红褐色的Fe(OH) 沉淀,
3 3
所以看到的现象是:有大量气泡生成,立即有红褐色沉淀生成,故答案为A。
6.(2023·江苏扬州·统考三模)用表面有油污的铁屑等原料可以制备 ,实验中的部分装置和
操作如下图所示,其中不能达到实验目的的是
A.用装置甲去除铁屑表面的油污
B.用装置乙溶解铁屑制备
C.用装置丙吸收铁屑溶解过程中产生的
D.用装置丁蒸干溶液,获得
【答案】D【解析】A.热的纯碱溶液碱性较强可使油脂水解生成溶水物质,从而去除油污,故A正确;B.常温下
铁屑与硫酸反应生成硫酸亚铁和氢气,可用此方法制取 ,故B正确;C.高锰酸钾具有强氧化性,
可用其吸收铁屑溶解过程产生的还原性气体 ,故C正确;D. 应通过蒸发浓缩、冷却结
晶的方法获得,故D错误;故选:D。
7.(2023·浙江温州·乐清市知临中学校考二模)下列有关铁及其化合物的实验方案,对应的现象和结论都
正确的是
选项 实验方案 现象 结论
将红热的铁与水蒸气在高温条
反应结束后有黑色固体生 铁与水蒸气在高温下反
A 件下反应,反应结束后,将磁
成,且该固体被磁铁吸引 应,生成
铁靠近产物
为了验证 的还原性,取
B 溶液于试管中,加入酸 酸性高锰酸钾溶液紫色褪去 具有还原性
性高锰酸钾溶液
取 溶液与试管中,
加入稀盐酸前,溶液由黄色 和 既发生氧化还
逐滴加入 溶液至过
C 变为红棕色。加入稀盐酸和 原反应,也发生双水解
量。再加入过量稀盐酸和
溶液后产生白色沉淀
溶液
向少量蒸馏水的试管里滴加2
与 的配位能力小
D 滴 溶液,然后再 溶液变血红色
于
滴加2滴硫氰化钾溶液
【答案】C
【解析】A.将红热的铁与水蒸气在高温条件下反应,反应结束后,将磁铁靠近产物,该固体被磁铁吸引,
该固体可以是Fe也可以是 ,并不能确定一定生成 ,A错误;B.Cl-也具有还原性,可以使酸
性高锰酸钾溶液褪色,并不能确定是 使高锰酸钾褪色,B错误;C.取 溶液与试管中,逐滴
加入 溶液至过量。再加入过量稀盐酸和 溶液,加入稀盐酸前,溶液由黄色变为红棕色,说明
发生水解反应产生了 。加入稀盐酸和 溶液后产生不溶于盐酸的白色沉淀 ,说明Fe3+将
氧化为 ,C正确;D.向少量蒸馏水的试管里滴加2滴 溶液,然后再滴加2滴硫氰
化钾溶液,无明显现象,现象错误,D错误。故选C。
8.(2023·上海·统考模拟预测)月球土壤中富含铁元素,主要以铁单质和亚铁离子的形式存在,但嫦娥五
号取回的微陨石撞击处的月壤样品中存在大量的三价铁,有可能是以下哪个原因造成的
A. B.C. D.
【答案】A
【解析】A.月球表面的铁元素以铁单质和亚铁离子形式存在,FeO中Fe为+2价,FeO可能反应生成Fe
和Fe O,Fe O 中含有三价铁,A正确;B.Fe O 分解生成Fe O 和FeO,虽然Fe O 中含有三价铁,但是
3 4 3 4 3 4 2 3 2 3
四氧化三铁中含有较多三价铁,无法体现月球表面的铁元素主要以铁单质和亚铁离子的形式存在,B错误;
C.月球表面没有氧气,FeO无法被氧化生成Fe O,C错误;D.月球表面铁元素主要以铁单质和亚铁离
2 3
子的形式存在,Fe O 中Fe为+3价,D错误;故答案选A。
2 3
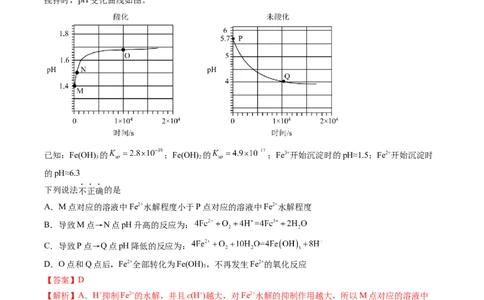
9.(2023·北京房山·统考一模)室温下,向新制酸化的和未酸化的0.1 mol·L-1的FeSO 溶液中通入氧气且
4
搅拌时,pH变化曲线如图。
已知:Fe(OH) 的 ;Fe(OH) 的 ;Fe3+开始沉淀时的pH≈1.5;Fe2+开始沉淀时
3 2
的pH≈6.3
下列说法不正确的是
A.M点对应的溶液中Fe2+水解程度小于P点对应的溶液中Fe2+水解程度
B.导致M点→N点pH升高的反应为:
C.导致P点→Q点pH降低的反应为:
D.O点和Q点后,Fe2+全部转化为Fe(OH) ,不再发生Fe2+的氧化反应
3
【答案】D
【解析】A.H+抑制Fe2+的水解,并且c(H+)越大,对Fe2+水解的抑制作用越大,所以M点对应的溶液中
Fe2+水解程度小于P点对应溶液中Fe2+水解程度,A正确;B.从图中可以看出,酸化的溶液中随着时间的
推移,溶液的pH增大,说明H+参予了反应,pH<1.5时,无Fe(OH) 沉淀生成,则导致M点→N点pH升
3
高的反应为: ,B正确;C.由图可知,未酸化的溶液中,随着时间的推移,
溶液的pH减小,表明有H+生成,P点→Q点时,pH>1.5,Fe3+→Fe(OH) ,反应的离子方程式为:
3
,C正确;D.M点→N点pH升高,发生反应:
,O点pH接近1.7,则Fe3+水解生成Fe(OH) 沉淀,二个反应同时进行,从
3
而导致pH变化不大,所以O点的反应体系中仍发生Fe2+的氧化反应,D不正确;故选D。10.(2023·江苏南京·统考模拟预测)下列铁及其化合物的性质与用途不具有对应关系的是
A.FeCO 受热易分解,可用作补血剂
3
B.Fe粉具有还原性,可用作食品的抗氧化剂
C.Fe O 质地致密,可用作铁件的防腐保护层
3 4
D.KFeO 具有强氧化性,可用于自来水的杀菌消毒
2 4
【答案】A
【解析】A.FeCO 作为补铁剂因为其含有铁元素,A项不具有对应关系;B.铁粉具有还原性,可与O 发
3 2
生反应,所以它作为抗氧化剂,B项具有对应关系;C.Fe O 质地致密可阻止其他物质与铁反应,可用作
3 4
铁件的防腐保护层,C项具有对应关系;D.KFeO 具有强氧化性可对水进行消毒,同时产生的Fe3+产生
2 4
胶体具有吸附水中浮游生物作用,D项具有对应关系;故选A。
考点二 铁及其化合物制备的工艺流程
1.(2023·江苏淮安·淮阴中学校考模拟预测)亚铁氰化钾 是一种黄色颜料。以含铁废水[主
要成分为 ,含少量 , 等]为原料合成亚铁氰化钾的工艺流程如下:
下列说法不正确的是
A.“调pH”时选用的试剂X可以是 或者
B.还原”后可用 溶液检验 是否被完全还原
C.“滤渣Ⅱ”的主要成分是
D.该反应条件下, 的溶解度小于
【答案】B
【分析】含铁废水中含有Fe (SO ) 及少量NiSO ,CuSO 等,向其中加入FeO或NiO,反应消耗溶液中的
2 4 3 4 4
H+,调整溶液pH,弃去滤液,再向固体中同时加入HSO 、Fe,HSO 溶解Fe(OH) 生成Fe3+,Fe与溶液
2 4 2 4 3
中Fe (SO ) 反应产生FeSO ,然后加入NaCN、CaCl ,FeSO 、CaCl 加入反应器后过滤得到滤渣CaSO,
2 4 3 4 2 4 2 4
滤液最后得到KFe(CN) ,说明反应器中还生成NaFe(CN) ,根据元素守恒知还生成NaCl,向滤液中加入
4 6 4 6
NaCO,得到更难溶的CaCO ,在转化罐中加入KCl溶液,过滤、洗涤、干燥得到KFe(CN) ,说明在转
2 3 3 4 6
化罐中发生反应,溶解度大的NaFe(CN) 转化为溶解度较小的KFe(CN) 。
4 6 4 6
【解析】A.由于以含铁废水[主要成分为Fe (SO ),含少量NiSO ,CuSO 等] ,“调pH”时不能引入杂质
2 4 3 4 4
元素,结合废水成分可知选用的试剂X可以是Fe O 或者 ,A正确;B.Fe3+与KSCN作用使溶液
2 3
变为红色,“还原”后加入KSCN溶液,若溶液不变红色,说明Fe3+被完全还原,据此检验Fe3+的存在,
可以检验Fe2+,不能证明 是否被完全还原,B错误;C.由分析可知,“滤渣Ⅱ”的主要成分是 ,C正确;D.由分析可知, 的溶解度小于 ,D正确;故选
B。
2.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)工业上,利用硫酸亚铁为原料,通过铁黄(FeOOH,一
种不溶于水的黄色固体)制备高铁酸钾( ),可降低生产成本且产品质量优。工艺流程如下:
下列说法错误的是
A.制备 的反应类型为复分解反应
B.铁黄制备高铁酸钠的离子方程式为:
C.制备NaClO时,可通过加热的方式加快反应速率
D.高铁酸钾可作水处理剂,既能杀菌消毒,又能吸附絮凝
【答案】C
【分析】硫酸亚铁中+2价的铁具有还原性,氧气具有氧化性,两者反应生成铁黄,反应为:12Fe2+
+3O +2H O=4FeOOH+8Fe3+,氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的化学方程式为:
2 2
Cl+2NaOH═NaCl+NaClO+H O,铁黄和次氯酸钠反应生成高铁酸钠,
2 2
2FeOOH+3NaClO+4NaOH=2Na FeO+3NaCl+3HO,高铁酸钠在溶液中溶解度大于高铁酸钾,加入氯化钾,
2 4 2
高铁酸钠在溶液中转化成高铁酸钾。
【解析】A.制备KFeO 的反应为NaFeO+2KCl=K FeO+2NaCl,为复分解反应,故A正确;B.铁黄和次
2 4 2 4 2 4
氯酸钠反应生成高铁酸钠,2FeOOH+3NaClO+4NaOH=2Na FeO+3NaCl+3HO,离子方程式为:
2 4 2
,故B正确;C.制备NaClO时,加热会反应生成
NaClO,不能得到NaClO,故C错误;D.高铁酸钾可作水处理剂,高铁酸根离子具有强氧化性,能杀菌
3
消毒,同时生成的铁离子水解生成氢氧化铁胶体,能吸附絮凝,故D正确;故选:C。
3.(2023·广东江门·校联考模拟预测)柠檬酸铁铵是一种常见的补铁剂,其制备流程如下:
下列说法错误的是
A.基态Fe原子的价层电子排布式为3d64s2
B.可用铁氰化钾检验Fe2+是否完全转化为Fe3+
C.碳酸根离子和硫酸根离子的空间结构均为正四面体形
D.步骤⑤一系列操作包括蒸发浓缩,冷却结晶,过滤、洗涤,干燥【答案】C
【解析】A.Fe原子序数为26,核外电子排布为 ,价电子排布式为3d64s2,故A正确;B.检验
Fe2+是否完全转化为Fe3+,需要检验亚铁离子是否剩余,可用在待测溶液中加入铁氰化钾观察是否有蓝色
沉淀,故B正确;C.碳酸根离子的空间结构为平面三角形,C项错误;D.步骤⑤是从柠檬酸亚铁铵中得
到晶体的操作,应进行蒸发浓缩,再冷却结晶,然后过滤晶体,洗涤晶体后干燥,故D正确;故选:C。
4.(2023·湖北·校联考模拟预测) 是制备硫化物全固态锂电池高能正极材料的原料。一种制备 材
料的微型流程如下:
下列叙述正确的是
A.“混合溶液”时要用到烧杯、玻璃棒
B.“系列操作”得到的滤液,可再采用分液的方法循环利用
C.“反应器”温度越高,越有利于制备
D.乙醇和硝酸不能存放在同一个橱柜里
【答案】D
【分析】无水乙醇与HF混合,将该混合溶液转移入反应器中加硝酸铁晶体,120℃下发生反应生成FeF;
3
经蒸发浓缩、冷却结晶得到FeF·0.33H O,再在Ar气氛中,经灼烧得到FeF。
3 2 3
【解析】A.“混合溶液”由HF和乙醇组成,HF腐蚀玻璃,因此应选用塑料烧杯盛放,故A错误;
B.“系列操作”得到的滤液中含有乙醇和硝酸,可利用沸点差异采用蒸馏分离回收,故B错误;C.温度
过高导致硝酸铁分解,同时乙醇大量挥发,不利于产物的生成,故C错误;D.乙醇和硝酸分别属于有机
醇类和强酸类,且两者一定条件下能发生反应,因此不能存放在同一橱柜中,故D正确;故选:D。
5.(2023·山东济南·统考三模)生产软磁铁氧体的主要原料是α-FeOOH,以硫铁矿(主要成分是FeS,含
2
少量Al O、SiO 和Fe O)为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的是
2 3 2 3 4
物质
开始沉淀pH(25℃) 1.9 7.6 4.0
沉淀完全pH(25℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成
【答案】B
【分析】硫铁矿焙烧主要发生的反应方程式为:4FeS+11O 2Fe O+8SO,然后加入稀硫酸进行酸浸,
2 2 2 3 2
反应原理有:Fe O+3H SO =Fe (SO )+3H O、Al O+3H SO =Al(SO )+3H O、
2 3 2 4 2 4 3 2 2 3 2 4 2 4 3 2
Fe O+4H SO =Fe (SO )+4H O+FeSO ,然后过滤得到滤渣A,主要成分为SiO,试剂a为还原性铁粉,主
3 4 2 4 2 4 3 2 4 2
要目的为将Fe3+转化为Fe2+,便以后续步骤中除去Al3+,过滤得到滤渣B,主要成分为Fe,加入试剂b调节
溶液pH为5.2~7.6将Al3+完全沉淀,而除去过滤得到滤渣C,主要成分为Al(OH) ,向滤液中主要含有
3
Fe2+加入过氧化氢和氨水,产生沉淀FeOOH,过滤得到滤液D,主要成分为(NH )SO 。
4 2 4
【解析】A.由分析可知,“焙烧”的产物之一SO ,可以转化为SO ,然后SO +H O=HSO ,故可用于
2 3 3 2 2 4
工业制硫酸,A正确;B.由分析可知,“试剂a”的主要目的是将Fe3+完全还原为Fe2+,可以为FeS,但主
要目的不是除去过量硫酸,B错误;C.由分析可知,“试剂b” 的目的为调节溶液pH为5.2~7.6将Al3+完
全沉淀,故可以为氨水,C正确;D.“沉淀”时,pH过高则溶液中的OH-浓度过大,将生成Fe(OH) 沉
3
淀,pH过低即溶液中H+浓度过大,不利于生成 ,D正确;故答案为:B。
考点三 铁及其化合物的有关计算
1.(2023·山东聊城·统考二模)已知Zn及其化合物的性质与Al及其化合物的性质相似。实验室利用废旧
镀锌铁皮(Fe元素的质量分数为z)制备磁性Fe O 胶体粒子的过程为:①碱溶:取xg镀锌铁皮于烧杯中,
3 4
加入足量NaOH溶液,加热、过滤、水洗;②酸溶、氧化:向所得不溶物中加入稀硫酸,调节溶液pH始
终保持在1〜2之间并加入NaClO溶液;③碱溶、分离:再向溶液中滴加NaOH溶液并加热,同时向溶液
中持续通入N,充分反应,分离得到ygFe O 胶体粒子,下列说法正确的是
2 3 4
A.①中“过滤”所得的滤液中含有Zn2+
B.②中“氧化”时加入的NaClO要过量
C.③中“分离”操作中包括过滤
D.Fe O 胶体粒子的产率为
3 4
【答案】D
【分析】由题意可知,制备磁性四氧化三铁胶体粒子的过程为废旧镀锌铁皮中加入足量氢氧化钠溶液共热
碱浸,将锌转化为NaZnO,过滤、水洗得到含有偏锌酸钠的滤液和不溶物;将不溶物加入稀硫酸调节溶
2 2
液pH始终保持在1〜2之间酸溶,将铁转化为亚铁离子后,加入适量次氯酸钠溶液将亚铁离子部分氧化为
铁离子,再向溶液中滴加氢氧化钠溶液并加热,同时向溶液中持续通入氮气充分反应将亚铁离子氧化为四
氧化三铁,用渗析的方法分离得到四氧化三铁胶体粒子。
【解析】A.由分析可知,①中过滤所得的滤液中含有 ,不含有锌离子,故A错误;B.由分析可知,
②中加入适量次氯酸钠溶液的目的是将亚铁离子部分氧化为铁离子,若加入过量次氯酸钠溶液会将亚铁离
子完全氧化为铁离子,不可能碱溶反应得到四氧化三铁,故B错误;C.由分析可知,③中分离操作为用
渗析的方法分离得到四氧化三铁胶体粒子,故C错误;D.由题给数据可知,四氧化三铁胶体粒子的产率为 ×100%= ,故D正确;故选D。
2.(2023·广东梅州·统考三模)价一类二维图和实验是学习元素及其化合物的重要方法。铁及其化合物的
价一类二维图如图所示。下列说法正确的是
A.高温时,a与水蒸气反应转化为c
B.若f、g都是盐酸盐,则这两种物质均可通过化合反应获得
C.d可与足量的HI溶液发生复分解反应得到
D.若b和c的混合物中 ,则b和c的质量比为
【答案】B
【分析】根据铁元素的化合价以及物质种类可知,a为铁单质,b为FeO,c为Fe O,d为Fe(OH) ,e为
2 3 3
Fe(OH) ,f为亚铁盐,g为铁盐,h为高铁酸盐。
2
【解析】A.a为 ,高温时 与水蒸气反应转化为 ,A项错误;B.f、g分别为 、 ,两
者均可通过化合反应获得,即 、 ,B项正确;C.d为氢氧化铁,
可中的+3价铁具有氧化性, 具有还原性,两者发生氧化还原反应生成亚铁盐,得不到铁盐,C
项错误;D.b和c分别为 和 ,设 的物质的量为 , 的物质的量为 ,则有
,解得 ,则 和 的质量比为 ,D项错误;
故选B。
3.(2023·山东烟台·校联考模拟预测)实验室对某铁的氧化物(Fe O)进行如下实验。下列说法错误的是
x
A.
B.溶液A为 和 混合溶液
C.反应②生成标准状况下1.12 LD.Zn至少参加了3个氧化还原反应
【答案】B
【分析】反应①为硫酸和铁的氧化物反应,根据硫酸的物质的量n(H SO )=0.15L×1mol/L=0.15mol结合O
2 4
原子守恒可知,Fe O的物质的量小于等于0.15mol,故有n(Fe O)×(56x+16)=6.08g,解得n(Fe O)=0.1mol时,
x x x
x=0.8,设Fe O中+2价的铁为a个,则+3价的铁为(0.8-a)个,根据化合价之和等于0可知,2a+3(0.8-
x
a)=2,解得a=0.4,即含有Fe2+为0.4,Fe3+为0.4,故6.08gFe O中含有Fe2+为0.04mol,Fe3+为0.04mol,反
x
应①后剩余HSO 为0.15mol-0.1mol=0.05mol,故反应②为Zn+2Fe3+=Zn2++2Fe2+、Zn+2H+=Zn2++H ↑、
2 4 2
Zn+Fe2+=Zn2++Fe。
【解析】A.由分析可知, ,A正确;B.由分析可知,反应②为Zn+2Fe3+=Zn2++2Fe2+、
Zn+2H+=Zn2++H ↑、Zn+Fe2+=Zn2++Fe,根据硫酸根守恒可知,若溶液A为ZnSO 溶液则溶解的Zn的质量为
2 4
0.15mol×65g/mol=9.75g,即Zn过量,说明溶液A中不可能含有FeSO ,B错误;C.由分析可知,反应①
4
后剩余HSO 为0.15mol-0.1mol=0.05mol,反应②中: ,解得V=1.12L,
2 4
即生成标准状况下1.12 L ,C正确;D.由分析可知,反应②为Zn+Fe3+=Zn2++Fe2+、Zn+2H+=Zn2+
+H ↑、Zn+Fe2+=Zn2++Fe,Zn至少参加了3个氧化还原反应,D正确;故答案为:B。
2
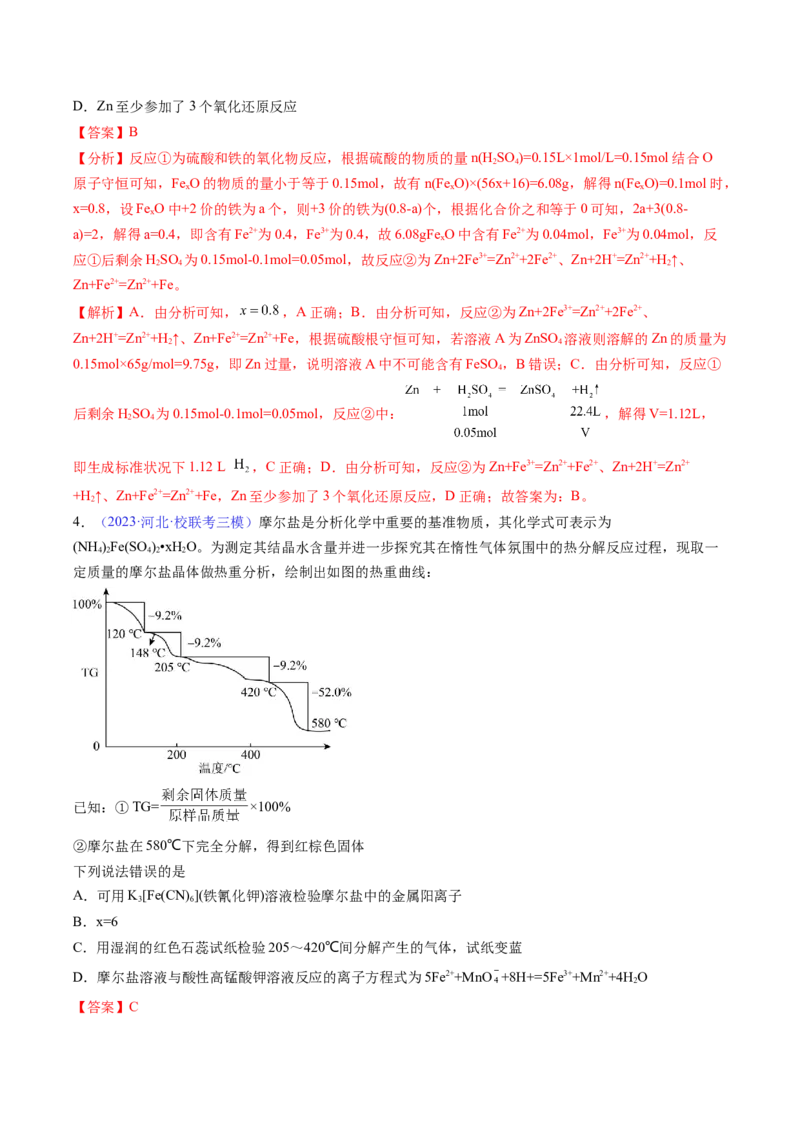
4.(2023·河北·校联考三模)摩尔盐是分析化学中重要的基准物质,其化学式可表示为
(NH )Fe(SO )•xH O。为测定其结晶水含量并进一步探究其在惰性气体氛围中的热分解反应过程,现取一
4 2 4 2 2
定质量的摩尔盐晶体做热重分析,绘制出如图的热重曲线:
已知:①TG= ×100%
②摩尔盐在580℃下完全分解,得到红棕色固体
下列说法错误的是
A.可用K[Fe(CN) ](铁氰化钾)溶液检验摩尔盐中的金属阳离子
3 6
B.x=6
C.用湿润的红色石蕊试纸检验205~420℃间分解产生的气体,试纸变蓝
D.摩尔盐溶液与酸性高锰酸钾溶液反应的离子方程式为5Fe2++MnO +8H+=5Fe3++Mn2++4H O
2
【答案】C【解析】A.摩尔盐中含有的金属阳离子是 ,能用 溶液检验,A正确;B.摩尔盐在
下完全分解,得到的红棕色固体为 ,设 为 ,则根据铁元素守恒可
知,摩尔盐在 下完全分解,得到的 为 ,质量为 ,由图可知,最终
,则最初 摩尔盐的质量为 ,即摩尔盐的
相对分子质量为392,故 ,解得 ,B正确;C.加热首先失去结晶水,失
去全部结晶水时的失重率 ,因为 ,所以 间分
解产生的气体为水,水不能使湿润的红色石蕊试纸变蓝,C错误;D.摩尔盐溶液与酸性高锰酸钾溶液反
应的离子方程式为 ,D正确;故选C。
5.(2023·浙江舟山·统考二模)由铜粉、铁粉、无水硫酸铜粉末组成的混合物22.4g,等分为两份。第一
份投入有足量水的甲烧杯后充分搅拌,最终剩下8.00g 固体;第二份置于乙烧杯中,加入足量的91.5g稀
硫酸,搅拌并充分反应后,杯中留有2.50g红色固体和100g浅绿色溶液(溶液中只含有一种溶质FeSO )。
4
求:
(1)原22.4g混合物中CuSO 的质量
4
(2)乙烧杯溶液中FeSO 的质量分数 。
4
【答案】(1)6.74g (2)18.4%
【解析】(1)由乙杯知:11.2+91.5=102.7(g)
放出H 的质量为:102.7-100-2.5=0.2(g)
2
(溶液中溶质仅为FeSO ,说明发生反应为Fe+Cu2+=Fe2+ +Cu,Fe+ 2H+=Fe2+ +H )
4 2
设甲杯中11.2g混合物中有CuSO Xg,则11.2-X+64X/160-56X/160=8.00g X=3.37g
4
(式中64X/160是被Fe置换出的Cu的量;56X/160是由于置换铜而溶解的Fe的量)
22.4g混合物中CuSO 有3.37×2=6.74g
4
(2)22.4g混合物中,CuSO 质量:3.37×2=6.74g
4
22.4g混合物中,含Fe量:
0.2÷2×56×2+6.74÷160×56=13.55(g)
FeSO 溶液的质量分数为:13.55÷2×152÷56÷100×100%=18.4%
4
或者列出总式正确也得分:(0.2/2 + 3.37/160 )×152÷100×100% = 18.4%