文档内容
专题 13 元素及其化合物知识的综合应用
2020年高考真题
1.(2020年新课标Ⅱ)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,
又是高效、广谱的灭菌消毒剂。回答下列问题:
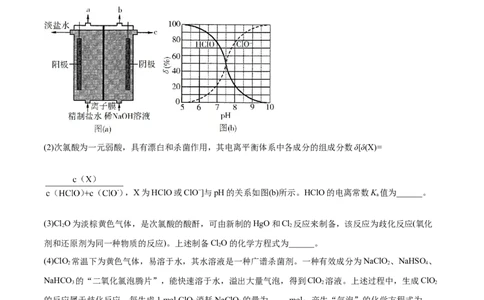
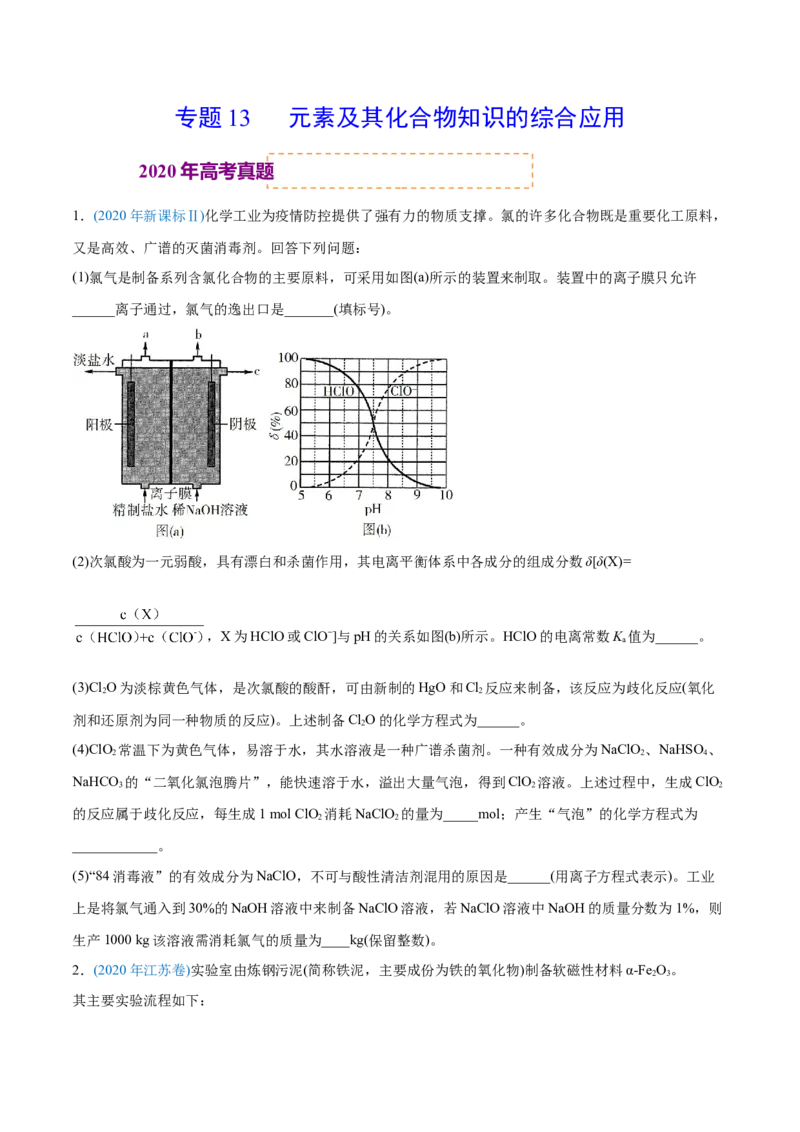
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许
______离子通过,氯气的逸出口是_______(填标号)。
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X)=
,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数K 值为______。
a
(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反应(氧化
2 2
剂和还原剂为同一种物质的反应)。上述制备ClO的化学方程式为______。
2
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO、NaHSO、
2 2 4
NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,生成ClO
3 2 2
的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量为_____mol;产生“气泡”的化学方程式为
2 2
____________。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______(用离子方程式表示)。工业
上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则
生产1000 kg该溶液需消耗氯气的质量为____kg(保留整数)。
2.(2020年江苏卷)实验室由炼钢污泥(简称铁泥,主要成份为铁的氧化物)制备软磁性材料α-Fe O。
2 3
其主要实验流程如下:(1)酸浸:用一定浓度的HSO 溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁
2 4
元素浸出率的有___________(填序号)。
A.适当升高酸浸温度
B.适当加快搅拌速度
C.适当缩短酸浸时间
(2)还原:向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe2+外,
还会生成___________(填化学式);检验Fe3+是否还原完全的实验操作是______________。
(3)除杂:向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀除去。若溶液的pH偏低、将会
4 2
导致CaF 沉淀不完全,其原因是___________[ , ]。
2
(4)沉铁:将提纯后的FeSO 溶液与氨水-NH HCO 混合溶液反应,生成FeCO 沉淀。
4 4 3 3
①生成FeCO 沉淀的离子方程式为____________。
3
②设计以FeSO 溶液、氨水- NHHCO 混合溶液为原料,制备FeCO 的实验方案:__。
4 4 3 3
(FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5)。
3 2
3.(2020年江苏卷)次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。 NaClO可用于
3 3 3 2
制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________;
2
用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用
减弱,其原因是__________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标
准。实验检测原理为
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸
和过量KI溶液,密封在暗处静置5min;用 NaSO 标准溶液滴定至溶液呈微黄色,加入淀
2 2 3
粉指示剂继续滴定至终点,消耗NaSO 溶液20.00mL。
2 2 3
①通过计算判断该样品是否为优质品_______。(写出计算过程,)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________(填“偏高”或“偏低”)。
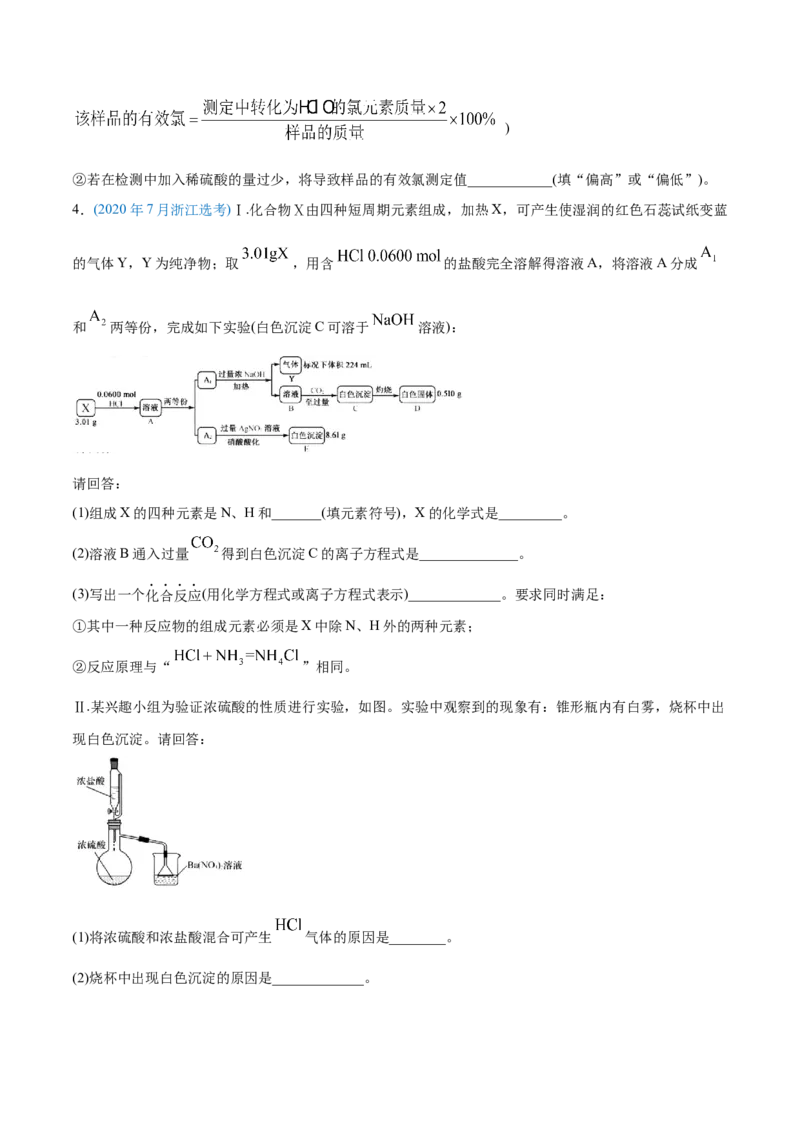
4.(2020年7月浙江选考)Ⅰ.化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝
的气体Y,Y为纯净物;取 ,用含 的盐酸完全溶解得溶液A,将溶液A分成
和 两等份,完成如下实验(白色沉淀C可溶于 溶液):
请回答:
(1)组成X的四种元素是N、H和_______(填元素符号),X的化学式是_________。
(2)溶液B通入过量 得到白色沉淀C的离子方程式是______________。
(3)写出一个化合反应(用化学方程式或离子方程式表示)_____________。要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“ ”相同。
Ⅱ.某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯中出
现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生 气体的原因是________。
(2)烧杯中出现白色沉淀的原因是_____________。2020届高考模拟试题
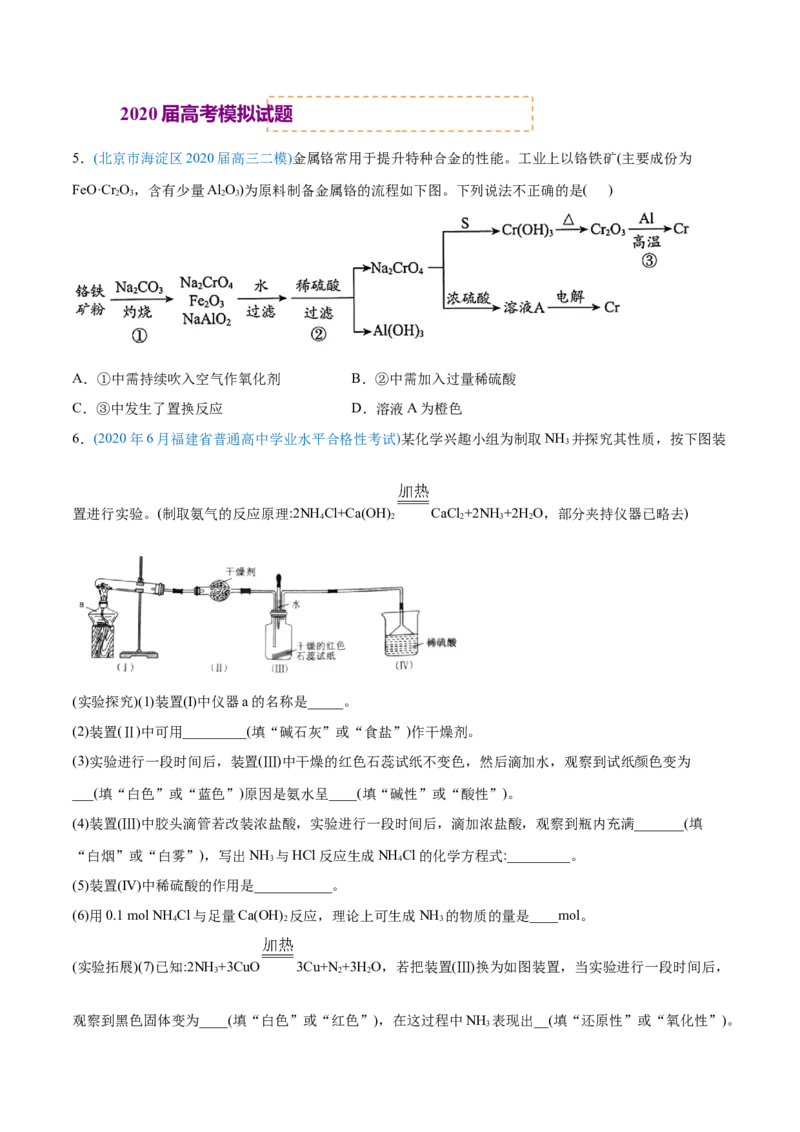
5.(北京市海淀区2020届高三二模)金属铬常用于提升特种合金的性能。工业上以铬铁矿(主要成份为
FeO·Cr O,含有少量Al O)为原料制备金属铬的流程如下图。下列说法不正确的是( )
2 3 2 3
A.①中需持续吹入空气作氧化剂 B.②中需加入过量稀硫酸
C.③中发生了置换反应 D.溶液A为橙色
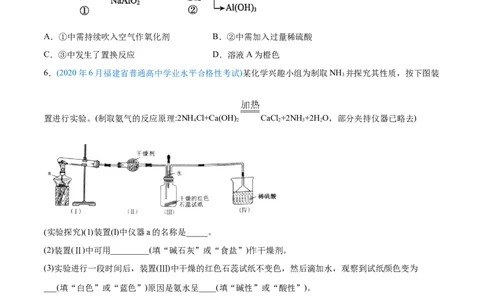
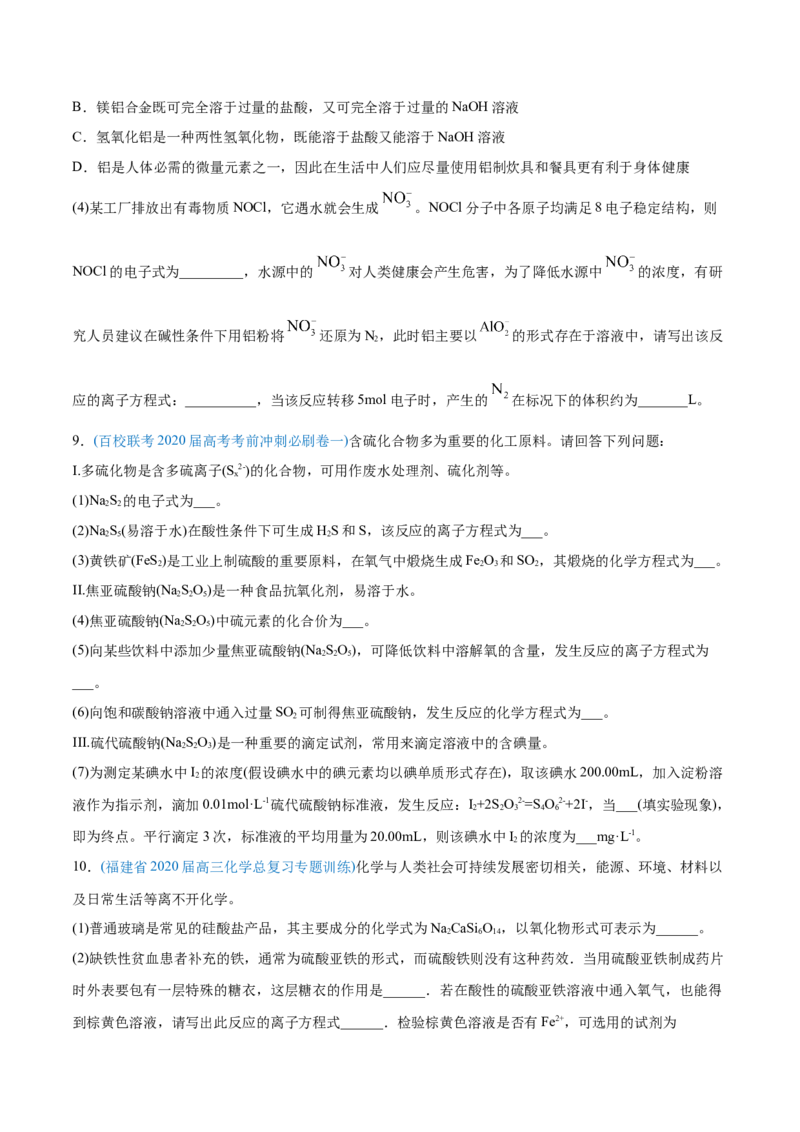
6.(2020年6月福建省普通高中学业水平合格性考试)某化学兴趣小组为制取NH 并探究其性质,按下图装
3
置进行实验。(制取氨气的反应原理:2NHCl+Ca(OH) CaCl +2NH+2H O,部分夹持仪器已略去)
4 2 2 3 2
(实验探究)(1)装置(I)中仪器a的名称是_____。
(2)装置(Ⅱ)中可用_________(填“碱石灰”或“食盐”)作干燥剂。
(3)实验进行一段时间后,装置(Ⅲ)中干燥的红色石蕊试纸不变色,然后滴加水,观察到试纸颜色变为
___(填“白色”或“蓝色”)原因是氨水呈____(填“碱性”或“酸性”)。
(4)装置(Ⅲ)中胶头滴管若改装浓盐酸,实验进行一段时间后,滴加浓盐酸,观察到瓶内充满_______(填
“白烟”或“白雾”),写出NH 与HCl反应生成NH Cl的化学方程式:_________。
3 4
(5)装置(IV)中稀硫酸的作用是___________。
(6)用0.1 mol NH Cl与足量Ca(OH) 反应,理论上可生成NH 的物质的量是____mol。
4 2 3
(实验拓展)(7)已知:2NH+3CuO 3Cu+N +3H O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,
3 2 2
观察到黑色固体变为____(填“白色”或“红色”),在这过程中NH 表现出__(填“还原性”或“氧化性”)。
3(知识应用)(8)氨气是一种重要的化工原料。写出它的一种用途:__________。
7.(安徽省六安市第一中学2020届高三下学期第八次模拟)工业上以铝土矿(主要成分是Al O 和少量的
2 3
SiO、Fe O 杂质)为原料制取铵明矾晶体[NH Al(SO )·12H O]的工艺流程如图所示:
2 2 3 4 4 2 2
请回答下列问题:
(1)试剂I为___;试剂Ⅱ为___;滤渣a的化学式为___。
(2)证明铁元素已全部转化为滤渣b的实验方法是___。
(3)滤液Ⅱ中通入足量CO 进行酸化,从而得到固体c,若用盐酸进行酸化是否可以?___,请说明理由:
2
___。
(4)由固体d制取铵明矾溶液的化学方程式为___,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操
作名称)蒸发浓缩、冷却结晶、___。
(5)NH Al(SO ) 溶液呈___(“酸性”、“碱性”或“中性”),原因是___(用离子方程式表示)。
4 4 2
(6)若NH Al(SO ) 溶液、NH HCO 溶液和NH Cl溶液中的NH +的物质的量浓度相等,则三种铵盐溶液的浓
4 4 2 4 3 4 4
度从小到大的顺序为___。
8.(重庆市巴蜀中学2020届高考适应性月考一)铝(熔点660℃)是一种应用广泛的金属,工业上用 (熔
点2045℃)和冰晶石( )混合熔融后电解制得。请回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,其原因是__________,冶金工业上常用金属铝作还原剂冶炼钒、
铬、锰等金属,请写出铝与VO 在高温下反应的化学方程式:___________。
2 5
(2)将 液和 溶液混合制取 。该实验用于盛装NaF溶液的试剂瓶
_________(填“能”或“不能”)用玻璃瓶,原因是_______。
(3)下列关于铝元素的叙述不正确的是__________(填序号)。
A.铝是人类最早使用的金属B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成 。NOCl分子中各原子均满足8电子稳定结构,则
NOCl的电子式为_________,水源中的 对人类健康会产生危害,为了降低水源中 的浓度,有研
究人员建议在碱性条件下用铝粉将 还原为N,此时铝主要以 的形式存在于溶液中,请写出该反
2
应的离子方程式:__________,当该反应转移5mol电子时,产生的 在标况下的体积约为_______L。
9.(百校联考2020届高考考前冲刺必刷卷一)含硫化合物多为重要的化工原料。请回答下列问题:
I.多硫化物是含多硫离子(S 2-)的化合物,可用作废水处理剂、硫化剂等。
x
(1)Na S 的电子式为___。
2 2
(2)Na S(易溶于水)在酸性条件下可生成HS和S,该反应的离子方程式为___。
2 5 2
(3)黄铁矿(FeS )是工业上制硫酸的重要原料,在氧气中煅烧生成Fe O 和SO ,其煅烧的化学方程式为___。
2 2 3 2
II.焦亚硫酸钠(Na SO)是一种食品抗氧化剂,易溶于水。
2 2 5
(4)焦亚硫酸钠(Na SO)中硫元素的化合价为___。
2 2 5
(5)向某些饮料中添加少量焦亚硫酸钠(Na SO),可降低饮料中溶解氧的含量,发生反应的离子方程式为
2 2 5
___。
(6)向饱和碳酸钠溶液中通入过量SO 可制得焦亚硫酸钠,发生反应的化学方程式为___。
2
III.硫代硫酸钠(Na SO)是一种重要的滴定试剂,常用来滴定溶液中的含碘量。
2 2 3
(7)为测定某碘水中I 的浓度(假设碘水中的碘元素均以碘单质形式存在),取该碘水200.00mL,加入淀粉溶
2
液作为指示剂,滴加0.01mol·L-1硫代硫酸钠标准液,发生反应:I+2S O2-=S O2-+2I-,当___(填实验现象),
2 2 3 4 6
即为终点。平行滴定3次,标准液的平均用量为20.00mL,则该碘水中I 的浓度为___mg·L-1。
2
10.(福建省2020届高三化学总复习专题训练)化学与人类社会可持续发展密切相关,能源、环境、材料以
及日常生活等离不开化学。
(1)普通玻璃是常见的硅酸盐产品,其主要成分的化学式为NaCaSi O ,以氧化物形式可表示为______。
2 6 14
(2)缺铁性贫血患者补充的铁,通常为硫酸亚铁的形式,而硫酸铁则没有这种药效.当用硫酸亚铁制成药片
时外表要包有一层特殊的糖衣,这层糖衣的作用是______.若在酸性的硫酸亚铁溶液中通入氧气,也能得
到棕黄色溶液,请写出此反应的离子方程式______.检验棕黄色溶液是否有Fe2+,可选用的试剂为______(填字母)。
A.稀硝酸B.浓硫酸C.KSCN溶液D.酸性高锰酸钾溶液
(3)从降低成本和减少环境污染的角度考虑,制取硫酸铜最好的方法是______(填字母)。
A.铜和浓硫酸反应 B.铜和稀硫酸反应
C.氧化铜和硫酸反应 D.铜与Fe (SO ) 溶液反应
2 4 3
(4)实验室用硫酸铜晶体配制一定物质的量浓度的硫酸铜溶液,下列操作将使所配溶液物质的量浓度偏高的
是______(填字母)。
A.所用的硫酸铜晶体已经部分风化失水
B.移液时不小心溅出少许溶液
C.容量瓶查漏后未经干燥就直接使用
D.定容时俯视容量瓶刻度线
E.未洗涤烧杯和玻璃棒