文档内容
专题 13 金属材料及金属矿物的开发利用
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 铜及其化合物的结构、性质及应用
考点二 铜及其化合物制备的工艺流程
考点三 金属矿物的开发利用
考点一 铜及其化合物的结构、性质及应用
1.(2023·湖北·统考二模)湖北随州出土的曾侯乙编钟属于青铜制品,先秦《考工记》记载:“金有六齐,
六分其金而锡居其一,谓之钟鼎之齐,……”。下列有关说法错误的是
A.青铜是一种铜锡合金
B.青铜硬度大但熔点比纯铜低
C.用硝酸处理青铜表面的铜锈[主要成分 ]
D.现代工艺采用电解精炼提纯铜,用粗铜作阳极
2.(2023·河北邢台·统考一模)中国古代涉及的“铜”文化丰富多彩。下列说法错误的是
A.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
B.诗句“庐山山南刷铜绿”中的“铜绿”借指的是 的颜色
C.铸造“铜钱儿”用的材料黄铜是单质铜
D.“石胆化铁为铜”中涉及金属键的断裂
3.(2023·上海·模拟预测)在稀硫酸中加入铜粉,铜粉不溶解,再加入物质X后铜粉逐渐溶解,X可能是
A.HCl B.Fe (SO ) C.KS D.FeSO
2 4 3 2 4
4.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)西汉东方朔所撰的《申异经·中荒经》:“西北有宫,
黄铜为墙,题曰地皇之宫”。文中“黄铜”主要成分是铜锌,含少量锡、铅等。下列说法错误的是
A.铜锈的主要成分为 ,俗称铜绿
B.相关金属元素还原性由强到弱的顺序为:Zn>Sn>Pb>Cu
C.黄铜制作的高洪太铜锣应保存在干燥处
D.用灼烧法可区别“黄铜”和黄金首饰
5.(2023·北京西城·北京四中校考模拟预测)10℃时,分别向4支小试管中滴加8滴1mol/LCuSO 溶液,
4
再分别向其中滴加2mol/LNaOH溶液,边滴加边振荡,实验数据及现象如下表:
试管编号 1 2 3 4
12 16
滴加NaOH溶液的量 2滴 6滴
滴 滴
立即观察沉淀的颜色 浅绿色 浅绿色 蓝色 蓝色
1
原创精品资源学科网独家享有版权,侵权必究!酒精灯加热浊液后沉淀的颜色 浅绿色 浅绿色 黑色 黑色
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl 溶液,产生大量白色沉淀。取
2
蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。
下列说法不正确的是
A.由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜
B.CuSO 溶液与NaOH溶液反应时,其相对量不同可以得到不同的产物
4
C.试管3、4中的固体在加热过程中发生了反应:Cu(OH) CuO+HO
2 2
D.取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
6.(2023·福建福州·福州三中校考模拟预测)某同学进行如下实验:
实验 实验现象
溶液变蓝,液面上方呈浅红棕色;至不再产生气泡
ⅰ 将铜粉加入试管中,再加入稀
时,铜粉有剩余,余液呈酸性
ⅱ 继续向ⅰ中试管加入少量固体 又产生气泡,铜粉减少,液面上方呈浅红棕色
取饱和 溶液,加入少量固体
ⅲ 无明显变化
和铜粉
下列说法不正确的是
A. 氧化性的强弱与其浓度大小有关
B.ⅰ、ⅱ中铜粉减少的原因能用相同的离子反应解释
C.ⅰ中余液呈酸性的主要原因是
D.用一定浓度的 与 也能使铜粉溶解
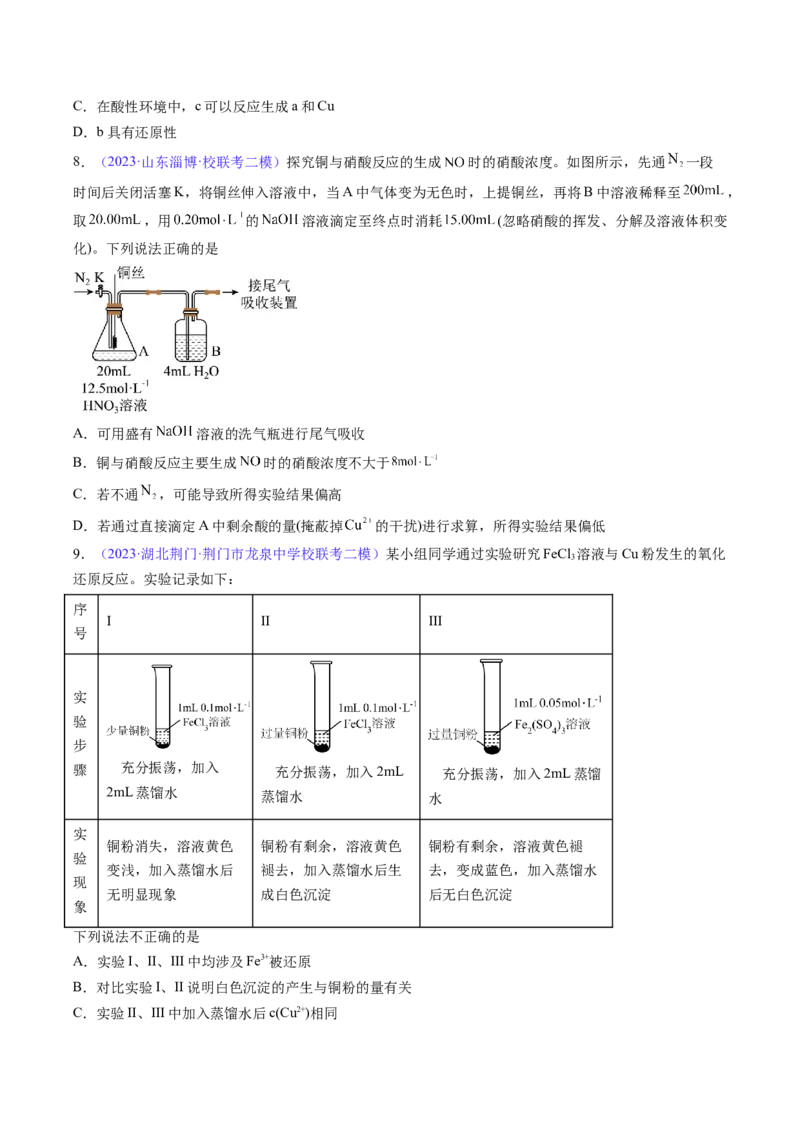
7.(2023·山东·日照一中校联考模拟预测)铜及含铜微粒的价荷图如图所示。下列推断不合理的是
A.要使Cu变成a可以加入稀盐酸和过氧化氢的混合溶液
B. 转化成 需要加碱C.在酸性环境中,c可以反应生成a和Cu
D.b具有还原性
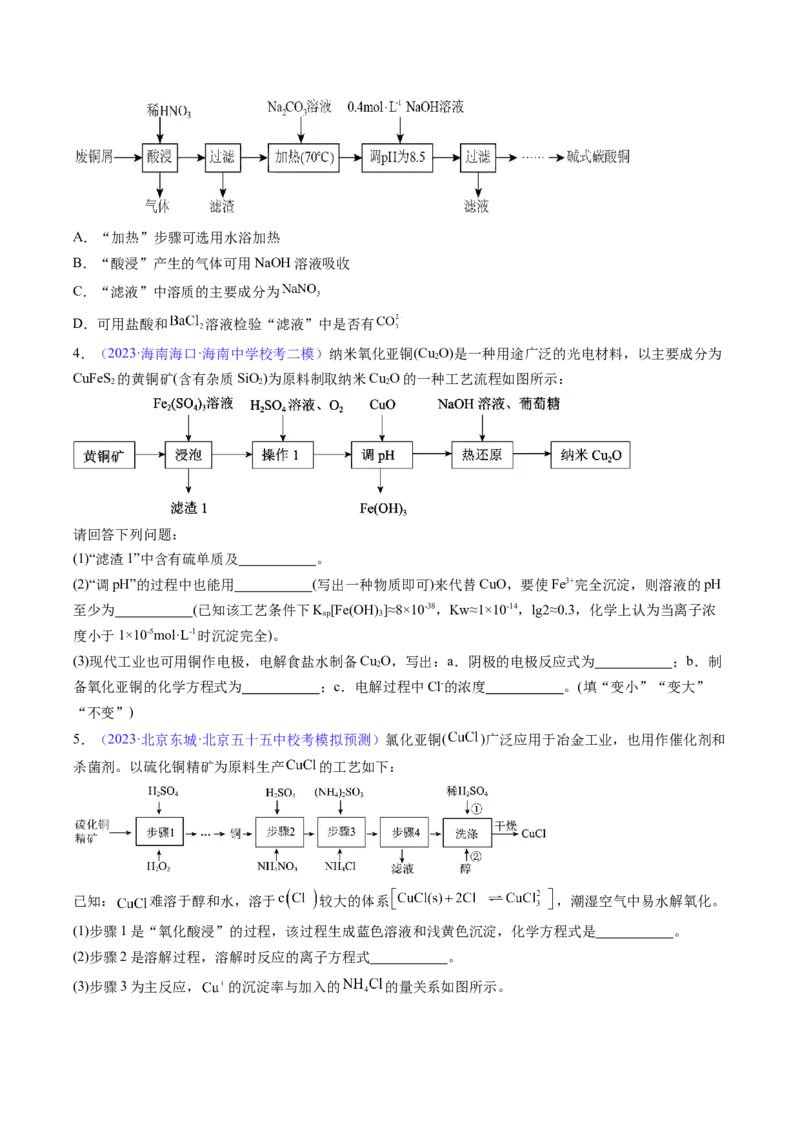
8.(2023·山东淄博·校联考二模)探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通 一段
时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至 ,
取 ,用 的 溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及溶液体积变
化)。下列说法正确的是
A.可用盛有 溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成 时的硝酸浓度不大于
C.若不通 ,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果偏低
9.(2023·湖北荆门·荆门市龙泉中学校联考二模)某小组同学通过实验研究FeCl 溶液与Cu粉发生的氧化
3
还原反应。实验记录如下:
序
I II III
号
实
验
步
骤 充分振荡,加入 充分振荡,加入2mL 充分振荡,加入2mL蒸馏
2mL蒸馏水
蒸馏水 水
实
铜粉消失,溶液黄色 铜粉有剩余,溶液黄色 铜粉有剩余,溶液黄色褪
验
变浅,加入蒸馏水后 褪去,加入蒸馏水后生 去,变成蓝色,加入蒸馏水
现
无明显现象 成白色沉淀 后无白色沉淀
象
下列说法不正确的是
A.实验I、II、III中均涉及Fe3+被还原
B.对比实验I、II说明白色沉淀的产生与铜粉的量有关
C.实验II、III中加入蒸馏水后c(Cu2+)相同D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
10.(2023·辽宁沈阳·东北育才学校校考模拟预测)2.28 g铜镁合金完全溶解于75 mL密度为1.40 g/mL、
质量分数为63%的浓硝酸中,得到 和 的混合气体1680 mL(标准状况),向反应后的溶液中加入
l.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到3.81 g沉淀,下列说法正确的是
A.该合金中,镁的物质的量为0.03 mol
B. 和 混合气体的平均相对分子质量约为55.2
C.得到3.81 g沉淀时,加入NaOH溶液的体积为900 mL
D.该浓硝酸中 的物质的量浓度为12.0 mol/L
考点二 铜及其化合物制备的工艺流程
1.(2023·重庆万州·重庆市万州第二高级中学校考模拟预测)实验室从含有少量氧化铁杂质的废铜粉制取
无水硫酸铜的实验步骤如下图:
下列有关说法正确的是
A.溶解废铜粉“过量酸”是指稀硝酸
B.气体A是Cl,将亚铁离子氧化为铁离子
2
C.生成沉淀D的离子方程式可以为3CuO+2Fe3++3H O=2Fe(OH) ↓+3Cu2+
2 3
D.从溶液中得到的无水硫酸铜的方法是冷却结晶
2.(2023·江苏盐城·盐城市伍佑中学校考模拟预测)一种利用废铜渣(主要成分CuO,及少量 、
等杂质)制备超细铜粉的流程如下:
下列说法正确的是
A.“酸浸”所得滤渣的主要成分为
B.若向“沉铁”后所得滤液中加入乙醇,析出的深蓝色晶体为
C.“沉铜”发生的反应为复分解反应
D.“转化”后所得滤液中含有的主要阳离子: 、 、
3.(2023·山东济宁·统考一模)碱式碳酸铜[Cu (OH) CO]是一种用途广泛的化工原料,实验室中以废铜屑
2 2 3
为原料,制取碱式碳酸铜的流程如下。下列说法错误的是A.“加热”步骤可选用水浴加热
B.“酸浸”产生的气体可用NaOH溶液吸收
C.“滤液”中溶质的主要成分为
D.可用盐酸和 溶液检验“滤液”中是否有
4.(2023·海南海口·海南中学校考二模)纳米氧化亚铜(Cu O)是一种用途广泛的光电材料,以主要成分为
2
CuFeS 的黄铜矿(含有杂质SiO)为原料制取纳米Cu O的一种工艺流程如图所示:
2 2 2
请回答下列问题:
(1)“滤渣1”中含有硫单质及 。
(2)“调pH”的过程中也能用 (写出一种物质即可)来代替CuO,要使Fe3+完全沉淀,则溶液的pH
至少为 (已知该工艺条件下K [Fe(OH) ]≈8×10-38,Kw≈1×10-14,lg2≈0.3,化学上认为当离子浓
sp 3
度小于1×10-5mol·L-1时沉淀完全)。
(3)现代工业也可用铜作电极,电解食盐水制备Cu O,写出:a.阴极的电极反应式为 ;b.制
2
备氧化亚铜的化学方程式为 ;c.电解过程中Cl-的浓度 。(填“变小”“变大”
“不变”)
5.(2023·北京东城·北京五十五中校考模拟预测)氯化亚铜( )广泛应用于冶金工业,也用作催化剂和
杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
已知: 难溶于醇和水,溶于 较大的体系 ,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是 。
(2)步骤2是溶解过程,溶解时反应的离子方程式 。
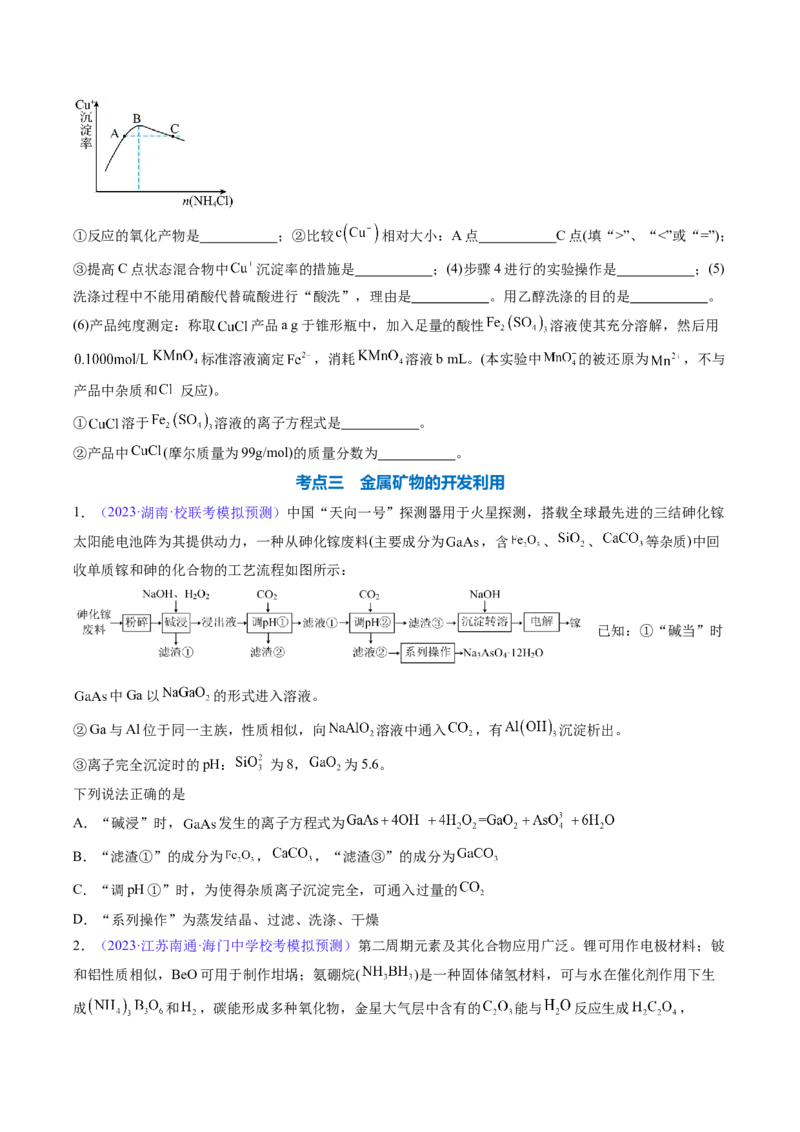
(3)步骤3为主反应, 的沉淀率与加入的 的量关系如图所示。①反应的氧化产物是 ;②比较 相对大小:A点 C点(填“>”、“<”或“=”);
③提高C点状态混合物中 沉淀率的措施是 ;(4)步骤4进行的实验操作是 ;(5)
洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是 。用乙醇洗涤的目的是 。
(6)产品纯度测定:称取 产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
标准溶液滴定 ,消耗 溶液b mL。(本实验中 的被还原为 ,不与
产品中杂质和 反应)。
① 溶于 溶液的离子方程式是 。
②产品中 (摩尔质量为99g/mol)的质量分数为 。
考点三 金属矿物的开发利用
1.(2023·湖南·校联考模拟预测)中国“天向一号”探测器用于火星探测,搭载全球最先进的三结砷化镓
太阳能电池阵为其提供动力,一种从砷化镓废料(主要成分为 ,含 、 、 等杂质)中回
收单质镓和砷的化合物的工艺流程如图所示:
已知:①“碱当”时
中Ga以 的形式进入溶液。
②Ga与Al位于同一主族,性质相似,向 溶液中通入 ,有 沉淀析出。
③离子完全沉淀时的pH: 为8, 为5.6。
下列说法正确的是
A.“碱浸”时, 发生的离子方程式为
B.“滤渣①”的成分为 , ,“滤渣③”的成分为
C.“调pH①”时,为使得杂质离子沉淀完全,可通入过量的
D.“系列操作”为蒸发结晶、过滤、洗涤、干燥
2.(2023·江苏南通·海门中学校考模拟预测)第二周期元素及其化合物应用广泛。锂可用作电极材料;铍
和铝性质相似,BeO可用于制作坩埚;氨硼烷( )是一种固体储氢材料,可与水在催化剂作用下生
成 和 ,碳能形成多种氧化物,金星大气层中含有的 能与 反应生成 ,是二元弱酸,有还原性,可与多种金属离子形成沉淀或络合物;聚四氟乙烯材料可制作酸碱通用
滴定管的活塞及化工反应器的内壁涂层。下列物质性质与用途具有对应关系的是
A.金属Li密度小,可用作电极材料
B.BeO硬度大,可制作耐高温的坩埚
C. 有还原性,可用作沉淀剂、络合剂
D.聚四氟乙烯耐酸碱腐蚀,可制作滴定管活塞
3.(2023·山东德州·统考二模)四氟硼酸锂( )化学性质稳定,可用作锂电(心脏起搏器电池等)或二次
锂离子电池电解液导电盐。其制备流程如图所示,下列说法错误的是
A.“不溶颗粒”主要成分为
B.实验室中模拟工艺流程时反应器3不能选用三颈圆底烧瓶
C.反应器2中反应为
D.粗产品经过负压下浓缩、冷却结晶即可得到纯净的四氟硼酸锂
4.(2023·河北邯郸·统考一模)“太空金属”钛广泛应用于新型功能材料等方面,工业上用钛铁矿(主要
成分是TiO,含少量FeO和Fe O)冶炼金属钛的工艺流程如图所示,下列说法正确的是
2 2 3
A.基态钛原子核外有4个未成对电子
B.金属Mg与TiCl 可在氮气气氛条件下进行反应
4
C.步骤II加热可促进TiO2+的水解
D.步骤III中可能发生的反应为TiO+2Cl+C TiCl +CO
2 2 4
5.(2023·福建·统考模拟预测)化学与生产生活密切相关,下列说法不正确的是
A.在室外大雪的时候 可以用作融雪剂,原因是因为其溶解的时候可以放热
B.铬是硬度最高的金属,常在不锈钢中添加
C. 为半导体,可做新型太阳能电池主要材料
D.氧化镁在工业生产中常用作耐火材料6.(2023·全国·模拟预测)实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的
化合价变化如图乙。已知:深蓝色溶液中生成了CrO。
5
下列说法正确的是
A.0~5s过程中,发生的离子反应为:
B.实验开始至30s,溶液中发生的总反应离子方程式为
C.30~80s过程中,Cr元素被氧化,可能是溶解的氧气和剩余的HO 所致
2 2
D.0s~80s时,溶液中含铬微粒依次发生氧化反应、还原反应和氧化反应