文档内容
专题 16 硫及其化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 硫及其化合物的结构、性质及应用
考点二 硫及其化合物制备的工艺流程
考点三 硫及其化合物的有关计算
考点一 硫及其化合物的结构、性质及应用
1.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)下列叙述正确的是
A. 和 均能通过金属单质与S化合制得
B. 与 分别通入到石蕊溶液中现象相同
C.一定条件下,NO和 均能转化成
D.常温下,浓硫酸和浓硝酸均能与Cu反应产生大量气体
【答案】C
【解析】A.Cu和S反应生成Cu S,故A错误;B. 通入到石蕊溶液中生成亚硫酸,溶液变红色;
2
通入到石蕊溶液中生成HCl和HClO,HClO具有漂白性,现象是溶液先变红后褪色,故B错误;C.NO
和O 混合后通入水中能够生成 , 和水反应生成 和NO,一定条件下,NO和 均能转
2
化成 ,故C正确;D.常温下,浓硫酸和Cu不反应,故D错误;故选C。
2.(2023·海南海口·海南华侨中学校考二模)硫及其化合物在工业生产中多有涉及。下列有关说法正确的
是
A.硫在过量的氧气中燃烧直接生成 B.将 通入 溶液中有白色沉淀生成
C. 的无水固体粉末显蓝色 D. 和 反应可生成S
【答案】D
【解析】A.硫燃烧只能得到 ,A项错误;B.盐酸的酸性大于亚硫酸的酸性,故 不与 溶液
反应,B项错误;C.无水 为白色,C项错误;D. 与 反应生成S、 ,D项正确;故选
D。
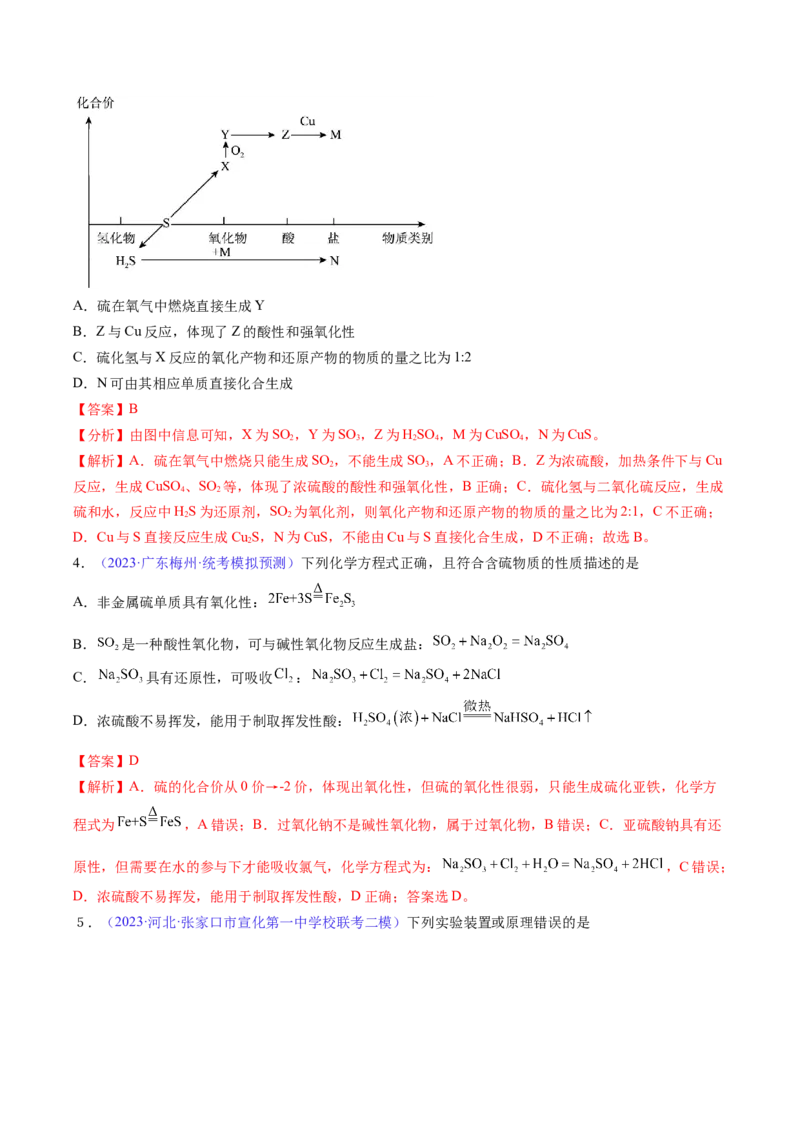
3.(2023·上海嘉定·统考一模)硫及其化合物的“价—类”二维图体现了化学变化之美。下列有关说法正
确的是
1
原创精品资源学科网独家享有版权,侵权必究!A.硫在氧气中燃烧直接生成Y
B.Z与Cu反应,体现了Z的酸性和强氧化性
C.硫化氢与X反应的氧化产物和还原产物的物质的量之比为1:2
D.N可由其相应单质直接化合生成
【答案】B
【分析】由图中信息可知,X为SO ,Y为SO ,Z为HSO ,M为CuSO ,N为CuS。
2 3 2 4 4
【解析】A.硫在氧气中燃烧只能生成SO ,不能生成SO ,A不正确;B.Z为浓硫酸,加热条件下与Cu
2 3
反应,生成CuSO 、SO 等,体现了浓硫酸的酸性和强氧化性,B正确;C.硫化氢与二氧化硫反应,生成
4 2
硫和水,反应中HS为还原剂,SO 为氧化剂,则氧化产物和还原产物的物质的量之比为2:1,C不正确;
2 2
D.Cu与S直接反应生成Cu S,N为CuS,不能由Cu与S直接化合生成,D不正确;故选B。
2
4.(2023·广东梅州·统考模拟预测)下列化学方程式正确,且符合含硫物质的性质描述的是
A.非金属硫单质具有氧化性:
B. 是一种酸性氧化物,可与碱性氧化物反应生成盐:
C. 具有还原性,可吸收 :
D.浓硫酸不易挥发,能用于制取挥发性酸:
【答案】D
【解析】A.硫的化合价从0价→-2价,体现出氧化性,但硫的氧化性很弱,只能生成硫化亚铁,化学方
程式为 ,A错误;B.过氧化钠不是碱性氧化物,属于过氧化物,B错误;C.亚硫酸钠具有还
原性,但需要在水的参与下才能吸收氯气,化学方程式为: ,C错误;
D.浓硫酸不易挥发,能用于制取挥发性酸,D正确;答案选D。
5.(2023·河北·张家口市宣化第一中学校联考二模)下列实验装置或原理错误的是A.制取SO B.验证漂白性 C.验证还原性 D.验证氧化性
2
【答案】B
【解析】A.铜与浓硫酸发生反应 可产生SO ,A正确;B.SO 使
2 2
酸性高锰酸钾褪色体现了SO 的还原性,B错误;C.SO 还原Fe3+得到亚铁离子,使溶液中的血红色消失,
2 2
体现了SO 的还原性,C正确;D.SO 与NaS发生氧化还原反应,产生淡黄色沉淀S,体现了SO 的氧化
2 2 2 2
性,D正确。故选B。
6.(2023·广东汕头·统考三模)硫及其化合物在生活中应用广泛,下列有关离子方程式书写正确的是
A.往亚硫酸中逐步通入 气体:
B.往 溶液中滴加盐酸:
C.往 溶液中通入过量 :
D.实验室利用 制备 :
【答案】B
【解析】A.HSO 是二元弱酸,离子方程式书写时不能拆,故往亚硫酸中逐步通入 气体,无自由移动
2 3
的离子参加反应,无离子方程式,其化学方程式为: ,A错误;B.往
溶液中滴加盐酸生成SO 、S和NaCl、HO,该反应的离子方程式为:
2 2
,B正确;C.往 溶液中通入过量 生成NaHSO,该反应的离子
3
方程式为: ,C错误;D.实验室利用 和70%的浓硫酸反应制备 ,该反应的离
子方程式为: ,D错误;故答案为:B。
7.(2023·江苏扬州·扬州中学校考模拟预测)实验室进行SO 性质探究,下列实验原理和装置不能达到
2
实验目的的是A.制取SO B.探究溶解性
2
C.探究氧化性 D.吸收尾气SO
2
【答案】A
【解析】A.铜与浓硫酸共热反应生成硫酸铜、二氧化硫和水,题给装置缺少酒精灯,不能用于制备二氧
化硫,故A错误;B.二氧化硫易溶于水,将充满二氧化硫的试管倒扣在水中,二氧化硫溶解导致试管中
压强减小,水会进入试管中,则题给装置能用于探究二氧化硫的溶解性,故B正确;C.二氧化硫具有弱
氧化性,能与氢硫酸溶液反应生成硫沉淀和水,则题给装置能用于探究二氧化硫的氧化性,故C正确;
D.二氧化硫是酸性氧化物,能与氢氧化钠溶液反应生成亚硫酸钠和水,则题给装置能用于吸收二氧化氯,
防止污染空气,故D正确;故选A。
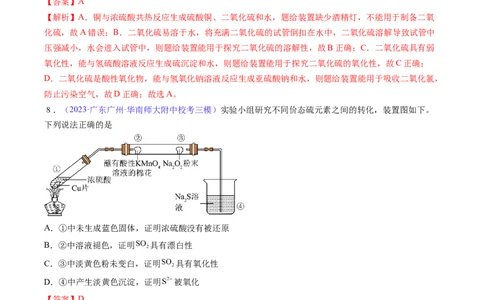
8.(2023·广东广州·华南师大附中校考三模)实验小组研究不同价态硫元素之间的转化,装置图如下。
下列说法正确的是
A.①中未生成蓝色固体,证明浓硫酸没有被还原
B.②中溶液褪色,证明 具有漂白性
C.③中淡黄色粉未变白,证明 具有氧化性
D.④中产生淡黄色沉淀,证明 被氧化
【答案】D
【分析】铜和浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,浓硫酸体现强氧化性、酸性,浓硫酸
还会吸收生成的水,二氧化硫能使酸性高锰酸钾溶液褪色,与过氧化钠反应生成白色固体,通入硫化钠溶
液中出现浑浊。
【解析】A.①中由于浓硫酸会吸收水分,而且反应是复杂的,不一定能看到有蓝色,但浓硫酸反应生成
二氧化硫,说明浓硫酸被还原,故A错误;B.②中溶液褪色,是二氧化硫 酸性高锰酸钾溶液发生氧化还
原反应,证明 具有还原性,故B错误;C.③中淡黄色粉未变白,是过氧化钠和二氧化硫反应生成硫
酸钠,证明 具有还原性,故C错误;D.④中产生淡黄色沉淀,沉淀是二氧化硫和硫离子反应生成硫
单质,硫化钠中硫化合价升高,证明 被氧化,故D正确。综上所述,答案为D。9.(2023·上海静安·统考二模)自然界与人类活动对硫的循环均能产生影响。下列说法错误的是
A.火山口温度过高,附近的单质硫会被O 直接氧化为SO
2 3
B.大气中的SO 会形成酸雨,最终以HSO 进入地面或海洋
2 2 4
C.工业排放的SO 尾气可与CaO和O 反应生成CaSO
2 2 4
D.常温下,浓HSO 能使铁片钝化是由于其具有强氧化性
2 4
【答案】A
【解析】A.单质硫与O 反应只能变为SO ,SO 和O 在催化剂、加热条件下可逆反应生成SO ,故A错
2 2 2 2 3
误;B.大气中的SO 会形成酸雨,二氧化硫和水反应生成亚硫酸,亚硫酸钡氧气氧化为硫酸,因此最终
2
以HSO 进入地面或海洋,故B正确;C.工业排放的SO 尾气可与CaO和O 反应生成CaSO,因此常用
2 4 2 2 4
氧化钙处理工业排放的SO 尾气,故C正确;D.浓硫酸具有强氧化性,因此常温下,浓HSO 能使铁片
2 2 4
钝化,故D正确。
综上所述,答案为A。
10.(2023·上海宝山·统考一模)下列关于硫及其化合物的说法正确的是
A.硫单质易溶于水
B. 通入 溶液中生成 沉淀
C. 可作钡餐
D.浓硫酸可保存在铁罐中
【答案】D
【解析】A.硫单质难溶于水,微溶于酒精,故A错误;B.亚硫酸的酸性弱于盐酸,二氧化硫不能与氯
化钡溶液反应,故B错误;C.碳酸钡能与胃液中的盐酸反应生成有毒的氯化钡,不能做钡餐,故C错误;
D.铁在浓硫酸发生钝化,反应生成的致密氧化层薄膜阻碍反应的继续进行,所以浓硫酸可保存在铁罐中,
故D正确;故选D。
考点二 硫及其化合物制备的工艺流程
1.(2023·湖南邵阳·统考二模)某化学兴趣小组设计一种从硫矿石(主要成分为硫黄及少量FeS)中提取硫
2
黄的方法如下:
查阅资料:S的熔点为115.2℃; 的沸点为46.2℃。
下列说法错误的是
A.单质硫是分子晶体
B.过程①中 可用乙醇代替
C.过程③的目的是使 挥发,同时使硫从水中析出D.将趁热过滤所得滤渣煅烧: ,反应中每生成1 mol ,转移电子的物
质的量为5.5 mol
【答案】B
【分析】将硫矿石粉碎,在120℃条件下将S变为液体,过滤,得到液态硫,再加入二硫化碳进行萃取,
过滤,用70~75℃的热水淋浴,将 变为气态,而液态硫变为固态,经过一系列过程得到纯硫。
【解析】A.硫是非金属单质,单质硫是分子晶体,故A正确;B.硫是难溶于水,微溶于酒精,易溶于
,因此过程①中 不可用乙醇代替,故B错误;C.S的熔点为115.2℃; 的沸点为46.2℃,因此
过程③的目的是使 挥发,同时使硫从水中析出,故C正确;D.将趁热过滤所得滤渣煅烧:
,根据方程式分析,生成8mol ,转移44mol电子,因此反应中每生成
1 mol ,转移电子的物质的量为5.5 mol,故D正确。综上所述,答案为B。
2.(2023·湖南长沙·长沙市明德中学校考模拟预测)硫代硫酸钠(Na SO)可用做分析试剂及鞣革还原剂。
2 2 3
它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠 的装置
如下。下列说法错误的是
A.b中反应的离子方程式为 或
B.c中试剂为硫化钠和碳酸钠混合溶液
C.为了保证硫代硫酸钠的产量,实验中通入的SO 必须过量
2
D.d中试剂可以是NaOH溶液也可以是HO
2 2
【答案】C
【分析】b中产生二氧化硫,通入装置c中,与硫化钠和碳酸钠的混合溶液发生反应制备硫代硫酸钠,二氧化硫有刺激性气
味,有毒,因此d是尾气处理装置;
【解析】A.可以用70%的浓硫酸制备二氧化硫,b中反应的离子方程式可表示为 或
,A项正确;B.在c中发生反应: ,故c中试剂为
硫化钠和碳酸钠的混合液,B项正确;C.若通入的二氧化硫过量,则溶液显酸性,硫代硫酸钠会分解,C项错误;D.d是
尾气处理装置,目的是除去二氧化硫,则可以是NaOH溶液也可以是 ,D项正确;答案选C。
3.(2023·河北·校联考三模)硫化锂(Li S)是一种潜在的锂电池的电解质材料,某化学兴趣小组选择下列
2
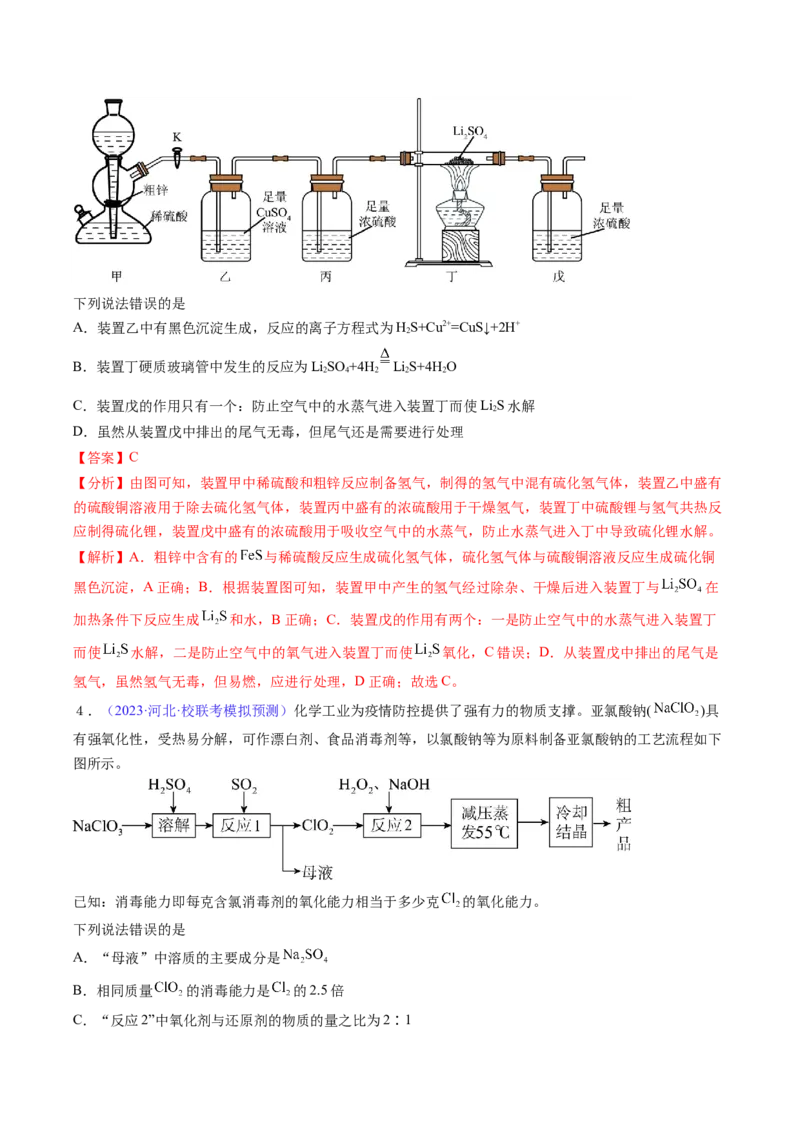
实验装置制备硫化锂。已知:粗锌中含少量Cu和FeS;LiS易潮解、易水解,在加热条件下易被氧化。
2下列说法错误的是
A.装置乙中有黑色沉淀生成,反应的离子方程式为HS+Cu2+=CuS↓+2H+
2
B.装置丁硬质玻璃管中发生的反应为LiSO +4H LiS+4HO
2 4 2 2 2
C.装置戊的作用只有一个:防止空气中的水蒸气进入装置丁而使LiS水解
2
D.虽然从装置戊中排出的尾气无毒,但尾气还是需要进行处理
【答案】C
【分析】由图可知,装置甲中稀硫酸和粗锌反应制备氢气,制得的氢气中混有硫化氢气体,装置乙中盛有
的硫酸铜溶液用于除去硫化氢气体,装置丙中盛有的浓硫酸用于干燥氢气,装置丁中硫酸锂与氢气共热反
应制得硫化锂,装置戊中盛有的浓硫酸用于吸收空气中的水蒸气,防止水蒸气进入丁中导致硫化锂水解。
【解析】A.粗锌中含有的 与稀硫酸反应生成硫化氢气体,硫化氢气体与硫酸铜溶液反应生成硫化铜
黑色沉淀,A正确;B.根据装置图可知,装置甲中产生的氢气经过除杂、干燥后进入装置丁与 在
加热条件下反应生成 和水,B正确;C.装置戊的作用有两个:一是防止空气中的水蒸气进入装置丁
而使 水解,二是防止空气中的氧气进入装置丁而使 氧化,C错误;D.从装置戊中排出的尾气是
氢气,虽然氢气无毒,但易燃,应进行处理,D正确;故选C。
4.(2023·河北·校联考模拟预测)化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠( )具
有强氧化性,受热易分解,可作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
图所示。
已知:消毒能力即每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
下列说法错误的是
A.“母液”中溶质的主要成分是
B.相同质量 的消毒能力是 的2.5倍
C.“反应2”中氧化剂与还原剂的物质的量之比为2∶1D.“减压蒸发”可以降低蒸发时的温度,提高产品产率
【答案】B
【分析】由题给流程可知,反应1为二氧化硫与稀硫酸、氯酸钠反应生成硫酸钠、二氧化氯和水,反应2
为二氧化氯与过氧化氢、氢氧化钠混合溶液反应生成亚氯酸钠、氧气和水,反应得到的亚氯酸钠在55℃条
件下减压蒸发、冷却结晶、过滤得到亚氯酸钠粗产品。
【解析】A.根据元素转化分析可知“母液”中溶质的主要成分是 ,A项正确;B.1 mol 完全
反应转化2 mol ,1 mol 完全反应转化5 mol ,所以等物质的量 的消毒能力是 的2.5倍,
B项错误;C.“反应2”中发生反应的化学方程式为 ,氧
化剂与还原剂的物质的量之比为2∶1,C项正确;D.温度过高, 会分解,所以采用“减压蒸发”
可以降低蒸发时的温度,提高产品产率,D项正确;故选B。
5.(2023·江苏·模拟预测)实验室模拟制备亚硝酰硫酸( )的反应装置如图所示。已知:亚硝酰硫
酸溶于硫酸,遇水易分解。下列说法错误的是
A.装置A中应使用70%的浓硫酸
B.装置B、D中浓硫酸作用不同
C.装置C中反应为
D.虚线框内的装置可以换为盛有碱石灰的干燥管
【答案】B
【分析】利用亚硫酸钠固体和硫酸反应制备二氧化硫气体,为防止亚硝酰硫酸遇水分解,故在干燥的条件
下制备亚硝酰硫酸,最后尾气吸收过量二氧化硫,防止污染空气。
【解析】A.利用亚硫酸钠固体和硫酸反应制备二氧化硫气体,98%的浓硫酸的很难电离出H+,故一般选
用70%的硫酸,A正确;B.亚硝酰硫酸遇水易分解,装置B中的浓硫酸的作用是干燥SO 气体,防止水
2
蒸气进入装置C中,装置D中的浓硫酸的作用是防止装置E中的水蒸气进入装置C中,B错误;C.装置
C中反应为 ,C正确;D.虚线框内的装置可以换为盛有碱石灰的干燥管,既可以
吸收尾气又可以防止空气中的水蒸气进入装置C,D正确;故选B。
考点三 硫及其化合物的有关计算1.(2023·上海金山·统考二模)将一定量锌与100 mL 18 mol∙L−1的浓硫酸充分反应,锌完全溶解时产生
0.8 mol气体(不考虑气体在溶液中的溶解),将反应后的溶液稀释至400 mL,测得溶液中c(H+)=x mol∙L−1,
则下列叙述错误的是
A.共消耗锌48.0 g B.共转移电子1.6 mol
C.气体中 D.生成气体体积约为17.92 L(STP)
【答案】A
【解析】A.根据Zn+2HSO (浓)=ZnSO+SO ↑+2HO、Zn+HSO =ZnSO+H↑,无论那个反应,产
2 4 4 2 2 2 4 4 2
生气体与消耗锌的物质的量之比为1:1,产生0.8 mol气体,则共消耗锌物质的量为0.8mol,质量为
0.8mol×65g∙mol−1=52.0 g,故A错误;B.根据A选项分析消耗0.8mol锌,则共转移电子1.6 mol,故B正
确;C.100 mL 18 mol∙L−1的浓硫酸,其物质的量为1.8mol,将反应后的溶液稀释至400 mL,测得溶液中
c(H+)=x mol∙L−1,则剩余硫酸物质的量为0.2xmol,共消耗硫酸物质的量为(1.8−0.2x)mol,设生成氢气物质
的量为mmol,生成二氧化硫气体物质的量为nmol,则有m+n=0.8,m+2n=1.8−0.2x,解得n=1−0.2x,
m=0.2x−0.2,则气体中 ,故C正确;D.根据产生0.8 mol气体,则生成气体体积约为
0.8mol×22.4L∙mol−1=17.92 L(STP),故D正确。
综上所述,答案为A。
2.(2023·广东肇庆·高要一中校考二模)对下列事实的解释正确的是
A.二氧化硫气体能用浓硫酸干燥,是因为二氧化硫无还原性
B.医疗上可用硫酸钡作钡餐,是因为硫酸钡可以阻挡X射线通过且不溶于强酸
C.向50 mL 18 mol·L-1的HSO 溶液中加入足量的铜片加热充分反应后,被还原的HSO 的物质的量等于
2 4 2 4
0.45 mol
D.常温下,浓HSO 可以用铝制容器贮存,说明铝与浓HSO 不反应
2 4 2 4
【答案】B
【解析】A.二氧化硫具有还原性,但不能被浓硫酸氧化,故A错误;B.硫酸钡作X射线透视肠胃的内
服药是因为硫酸钡不溶于盐酸,故B正确;C.因随着反应的进行,硫酸的浓度降低,稀硫酸不能与铜反
应,被还原的HSO 的物质的量小于0.45 mol,故C错误;D.因常温下浓硫酸使铝钝化(化学变化),
2 4
形成致密的氧化膜阻碍了反应的继续进行,故D错误;故选B。
3.(2023·山东泰安·统考一模)已知NaSO +S= Na SO,实验室用下述方法制备 固体:①铜和
2 3 2 2 3
浓硫酸加热产生 ;②将 通入含 和 的混合溶液,溶液先变浑浊,后逐渐澄清,反应结
束;③将溶液经浓缩结晶、过滤洗涤等操作得到 产品。下列说法错误的是
A.①中消耗 转移
B.②中溶液先变浑浊的原因:2NaS+3SO= 2Na SO +3S↓
2 2 2 3
C.为提高产品的纯度,混合液中 的最佳比例为1∶2
D.用适量 溶液吸收②中逸出的 、 气体,吸收液可直接返回到步骤②【答案】C
【解析】A.①中反应为 ,电子转移为: ,消耗
转移 ,A正确;B.硫离子具有还原性,②中溶液先变浑浊的原因二氧化硫和硫离子反应
生成硫单质,B正确;C.NaSO +S= Na SO,亚硫酸酸钠和硫反应物质的量为1:1;由反应可知,
2 3 2 2 3
2NaS+3SO= 2Na SO +3S,该反应生产亚硫酸酸钠和硫反应物质的量为2:3;故还需要1份碳酸钠和二氧
2 2 2 3
化硫生成1份亚硫酸钠,故混合液中 的最佳比例为2:1,C错误;D.氢氧化钠和二氧
化碳、二氧化硫反应分别生成碳酸钠、亚硫酸钠,吸收液可直接返回到步骤②循环利用,D正确;故选
C。
4.(2023·重庆万州·重庆市万州第二高级中学校考模拟预测)某学习小组探究铁丝(含杂质碳)与浓硫酸的
反应,反应装置如下图。下列说法错误的是
A.无法直接使用pH试纸来判断反应后硫酸是否剩余
B.可用KSCN和K[Fe(CN) ]检验反应后溶液中铁元素的价态
3 6
C.将22.4mL(标准状况下)反应生成的气体通入足量氯水中,再滴加足量BaCl 溶液,最终得到0.233g沉
2
淀
D.生成的气体通入BaCl 溶液产生白色浑浊,可能是硫酸蒸气逸出或部分SO 被氧化所致
2 2
【答案】C
【分析】铁和浓硫酸在加热的条件下反应生成硫酸铁、二氧化硫、水,随着反应的进行,浓硫酸变稀,铁
和稀硫酸反应生成硫酸亚铁和氢气。
【解析】A.生成物中含有SO ,SO 溶于水生成HSO ,使溶液显酸性,因此不能直接使用pH试纸来判
2 2 2 3
断反应后硫酸是否剩余,A项正确;B.K[Fe(CN) ]与Fe2+作用产生蓝色沉淀,K[Fe(CN) ]可检验Fe2+,
3 6 3 6
KSCN与Fe3+作用,溶液变红色,KSCN可检验Fe3+,B项正确;C.反应生成的气体中含有SO 、H,混
2 2
合气体的总物质的量为 ,若气体都为SO ,根据S元素守恒,生成沉淀的物质的量为
2
0.001mol,则产生沉淀的质量为 ,但实际上,SO 物质的量小于0.001mol,则
2
沉淀质量小于0.233g,C项错误;D.生成的气体通入BaCl 溶液,由于硫酸蒸气逸出或部分SO 被氧化生
2 2
成 ,会和Ba2+反应生成BaSO 白色沉淀,D项正确;答案选C。
4
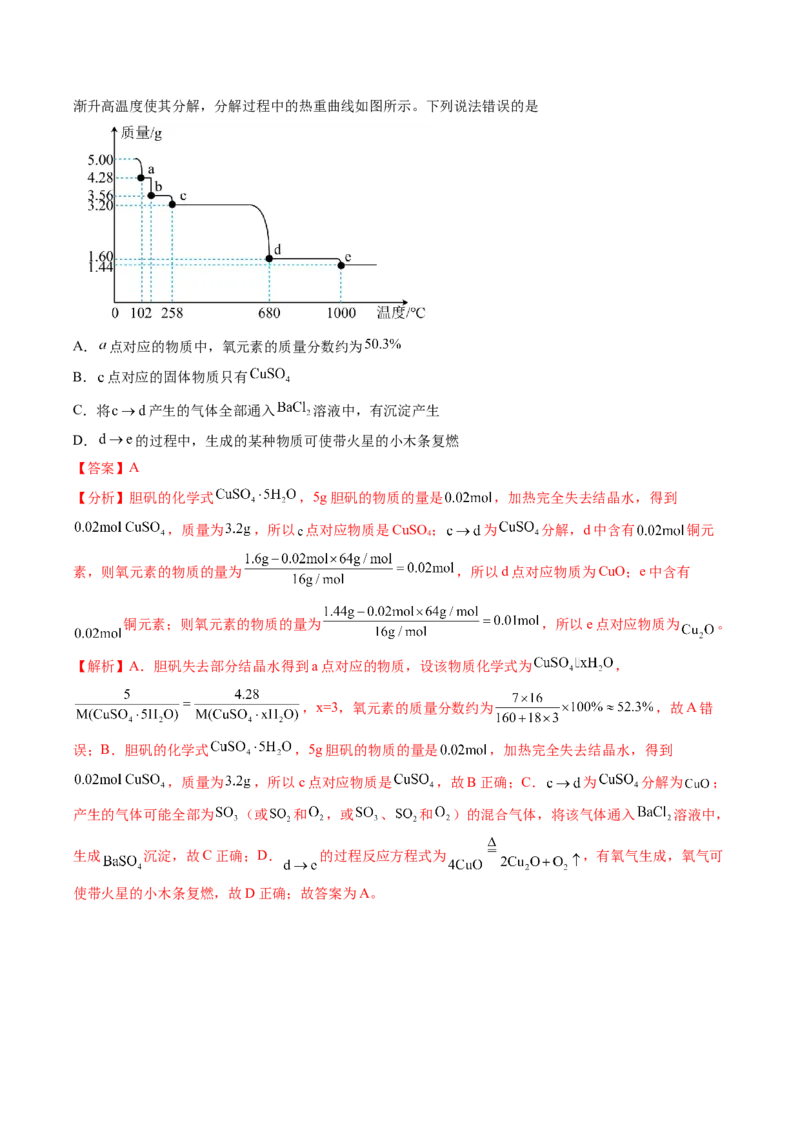
5.(2024秋·吉林通化·高三校考)将 胆矾 无其他杂质 置于氮气氛流中,然后对其进行加热,逐渐升高温度使其分解,分解过程中的热重曲线如图所示。下列说法错误的是
A. 点对应的物质中,氧元素的质量分数约为
B. 点对应的固体物质只有
C.将 产生的气体全部通入 溶液中,有沉淀产生
D. 的过程中,生成的某种物质可使带火星的小木条复燃
【答案】A
【分析】胆矾的化学式 ,5g胆矾的物质的量是 ,加热完全失去结晶水,得到
,质量为 ,所以 点对应物质是CuSO ; 为 分解,d中含有 铜元
4
素,则氧元素的物质的量为 ,所以d点对应物质为CuO;e中含有
铜元素;则氧元素的物质的量为 ,所以e点对应物质为 。
【解析】A.胆矾失去部分结晶水得到a点对应的物质,设该物质化学式为 ,
,x=3,氧元素的质量分数约为 ,故A错
误;B.胆矾的化学式 ,5g胆矾的物质的量是 ,加热完全失去结晶水,得到
,质量为 ,所以c点对应物质是 ,故B正确;C. 为 分解为 ;
产生的气体可能全部为 (或 和 ,或 、 和 )的混合气体,将该气体通入 溶液中,
生成 沉淀,故C正确;D. 的过程反应方程式为 ,有氧气生成,氧气可
使带火星的小木条复燃,故D正确;故答案为A。