文档内容
专题 26 化学反应速率
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 化学反应速率的概念及计算
考点二 影响化学反应速率的因素
考点一 化学反应速率的概念及计算
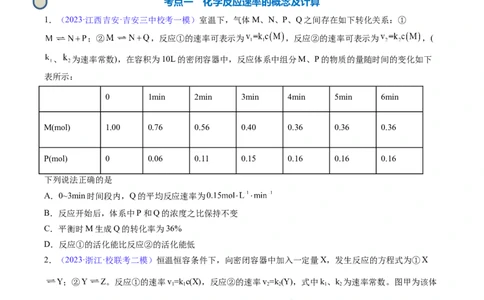
1.(2023·江西吉安·吉安三中校考一模)室温下,气体M、N、P、Q之间存在如下转化关系:①
;② ,反应①的速率可表示为 ,反应②的速率可表示为 ,(
、 为速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的变化如下
表所示:
0 1min 2min 3min 4min 5min 6min
M(mol) 1.00 0.76 0.56 0.40 0.36 0.36 0.36
P(mol) 0 0.06 0.11 0.15 0.16 0.16 0.16
下列说法正确的是
A.0~3min时间段内,Q的平均反应速率为
B.反应开始后,体系中P和Q的浓度之比保持不变
C.平衡时M生成Q的转化率为36%
D.反应①的活化能比反应②的活化能低
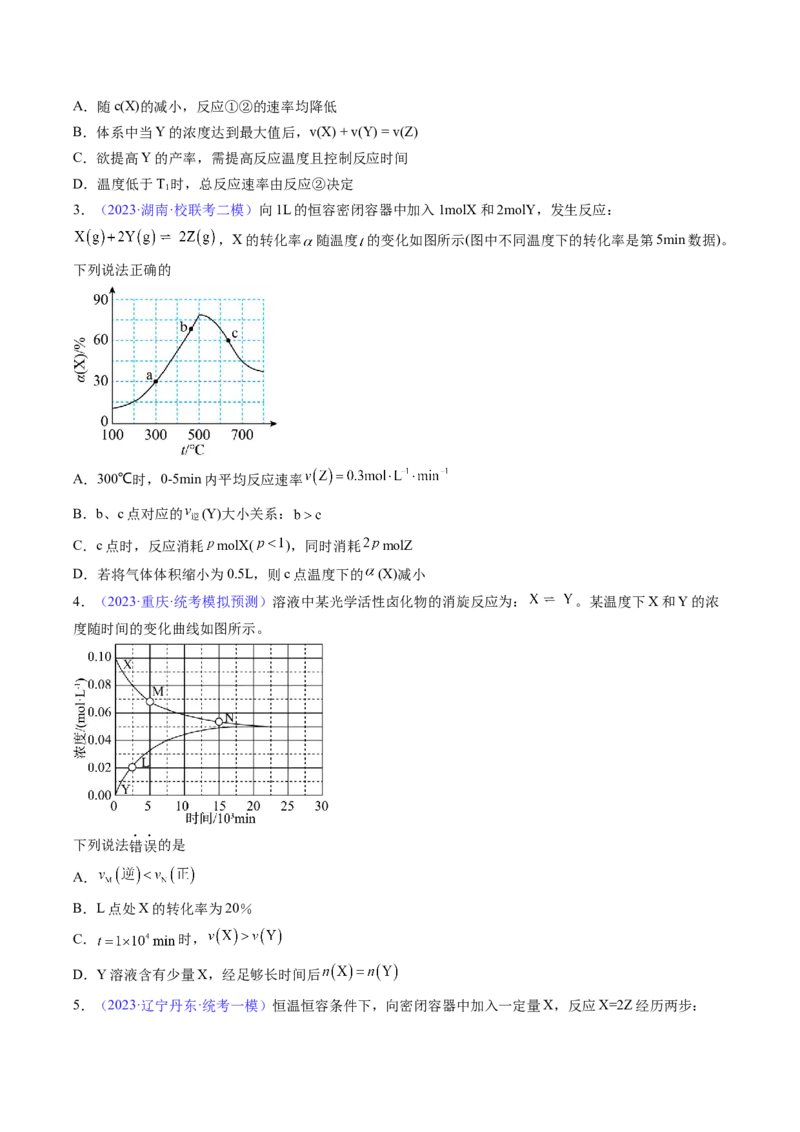
2.(2023·浙江·校联考二模)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①X
Y;②Y Z。反应①的速率v=kc(X),反应②的速率v=k(Y),式中k、k 为速率常数。图甲为该体
1 1 2 2 1 2
系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的lnk~ 曲线。下列说法不正确的是
1
原创精品资源学科网独家享有版权,侵权必究!A.随c(X)的减小,反应①②的速率均降低
B.体系中当Y的浓度达到最大值后,v(X) + v(Y) = v(Z)
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
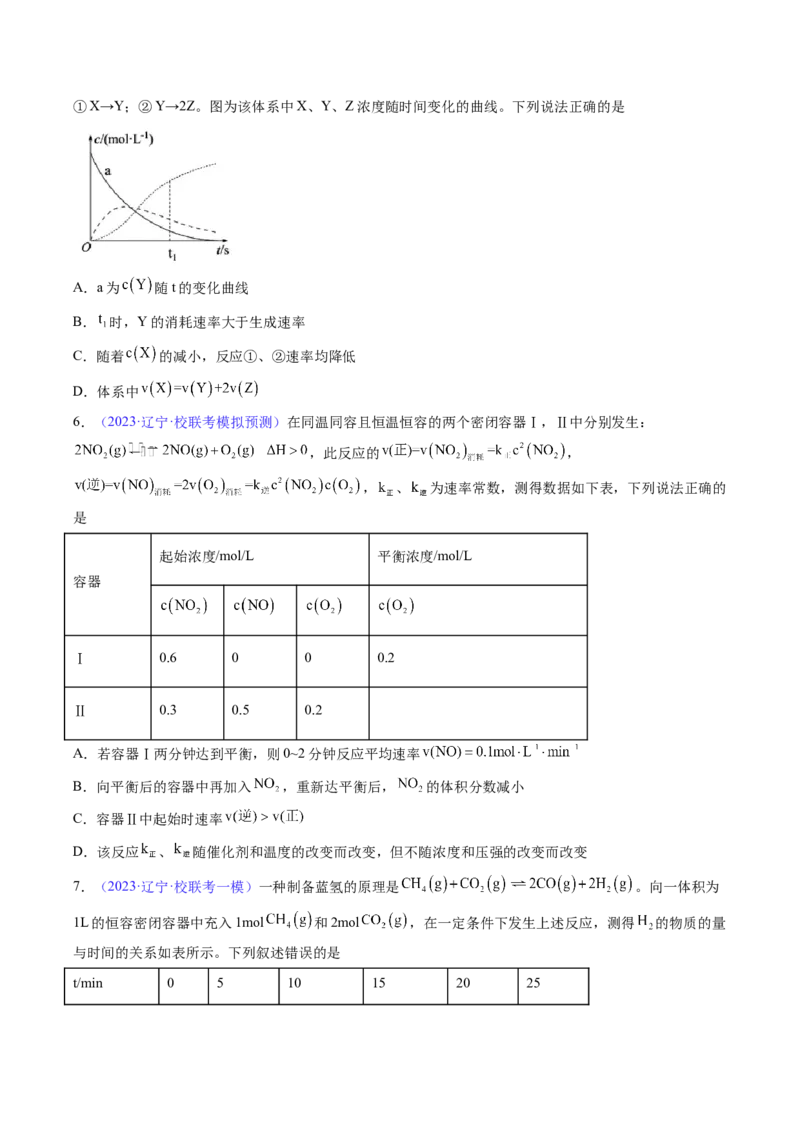
3.(2023·湖南·校联考二模)向1L的恒容密闭容器中加入1molX和2molY,发生反应:
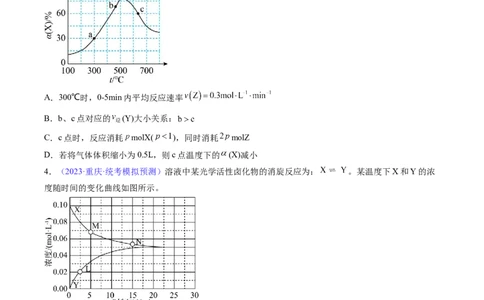
,X的转化率 随温度 的变化如图所示(图中不同温度下的转化率是第5min数据)。
下列说法正确的
A.300℃时,0-5min内平均反应速率
B.b、c点对应的 (Y)大小关系:
C.c点时,反应消耗 molX( ),同时消耗 molZ
D.若将气体体积缩小为0.5L,则c点温度下的 (X)减小
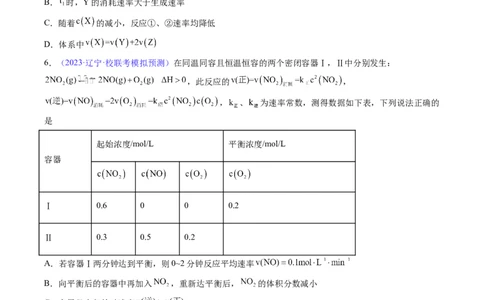
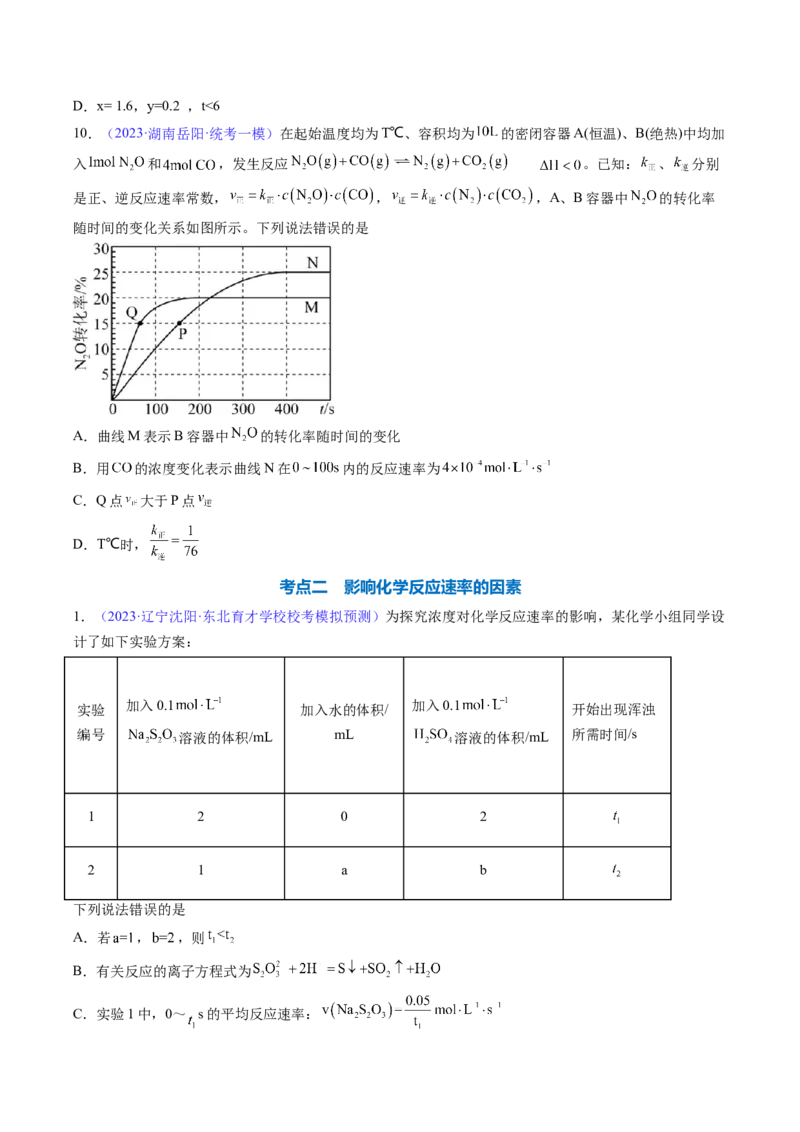
4.(2023·重庆·统考模拟预测)溶液中某光学活性卤化物的消旋反应为: 。某温度下X和Y的浓
度随时间的变化曲线如图所示。
下列说法错误的是
A.
B.L点处X的转化率为20%
C. 时,
D.Y溶液含有少量X,经足够长时间后
5.(2023·辽宁丹东·统考一模)恒温恒容条件下,向密闭容器中加入一定量X,反应X=2Z经历两步:①X→Y;②Y→2Z。图为该体系中X、Y、Z浓度随时间变化的曲线。下列说法正确的是
A.a为 随t的变化曲线
B. 时,Y的消耗速率大于生成速率
C.随着 的减小,反应①、②速率均降低
D.体系中
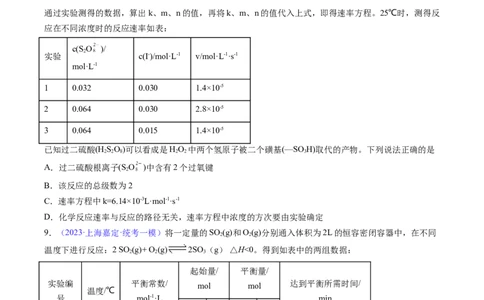
6.(2023·辽宁·校联考模拟预测)在同温同容且恒温恒容的两个密闭容器Ⅰ,Ⅱ中分别发生:
,此反应的 ,
, 、 为速率常数,测得数据如下表,下列说法正确的
是
起始浓度/mol/L 平衡浓度/mol/L
容器
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
A.若容器Ⅰ两分钟达到平衡,则0~2分钟反应平均速率
B.向平衡后的容器中再加入 ,重新达平衡后, 的体积分数减小
C.容器Ⅱ中起始时速率
D.该反应 、 随催化剂和温度的改变而改变,但不随浓度和压强的改变而改变
7.(2023·辽宁·校联考一模)一种制备蓝氢的原理是 。向一体积为
1L的恒容密闭容器中充入1mol 和2mol ,在一定条件下发生上述反应,测得 的物质的量
与时间的关系如表所示。下列叙述错误的是
t/min 0 5 10 15 20 25/mol 0 0.5 0.75 0.85 0.9 0.9
A.0~10min,
B.CO的体积分数不变时,反应达到平衡状态
C.上述反应中, 的转化率大于 的转化率
D.其他条件不变。若加入高效催化剂,则 的转化率达到45%时所用时间小于20min
8.(2023·河北秦皇岛·昌黎一中校考模拟预测)化学反应速率与反应物浓度的关系式(称为速率方程)是通
过实验测定的。以反应SO +2I-=2SO +I 为例,可先假设该反应的速率方程为v=kcm(S O )cn(I-),然后
2 2 2
通过实验测得的数据,算出k、m、n的值,再将k、m、n的值代入上式,即得速率方程。25℃时,测得反
应在不同浓度时的反应速率如表:
c(SO )/
2
实验 c(I-)/mol·L-1 v/mol·L-1·s-1
mol·L-1
1 0.032 0.030 1.4×10-5
2 0.064 0.030 2.8×10-5
3 0.064 0.015 1.4×10-5
已知过二硫酸(H SO)可以看成是HO 中两个氢原子被二个磺基(—SO H)取代的产物。下列说法正确的是
2 2 8 2 2 3
A.过二硫酸根离子(S O )中含有2个过氧键
2
B.该反应的总级数为2
C.速率方程中k=6.14×10-3L·mol-1·s-1
D.化学反应速率与反应的路径无关,速率方程中浓度的方次要由实验确定
9.(2023·上海嘉定·统考一模)将一定量的SO (g)和O(g)分别通入体积为2L的恒容密闭容器中,在不同
2 2
温度下进行反应:2 SO(g)+ O (g) 2SO (g)△H<0。得到如表中的两组数据:
2 2 3
起始量/ 平衡量/
实验编 平衡常数/ 达到平衡所需时间/
mol mol
温度/℃
号 mol-1·L min
SO O SO O
2 2 2 2
1 T K 4 2 x 0.8 6
1 1
2 T K 4 2 0.4 y t
2 2
下列说法不正确的是
A.实验1在前6min的平均反应速率υ(SO )=0.2 mol·L-1·min-1
2
B.T、T 的关系:T > T
1 2 1 2
C.K、K 的关系:K>K
1 2 2 1D.x= 1.6,y=0.2 ,t<6
10.(2023·湖南岳阳·统考一模)在起始温度均为T℃、容积均为 的密闭容器A(恒温)、B(绝热)中均加
入 和 ,发生反应 。已知: 、 分别
是正、逆反应速率常数, , ,A、B容器中 的转化率
随时间的变化关系如图所示。下列说法错误的是
A.曲线M表示B容器中 的转化率随时间的变化
B.用 的浓度变化表示曲线N在 内的反应速率为
C.Q点 大于P点
D.T℃时,
考点二 影响化学反应速率的因素
1.(2023·辽宁沈阳·东北育才学校校考模拟预测)为探究浓度对化学反应速率的影响,某化学小组同学设
计了如下实验方案:
实验 加入0.1 加入水的体积/ 加入0.1 开始出现浑浊
编号 溶液的体积/mL mL 溶液的体积/mL 所需时间/s
1 2 0 2
2 1 a b
下列说法错误的是
A.若 , ,则
B.有关反应的离子方程式为
C.实验1中,0~ s的平均反应速率:D.实验1比实验2先出现乳白色浑浊
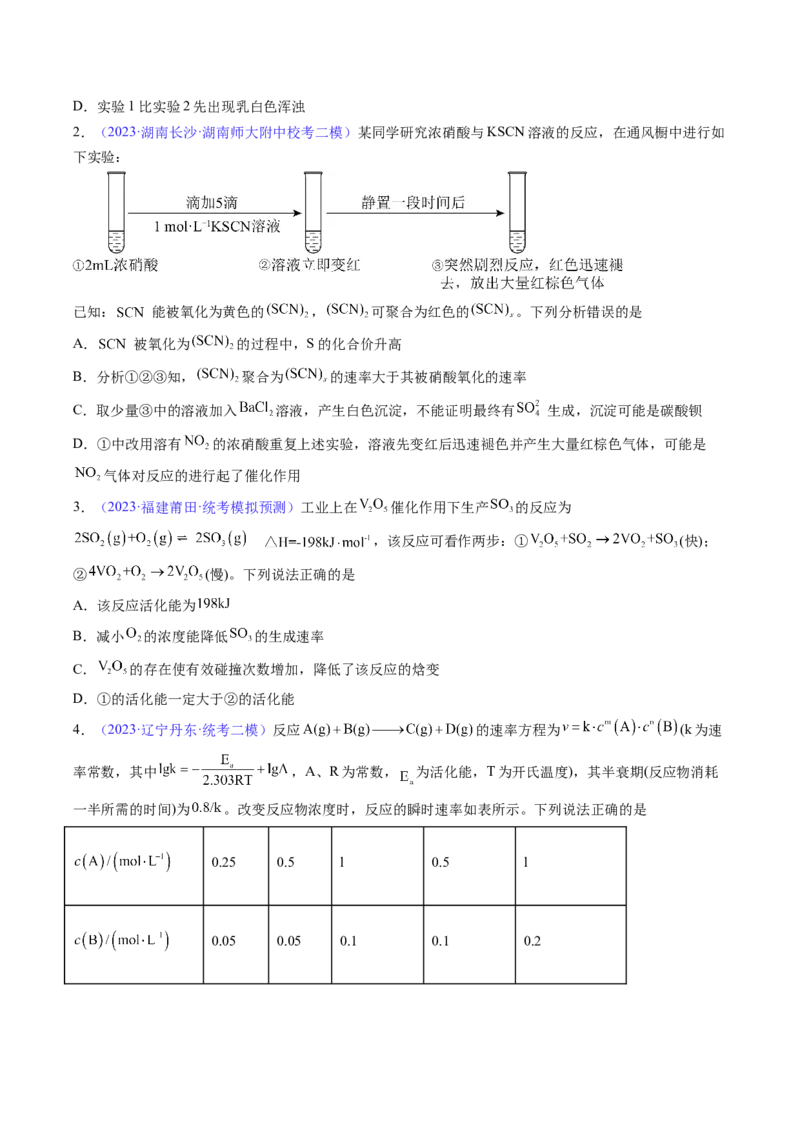
2.(2023·湖南长沙·湖南师大附中校考二模)某同学研究浓硝酸与KSCN溶液的反应,在通风橱中进行如
下实验:
已知: 能被氧化为黄色的 , 可聚合为红色的 。下列分析错误的是
A. 被氧化为 的过程中,S的化合价升高
B.分析①②③知, 聚合为 的速率大于其被硝酸氧化的速率
C.取少量③中的溶液加入 溶液,产生白色沉淀,不能证明最终有 生成,沉淀可能是碳酸钡
D.①中改用溶有 的浓硝酸重复上述实验,溶液先变红后迅速褪色并产生大量红棕色气体,可能是
气体对反应的进行起了催化作用
3.(2023·福建莆田·统考模拟预测)工业上在 催化作用下生产 的反应为
,该反应可看作两步:① (快);
② (慢)。下列说法正确的是
A.该反应活化能为
B.减小 的浓度能降低 的生成速率
C. 的存在使有效碰撞次数增加,降低了该反应的焓变
D.①的活化能一定大于②的活化能
4.(2023·辽宁丹东·统考二模)反应 的速率方程为 (k为速
率常数,其中 ,A、R为常数, 为活化能,T为开氏温度),其半衰期(反应物消耗
一半所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
0.25 0.5 l 0.5 l
0.05 0.05 0.1 0.1 0.21.6 3.2 3.2
A.
B.
C.在过量的B存在时,A剩余25%所需的时间是
D.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快
5.(2023·山东泰安·统考三模)已知 的速率方程为 (k为速率常
数,只与温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
6.(2023·浙江宁波·镇海中学校考模拟预测)一定温度下,利用测压法在刚性反应器中研究固体催化剂作
用下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:
t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为
B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
7.(2023·北京西城·北师大实验中学校考三模)为探究 与金属盐溶液能否反应,完成如下实验:
实验1 向 溶液中通入 ,溶液仍为蓝色且无固体析出。
实验2 以多孔石墨电极电解 溶液。电解开始时石墨电极表面几乎没有气泡,一段时间后逐渐产生
气泡。电解一段时间后,关闭电源,迅速取出阴极多孔石墨电极。
实验3 将实验2中阴极电极插入 溶液, 左右电极表面析出红色固体。将电极取出后清洗后再插入 溶液,表面变为灰白色固体,该固体溶于硝酸。
实验4 将实验2中阴极电极插入 溶液,立即析出白色固体,速度快于实验3。
以下说法不正确的是
A.由实验1可知,该条件下 无法还原
B.实验2中开始时几乎没有气体出现的原因可能是多孔石墨电极吸附生成的气体
C.对比实验1和实验3可以推测吸附在石墨中的 的反应活性强于气体中的
D.实验4中 溶液中析出金属单质速率更快的原因是 的氧化性更强
8.(2023·江西宜春·江西省宜丰中学校考模拟预测)已知总反应:
kJ⋅mol ( )的速率方程为{ ,k为速率常数],该反应机理可分为两步:
(1) 快
(2) 慢[速率方程 , 为速率常数,该反应速率
近似认为是总反应的速率]。下列叙述正确的是
A.
B.当 时,总反应达到平衡
C.总反应中生成物的总键能比反应物的总键能小a kJ•mol
D.恒容时,增大 的浓度能增加单位体积内活化分子的百分数,加快反应速率
9.(2023·山东潍坊·统考二模)实验小组探究双氧水与 的反应,实验方案如下表:
序号 ① ② ③
实验
装置
及操
作
溶液立即变为黄色, 溶液立即变为棕黄色,产生少量
实验 产生大量无色气体; 无色气体;溶液颜色逐渐加深,
无明显变化
现象 溶液温度升高;最终 温度无明显变化;最终有紫黑色
溶液仍为黄色 物质析出
下列说法正确的是
A. 对 的分解有催化作用
B.对比②和③,酸性条件下 氧化 的速率更大C.实验②③中的温度差异说明, 氧化 的反应放出大量热
D.对比②和③,③中的现象可能是因为 分解的速率大于 氧化 的速率
10.(2023·河北·校联考模拟预测)某兴趣小组同学将 的酸性 溶液和 溶液按如下比
例混合,探究浓度对反应速率的影响。
序号 温度
① 20℃
② 20℃
现象:实验①溶液很快由紫色变为青绿色,而实验②慢一点;变为青绿色后,实验②溶液很快褪至无色,
而实验①褪色慢一点。
资料: 与 很难形成配合物; (青绿色), 有强氧化性,而
氧化性极弱。
下列说法错误的是
A.
B. 溶液中能通过加盐酸酸化调
C.溶液由青绿色褪至无色过程中,实验①中 较小,导致褪色速率较慢
D.由实验可知,加入 越多, 溶液由紫色褪至无色的速率越快