文档内容
专题二 能力提升检测卷
一、选择题(本题共20小题,每小题4分,共80分)
1.古代文学中蕴含许多化学知识,下列说法正确的是。
A.成语“水滴石穿”中只发生了物理变化
B.俗语“卤水点豆腐”中“卤水”指的是氯水
C.“客从南溟来,遗我泉客珠”中珍珠的主要成分是碳酸钙
D.“丹砂 烧之成水银,积变又还成丹砂”,该过程涉及可逆反应
【答案】C
【解析】A.“水滴石穿”的过程中二氧化碳溶于水后,与石头(主要成分为碳酸钙)反应生成了溶于水
的碳酸氢钙,使得石头逐渐溶解,该过程中不止发生了物理变化,还发生了化学变化,故A错误;
B.“卤水”是电解质溶液,溶质主要是氯化镁,豆浆属于胶体,电解质溶液能使胶体发生聚沉,故“卤
水”可使豆浆变为豆腐,故B错误;
C.珍珠为贝类内分泌作用而形成的含碳酸钙的矿物珠粒,因此主要成分是碳酸钙,故C正确;
D.在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,称为可逆反应,“丹砂
烧之成水银”的过程需要加热,“积变又还成丹砂”则在常温下即可发生,两者不是同时发生,因此不是
可逆反应,故D错误;故选C。
2.《天工开物》是我国珍贵的科技文献,下列记载中主要过程不涉及化学反应的是
A.凡石灰经火焚炼为用 B.烧铁器淬于胆矾水中,即成铜色也
C.凡墨烧烟凝质而为之 D.水沙中所出,大者名狗头金
【答案】D
【解析】凡石灰经火焚炼为用,为石灰石高温煅烧生成氧化钙和二氧化碳,涉及化学反应,A与题意不
符;
烧铁器淬于胆矾水中,即成铜色也,为铁与硫酸铜反应生成硫酸亚铁和铜,涉及化学反应,B与题意不
符;凡墨烧烟凝质而为之,墨是由烟(炭黑)和胶二者结合而成的,涉及化学反应,C与题意不符;水沙中
所出,块大的黄金为狗头金,不涉及化学反应,D符合题意;答案为D。
3.下列有关说法正确的是
A.氧化钾溶于水能导电,所以氧化钾是电解质
B.强电解质一定是含有离子键,弱电解质中一定含弱极性共价键
C.酸性氧化物不一定是非金属氧化物,碱性氧化物都是金属氧化物D.纳米铁粉分散在水中形成胶体,可以通过吸附的方式高效地去除被污染水体中的 、 、
、 等重金属离子
【答案】C
【解析】氧化钾溶于水能导电,是氧化钾和水反应生成的氢氧化钾导电,不能推出氧化钾是电解质,A错
误;强电解质不一定含有离子键,比如HCl等强酸均是强电解质,均不含离子键,B错误;酸性氧化物不
一定是非金属氧化物,如MnO,碱性氧化物都是金属氧化物,C正确;纳米铁粉去除被污染水体中的
2 7
、 、 、 等重金属离子,是因为铁可以将这些离子还原,不是吸附作用,D错误;故
选C。
4.德国著名行业杂志《应用化学》上曾刊登介绍:某中德联合研究小组设计制造了一种“水瓶”,用富
勒烯 (C )的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确
60
的是
A.“水瓶”、 都是混合物
B.熔点:金刚石
C.一定条件下,石墨转化为 是物理变化
D.磷酸钙是强电解质,其组成元素均为短周期元素
【答案】B
【解析】 是纯净物,A错误;金刚石是原子晶体,C 是分子晶体,所以熔点:金刚石
60
,B正确;一定条件下,石墨转化为 是化学变化,C错误;磷酸钙是强电解质,钙为长周期元
素,D错误;
故选B。
5.下列材料的主要成分属于有机物的是
A.国家速滑馆用于蒸发制冷的材料-二氧化碳
B.长征五号的整流罩前锥段材料-聚甲基丙烯酰亚胺
C.港珠澳大桥锚具材料-特殊工艺的低碳钢D.我国自主研发的5G芯片的材料-硅
【答案】B
【解析】二氧化碳是无机物,A项错误;聚甲基丙烯酰亚胺是有机物,B项正确;低碳钢属于合金,C项
错误;硅属于单质,不属于有机物,D项错误;答案选B。
6.中国科学家以二氧化碳为碳源,在470℃、80Mpa下与金属钠反应合成出金刚石。下列说法不正确的是
A.金属钠在反应中作还原剂
B.反应中生成的氧化产物为NaO
2 2
C.二氧化碳转变为金刚石发生的是还原反应
D.钠被氧化最终生成碳酸钠
【答案】B
【解析】A.金属钠和二氧化碳反应生成金刚石,反应中碳元素化合价降低、钠元素化合价升高,钠作还
原剂,故A正确;
B.金属钠和二氧化碳的反应中碳元素化合价降低、钠元素化合价升高,生成的氧化产物不可能是NaO,
2 2
故B错误;
C.二氧化碳转变为金刚石,碳元素化合价降低,二氧化碳发生还原反应,故C正确;
D.钠与二氧化碳反应生成金刚石和氧化钠,氧化钠和二氧化碳反应生成碳酸钠,故D正确;故选B。
7.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.能与金属铝作用产生H 的溶液:K+、Ca2+、Br-、
2
B. =1×10−12的溶液:K+、Na+、 、
C.0.1 mol∙L−1 KFe(SO ) 溶液:Mg2+、Al3+、SCN-、
4 2
D.通入大量SO 气体的溶液中:Na+、 、NH 、
2
【答案】B
【解析】能与金属铝作用产生H 的溶液,说明可能是酸或碱,Ca2+、OH-、 生成CaSO 沉淀,H+与
2 3
生成气体,故A不符合题意; =1×10−12的溶液,说明溶液显碱性,K+、Na+、CO2-、
3
都共存,故B符合题意;0.1 mol∙L−1 KFe(SO ) 溶液,Fe3+与SCN-反应,故C不符合题意;通入大量SO
4 2 2气体的溶液,HSO 与SO2-反应生成HSO-,故D不符合题意。综上所述,答案为B。
2 3 3 3
8.在2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O反应中,下列说法正确的是
4 2 2 2
A.氧化产物与还原产物物质的量之比5∶2
B.2molKMnO 完全反应,转移的电子数为16N
4 A
C.KCl、MnCl 是氧化产物
2
D.HCl是还原剂被还原
【答案】A
【解析】A.在2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O反应中,氧化产物是Cl,还原产物是MnCl ,
4 2 2 2 2 2
所以氧化产物与还原产物物质的量之比5∶2,故A正确;
B.反应中Mn的化合价由+7降低到+2,2molKMnO 完全反应,转移的电子数为10N ,故B错误;
4 A
C.该反应中KMnO 做氧化剂,HCl做还原剂,Cl 是氧化产物,MnCl 是还原产物,故C错误;
4 2 2
D.该反应中KMnO 做氧化剂被还原,HCl做还原剂被氧化,D错误;故选A。
4
9.下列离子方程式书写正确的是( )
A.向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H S↑
2
B.用铜电极电解氯化钙溶液:2Cl-+2H O =======Cl↑+H ↑+2OH-
2 2 2
C.将FeI 溶液和稀硝酸混合:Fe2++4H++ =Fe3++2H O+NO↑
2 2
D.Mg(HCO ) 溶液中加入足量NaOH溶液:Mg2++2 +2OH-=MgCO↓+CO2-+2H O
3 2 3 3 2
【答案】A
【解析】向硫酸铜溶液中加入过量的NaHS溶液,反应生成硫化铜沉淀和硫化氢气体:Cu2++2HS-=CuS↓
+H S↑,故A正确;用铜电极电解氯化钙溶液,阳极是铜失去电子变为铜离子,阴极是水中氢离子得到电
2
子变为氢气:Cu+2H O =======H↑+Cu(OH) ↓,故B错误;将FeI 溶液和稀硝酸混合,碘离子的还原性
2 2 2 2
大于亚铁离子还原性,因此碘离子先与硝酸反应,故C错误;Mg(HCO ) 溶液中加入足量NaOH溶液,镁
3 2
离子变为氢氧化镁沉淀:Mg2++2HCO-+4OH-=Mg(OH) ↓+2CO2-+2H O,故D错误。综上所述,答案为
3 2 3 2
A。
10.SO 气体与足量Fe (SO ) 溶液完全反应后,再加入KCr O 溶液,发生如下化学反应:①SO +2Fe3+
2 2 4 3 2 2 7 2
+2H O=SO +2Fe2++4H+;②Cr O +6Fe2++14H+=2Cr3++6Fe3++7H O。则下列有关说法不正确的是
2 2 2
A.氧化性:Cr O >Fe3+>SO
2 2
B.标准状况下,若有6.72 L SO 参加反应,则最终消耗0.2mol K Cr O
2 2 2 7C.反应②中,每有1mol KCr O 参加反应,转移电子的数目为6N
2 2 7 A
D.由上述反应原理推断:KCr O 能将NaSO 氧化成NaSO
2 2 7 2 3 2 4
【答案】B
【解析】A.由①可知,Fe元素的化合价降低,则氧化性为Fe3+>SO ,由②可知,Cr元素的化合价降
2
低,则氧化性为Cr O >Fe3+,则氧化性:Cr O >Fe3+>SO ,故A正确;
2 2 2
B.6.72 L SO (标准状况)参加反应,物质的量是6.72L÷22.4L/mol=0.3mol,由上述两个反应可知,存在
2
3SO ~Cr O ,则最终消耗0.1molKCr O,故B错误;
2 2 2 2 7
C.每有1mol KCr O 参加反应,转移电子为1mol×2×(6-3)=6mol,即转移电子的数目为6N ,故C正
2 2 7 A
确;
D.因氧化性为Cr O >SO ,则KCr O 能将NaSO 氧化成NaSO ,故D正确;
2 2 2 2 7 2 3 2 4
故选B。
11.某溶液中含有的溶质是FeBr 、FeI,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加
2 2
KSCN溶液,溶液变为红色,则下列叙述正确的是( )
①原溶液中的Br-一定被氧化
②通入氯气之后原溶液中的Fe2+一定有部分或全部被氧化
③不能确定通入氯气后的溶液中是否存在Fe2+
④若取少量所得溶液,再加入CCl 溶液,静置、分液,向上层溶液中加入足量的AgNO 溶液,只产生白
4 3
色沉淀,说明原溶液中的I-、Fe2+,Br-均被完全氧化
A.①②③ B.②③④ C.①③④ D.①②③④
【答案】B
【解析】在FeBr 和FeI 混合液中存在三种还原性不同的离子,它们的还原性:I->Fe2+>Br-,通入的氯气
2 2
先氧化碘离子,然后氧化二价铁,最后氧化溴离子,向反应后的溶液中滴加KSCN溶液,结果溶液变为红
色,说明碘离子全部被氧化,二价铁部分或全部被氧化,溴离子可能被氧化,据此分析解答。①没有实验
现象说明Br-被氧化或没有被氧化,原溶液中的Br-可能被氧化,故①错误;②没有实验现象说明Fe2+完全
氧化,通入氯气之后原溶液中的二价铁部分或全部被氧化,故②正确;③没有实验现象说明Fe2+完全氧
化,所以不能确定通入氯气之后的溶液中是否存在Fe2+,故③正确;④若取少量所得溶液,再加入CCl 溶
4
液,静置、分液,向上层溶液中加入足量的AgNO 溶液,只产生白色沉淀,说明原溶液中的Br-被完全氧
3
化,I-、Fe2+均被完全氧化,故④正确;正确的有②③④,故选B。12.在水溶液中,RO 和Mn2+发生反应:RO +3Mn2++3H O=R-+3MnO↓+6H+,则RO 中R元素的化合
2 2
价和原子最外层电子数分别为
A.+4、6 B.+7、7 C.+5、7 D.+5、5
【答案】C
【解析】根据电荷守恒:-n+6=6-1,n=1,故RO ,中设R的化合价x,O为-2价,x-6=-1,x=+5,由方程
式中,R元素的还原产物为R-可知,R得到1个电子达到8电子稳定状态,故R原子最外层7个电子。故
选C。
13.ClO 是一种高效安全的绿色杀菌剂,下列有关ClO 的制备与杀菌作用的说法中不合理的是
2 2
A.可用Cl 和NaClO 反应制备ClO ,其中n(氧化剂)∶n(还原剂)=1∶2
2 2 2
B.ClO 在强碱性环境中使用失效:2ClO +2OH-= + +H O
2 2 2
C.ClO 处理饮用水时残留的 ,可用FeSO 除去: +2Fe2++4H+=2Fe3++Cl-+2H O
2 4 2
D.等物质的量的ClO 的杀菌效果比Cl、HClO的强
2 2
【答案】C
【解析】氯气的化合价从0升高到+4价,NaClO 中化合价从+5价到+4价,所以氧化剂和还原剂的比例为
3
1:2,正确,不选A;二氧化氯在强碱性环境中自身腐蚀氧化还原反应,正确,不选B;方程式点和不守
恒,错误,选C;二氧化氯做为氧化剂,由+4价降低到-1价,杀菌效果比氯气、次氯酸强,正确,不选
D。
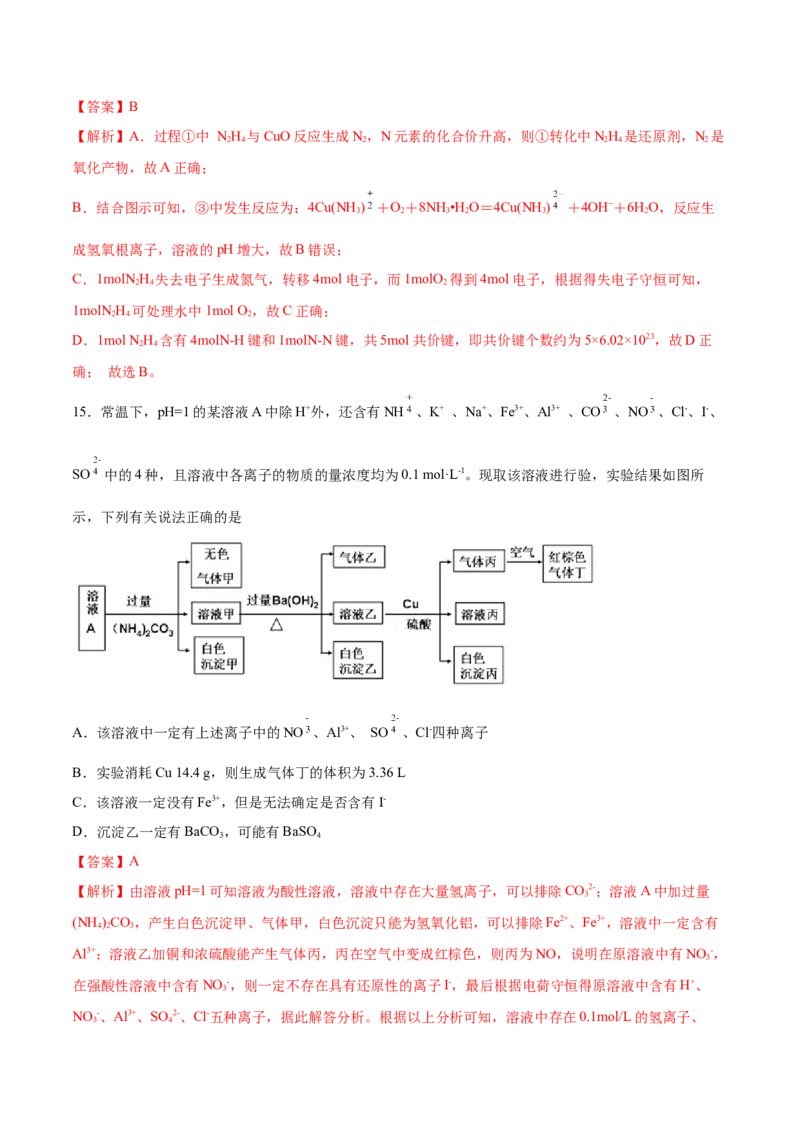
14.联氨(N H)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述
2 4
错误的是
A.过程①中生成的N 是氧化产物
2
B.过程③中发生反应后溶液的pH减小
C.1mol NH 可处理锅炉水中1mol O
2 4 2
D.1mol NH 含有的共价键数约为5×6.02×1023
2 4【答案】B
【解析】A.过程①中 NH 与CuO反应生成N,N元素的化合价升高,则①转化中NH 是还原剂,N 是
2 4 2 2 4 2
氧化产物,故A正确;
B.结合图示可知,③中发生反应为:4Cu(NH ) +O+8NH •H O=4Cu(NH ) +4OH−+6HO,反应生
3 2 3 2 3 2
成氢氧根离子,溶液的pH增大,故B错误;
C.1molN H 失去电子生成氮气,转移4mol电子,而1molO 得到4mol电子,根据得失电子守恒可知,
2 4 2
1molN H 可处理水中1mol O,故C正确;
2 4 2
D.1mol NH 含有4molN-H键和1molN-N键,共5mol共价键,即共价键个数约为5×6.02×1023,故D正
2 4
确; 故选B。
15.常温下,pH=1的某溶液A中除H+外,还含有NH 、K+ 、Na+、Fe3+、Al3+ 、CO 、NO 、Cl-、I-、
SO 中的4种,且溶液中各离子的物质的量浓度均为0.1 mol·L-1。现取该溶液进行验,实验结果如图所
示,下列有关说法正确的是
A.该溶液中一定有上述离子中的NO 、Al3+、 SO 、Cl-四种离子
B.实验消耗Cu 14.4 g,则生成气体丁的体积为3.36 L
C.该溶液一定没有Fe3+,但是无法确定是否含有I-
D.沉淀乙一定有BaCO ,可能有BaSO
3 4
【答案】A
【解析】由溶液pH=1可知溶液为酸性溶液,溶液中存在大量氢离子,可以排除CO2-;溶液A中加过量
3
(NH )CO,产生白色沉淀甲、气体甲,白色沉淀只能为氢氧化铝,可以排除Fe2+、Fe3+,溶液中一定含有
4 2 3
Al3+;溶液乙加铜和浓硫酸能产生气体丙,丙在空气中变成红棕色,则丙为NO,说明在原溶液中有NO -,
3
在强酸性溶液中含有NO -,则一定不存在具有还原性的离子I-,最后根据电荷守恒得原溶液中含有H+、
3
NO -、Al3+、SO 2-、Cl-五种离子,据此解答分析。根据以上分析可知,溶液中存在0.1mol/L的氢离子、
3 40.1mol/L的铝离子,0.1mol/L NO-;溶液中阳离子带有的电荷为:(0.1mol/L×1)+(0.1mol/L×3)
3
=0.4mol/L;而溶液中除了存在0.1mol/L的硝酸根离子外,根据电荷守恒,还应该含有SO 2-离子和Cl-,所
4
以该溶液中一定有NO -、Al3+、SO 2-、Cl-四种离子,故A正确;根据反应方程式
3 4
3Cu+8HNO (稀)═3Cu(NO )+2NO↑+4HO可知,若消耗14.4g铜,n(Cu)= =0.225mol,根据反应
3 3 2 2
方程式中Cu与NO的物质的量关系可知生成一氧化氮气体的物质的量为n(NO)= n(Cu)=
×0.225mol=0.15mol;由于没有告诉条件是否是标准状况下,所以0.15mol一氧化氮的体积不一定为
3.36L,故B错误;根据上述分析可知,在强酸性溶液中含有NO -,溶液具有强氧化性,则一定不存在具
3
有还原性的离子I-,故C错误;根据上述分析可知,溶液中含有硫酸根离子,所以沉淀乙中一定含有
BaCO 、BaSO,故D错误;故答案A。
3 4
16.某离子反应涉及H+、Bi3+、 、 、Mn2+、HO六种微粒。其中c( )随反应进行逐渐增
2
大。下列判断错误的是
A.氧化剂与还原剂的物质的量之比为2:5
B.氧化性: 大于
C.反应后溶液的pH值增大
D.若有1mol还原剂参加反应,转移电子的物质的量为5mol
【答案】A
【解析】c(MnO )随反应进行逐渐增大,MnO 应是生成物,则Mn2+为反应物,Mn元素化合价发生升
高,具有氧化性的BiO 为反应物,由Bi元素守恒可知Bi3+是生成物,则反应的方程式应为5BiO +2Mn2+
+14H+=5Bi3++2MnO +7H O,以此解答该题。
2
A.Mn元素化合价发生升高,则Mn2+为还原剂,Bi元素的化合价降低,则BiO 为氧化剂,所以氧化剂与
还原剂的物质的量之比为5:2,故A错误;B.由反应5 BiO +2Mn2++14H+=5Bi3++2 MnO +7H O,氧化剂是BiO ,氧化产物是 ,则氧化性:
2
BiO > ,故B正确;
C.由反应5 BiO +2Mn2++14H+=5Bi3++2 MnO +7H O可知,反应消耗H+,pH值增大,故C正确;
2
D.Mn元素化合价由+2升高到+7,则若有1mol还原剂参加反应,转移电子的物质的量为(7-2)
×1mol=5mol,故D正确。故选A。
17.常温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中:K+、Mg2+、MnO 、SO
B.c(Fe3+ )=1 mol·L-1的溶液中:Ca2+、Cu2+、SCN-、Cl-
C. =1×10-13mol·L-1的溶液中:Ba2+、K+、Cl-、NO
D.能使甲基橙变红的溶液中:Na+、NH 、I-、ClO-
【答案】C
【解析】K+、Mg2+、MnO 、SO2- 之间不发生反应,能大量共存,但MnO 在溶液中为紫红色,与题意
4
不符,故A不符合题意;c(Fe3+ )=1 mol·L-1的溶液中含有大量Fe3+,Fe3+与SCN-之间发生络合反应,不
能大量共存,故B不符合题意; =1×10-13mol·L-1的溶液中呈碱性,Ba2+、K+、Cl-、NO 之间
不反应,都不与OH-反应,能够大量共存,故C符合题意;能使甲基橙变红的溶液呈酸性,H+、I-都与
ClO-反应,不能大量共存,故D不符合题意;答案选C。
18.用CuS、Cu S处理酸性废水中的 ,发生反应如下:
2
反应I:CuS+ +H+→Cu2++ +Cr3++H O(未配平)
2
反应II:Cu S+ +H+→Cu2++ +Cr3++H O(未配平)
2 2
下列有关说法不正确的是A.反应I中只有 是氧化产物而反应II中Cu2+、 都是氧化产物
B.反应II中还原剂、氧化剂的物质的量之比为3∶5
C.反应I、II中每处理1mol ,转移电子的数目相等
D.处理1mol 时反应I、II中消耗H+的物质的量相等
【答案】D
【解析】A.反应I中只有S元素被氧化,则只有 是氧化产物;反应II中有铜元素、硫元素均被氧
化,所以Cu2+、 都是氧化产物,故A正确;
B.根据电子守恒、电荷守恒和原子守恒规律配平后的方程式为:3Cu S+5 +46H+=6Cu2++3
2
+10Cr3++23H O,氧化剂为 ,还原剂为Cu S,则反应II中还原剂、氧化剂的物质的量之比为3∶5,故
2 2
B正确;
C.根据电子守恒、电荷守恒和原子守恒规律配平后的方程式为:反应I:3CuS+4 +32H+=3Cu2++3
+8Cr3++16H O,反应II:3Cu S+5 +46H+=6Cu2++3 +10Cr3++23H O,反应I中每处理1mol
2 2 2
,转移电子物质的量6mol,反应II中每处理1mol ,转移电子物质的量6mol,故转移电子的
数目相等,故C正确;
D.根据电子守恒、电荷守恒和原子守恒规律配平后的方程式为:反应I:3CuS+4 +32H+=3Cu2++3
+8Cr3++16H O,反应II:3Cu S+5 +46H+=6Cu2++3 +10Cr3++23H O;处理1mol 时反
2 2 2
应I中消耗H+的物质的量8mol,处理1mol 时反应II中消耗H+的物质的量9.2mol,消耗H+的物质的
量不相等,故D错误;故选D。
19.常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.澄清透明的溶液中:Fe3+、Mg2+、SCN-、Cl-B.由水电离产生的 c(H+)=10-13mol·L-1的溶液:K+、Na+、ClO‒、AlO
C.pH=7的溶液中:Fe3+、NH 、NO 、SO
D.在酸性KMnO 溶液中:K+、Na+、I-、SO
4
【答案】B
【解析】Fe3+与SCN-之间会发生络合反应,在溶液中不能大量共存,A不符合题意;由水电离产生的
c(H+)=10-13mol·L-1的溶液可能呈现酸性或碱性,K+、Na+、ClO‒、AlO 在碱性条件下不反应可共存,B符合
题意;Fe3+在pH=7的溶液中会生成氢氧化铁沉淀,不能在此溶液中共存,C不符合题意;酸性KMnO 具
4
有强氧化性,可与I-发生氧化还原反应,在溶液中不共存,D不符合题意;故选B。
20.十九大报告指出:“坚持全民共治、源头防治,持续实施大气污染防治行动,打赢蓝天保卫战!”,
以NO 和燃煤为主的污染综合治理是当前重要的研究课题。CO与NO是汽车尾气中污染大气的成分,研
x 2
究表明CO与NO在Fe+作用下生成无害气体,发生反应的能量变化及反应历程如图所示,两步反应分别
2
为:①NO+Fe+=N +FeO+(慢);②FeO++CO=CO+Fe+(快)。下列说法不正确的是
2 2 z
A.反应①是氧化还原反应,反应②是非氧化还原反应
B.两步反应均为放热反应,总反应的化学反应速率由反应①决定
C.Fe+使反应的活化能减小,FeO+是中间产物
D.若转移1mol电子,则消耗标况下11.2LN O
2
【答案】A
【解析】A.由反应①NO+Fe+=N +FeO+(慢)可知,铁元素、氮元素化合价发生改变,由反应②FeO+
2 2
+CO=CO +Fe+可知,铁元素、碳元素化合价发生改变,二个反应均有元素化合价的升降,因此都是氧化还
2
原反应,故A错误;
B.由图可知,Fe++N O→FeO++N 、FeO++CO→Fe++CO 两步中均为反应物总能量大于生成物总能量,所
2 2 2以两个反应都是放热反应,总反应的化学反应速率由速率慢的反应①决定,故B正确;
C.Fe+作催化剂,使反应的活化能减小,增大反应速率,FeO+是反应过程中产生的物质,因此是中间产
物,故C正确;
D.由总反应方程式NO+CO N+CO 可知,N元素由+1价得电子变为0价,C元素由+2价失2个电子
2 2 2
变为+4价,即转移2mol电子消耗1molN O,则转移1mol电子,则消耗NO为0.5mol,即标况下
2 2
11.2LN O,故D正确;答案为A。
2
二、非选择题(本题共2小题,每小题10分,共20分)
21.(10分)有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO、SO、Cl
-、I-、HCO,实验如下:
实验步骤 实验现象
(1)用玻璃棒蘸取少量该溶液,点在pH试纸中部 试纸变为红色
(2)取少量该溶液,加入Cu片和浓硫酸,加热 有无色气体产生,气体遇空气可以变成红棕色
(3)取少量该溶液,加入BaCl 溶液 有白色沉淀生成
2
(4)取(3)中反应后的上层清液,加入AgNO 溶液 有稳定的白色沉淀生成,且不溶于稀硝酸
3
有白色沉淀生成,当NaOH过量时,沉淀部分溶
(5)取少量该溶液,加入NaOH溶液
解
由此判断:(1)溶液中一定存在的离子是____________;溶液中肯定不存在的离子是______________。
(2)写出实验步骤(2)中所发生反应的离子方程式:___________________________
________________________________________________________________________。
(3)为了进一步确定其他离子,应该补充的实验及对应欲检验离子的名称:____________
________________________________________________________________________。
【解析】本题要求为无色透明溶液,则Fe2+不能大量存在。步骤(1)pH试纸变红,说明溶液显酸性,HCO
不能大量存在;步骤(2)说明有NO,在酸性条件下NO有强氧化性,因此还原性的离子I-不能大量存在;
步骤(3)说明有SO,Ba2+不能大量存在;步骤(4)不能说明有Cl-,因为步骤(3)中引入了Cl-;步骤(5)说明
有Mg2+和Al3+。
【答案】(1)NO、SO、Mg2+、Al3+ Fe2+、HCO、I-、Ba2+
(2)3Cu+8H++2NO=====3Cu2++2NO↑+4HO
2
(3)K+的检验可以用焰色反应;Cl-的检验:向溶液中加足量的Ba(NO ) 溶液,过滤后向滤液中加AgNO 溶
3 2 3
液,再加稀硝酸,产生白色沉淀且不溶解,可证明有Cl-存在
22.(10分)磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)下图所示为提纯白磷样品(含惰性杂质)的工艺流程。过程Ⅰ中,被还原的元素是________(填元素符
号),过程Ⅲ的化学方程式为______________________________。(2)磷酸钒锂/碳复合材料[Li V(PO )/C]是常用的电极材料,其制备流程如下:
3 2 4 3
①复合材料中V的化合价为______________,C的作用是____________________。
②V O 与HC O 反应生成V(C O) 的化学方程式为_______________________;
2 5 2 2 4 2 2 4 3
“洗涤”时用乙醇而不用水的目的是________________________________。
③锂离子电池是一种二次电池,又称“摇椅”电池。若用和LiC 和LiV(PO )/C作电极,放电时的电池总
x 6 3 2 4 3
反应为LiC +Li V(PO )===Li V(PO )+C ,则电池充电时阳极的电极反应式为
x 6 3-x 2 4 3 3 2 4 3 6
_________________________________________________________。
【解析】(1)根据图像,过程Ⅰ中白磷与硫酸铜溶液反应生成磷酸和Cu P,其中P元素和Cu元素的化合价
3
均降低,被还原;过程Ⅲ中反应物为Ca (PO )、SiO 和C,生成物为CaSiO 、CO和P,反应的化学方程
3 4 2 2 3 4
式为2Ca (PO )+6SiO+10C===6CaSiO +10CO↑+P;(2)①磷酸钒锂/碳复合材料[Li V(PO )/C]中磷酸根
3 4 2 2 3 4 3 2 4 3
离子显-3价,锂显+1价,因此V的化合价为+3价,该复合材料是常用的电极材料,C为导体,可以增
强复合材料的导电性;②VO 与HC O 反应生成V(C O) 过程中V的化合价由+5价降低为+3价,则草
2 5 2 2 4 2 2 4 3
酸被氧化生成二氧化碳,根据得失电子守恒和原子守恒,反应的化学方程式为VO+5HC O===V (C O)
2 5 2 2 4 2 2 4 3
+4CO↑+5HO;LiV(PO ) 能够溶于水,“洗涤”时用乙醇而不用水,可以减少产品损耗;③该锂离子
2 2 3 2 4 3
电池放电时的电池总反应为LiC +Li V(PO )===Li V(PO )+C ,则充电时电池的总反应为LiV(PO )
x 6 3-x 2 4 3 3 2 4 3 6 3 2 4 3
+C ===LiC +Li V(PO ),充电时阳极发生氧化反应,电极反应为LiV(PO )-xe-===Li V(PO )+
6 x 6 3-x 2 4 3 3 2 4 3 3-x 2 4 3
xLi+。
【答案】(1)Cu、P 2Ca (PO )+6SiO+10C===6CaSiO +10CO↑+P (2)①+3 增强复合材料的导电性
3 4 2 2 3 4
②VO+5HC O===V (C O)+4CO↑+5HO 减少产品损耗 ③LiV(PO )-xe-===Li V(PO )+xLi
2 5 2 2 4 2 2 4 3 2 2 3 2 4 3 3-x 2 4 3
+