文档内容
沉淀溶解平衡、络合平衡图像的分析应用
(选择题1~5题,每小题4分,6~11题,每小题5分,共50分)
1.(2024·贵阳模拟)已知:pAg=-lg c(Ag+),常温下向10 mL 0.1 mol·L-1AgNO 溶液中滴加0.1 mol·L-1NaCl溶
3
液的滴定曲线 Ⅰ 如图所示。已知:K (AgCl)>K (AgI)。下列说法正确的是( )
sp sp
A.常温下,K (AgCl)=1.0×10-5.87
sp
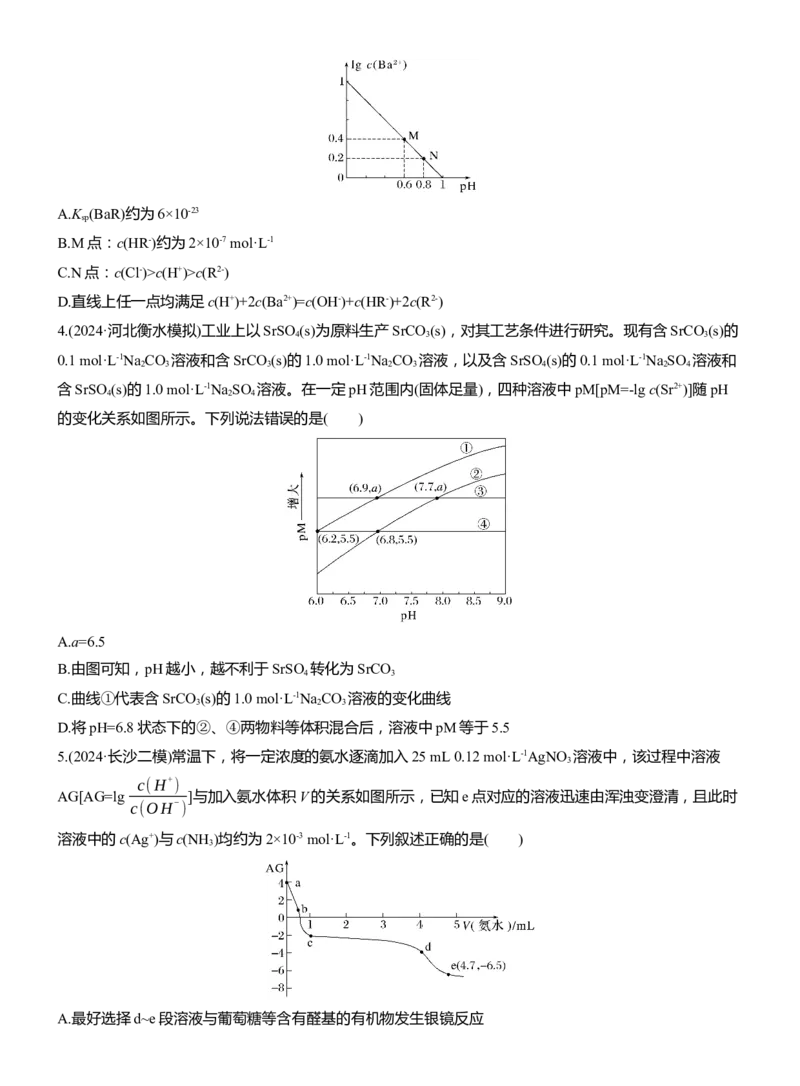
B.溶液中水的电离程度:a=cc(H+)>c(R2-)
D.直线上任一点均满足c(H+)+2c(Ba2+)=c(OH-)+c(HR-)+2c(R2-)
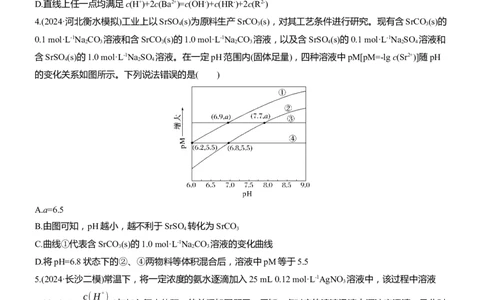
4.(2024·河北衡水模拟)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有含SrCO (s)的
4 3 3
0.1 mol·L-1Na CO 溶液和含SrCO (s)的1.0 mol·L-1Na CO 溶液,以及含SrSO (s)的0.1 mol·L-1Na SO 溶液和
2 3 3 2 3 4 2 4
含SrSO (s)的1.0 mol·L-1Na SO 溶液。在一定pH范围内(固体足量),四种溶液中pM[pM=-lg c(Sr2+)]随pH
4 2 4
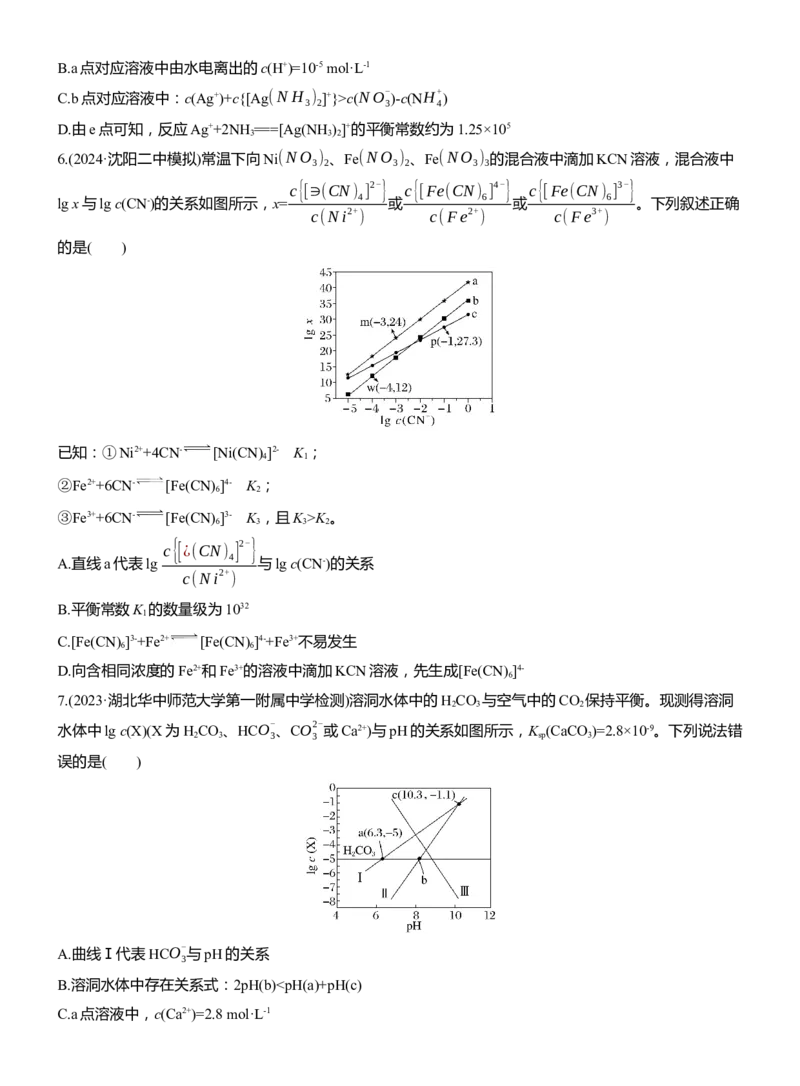
的变化关系如图所示。下列说法错误的是( )
A.a=6.5
B.由图可知,pH越小,越不利于SrSO 转化为SrCO
4 3
C.曲线①代表含SrCO (s)的1.0 mol·L-1Na CO 溶液的变化曲线
3 2 3
D.将pH=6.8状态下的②、④两物料等体积混合后,溶液中pM等于5.5
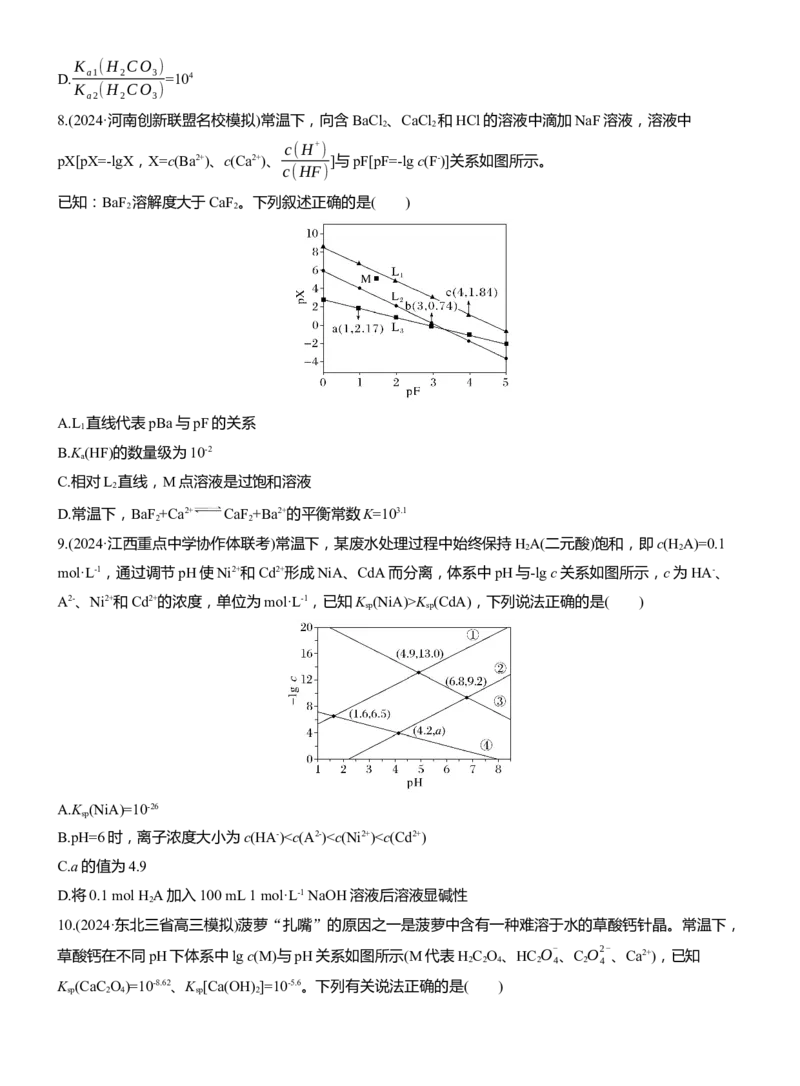
5.(2024·长沙二模)常温下,将一定浓度的氨水逐滴加入25 mL 0.12 mol·L-1AgNO 溶液中,该过程中溶液
3
c(H+
)
AG[AG=lg ]与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时
c(OH-
)
溶液中的c(Ag+)与c(NH )均约为2×10-3 mol·L-1。下列叙述正确的是( )
3
A.最好选择d~e段溶液与葡萄糖等含有醛基的有机物发生银镜反应B.a点对应溶液中由水电离出的c(H+)=10-5 mol·L-1
C.b点对应溶液中:c(Ag+)+c{[Ag(N H ) ]+}>c(NO- )-c(NH+ )
3 2 3 4
D.由e点可知,反应Ag++2NH ===[Ag(NH ) ]+的平衡常数约为1.25×105
3 3 2
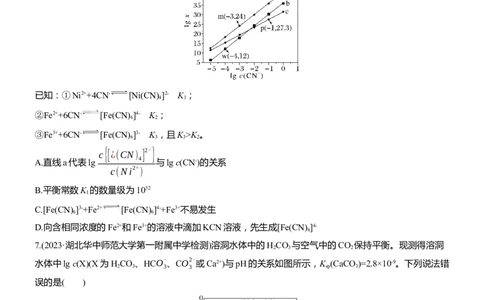
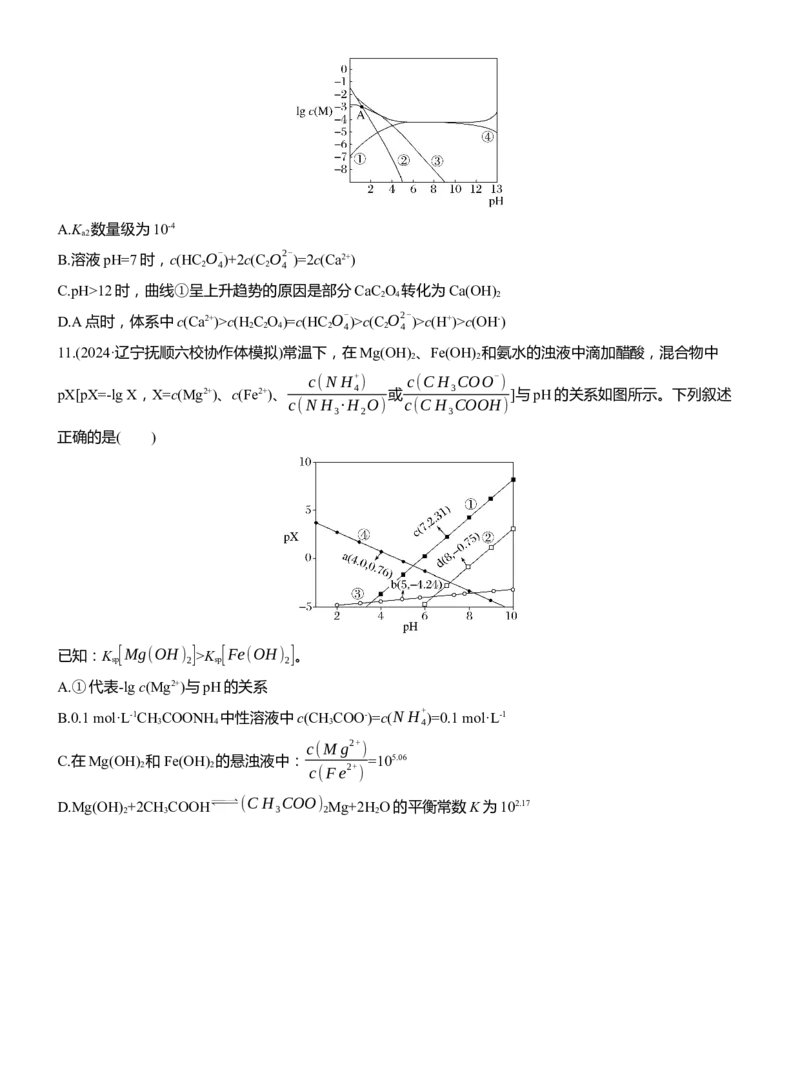
6.(2024·沈阳二中模拟)常温下向Ni(NO ) 、Fe(NO ) 、Fe(NO ) 的混合液中滴加KCN溶液,混合液中
3 2 3 2 3 3
c{[∋(CN) ] 2-} c{[Fe(CN) ] 4-} c{[Fe(CN) ] 3-}
lg x与lg c(CN-)的关系如图所示,x= 4 或 6 或 6 。下列叙述正确
c(Ni2+
)
c(Fe2+
)
c(Fe3+
)
的是( )
已知:①Ni2++4CN- [Ni(CN) ]2- K ;
4 1
②Fe2++6CN- [Fe(CN) ]4- K ;
6 2
③Fe3++6CN- [Fe(CN) ]3- K ,且K >K 。
6 3 3 2
c{[¿(CN) ] 2-}
A.直线a代表lg 4 与lg c(CN-)的关系
c(Ni2+
)
B.平衡常数K 的数量级为1032
1
C.[Fe(CN) ]3-+Fe2+ [Fe(CN) ]4-+Fe3+不易发生
6 6
D.向含相同浓度的Fe2+和Fe3+的溶液中滴加KCN溶液,先生成[Fe(CN) ]4-
6
7.(2023·湖北华中师范大学第一附属中学检测)溶洞水体中的H CO 与空气中的CO 保持平衡。现测得溶洞
2 3 2
水体中lg c(X)(X为H CO
、HCO- 、CO2-
或Ca2+)与pH的关系如图所示,K (CaCO )=2.8×10-9。下列说法错
2 3 3 3 sp 3
误的是( )
A.曲线Ⅰ代表HCO-
与pH的关系
3
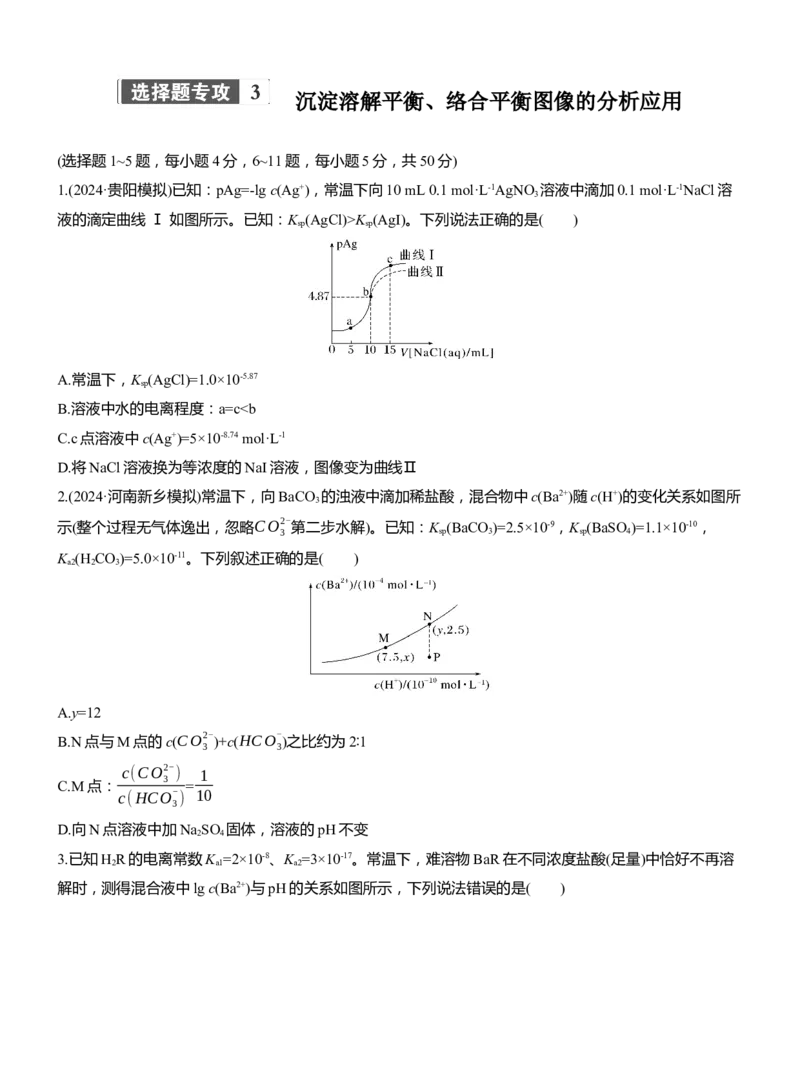
B.溶洞水体中存在关系式:2pH(b)K (CdA),下列说法正确的是( )
sp sp
A.K (NiA)=10-26
sp
B.pH=6时,离子浓度大小为c(HA-)12时,曲线①呈上升趋势的原因是部分CaC O 转化为Ca(OH)
2 4 2
D.A点时,体系中c(Ca2+)>c(H C O )=c(HC
O-
)>c(C
O2-
)>c(H+)>c(OH-)
2 2 4 2 4 2 4
11.(2024·辽宁抚顺六校协作体模拟)常温下,在Mg(OH) 、Fe(OH) 和氨水的浊液中滴加醋酸,混合物中
2 2
c(N H+ ) c(CH COO- )
pX[pX=-lg X,X=c(Mg2+)、c(Fe2+)、 4 或 3 ]与pH的关系如图所示。下列叙述
c(N H ·H O) c(CH COOH)
3 2 3
正确的是( )
已知:K [Mg(OH) ]>K [Fe(OH) ]。
sp 2 sp 2
A.①代表-lg c(Mg2+)与pH的关系
B.0.1 mol·L-1CH COONH 中性溶液中c(CH COO-)=c(N H+ )=0.1 mol·L-1
3 4 3 4
c(M g2+ )
C.在Mg(OH) 和Fe(OH) 的悬浊液中: =105.06
2 2 c(Fe2+
)
D.Mg(OH)
2
+2CH
3
COOH (CH
3
COO)
2
Mg+2H
2
O的平衡常数K为102.17答案精析
1.C
2.A [N点c(Ba2+)=2.5×10-4 mol·L-1,根据K (BaCO
)=2.5×10-9,则N点c(CO2-
)=1×10-5 mol·L-1,整个过程
sp 3 3
无气体逸出,忽略CO2- 第二步水解,存在元素守恒:c(Ba2+)=c(CO2- )+c(HCO- ),则c(HCO-
)=2.4×10-4
3 3 3 3
c(H+ )·c(CO2-
)
3
mol·L-1,K (H CO )= =5.0×10-11,计算可得c(H+)=1.2×10-9 mol·L-1,则y=12,A正确;根据
a2 2 3 c(HCO-
)
3
元素守恒:c(Ba2+)=c(CO2- )+c(HCO- ),N点与M点的c(CO2- )+c(HCO-
)之比即两点c(Ba2+)之比,N点
3 3 3 3
c(H+ )·c(CO2-
)
3
c(Ba2+)=2.5×10-4 mol·L-1,M点c(H+)=7.5×10-10 mol·L-1,K (H CO )= =5.0×10-11,可得15c(
a2 2 3 c(HCO-
)
3
CO2- )=c(HCO- ),则c(Ba2+)=16c(CO2- ),K (BaCO )=c(Ba2+)·c(CO2- )=2.5×10-9,求得c(CO2- )=1.25×10-5
3 3 3 sp 3 3 3
2.5×10-4
mol·L-1,c(Ba2+)=2×10-4
mol·L-1,N点与M点的c(CO2- )+c(HCO-
)之比为 =5∶4,M点:
3 3 2×10-4
c(CO2-
) 1
3
= ,B、C错误;向N点溶液中加硫酸钠固体,溶液中硫酸根离子浓度增大,硫酸根离子与钡
c(HCO- ) 15
3
离子反应生成更难溶的硫酸钡,钡离子浓度减小,碳酸钡向沉淀溶解的方向移动,CO2- 浓度增大,CO2-
3 3
水解使溶液呈碱性,则溶液的pH增大,D错误。]
c(Ba2+
)
3.D [直线上,lg c(Ba2+)+pH=1,即 =10;难溶物BaR与足量盐酸发生反应:BaR+2H+ Ba2+
c(H+
)
c2 (H+ )·c(R2-
)
+H R,溶液中存在c(Ba2+)≈c(H R),K ·K = ,K (BaR)=c(Ba2+)·c(R2-)=K ·K ×
2 2 a1 a2 c(H R) sp a1 a2
2
c(Ba2+ )·c(H R)
2 =2×10-8×3×10-17×100=6×10-23,A正确;M点,c(H+)=10-0.6 mol·L-1,c(Ba2+)≈c(H R)=100.4
c2 (H+
)
2
K ×c(H R) 2×10-8×100.4
a1 2
mol·L-1,c(HR-)= = =2×10-7 mol·L-1,B正确;溶液中溶质为BaCl 、H R、
c(H+
)
10-0.6 2 2
c2 (H+ )·c(R2-
)
HCl,K ·K = ,N点时,c(H+)=10-0.8 mol·L-1,c(Ba2+)≈c(H R)=100.2 mol·L-1,则c(R2-)=
a1 a2 c(H R) 2
2
c(Ba2+ ) 100.2
×K ·K = ×2×10-8×3×10-17 mol·L-1=6×10-23.2 mol·L-1,c(Cl-)最大,所以N点:
c2 (H+ ) a1 a2 (10-0.8 ) 2
c(Cl-)>c(H+)>c(R2-),C正确;直线上任一点均满足电荷守恒:c(H+)+2c(Ba2+)=c(OH-)+c(HR-)+2c(R2-)+c(Cl-),
所以c(H+)+2c(Ba2+)>c(OH-)+c(HR-)+2c(R2-),D错误。]
4.D [温度不变时,K (SrCO )和K (SrSO )均不变;Na CO
溶液中存在水解平衡:CO2-
+H O
HCO-
sp 3 sp 4 2 3 3 2 3
+OH-、HCO-
+H O H CO
+OH-,随着pH的增大,溶液中CO2-
的浓度增大,溶液中Sr2+的浓度减小,
3 2 2 3 3pM增大,pH相同时1.0 mol·L-1 Na CO
溶液中CO2-
的浓度大于0.1 mol·L-1 Na CO
溶液中CO2-
的浓度,故
2 3 3 2 3 3
曲线①代表含SrCO (s)的1.0 mol·L-1 Na CO 溶液的变化曲线,曲线②代表含SrCO (s)的0.1 mol·L-1 Na CO
3 2 3 3 2 3
溶液的变化曲线;Na SO
属于强酸强碱盐,随着pH的增大,溶液中SO2- 的浓度不变,SO2-
浓度越大、
2 4 4 4
Sr2+的浓度越小、pM越大,故曲线③代表含SrSO (s)的1.0 mol·L-1 Na SO 溶液的变化曲线,曲线④代表含
4 2 4
SrSO (s)的0.1 mol·L-1 Na SO 溶液的变化曲线,由曲线④的数据可计算K (SrSO )=10-5.5×0.1=10-6.5。温度不
4 2 4 sp 4
10-6.5
变,K (SrSO )不变,根据分析,曲线③上c(Sr2+)= mol·L-1=10-6.5 mol·L-1,pM=-lg 10-6.5=6.5,即
sp 4 1.0
a=6.5,A项正确;SrSO 转化为SrCO 的反应:SrSO
(s)+CO2-
(aq) SrCO
(s)+SO2-
(aq),溶液pH越小,
4 3 4 3 3 4
CO2-
浓度减小,平衡逆向移动,越不利于SrSO 转化为SrCO ,B项正确;将pH=6.8状态下的②、④两物
3 4 3
料等体积混合后,相当于稀释,瞬间Sr2+的浓度不变,但CO2- 、SO2-
的浓度减小,故固体溶解,Sr2+浓度
3 4
增大,pM减小,即pM<5.5,D项错误。]
5.B [e点所得溶液为银氨溶液,则与葡萄糖等含有醛基的有机物发生银镜反应最好选用e点溶液,故A错
c(H+
)
误;a点没有加入氨水,溶液为硝酸银溶液,水解促进水的电离,AG=lg =4,c(H+)=10-5 mol·L-1,
c(OH-
)
由水电离出的c(H+)=10-5 mol·L-1,故B正确;由图可知,b点溶液中AG大于0,溶液中氢离子浓度大于氢
氧根离子浓度,由电荷守恒关系c(Ag+)+c{[Ag(NH )
]+}+c(NH+ )+c(H+)=c(OH-)+c(NO-
)可知,溶液中c(Ag+)
3 2 4 3
+c{[Ag(NH ) ]+}K ,推出直线a代表lg 6 与lg c(CN-)的关系,直线b代表lg 6
3 2 c(Fe3+
)
c(Fe2+
)
c{[∋(CN) ] 2- }
与lg c(CN-)的关系,直线c代表lg 4 与lg c(CN-)的关系,A错误;将p点坐标代入
c(Ni2+
)
1027.3
x =K ·c4(CN-),推出K = =1031.3,数量级为1031,B错误;[Fe(CN) ]3-+Fe2+ [Fe(CN) ]4-+Fe3+反应平
1 1 1 (10-1
)
4 6 6
c(Fe3+ )·c{[Fe(CN) ] 4- } c(Fe3+ )·c{[Fe(CN) ] 4- }·c6 (CN- ) K 1036
6 6 2
衡常数K= = = = =10-6,平衡常数较
c(Fe2+ )·c{[Fe(CN) ] 3- } c(Fe2+ )·c{[Fe(CN) ] 3- }·c6 (CN- ) K 1042
6 6 3
小,反应不易发生,C正确;因为K >K ,因此向含相同浓度的Fe2+、Fe3+的溶液中滴加KCN溶液,先生
3 2
成[Fe(CN) ]3-,D错误。]
67.B
[随着pH增大,溶液碱性增强,HCO- 、CO2- 浓度均增大,pH较小时c(HCO- )>c(CO2-
),故曲线Ⅰ为
3 3 3 3
HCO- 与pH的关系,曲线Ⅱ为CO2- 与pH的关系,曲线Ⅲ为Ca2+与pH的关系,A正确;K =
3 3 a1
c(H+ )·c(HCO- ) c(H+ )·c(CO2- ) K (H CO )
3 =10-6.3,K = 3 =10-10.3, a1 2 3 =104,D正确;b点时,c(CO2-
c(H CO ) a2 c(HCO- ) K (H CO ) 3
2 3 3 a2 2 3
c2 (H+ )·c(CO2-
)
)=c(H CO ),K ·K =10-6.3×10-10.3= 3 =c2 (H+),pH(b)=8.3,由此可知2pH(b)=pH(a)+pH(c),B
2 3 a1 a2 c(H CO ) b
2 3
c2 (H+ )·c(CO2-
)
(10-6.3
)
2×c(CO2-
)
错误;a点溶液中,pH=6.3,K ·K = 3 = 3 =10-6.3×10-10.3,则c(CO2- )=10-9
a1 a2 c(H CO ) 10-5 3
2 3
K (CaCO )
sp 3
mol·L-1,c(Ca2+)= mol·L-1=2.8 mol·L-1,C正确。]
10-9
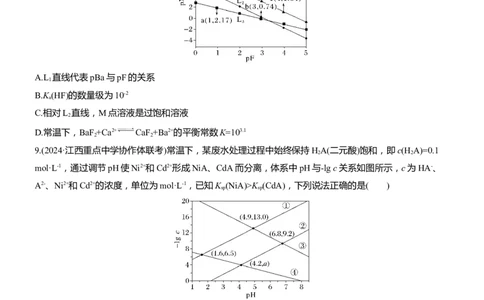
8.D [根据图像中L 和L 的斜率相等,L 斜率较小且结合BaF 、CaF 组成相同可知:BaF 、CaF 直线的
1 2 3 2 2 2 2
c(H+
)
斜率相等,故L 代表p ~pF关系;又因为BaF 溶解度大于CaF ,所以K (BaF )>K (CaF ),即L 代
3 c(HF) 2 2 sp 2 sp 2 1
c(H+
)
表pCa~pF关系,L 代表pBa~pF关系,A错误;根据分析且利用图中a点坐标数据计算:K(HF)=
2 a c(HF)
×c(F-)=10-2.17×10-1=10-3.17,数量级为10-4,B错误;L 是BaF 的饱和溶液,而M点的QK (CdA),由此可
sp sp
知曲线①代表Cd2+,曲线②代表Ni2+。曲线②③交点,c(Ni2+)=c(A2-)=10-9.2 mol·L-1,则有
K (NiA)=c(Ni2+)·c(A2-)=10-18.4,故A错误;由图可知pH=6时,离子浓度大小为
sp
c(HA-)>c(Ni2+)>c(A2-)>c(Cd2+),故B错误;取曲线④上点(1.6,6.5),该点c(H+)=10-1.6 mol·L-1,c(HA-)=10-6.5
c(H A- )·c(H+ ) 10-6.5×10-1.6
mol·L-1,c(H A)=0.1 mol·L-1,K = = =10-7.1,将点(4.2,a)代入K =
2 a1 c(H A) 0.1 a1
2
c(H A- )·c(H+ ) 10-a×10-4.2
= =10-7.1,解得a=3.9,故C错误;取曲线③上点(6.8,9.2),该点c(H+)=10-6.8
c(H A) 0.1
2
c(A2- )·c2 (H+
)
c(A2- )·c2 (H+
)
10-9.2×(10-6.8
)
2
mol·L-1,c(A2-)=10-9.2 mol·L-1,K ·K = ,则K = = =10-14.7,
a1 a2 c(H A) a2 c(H A)·K 0.1×10-7.1
2 2 a1K 10-14
w
将0.1 mol H A加入100 mL 1 mol·L-1 NaOH溶液后得到NaHA溶液,HA-水解常数K = = =10-
2 h K 10-7.1
a1
6.9>K ,说明HA-水解程度大于电离程度,溶液显碱性,故D正确。]
a2
10.B [①表示C
O2-
、②表示H C O 、③表示HC
O-
、④表示Ca2+。HC
O-
H++C
O2-
,K =
2 4 2 2 4 2 4 2 4 2 4 a2
c(H+ )·c(C O2- )
2 4 ,①③相交时c(HC O- )=c(C O2- ),从图中可知此时pH大于4小于5,所以K 数量级为
c(HC O- ) 2 4 2 4 a2
2 4
10-5,故A错误;溶液pH=7时c(H+)=c(OH-),溶液中电荷守恒:c(HC
O-
)+2c(C
O2-
)+c(OH-)=2c(Ca2+)
2 4 2 4
+c(H+),所以c(HC
O-
)+2c(C
O2-
)=2c(Ca2+),故B正确;由图像可知,pH>12时,如pH=13,c(OH-)=0.1
2 4 2 4
mol·L-1、c(Ca2+)≈10-5 mol·L-1,此时Q[Ca(OH) ]=10-5×(10-1 ) 2=10-7