文档内容
专题六 原子结构 元素周期侓
必备知识 解读
一、弄清原子结构与周期表位置的关系
(1)周期数=电子层数:同周期元素电子层数相同,原子序数依次增大,半径遂渐减小。
(2)主族数=最外层电子数=最高正价数:同主族元素最外层电子数相同,电子层数依次增
大,原子半径依次增大,
(3)同主族元素原子序数相差:
2-3周期相差8,如:2-3周期 N与 P相差8;
7 15
3-4周期:IA、IIA族相差8,如:Na和K相差8,
IIIA、VIIA族相差18。如: P和 As和相差18。
15 33
(4)二、三周期的ⅡA与ⅢA族原子序数之差都为1,四、五周期的ⅡA与ⅢA族原子序数
之差都为11,六、七周期为25;
(5)0族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32、32。
(6)元素周期表中几个特殊的族
①没有非金属元素的族——ⅡA族;
②所含元素种类最多的族——ⅢB族(含有镧系、锕系);
③化合物种类最多的族——ⅣA族;
④最外层电子数不相同的族——零族。
二、掌握规律--
元素周期表中的有关规律
1、原子序数规律
(1)同主族、邻周期元素的原子序数差:①元素周期表中左侧元素(ⅠA、ⅡA族):同主族
相邻两元素中,Z(下)=Z(上)+上一周期元素所在周期的元素种类数目;
②元素周期表中右侧元素(ⅢA~ⅦA族):
同主族相邻两元素中,Z(下)=Z(上)+下一周期元素所在周期的元素种类数目。
(2)同周期的ⅡA和ⅢA的原子序数差可能为1,11,25。
2、元素化合价规律
(1)主族元素的最高正化合价=它所在的族序数=最外层电子数(即价电子数),但要注意F无
正价,O一般不显正价。
(2)只有非金属元素才有负价,非金属元素的最高正价与它的负化合价的绝对值之和等于
8。(3)若某原子的最外层电子数为奇数(m),则正常化合价为奇数,从+1价到+m价,若出现偶数
则为非正常化合价,其氧化物为不成盐氧化物,如NO、NO。
2
(4)若某原子的最外层电子数为偶数(n),则元素的正常化合价为一系列偶数,例如
-2 +4 +6。
S、S、S
3、微粒半径大小比较的一般规律
(1)同周期(除0族外),随原子序数的递增,原子半径由大到小,如Na>Mg>Al;
(2)同主族,随原子序数的递增,原子半径、离子半径由小到大,如LiZ(B)>Z(A);原子半径
r(C)>r(A)>r(B);A、B、C若为非金属元素,则非金属性B>A>C,单质的氧化性B>A>C
等。
三、比较元素及化合物的性质比较元素的性质主要有:
1.比较原子或离子半径大小
2.金属性和非金属性
3.最高价氧化物对应水化物的碱性越强,金属性越强
4.最高价氧化物对应水化物的酸性越强,非金属性越强
5.气态氢化物的还原性越弱,非金属性越强;气态氢化物越稳定,非金属性越强
6.气态氢化物水溶液的酸性强弱,与非金属性越强弱无关。
7.气态氢化物、氧化物等物质的溶沸点
四、书写电子式,
1.几种电子式的书写方法
(1)原子:把原子的最外层电子全部排列在元素符号周围。
(2)阳离子:金属阳离子的电子式就是其离子符号。复杂的阳离子要用“[ ]”如:HO+
3
和NH_
(3)非金属阴离子:将得到的电子也都标在元素符号周围,并将符号用“[ ]”括上,右上
角标出所带的电荷数。
(4)共价化合物(或单质):用点将每个原子的最外层电子表示出来,最外层有几个电子就打
几个点,每个原子的周围都形成8电子(或2电子)稳定结构。
(5)离子化合物:分别画出阴、阳离子的电子式,同种离子不相邻。
2.对比书写电子式
—OH________________,OH-___________,
HO+________________,NH___________,
3
NH________________。
2
HClO________________,CCl ___________,
4
CO ________________,CS ___________,
2 2
COS________________,HCHO___________,
CH________________,(CN) ___________,
2 4 2
(SCN)________________,COCl ___________,
2 2
NH________________。
2 4
Na S________________,NaH___________,
2
NH H________________,NaCN___________,
4
NaSCN________________,NaBH ___________。
4四、分子间的作用力和氢键
1.分子间作用力只针对分子晶体,分子晶体内部存在共价键,分子之间存在分子间的作用
力。
(1)定义:把分子结合在一起的作用力,又称范德华力。
(2)特点:分子间作用力比化学键弱得多,它主要影响物质的熔沸点、溶解性等物理性质,而化学键主要影响物质的化学性质。
(3)规律:一般来说,对于组成与结构相似的物质,相对分子质量越大,分子间作用力越大,物
质的熔、沸点也越高。例如:熔、沸点:I>Br>Cl>F。
2 2 2 2
2.氢键
(1)定义:分子间存在的一种比分子间作用力大的相互作用。
(2)形成条件:通常是与N、O、F成键的H与其他N、O、F形成氢键。
(3)存在:氢键存在广泛,如蛋白质、醇、羧酸、HO、NH、HF等含H—F、H—N、H—O键的
2 3
分子之间。分子间氢键会使物质的熔点和沸点升高。
应考能力 解 密
一、根据原子结构和周期表中的位置以及性质准确推断元素
1.元素周期表中周期、族、原子序数的关系推断
(1)同主族元素下周期元素是上周期元素的2倍:O、S
(2)同主族元素下周期元素是上周期元素的3倍:Be、Mg
2.位置与元素推断
(1)族序数等于周期数的元素:H、Be、Al。
(2)族序数等于周期数2倍的元素:C、S。
(3)族序数等于周期数3倍的元素:O。
(4)周期数是族序数2倍的元素:Li、Ca。
(5)周期数是族序数3倍的元素:Na、Ba。
(6)最高正价与最低负价代数和为零的短周期元素:H、C、Si。
(7)最高正价是最低负价绝对值3倍的短周期元素:S。
(8)除H外,原子半径最小的元素:F。
(9)最高正价不等于族序数的短周期元素:O(F无正价)。
3.核外电子排布与元素推断,根据元素的特殊的电子层结构推断元素
(1)最外层有1个电子的元素:H、Li、Na、K。
(2)最外层电子数等于次外层电子数的元素:Be、Ar。
(3)最外层电子数是次外层电子数2倍的元素:C。
(4)最外层电子数是次外层电子数3倍的元素:O。
(5)最外层电子数是内层电子数总数一半的元素:Li、P。
(6)次外层电子数是最外层电子数2倍的元素:Li、Si。(7)次外层电子数是其他各层电子总数2倍的元素:Li、Mg。
(8)次外层电子数与其他各层电子总数相等的元素:S。
(9)电子层数与最外层电子数相等的元素:H、Be、Al。
4.元素或物质的性质与元素推断
(1)元素的性质与元素推断
前三周期原子半径最大的:Na
第三同期离子半径最小的:Al
最高价氧化物水化物是强酸的:S 、N、Cl
最高价氧化物水化物是强碱的:Na
气态氢化物水溶液是强酸的:Cl
气态氢化物水溶液是强碱的:N
(2)主族元素性质的特殊性
氢 最轻的元素,其单质可以填充气球
形成化合物种类最多的元素;可形成自然界硬度最大的物质;简单氢化物中含氢质量
碳
分数最大的元素
氮 空气中含量最多的元素;气态氢化物的水溶液呈碱性的元素
地壳中含量最多的元素;简单氢化物的沸点最高的元素;氢化物在通常状况下呈液态
氧
的元素
最活泼的非金属元素;无正价的元素;无含氧酸的非金属元素;无氧酸可腐蚀玻璃的元
氟
素;气态氢化物最稳定的元素;阴离子的还原性最弱的元素
短周期元素中与水反应较剧烈的金属元素,最高价氧化物的水化物碱性最强的元素;
钠 短周期主族元素中原子半径最大的元素;与氧气在加热条件下反应生成过氧化物
(NaO)的元素;焰色反应为黄色的元素
2 2
地壳中含量最多的金属元素;最高价氧化物及其水化物既能与强酸反应,又能与强碱
铝
反应
硅 良好的半导体材料,地壳中含量第二的元素,能跟强碱溶液反应,还能被氢氟酸溶解
硫 淡黄色固体,它的氢化物可与其最高价氧化物对应水化物的浓溶液发生氧化还原反应
氯 短周期元素中最高价氧化物对应水化物酸性最强的元素
(3)常见物质的性质与元素推断
A.氢化物可以做致冷剂的是N,显碱性的氢化物是NH、NH。
3 2 4
B.氢化物沸点可能高于水的C,氢化物水溶液可以腐蚀玻璃F。
C.红棕色气体是NO,温室效率是CO,污染空气最严重的是SO。
2 2 2
D.半导体做芯片、光电池是Si,光导纤维是SiO。
2
E.不能用氯化物电解而只能用氧化物电解制备的是AI
F.最高价氧化物的水化物可以两两相互反应的是Na、AI、S或Na、AI、CI
G.已知浓度和PH,推断是强酸的是HCI,是强碱的是NaOH.H. 某三种元素的两种钠盐,相互反应,产生无色气体是H、O、S。
二.根据结构式推断元素
(1).根据化合物的结构式判断元素:
看某元素在结构式中化学键的数目,再椐共价键的数目,判断元素。
元素 C、Si B、N、P、As O、S F、Cl、H
共用电子对数 4 3 2 1
刚好形成这些共价键,就是电中性的,如果多一个共价键或少一个共价键,就会带电荷。
(2).注意NH+和BH- 、HO+、OH-的区别:
4 4 3
有O、S、N、P元素多一个共价键带正电荷,多的一定是和H结合的共价键,少一个共价键
带负电荷;
有B元素多一个共价键带负电荷,多的一定是和H结合的共价键,但是是H-。
(3)元素W、X、Y、Z的原子序数依次增大、且总和为24.
推断元素:X如果是B就带负电荷,如果是C就是电中性的,如果是N、P就带正电荷。由
此推断:X是B
三、比较元素及化合物的性质
1..比较原子或离子半径
(1).同周期从左到右,原子半径逐渐减小;
同主族从上到下,原子半径逐渐增大。
(2).同周期从左到右,阳离子半径逐渐减小,阴离子半径逐渐也减小,阴离子大于阳离
子;同主族从上到下,离子半径逐渐增大。
(3).上周期的阳离子和下周期的阴离子电子层结构相同, 电子层结构相同的离子,原子
序数越大,半径越小。
2..比较金属性和非金属性
(1).比较金属性:
就是比较金属的失电子能力,即金属的还原性;
在金属活动性顺序表中越靠前,金属性越强,置换反应。 单质与水或非氧化性酸反应越剧烈,金属性越强
阳离子氧化性越弱,金属性越强
最高价氧化物水化物的碱性强弱。
最高价氧化物对应水化物的碱性越强,金属性越强
元素在周期表中的位置:同周期的左边或同主族的下方元素的金属性强
(2).比较非金属性:
非金属性单质的氧化性
与H 化合越容易,气态氢化物越稳定,非金属性越强
2
阴离子还原性越弱,非金属性越强;
气态氢化物的还原性越弱,非金属性越强;
非金属性单质之间置换反应。
最高价氧化物水化物的酸性强弱。
最高价氧化物对应水化物的酸性越强,非金属性越强
元素在周期表中的位置:同周期的右边或同主族的上方元素的非金属性强
3.应用分子间的作用力和氢键从而比较熔沸点
(1).要比较物质的熔沸点,必须要了解物质的组成和晶体类型
由原子直接组成,叫原子晶体,无小分子,由共价键结合。原子晶体熔沸点很高,硬度
大,不溶于溶剂。如金刚石、晶体硅、二氧化硅等。
由原子先形成离子,再由离子组成物质,叫离子晶体,无小分子,由离子键或离子键、共
价键结合。熔沸点较高,硬度较大,一般易溶于水,难溶于有机溶剂。如:氯化钠等
由原子形成分子,再由分子组成物质,叫分子晶体,分子内有共价键,分子间存在分子间
作用力。熔沸点彽,硬度小,极性分子组成的物质,一般易溶于水,非极性分子组成
的物质,易溶于有机溶剂。如:水、氨气、硫等。
(2).比较物质的溶沸点的规律
.固体>液体>气体
.原子晶体>离子晶体>分子晶体
.分子间有氢键>相对分子质量大的物质>相对分子质量小的物质
.同是原子晶体或离子晶体:半径小的》半径大的
三、能否满足8电子稳定结构
1.原子序数≤5的原子不能满足8电子稳定结构
2.第N族元素,如果形成8-N个共用电子对,就满足8电子稳定结构;如果大于8-N个共用电子对,就不满足8电子稳定结构;
形成如下表所示的共价键数,可达8电子结构.
元素 C、Si N、P、As O、S F、Cl
共用电子对数 4 3 2 1
高考实例剖析
高考怎么考《原子结构 元素周期侓》,根据高考指挥棒来学习《原子结构 元素周期侓》
【高考实例一】根据原子结构和周期表中的位置以及性质准确推断元素
1.(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数
之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电
子数的2倍。下列说法正确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的沸点: D.最高价含氧酸的酸性:
【答案】D
【解析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,
Y原子最外层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于
第三周期,Y的最外层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则
X为Al元素,Q、X、Y、Z的最外层电子数之和为19,则Q、Z的最外层电子数之和为19-3-
4=12,主族元素的最外层电子数最多为7,若Q的最外层电子数为7,为F元素,Z的最外
层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,则Z的最外层电子数为
6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,为Cl元素;
综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解题。
A项:X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上
往下依次减弱,故非金属性:Q>X,A错误;
B项:由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点
Si>Al,即Y>X,B错误;
C项:含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为H O或NH
2 3
或HF,Z为Cl或S或P,其简单氢化物为HCl或H S或PH ,由于前者物质中存在分子间氢
2 3
键,而后者物质中不存在,故沸点Q>Z,C错误;D项:元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于
Si,因此最高价含氧酸酸性:Z>Y,D正确;
故答案为:D。
【实战演练】
1.(2022·江西九江·一模)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大,
Z、M同主族,M与Z组成的化合物的排放是形成酸雨的主要原因之一,X是元素周期表中
原子半径最小的元素,Y与Z相邻,下列说法正确的是
A.原子半径:M>Q>Z> Y
B.气态氢化物稳定性:Y>Z>Q>M
C.X、Y、Z、M四种元素至少能形成三种离子化合物
D.Q的氧化物对应水化物的酸性强于M的氧化物对应水化物
【答案】C
【解析】X、Y、Z、M、Q是五种原子序数依次增大的短周期主族元素,X是元素周期表中
原子半径最小的元素,则X为H元素;Z、M同主族,M与Z组成的化合物的排放是形成酸
雨的主要原因之一,则Z为O元素、M为S元素;Y与Z相邻,则Y为N元素;Q的原子序
数大于M,则Q为Cl元素。
A项:同周期元素,从左到右原子半径依次减小,则氧原子的原子半径小于氮原子,故A
错误;
B项:元素的非金属性越强,气态氢化物稳定性的稳定性越强,氧元素的非金属性强于氮
元素,则水的稳定性强于氨气,故B错误;
C项:氢、氮、氧、硫四种元素形成的硫酸铵、硫酸氢铵、亚硫酸铵、亚硫酸氢铵都是离
子化合物,故C正确;
D项:次氯酸是弱酸,酸性弱于硫酸,故D错误;
故选C。
2.(2022·陕西汉中·二模)短周期主族元素X、Y、Z、W的原子序数依次增大,X为宇宙中
含量最丰富的元素,Z原子能形成分别含10电子、18电子的两种阴离子,常温下,W的单
质能溶于Y的最高价氧化物对应水化物的稀溶液,但不溶于其浓溶液。下列叙述正确的是
A.原子半径大小顺序为:W>Z>Y>X
B.气态氢化物的稳定性:YHClO,C错误;
2 3
D项:己为HClO,O原子能形成2对共用电子对,H和Cl原子只能形成1对共用电子对,
结构式为H-O-Cl,即A-C-D,D错误;
故选:A。
【高考实例二】根据结构式推断元素
2.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子
序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的
是
A.原子半径:
B.非金属性:
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1
个共价键,X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原
子序数之和,则X为C元素、Y为O元素、Z为F元素、W为Si元素。
A项:同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O
>F,故A正确;
B项:同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非
金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C项:位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D项:原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
【实战演练】
1.(2022·江西·模拟预测)一种低毒杀虫剂的结构如图所示,其组成元素W、X、Y、Z、
M、Q为原子序数依次增大的短周期主族元素,其中W的原子核内只有1个质子,M原子
序数为Y原子最外层电子数的3倍。下列说法错误的是
A.简单氢化物沸点:Z>Y>Q
B.原子半径:M>Q>X>Y>>Z
C.W、X、Z和钠四种元素形成的离子化合物只能促进水的电离
D.该杀虫剂结构中既含有极性共价键又含有非极性共价键
【答案】C
【解析】元素W、X、Y、Z、M、Q为原子序数依次增大的短周期主族元素,其中W的原
子核内只有1个质子,则W为H元素;由结构可知,X形成4个共价键、Y形成3个共价键、
Z形成2个共价键,则X为C元素、Y为 N元素、Z为 O元素,Y原子最外层电子数为5,
M原子序数为Y原子最外层电子数的3倍,故M为P元素。Q形成2个共价键,则Q为S
元素,据此解答。
A项:Y、Z、Q的简单氢化物依次为NH 、H O、 H S,常温下,水为液体,而氨气、硫化
3 2 2
氢为气体,故水的沸点最高,而氨气分子之间形成氢键,氨气的沸点比硫化氢高,即沸点
H O>NH >H S,A项正确;
2 3 2
B项:电子层结构相同的原子,序数越大,半径越小,电子层越多,半径越大,故原子半
径M>Q>Y>Z,B项正确;
C项:W、X、Z和钠四种元素形成的离子化合物为NaHC O 时,HC O 的电离程度大于水解
2 4 2
程度,水的电离受到抑制,C项错误;
D项:由结构可知,该杀虫剂结构中既含有极性共价键又含有非极性共价键,D项正确;
故答案选C。
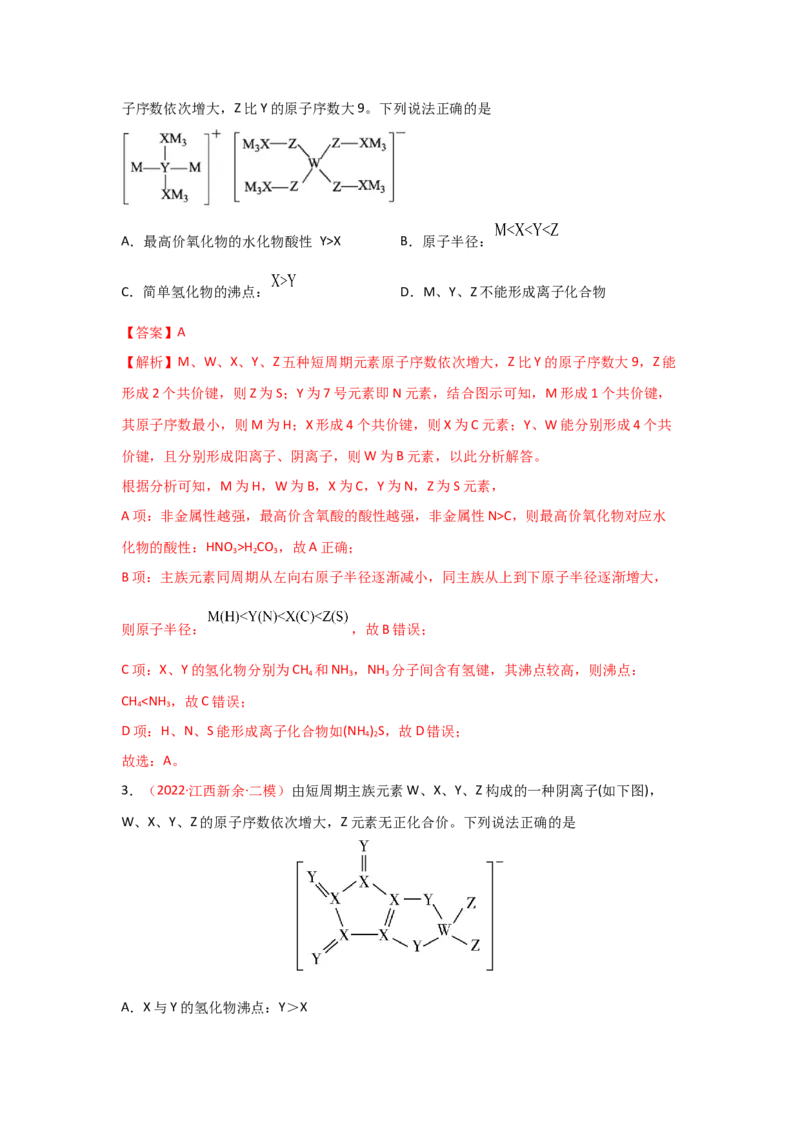
4.(2022·江西鹰潭·二模)某多孔储氢材料结构如图,M、W、X、Y、Z五种短周期元素原子序数依次增大,Z比Y的原子序数大9。下列说法正确的是
A.最高价氧化物的水化物酸性 Y>X B.原子半径:
C.简单氢化物的沸点: D.M、Y、Z不能形成离子化合物
【答案】A
【解析】M、W、X、Y、Z五种短周期元素原子序数依次增大,Z比Y的原子序数大9,Z能
形成2个共价键,则Z为S;Y为7号元素即N元素,结合图示可知,M形成1个共价键,
其原子序数最小,则M为H;X形成4个共价键,则X为C元素;Y、W能分别形成4个共
价键,且分别形成阳离子、阴离子,则W为B元素,以此分析解答。
根据分析可知,M为H,W为B,X为C,Y为N,Z为S元素,
A项:非金属性越强,最高价含氧酸的酸性越强,非金属性N>C,则最高价氧化物对应水
化物的酸性:HNO >H CO ,故A正确;
3 2 3
B项:主族元素同周期从左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,
则原子半径: ,故B错误;
C项:X、Y的氢化物分别为CH 和NH ,NH 分子间含有氢键,其沸点较高,则沸点:
4 3 3
CH X,因为X是碳,有多种氢化物,有的沸点高于水,
A项错误;
B项:同周期主族元素从左向右,元素原子半径逐渐减小,原子半径大小关系是:W > X >Y
> Z,B项错误;
C项:根据图可知,上图中各原子均满足8电子稳定结构,C项正确;
D项:W的最高价氧化物对应的水化物是硼酸,是一种弱酸,D项错误;
答案选C。