文档内容
专题十 工艺流程题 专题检验
(7 小题,共100分)
1.(2022·河南洛阳·三模)(14分)碳酸锶(SrCO )具有屏蔽X射线的功能,广泛应用于彩
3
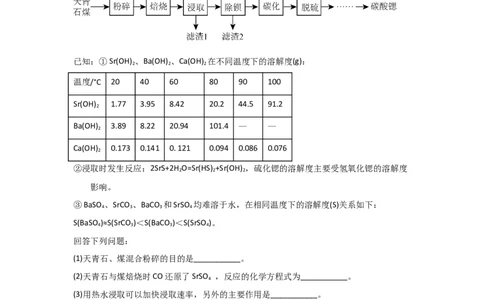
色显示装置、等离子显色装置的荧光屏玻璃中。工业上以天青石(主要成分为SrSO ,
4
含少量BaSO 和CaSO )和煤为原料生产碳酸锶。工艺流程如下:
4 4
已知:①Sr(OH) 、Ba(OH) 、Ca(OH) 在不同温度下的溶解度(g):
2 2 2
温度/°C 20 40 60 80 90 100
Sr(OH) 1.77 3.95 8.42 20.2 44.5 91.2
2
Ba(OH) 3.89 8.22 20.94 101.4 — —
2
Ca(OH) 0.173 0.141 0. 121 0.094 0.086 0.076
2
②浸取时发生反应:2SrS+2H O=Sr(HS) +Sr(OH) ,硫化锶的溶解度主要受氢氧化锶的溶解度
2 2 2
影响。
③BaSO 、SrCO 、BaCO 和SrSO 均难溶于水,在相同温度下的溶解度(S)关系如下:
4 3 3 4
S(BaSO )≈S(SrCO )<S(BaCO )<S(SrSO )。
4 3 3 4
回答下列问题:
(1)天青石、煤混合粉碎的目的是___________。
(2)天青石与煤焙烧时CO还原了SrSO ,反应的化学方程式为___________。
4
(3)用热水浸取可以加快浸取速率,另外的主要作用是___________。
(4)碳化过程控制条件让硫氢化锶吸收二氧化碳有利于产品质量的提高,并且可以提供硫化
氢使氢氧化锶转化为硫氢化锶。写出碳化时硫氢化锶吸收二氧化碳的化学方程式:
___________。
(5)若达到碳化终点后继续碳化,则会使产品产率降低,结合化学方程式解释原因:
___________,取碳化后的料浆滴入无色酚酞试剂,若___________表明到达碳化终
点。
(6)由于碳化所用的CO 中含有少量的O 、SO 等,在碳化时发生副反应,生成少量的
2 2 2SrSO 、SrSO ,所以要对碳化完成的碳酸锶浆进行脱硫处理。方法为加入纯碱,并加热
3 4
煮沸,写出脱硫过程SrSO 与纯碱反应的化学方程式___________。
4
【答案】(1)增大反应物接触面积,加快反应速率,提高原料的利用率
高温
(2)SrSO +4CO SrS+4CO
4 2
(3)促进锶的化合物的溶解,降低钙的化合物的溶解
(4)Sr(HS) +CO +H O=SrCO ↓+2H S
2 2 2 3 2
(5) 二氧化碳足量,发生反应SrCO +CO +H O=Sr(HCO ) ,造成产量下降 无色酚
3 2 2 3 2
酞不变红
Δ
(6)SrSO +Na CO SrCO +Na SO
4 2 3 3 2 4
【解析】天青石(主要成分为SrSO ,含少量BaSO 和CaSO )和煤粉碎后灼烧,SrSO 与碳生
4 4 4 4
成的CO反应生成SrS,利用热水浸取,过滤除去滤渣1,所得滤液除钡,过滤得到滤
渣2,向滤液中通入CO 炭化得到SrCO ,然后脱硫,通过一系列操作得到SrCO ,据此
2 3 3
解答。
(1)依据外界条件对反应速率的影响可知天青石、煤混合粉碎的目的是增大反应物接触面
积,加快反应速率,提高原料的利用率。
高温
(2)天青石与煤焙烧时CO还原了SrSO 生成SrS,反应的化学方程式为SrSO +4CO
4 4
SrS+4CO 。
2
(3)由于Sr(OH) 、Ba(OH) 的溶解度随温度升高而增大,Ca(OH) 的溶解度随温度升高而减
2 2 2
小,所以用热水浸取可以加快浸取速率,另外的主要作用是促进锶的化合物的溶解,
降低钙的化合物的溶解。
(4)碳化时硫氢化锶吸收二氧化碳生成SrCO 和H S,反应的化学方程式为Sr(HS) +CO +H O=
3 2 2 2 2
SrCO ↓+2H S。
3 2
(5)由于二氧化碳足量,发生反应SrCO +CO +H O=Sr(HCO ) ,造成产量下降,所以若达到碳
3 2 2 3 2
化终点后继续碳化,则会使产品产率降低;由于反应中有H S生成,其溶液显酸性,
2
所以取碳化后的料浆滴入无色酚酞试剂,若无色酚酞不变红表明到达碳化终点。
(6)根据原子守恒可知脱硫过程SrSO 与纯碱反应生成SrCO 和Na SO ,氟的化学方程式为
4 3 2 4Δ
SrSO +Na CO SrCO +Na SO 。
4 2 3 3 2 4
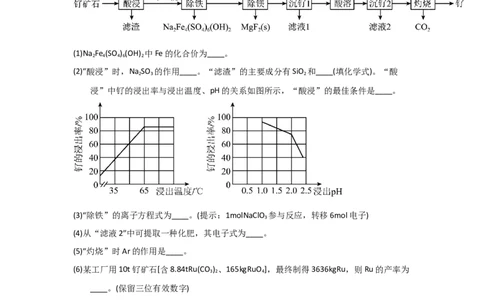
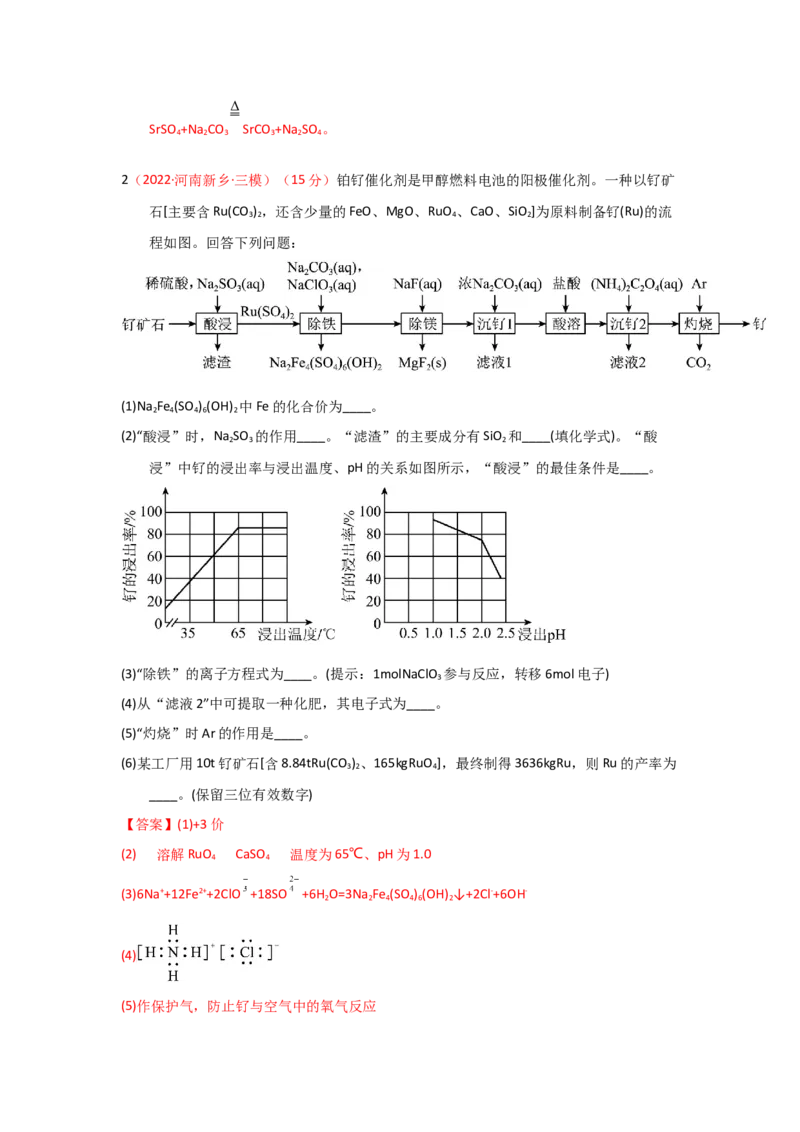
2(2022·河南新乡·三模)(15分)铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿
石[主要含Ru(CO ) ,还含少量的FeO、MgO、RuO 、CaO、SiO ]为原料制备钌(Ru)的流
3 2 4 2
程如图。回答下列问题:
(1)Na Fe (SO ) (OH) 中Fe的化合价为____。
2 4 4 6 2
(2)“酸浸”时,Na SO 的作用____。“滤渣”的主要成分有SiO 和____(填化学式)。“酸
2 3 2
浸”中钌的浸出率与浸出温度、pH的关系如图所示,“酸浸”的最佳条件是____。
(3)“除铁”的离子方程式为____。(提示:1molNaClO 参与反应,转移6mol电子)
3
(4)从“滤液2”中可提取一种化肥,其电子式为____。
(5)“灼烧”时Ar的作用是____。
(6)某工厂用10t钌矿石[含8.84tRu(CO ) 、165kgRuO ],最终制得3636kgRu,则Ru的产率为
3 2 4
____。(保留三位有效数字)
【答案】(1)+3价
(2) 溶解RuO CaSO 温度为65℃、pH为1.0
4 4
(3)6Na++12Fe2++2ClO +18SO +6H O=3Na Fe (SO ) (OH) ↓+2Cl-+6OH-
2 2 4 4 6 2
(4)
(5)作保护气,防止钌与空气中的氧气反应(6)87.8%
【解析】由题给流程可知,钌矿石中加稀硫酸和亚硫酸钠酸浸时,钌元素转化为硫酸钌,
氧化亚铁、氧化镁转化为硫酸亚铁、硫酸镁,氧化钙与稀硫酸反应生成硫酸钙,二氧
化硅与硫酸不反,过滤得到含有二氧化硅、硫酸钙的滤渣和含有硫酸钌的滤液;向滤
液中先后加入氯酸钠溶液、碳酸钠溶液将铁元素转化为生成Na Fe (SO ) (OH) 沉淀,过
2 4 4 4 2
滤得到Na Fe (SO ) (OH) 和滤液;向滤液中加入加氟化钠溶液将镁元素转化为氟化镁沉
2 4 4 4 2
淀,过滤得到氟化镁和滤液;向滤液中加入碳酸钠溶液将钌元素转化为碳酸钌沉淀,
过滤得到滤液1和碳酸钌;碳酸钌溶于盐酸得到氯化钌,向氯化钌溶液中加入草酸铵
溶液将氯化钌转化为草酸钌沉淀,过滤得到含有氯化铵的滤液2和草酸钌;在氩气氛
围中灼烧草酸钌制得钌。
(1)由化合价代数和等于0可知,Na Fe (SO ) (OH) 中铁元素的化合价为+3价,故答案为:+3
2 4 4 6 2
价;
(2)由分析可知,酸浸时加入亚硫酸钠溶液的目的是溶解四氧化钌,将四氧化钌转化为可溶
的硫酸钌;滤渣的主要成分为二氧化硅和硫酸钙;由图可知,温度为65℃、pH为1.0
时,钌的浸出率最大,则酸浸”最佳条件是温度为65℃、pH为1.0,故答案为:溶解
RuO ;CaSO ;温度为65℃、pH为1.0;
4 4
(3)由分析可知,加入氯酸钠溶液、碳酸钠溶液的目的是将铁元素转化为生成
Na Fe (SO ) (OH) 沉淀,反应的离子方程式为6Na++12Fe2++2ClO +18SO
2 4 4 4 2
+6H O=3Na Fe (SO ) (OH) ↓+2Cl-+6OH-,故答案为:6Na++12Fe2++2ClO +18SO
2 2 4 4 6 2
+6H O=3Na Fe (SO ) (OH) ↓+2Cl-+6OH-;
2 2 4 4 6 2
(4)由分析可知,滤液2的主要成分为离子化合物的氯化铵,电子式为
,故答案为: ;
(5)灼烧时氩气的作用是做保护气,否则反应得到的钌被空气中的氧气氧化,故答案为:作
保护气,防止钌与空气中的氧气反应;
(6)若10t钌矿石最终制得3636kg钌,由钌原子个数守恒可知,钌的产率为×100%=87.8%,故答案为:87.8%。
ZnSO
3.(2022·全国甲卷)(14分)硫酸锌( 4 )是制备各种含锌材料的原料,在防腐、电
ZnCO
镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 3,杂质
SiO
为 2以及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K
sp
4.01038 6.71017 2.21020 8.01016 1.81011
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
pH=5
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
NH H O Ca(OH) NaOH
A. 3 2 B. 2 C.
滤渣①的主要成分是_______、_______、_______。
80~90℃ KMnO MnO
(4)向 的滤液①中分批加入适量 4溶液充分反应后过滤,滤渣②中有 2,
该步反应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
H SO
(6)滤渣④与浓 2 4反应可以释放HF并循环利用,同时得到的副产物是_______、
_______。焙烧
【答案】(1)ZnCO ZnO+CO ↑
3 2
(2) 将焙烧后的产物碾碎,增大接触面积 增大硫酸的浓度等
(3) B Fe(OH) CaSO SiO
3 4 2
MnO-
(4)3Fe2++ 4+7H O=3Fe(OH) ↓+MnO ↓+5H+
2 3 2
(5)置换Cu2+为Cu从而除去
(6) CaSO MgSO
4 4
【解析】由题干信息,菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的
3 2
焙烧
化合物,结合流程图分析,菱锌矿焙烧,主要发生反应ZnCO ZnO+CO ↑,再加入
3 2
H SO 酸浸,得到含Zn2+、Ca2+、Mg2+、Fe2+、Fe3+、Cu2+的溶液,加入物质X调节
2 4
pH=5,结合表格数据,过滤得到Fe(OH) 、CaSO 、SiO 的滤渣①,滤液①中主要含有
3 4 2
Zn2+、Cu2+、Mg2+、Ca2+、Fe2+,再向滤液①中加入KMnO 溶液氧化Fe2+,过滤得到
4
Fe(OH) 和MnO 的滤渣②,滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,过滤后得
3 2
到滤渣③为Cu,再向滤液③中加入HF脱钙镁,过滤得到滤渣④为CaF 、MgF ,滤液
2 2
④为ZnSO 溶液,经一系列处理得到ZnSO ·7H O,据此分析解答。
4 4 2
焙烧
(1)由分析,焙烧时,生成ZnO的反应为:ZnCO ZnO+CO ↑;
3 2
(2)可采用将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等方式提高锌的浸取率;
(3)A.NH ·H O易分解产生NH 污染空气,且经济成本较高,故A不适宜;
3 2 3
B.Ca(OH) 不会引入新的杂质,且成本较低,故B适宜;
2
C.NaOH会引入杂质Na+,且成本较高,C不适宜;
故答案选B;
当沉淀完全时(离子浓度小于10-5mol/L),结合表格Ksp计算各离子完全沉淀时pH<5的只有
Fe3+,故滤渣①中有Fe(OH) ,又CaSO 是微溶物,SiO 不溶于酸,故滤渣①的主要成分
3 4 2
是Fe(OH) 、CaSO 、SiO ;
3 4 2
(4)向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反
4 3 2MnO-
应的离子方程式为3Fe2++ 4+7H O=3Fe(OH) ↓+MnO ↓+5H+;
2 3 2
(5)滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,故加入锌粉的目的为置换Cu2+为Cu从而
除去;
(6)由分析,滤渣④为CaF 、MgF ,与浓硫酸反应可得到HF,同时得到的副产物为CaSO 、
2 2 4
MgSO 。
4
4.(2022·河南商丘·三模)(14分)三氧化二砷(As O )可用于治疗急性早幼粒细胞白血
2 3
病。利用某酸性含砷废水(含H AsO 、H SO )可提取As O ,提取工艺流程如下:
3 3 2 4 2 3
已知:①As O 为酸性氧化物;②As S 易溶于过量的Na S溶液中,故加入FeSO ,的目的
2 3 2 3 2 4
是除去过量的S2-。
回答下列问题:
(1)废水中H AsO 中砷元素的化合价为____
3 3
(2)“焙烧”操作中,As S 参与反应的化学方程式为_____
2 3
(3)“碱浸”的目的___________,“滤渣Y”的主要成分是___________。(写化学式)。
(4)“氧化”操作的目的是___________(用离子方程式表示)。
(5)“还原”过程中H AsO 转化为H AsO 然后将“还原”后溶液加热,H AsO 分解为As O 。
3 4 3 3 3 3 2 3
某次“还原”过程中制得了1.98kgAs O ,则消耗标准状况下气体X的体积是
2 3
___________L。
(6)砷酸钠(Na AsO )可用于可逆电池,装置如图1所示,其反应原理为AsO +2H++2I-=AsO
3 4
+I +H O。探究pH对AsO 氧化性的影响,测得输出电压与pH的关系如图2所示。则a
2 2
点时,盐桥中K+___________(填“向左”“向右”或“不”)移动,c点时,负极的电
极反应为___________。【答案】(1)+3价
(2)
(3) 将 转化为 ,与 分离
(4)
(5)448
(6) 向左
【解析】向酸性含砷废水中加入硫化钠溶液和硫酸亚铁溶液,将亚砷酸转化为硫化砷和硫
化亚铁沉淀,过滤得到含有硫酸钠的滤液M和硫化砷、硫化亚铁;硫化砷和硫化亚铁
在空气中煅烧得到三氧化二砷、氧化铁和二氧化硫,则气体X为二氧化硫;向三氧化
二砷、氧化铁中加入氢氧化钠溶液碱浸,将三氧化二砷转化为亚砷酸钠,过滤得到氧
化铁滤渣Y和亚砷酸钠溶液;向亚砷酸钠溶液中加入过氧化氢溶液,将亚砷酸钠氧化
为砷酸钠,向砷酸钠溶液中加入稀硫酸酸化得到砷酸,通入二氧化硫气体将砷酸还原
为亚砷酸,亚砷酸受热分解生成三氧化二砷。
(1)由化合价代数和为0可知,亚砷酸中砷元素为+3价,故答案为:+3价;
(2)由分析可知,硫化砷在空气中煅烧生成三氧化二砷和二氧化硫,反应的化学方程式为
,故答案为: ;
(3)由分析可知,碱浸的目的是将三氧化二砷转化为亚砷酸钠,与不与氢氧化钠溶液反应的
氧化铁分离,滤渣Y为氧化铁,故答案为:将 转化为 ,与 分离;
;(4)加入过氧化氢溶液氧化操作的目的是亚砷酸钠与过氧化氢溶液反应生成砷酸钠和水,反
应的离子方程式为 ,故答案为:
;
(5)由分析可知,向砷酸钠溶液中加入稀硫酸酸化得到砷酸,通入二氧化硫气体将砷酸还原
为亚砷酸,亚砷酸受热分解生成三氧化二砷,由得失电子数目守恒可知,生成1.98kg
三氧化二砷时,反应消耗标准状况下二氧化硫的体积为 ×2× ×22.4L/
mol=448L,故答案为:448;
(6)由图可知,a点时,溶液pH为0,平衡向正反应方向移动,甲池中石墨电极为原电池的
正极,乙池中石墨电极为负极,则盐桥中钾离子向左侧甲池移动;c点时,溶液pH减
小,平衡向逆反应方向移动,乙池中石墨电极为正极,甲池中石墨电极为负极,在水
分子作用下,亚砷酸根在负极失去电子发生氧化反应生成砷酸根离子,电极反应式为
,故答案为:向左;
。
5.(2022·河南新乡·二模)(15分)某工业生产上用铜镍矿石(主要成分为CuS、NiS、
FeS、SiO 及不溶于酸的杂质)制备胆矾CuSO •5H O的流程如图。
2 4 2
已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相)Cu2+(aq)+2HR(org)
反
萃
萃
取
取
CuR (org)+2H+(aq)。
2
回答下列问题:(1)焙烧前粉碎的目的是____。
(2)“调节pH时,生成氢氧化铁沉淀的离子方程式为____,试剂X的最佳选择是___(填标
号)。
a.HCl b.NaOH c.H SO d.NH •H O
2 4 3 2
(3)25℃时,“调节pH”后,测得滤液中各离子浓度及相关数据如表所示。(lg2=0.3)
离子 Fe3+ Cu2+ Ni2+ Fe2+
浓度/(mol·L-1) 1.0×10-6 5.0 1.2 0
对应氢氧化物的K 6.4×10-38 2.2×10-20 2.0×10-15 8.0×10-16
sp
该滤液的pH为___;加入的Cu(OH) ____(填“已经”或“没有”)完全溶解。
2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反
应的化学方程式为___。
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为___。
(6)将得到的胆矾产品做热重分析,测得的数据如图所示。
已知:杂质不分解,250℃时,胆矾失去所有结晶水。则A点胆矾分解得到的物质为___(填
化学式);该胆矾产品的纯度为___(保留4位有效数字)。
【答案】(1)增大接触面积,提高反应速率
(2) 2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+, c
2 3
(3) 3.6 已经
(4)2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O
4 2 4 2
(5)向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复操作2~3次。
(6) CuSO •3H O 96.53%
4 2
【解析】由题中流程可知,铜镍矿石(主要成分为CuS、NiS、FeS、SiO 及不溶于酸的杂质)
2
粉碎焙烧,充分氧化,烟气的主要成分为二氧化硫,加稀硫酸酸浸,过滤,滤渣1为
SiO 和不溶于酸的杂质,滤液中加入H O ,氧化Fe2+生成Fe3+,再加入Cu(OH) 调节溶
2 2 2 2液pH,使Fe3+完全转化为Fe(OH) 沉淀,继续过滤,滤渣2为Fe(OH) ,滤液中加入HR
3 3
进行萃取,除去镍离子,有机相中加入硫酸进行反萃取,水相的主要成分为硫酸铜溶
液,加热蒸发,冷却结晶,过滤,洗涤,干燥即可获得产品;据此解答。
(1)由上述分析可知,焙烧前粉碎的目的是增大接触面积,提高反应速率,使矿石充分氧
化;答案为增大接触面积,提高反应速率。
(2)由上述分析可知,加入Cu(OH) 调节溶液pH,使Fe3+完全转化为Fe(OH) 沉淀,生成氢氧
2 3
化铁沉淀的离子方程式为2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+;由题中信息Cu2+(aq)
2 3
+2HR(org) 反 萃 萃 取 取 CuR (org)+2H+(aq)可知,要使平衡逆向移动,则增加H+浓度,即有
2
机相中加入硫酸进行反萃取,可以分离铜离子,还不会产生杂质,所以选项c正确;
答案为2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+;c。
2 3
(3)由题中表格数据可知,25℃时,“调节pH”后,测得滤液中c(Fe3+)=1.0×10-6mol/L,
c(Cu2+)=5.0mol/L,因为K [Fe(OH) ]= 6.4×10-38,所以c(Fe3+)×c3(OH-)= K [Fe(OH) ],则
sp 3 sp 3
K FeOH
sp 3 6.41038 K 11014 1
c(OH-)=3 c Fe3 = 3 =4×10-11mol/L,c(H+)= w = ×10-
1106 c(OH) 41011 4
3mol/L,pH=3+lg4=3+2lg2=3.6;又c(Cu2+)×c2(OH-)=5×(4×10-11)2=8×10-21<
K [Cu(OH) ]=2.2×10-20,所以Cu(OH) 已经完全溶解;答案为3.6;已经。
sp 2 2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,即
NiSO 与NaClO发生氧化还原反应,该反应的化学方程式为
4
2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O;答案为
4 2 4 2
2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O。
4 2 4 2
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流
下后,重复操作2~3次;答案为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,
重复操作2~3次。
(6)由题中信息和图示可知,杂质不分解,250℃时,胆矾失去所有结晶水,此时失重率为
34.75%,设产品总质量为m克,该胆矾产品的纯度为x,则CuSO ·5H O CuSO 5H O
4 2 4 2
250g 90g
25034.75%
,解之x= =96.53%;A点时,失
mgx mg34.75% 90
重率为13.90%,设A点胆矾分解得到的物质为CuSO •yH O,则
4 2
CuSO ·5H O CuSO ·yH O (5y)H O
4 2 4 2 2
250g 185yg
,所以
mg96.53% mg13.90% 25013.90%18(5y)96.53%
,解之y=3,所以A点胆矾分解得到的物质为CuSO •3H O;答案为CuSO •3H O;
4 2 4 2
96.53%。
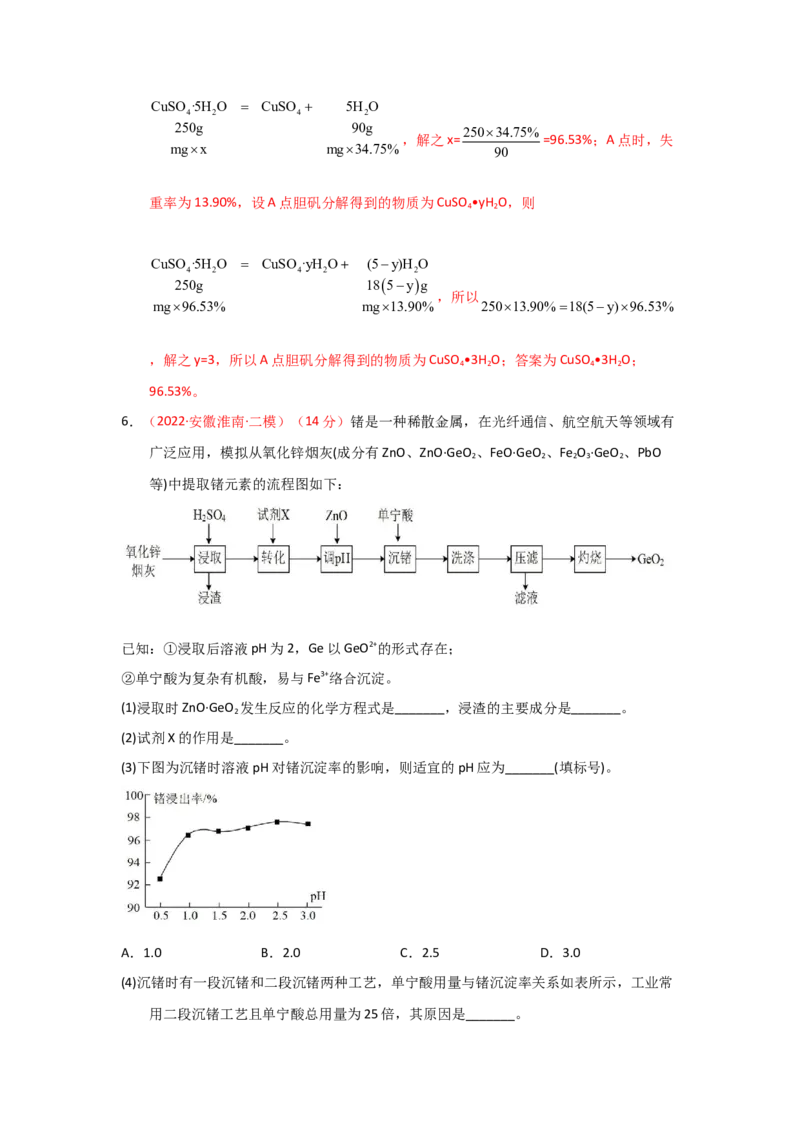
6.(2022·安徽淮南·二模)(14分)锗是一种稀散金属,在光纤通信、航空航天等领域有
广泛应用,模拟从氧化锌烟灰(成分有ZnO、ZnO·GeO 、FeO·GeO 、Fe O ·GeO 、PbO
2 2 2 3 2
等)中提取锗元素的流程图如下:
已知:①浸取后溶液pH为2,Ge以GeO2+的形式存在;
②单宁酸为复杂有机酸,易与Fe3+络合沉淀。
(1)浸取时ZnO·GeO 发生反应的化学方程式是_______,浸渣的主要成分是_______。
2
(2)试剂X的作用是_______。
(3)下图为沉锗时溶液pH对锗沉淀率的影响,则适宜的pH应为_______(填标号)。
A.1.0 B.2.0 C.2.5 D.3.0
(4)沉锗时有一段沉锗和二段沉锗两种工艺,单宁酸用量与锗沉淀率关系如表所示,工业常
用二段沉锗工艺且单宁酸总用量为25倍,其原因是_______。一段沉锗单宁酸总用量/倍 10 15 20 25 30
锗沉淀率/% 88.5 89.5 90.5 91.5 93.5
二段沉锗单宁酸总用量/倍 10 15 20 25 30
锗沉淀率/% 92 93.5 94.5 97 97.5
(5)可从滤液中回收的金属元素主要有_______。
(6)若用C H O表示单宁酸,压滤后的含锗沉淀表示为GeO(C H O) SO ,其在空气中灼烧会
2 2 2 2 2 4
得到SO 、H O、CO 三种气体,该反应方程式为_______。
2 2 2
【答案】(1) ZnO·GeO +2H SO =ZnSO +GeOSO +2H O PbSO
2 2 4 4 4 2 4
(2)还原Fe3+
(3)C
(4)单宁酸总用量相同时,二段沉锗时锗沉淀率更高;二段沉锗时,单宁酸用量超过25倍
后,沉淀率增大幅度较小
(5)Zn、Fe
灼烧
(6)2GeO(C H O) SO +7O 2GeO +8CO +4H O+2SO
2 2 2 4 2 2 2 2 2
【解析】由题给流程可知,向氧化锌烟灰中加入硫酸溶液浸取时,PbO与硫酸溶液反应生
成PbSO ,ZnO、ZnO·GeO 、FeO·GeO 、Fe O ·GeO 溶于硫酸溶液得到含有ZnSO 、
4 2 2 2 3 2 4
FeSO 、Fe (SO ) 、GeOSO ,过滤得到含有PbSO 的滤渣和含有ZnSO 、FeSO 、Fe (SO )
4 2 4 3 4 4 4 4 2 4
、GeOSO 的滤液;向滤液中先加入铁,将铁离子转化为亚铁离子,防止单宁酸沉锗
3 4
时,铁离子转化为沉淀,再加入氧化锌调节溶液pH至2.5,后加入单宁酸沉锗,经洗
涤、压滤得到含有ZnSO 、FeSO 的滤液和含锗沉淀;含锗沉淀在空气中灼烧GeO 。
4 4 2
(1)由分析可知,ZnO·GeO 与硫酸溶液反应生成ZnSO 、GeOSO 和水,反应的化学方程式为
2 4 4
ZnO·GeO +2H SO =ZnSO +GeOSO +2H O;滤渣的主要成分为硫酸铅,故答案为:
2 2 4 4 4 2
ZnO·GeO +2H SO =ZnSO +GeOSO +2H O;PbSO ;
2 2 4 4 4 2 4
(2)由分析可知,试剂X为铁,加入铁的目的是将铁离子转化为亚铁离子,防止单宁酸沉锗
时,铁离子也转化为沉淀,导致含锗沉淀中含有杂质,故答案为:还原Fe3+;
(3)由图可知,溶液pH为2.5时,锗沉淀率最高,所以沉锗时,溶液适宜的pH应为2.5,故
选C;
(4)由表格数据可知,当单宁酸总用量相同时,二段沉锗时锗沉淀率高于一段沉锗,所以工业常用二段沉锗工艺;二段沉锗时,单宁酸总用量增大,锗沉淀率增大,当用量超过
25倍后,沉淀率增大幅度较小,所以为节约生产成本,应选择单宁酸总用量为25倍
进行二段沉锗,故答案为:单宁酸总用量相同时,二段沉锗时锗沉淀率更高;二段沉
锗时,单宁酸用量超过25倍后,沉淀率增大幅度较小;
(5)由分析可知,滤液中含有ZnSO 、FeSO ,所以可从滤液中回收的金属元素为锌元素、铁
4 4
元素,故答案为:Zn、Fe;
(6)由题意可知,含锗沉淀在空气中灼烧发生的反应为GeO(C H O) SO 与空气中氧气反应生
2 2 2 4
成二氧化锗、二氧化碳、二氧化硫和水,反应的化学方程式为2GeO(C H O) SO +7O
2 2 2 4 2
灼烧 灼烧
2GeO +8CO +4H O+2SO ,故答案为:2GeO(C H O) SO +7O
2 2 2 2 2 2 2 4 2
2GeO +8CO +4H O+2SO 。
2 2 2 2
7.(2022·安徽芜湖·三模)(14分)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主
要成分为含锰化合物及FeS)与氧化锰矿(主要成分为MnO 等锰的氧化物)为原料制备硫
2
酸锰的工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O 、MgO。
4 2 3 2 3
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
物质 Fe(OH) Fe(OH) Mn(OH) Al(OH)
3 2 2 3
开始沉淀的pH 1.9 7.6 7.3 3.0
完全沉淀的pH 3.2 9.6 9.3 5.2
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______(2)若试剂a为MnO ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步
2
骤,造成的影响是_______。
(3)“中和除杂”时,应控制溶液的pH范围是_______。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1。则溶液中c(Mg2+)和c(Ca2+)的比值
=_______(已知:K (MgF )=6.4×10-10;K (CaF )=3.6×10-12)
sp 2 sp 2
(5)“碳化结晶”时发生反应的离子方程式为_______,选择NH HCO 而不选择Na CO 溶液的
4 3 2 3
原因是_______。
【答案】(1)除去矿物中的硫元素(或将硫化物转变为金属氧化物)
(2) MnO +4H++2Fe2+=Mn2++2Fe3++2H O Fe2+完全沉淀时Mn2+已经完全沉淀,造成Mn2+损
2 2
失
(3)5.2≤pH<7.3(或5.2~7.3)
(4)1600/9(177.8或177.78)
-
(5) Mn2++2HCO3=MnCO ↓+CO ↑+H O 碳酸钠溶液碱性强,会使Mn2+水解为Mn(OH)
3 2 2 2
【解析】高硫锰矿(主要成分为含锰化合物及FeS)与氧化锰矿混合焙烧,得到MnSO 、Fe O
4 2 3
及少量FeO、Al O 、MgO,加入硫酸,得到Mn2+、Fe2+、Fe3+、Mg2+、Al3+的酸性溶液,
2 3
加入二氧化锰将亚铁离子氧化为铁离子,再加入碳酸钙中和,将铁离子与铝离子以氢
氧化物的形式除去,加入MnF 氟化除杂,使溶液中的Mg2+、Ca2+沉淀完全,此时溶液
2
-
中的金属离子为锰离子,加入碳酸氢铵发生Mn2++2HCO3=MnCO ↓+CO ↑+H O,加入
3 2 2
硫酸溶解得硫酸锰溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等系列操作得
到硫酸锰晶体。
(1)高锰矿含有FeS, “混合焙烧”可以将金属硫化物转化为金属氧化物,同时除去硫元
素,故“混合焙烧”主要目的是除去矿物中的硫元素(或将硫化物转变为金属氧化
物);
(2)若试剂a为MnO ,氧化时用二氧化锰氧化亚铁离子生成三价铁离子,本身被还原成二价
2
锰离子,则氧化步骤发生反应的离子方程式为MnO +4H++2Fe2+=Mn2++2Fe3++2H O;若省
2 2
略“氧化”步骤,则铁元素只能以Fe2+形式除去,但是由表格可知除去亚铁离子的同
时锰离子也除去了,即造成的影响是Fe2+完全沉淀时Mn2+已经完全沉淀,造成Mn2+损
失;
(3)“中和除杂”的目的是使铝离子、铁离子完全沉淀且锰离子不沉淀,则由表格可知要控制溶液的pH范围是5.2≤pH<7.3(或5.2~7.3);
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+):c(Ca2+)=K (MgF ):
sp 2
K (CaF )=(6.4×10-10):(3.6×10-12)=1600/9(177.8或177.78);
sp 2
(5)“碳化结晶”时选择NH HCO ,生成碳酸锰,结合原子守恒、电荷守恒可知发生反应的离
4 3
-
子方程式为Mn2++2HCO3=MnCO ↓+CO ↑+H O;碳酸根离子水解程度大,碱性强,会
3 2 2
促进锰离子水解为氢氧化锰,故“碳化结晶”时不选择Na CO 溶液的原因是:碳酸钠
2 3
溶液碱性强,会使Mn2+水解为Mn(OH) 。
2