文档内容
专题十 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32
Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.关于氢键和分子间作用力,下列说法不正确的是( )
A.水在结冰时体积膨胀,是由于水分子之间存在氢键
B.NH 的稳定性很强,是因为其分子间能形成氢键
3
C.在氨水中水分子和氨分子之间也存在着氢键
D.分子间作用力较弱,破坏它所需能量较少
【答案】B
【解析】水在结冰时体积膨胀是由于水分子间以氢键互相联结,氢键有方向性和饱和性,所以形成的
晶体相对疏松,从而在结构上有许多空隙,造成体积膨胀,A项正确;NH 的稳定性取决于N—H键的稳
3
定性,而不是氢键,B项错误;氨分子和水分子之间主要是以氢键结合,氨气极易溶于水,所以在氨水中
水分子和氨分子之间存在氢键,C项正确;分子间作用力较弱,破坏它所需能量较少,D项正确。
2.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+
O――→CO+HO。下列有关说法正确的是( )
2 2 2
A.反应物和生成物都是非极性分子 B.0.5 mol HCHO含有1 mol σ键
C.HCHO、CO 分子的中心原子的杂化类型相同 D.HCHO能溶解在HO中
2 2
【答案】D
【解析】A项,HCHO、HO都是极性分子,错误;B项,根据结构式 可知,0.5 mol HCHO含
2
有1.5 mol σ键,错误;C项,HCHO、CO 分子的中心原子分别采用sp2、sp杂化,错误;D项,HCHO和
2
HO都属于极性分子,且分子间能形成氢键,所以HCHO能溶解在HO中,正确。
2 2
3.下列有关NO、NO和NH 的说法正确的是( )
3
A.NO的键角大于NH 的键角 B.NO的空间结构为直线形
3
C.NH 中的N原子杂化类型为sp2 D.NH 作配体是因为N原子存在空轨道
3 3
【答案】A
【解析】NO中N的孤电子对数为=0,价层电子对数为0+3=3,N为sp2杂化,NO为平面三角形结构,键角为120°,NH 中N的孤电子对数为=1,价层电子对数为1+3=4,N为sp3杂化,NH 为三角锥
3 3
形结构,键角为107°,前者键角大,A正确;NO中N的孤电子对数为=1,价层电子对数为1+2=3,N
为sp2杂化,NO为V形结构,B、C错误;NH 作配体是因为N有一对孤电子对,D错误。
3
4.下列关于[Cr(HO)Br ]Br·2H O的说法正确的是( )
2 4 2 2
A.配体为水分子,外界为Br-
B.中心离子的配位数为6
C.中心离子采取sp3杂化
D.中心离子的化合价为+2价,加入足量AgNO 溶液,所有Br-均以沉淀形式存在
3
【答案】B
【解析】[Cr(HO) Br ]Br·2H O中内界为[Cr(HO) Br ]+,Cr3+为中心离子,配体为HO、Br-,
2 4 2 2 2 4 2 2
配位数为6,外界为Br-,Cr3+提供的空轨道数为6,中心离子未采取sp3杂化。加入足量AgNO 溶液,只
3
有外界的Br-会以沉淀形式存在。
5.在通常条件下,下列比较正确的是( )
A.熔点:CO>KCl>SiO B.水溶性:HCl>CH >SO
2 2 4 2
C.键角:CH>H O>NH D.键能:H—F键>H—Cl键>H—Br键
4 2 3
【答案】D
【解析】晶体的熔点高低顺序一般为共价晶体>离子晶体>分子晶体,则熔点高低为SiO>KCl>CO ,
2 2
A错误;HCl和SO 均为极性分子,CH 为非极性分子,根据“相似相溶”规律,HCl和SO 在水中的溶解
2 4 2
度均大于CH,B错误;NH 、HO、CH 三种分子的中心原子均采取sp3杂化,CH 中C原子上没有孤电子
4 3 2 4 4
对,为正四面体形,NH 中N原子上有1对孤电子对,为三角锥形,HO中O原子上有2对孤电子对,为
3 2
V形,孤电子对数越多,键角越小,所以键角:CH>NH>H O,C错误;通常共价键键长越大,键能越
4 3 2
小,原子半径:FH—Cl键>H—
Br键,D正确。
6.下列关于物质结构与性质的说法中,不正确的是( )
A.I AsF 晶体中存在I,I的空间结构为V形
3 6
B.Cu的价电子排布图为
C.水分子间存在氢键,故HO的熔、沸点及稳定性均大于HS
2 2
D.第四周期元素中,Ga的第一电离能低于Zn
【答案】C
【解析】I的价层电子对数=2+=4,含有2个孤电子对,故空间结构为V形,A正确;Cu的价电子排布式为3d104s1,由此可知其价电子排布图正确,B正确;非金属简单氢化物的熔、沸点与氢键和范德华
力有关,而稳定性与键能有关,HO中H—O的键能大于HS中H—S的键能,C错误;Zn的核外电子排
2 2
布为[Ar]3d104s2,电子所在的轨道均处于全充满状态,较稳定,故第一电离能大于Ga,D正确。
7.下列各组物质中,按熔点由低到高的顺序排列正确的是( )
A.O、I、Hg B.CO、KCl、SiO
2 2 2
C.Na、K、Rb D.Na、Al、Mg
【答案】B
【解析】A中Hg在常温下为液态,而I 为固态,故A错;B中SiO 为原子晶体,其熔点最高,CO是
2 2
分子晶体,其熔点最低,故B正确;C中Na、K、Rb价电子数相同,其原子半径依次增大,金属键依次减
弱,熔点逐渐降低,故C错;D中Na、Mg、Al价电子数依次增多,原子半径逐渐减小,金属键依次增
强,熔点逐渐升高,故D错误。
8.下列晶体的分类正确的一组是( )
选项 离子晶体 原子晶体 分子晶体 金属晶体
A CaC 石墨 Ar Hg
2
B 玻璃 金刚石 CHCHOH Ag
3 2
C CHCOONa SiC Mg
3
D Ba(OH) Si C NaH
2 60
【答案】C
【解析】石墨的层与层之间是分子间作用力,而碳原子间是共价键,石墨之中也会有自由电子在层与
层间移动,石墨属于混合型晶体,故A不选;玻璃是硅酸钠、硅酸钙和二氧化硅的混合物,不是纯净物,
不属于离子晶体,故B不选;CHCOONa是由醋酸根离子和钠离子组成的离子晶体,碳化硅是由碳原子和
3
硅原子组成的原子晶体,属于有机物,属于分子晶体,镁是由金属阳离子和自由电子组成的金属晶体,故
C选;NaH是钠离子和氢离子形成的离子晶体,不属于金属晶体,故D不选。
9.硫化锂是目前正在开发的锂离子电池的新型固体电解质,为立方晶系晶体。离子位置按图示坐标
系为:Li+(0.25,0.25,0.25);(0.25,0.75,0.25);(0.75,0.25,0.25);(0.75,0.75,0.25);…S2-:(0,0,0);
(0.5,0.5,0);(0.5,0,0.5);(0,0.5,0.5);…则硫化锂晶胞沿z轴投影的俯视图(其中“ ”表示Li+,“ ”表示
S2-)为( )
【答案】A【解析】硫化锂为立方晶系晶体,由离子坐标可知,S2-处于晶胞顶点与面心,Li+处于晶胞的体心,
沿z轴投影的俯视,S2-处于正方形中心、顶角与边中心,Li+处于正方形内部对角线上且关于中心对称,
“ ”表示Li+,“ ”表示S2-,则俯视图为 ,故选A。
10.下列说法正确的是( )
A.同一原子中3s、3p、3d、4s能量依次升高
B.某原子核外电子由1s22s22p63s23p1→1s22s22p63s13p2,原子放出能量
C.p能级的原子轨道呈哑铃形,随着能层数的增加,p能级原子轨道数也在增多
D.按照泡利原理,在同一个原子中不可能存在两个运动状态完全相同的电子
【答案】D
【解析】多电子原子中,根据构造原理,各能级能量高低顺序:①相同能层而不同能级的能量高低 ns
<np<nd<nf,②能层不同时的能量高低2s<3s<4s,2p<3p<4p;③不同能层不同能级的能量高低ns<(n
-2)f<(n-1)d<np,所以同一原子中,3s、3p、4s、3d 能量依次升高,故A错误;3s能级上的电子比3p
能级上的电子能量更低,所以原子核外电子由 1s22s22p63s23p1→1s22s22p63s13p2,原子要吸收能量,故B错
误;p轨道是哑铃形的,任何能层的p能级都有3个原子轨道,与能层的大小无关,故C错误;在多电子
的原子中,电子填充在不同的能层,能层又分不同的能级,同一能级又有不同的原子轨道,每个轨道中最
多可以填充两个电子,自旋状态相反,在一个基态多电子的原子中,不可能有两个运动状态完全相同的电
子,故D正确。
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.如图三条曲线表示C、Si和P元素的前四级电离能变化趋势。下列说法正确的是( )
A.元素电负性:c>b>a
B.气态氢化物的稳定性:c>a>b
C.气态氢化物的相对分子质量:a>b>cD.第五电离能I:a>c>b
5
【答案】D
【解析】同主族元素自上而下第一电离能逐渐减小,P元素3p能级为半满稳定状态,第一电离能高于
同周期相邻元素的,故Si的第一电离能最小,由图中第一电离能可知,c为Si,P原子第四电离能为失去
3s2中1个电子,3s2为稳定状态,与第三电离能相差较大,可知 b为P、a为C。同周期主族元素自左而右
电负性逐渐增大,同主族元素自上而下电负性逐渐减小,则Si的电负性最小,故A错误;Si的非金属性最
弱,非金属性越强,气态氢化物越稳定,则 SiH 的稳定性最差,故B错误;气态氢化物的相对分子质量
4
b>c>a,故C错误;C、Si失去4个电子后最外层分别为1s2、2s22p6稳定状态,能量更低,再失去1个电子
时,第五电离能与第四电离能相差较大,P失去4个电子最外层为3s1状态,第四电离能与第五电离能相差
不大,故第五电离能C>Si>P,故D正确。
12.X、Y、Z、W是同一短周期的主族元素,原子序数依次增大;基态X的价层电子轨道表示式为
,Z最外层电子数是其次外层电子数的3倍;四种元素与锂组成的化合物结构如图(箭头表示配
位键)。下列说法正确的是( )
A.四种元素中第一电离能最大的是Z
B.Y和Z形成的化合物常温下均易溶于水
C.X的最高价氧化物对应的水化物是一种强酸
D.Z和W分别与氢元素形成的10电子化合物的沸点:前者高于后者
【答案】D
【解析】由题意可知,X、Y、Z、W分别为B、C、O、F。根据同一周期从左往右第一电离能呈增大
趋势,ⅡA族与ⅤA族反常,故四种元素中第一电离能最大的是W(F),故A错误;Y和Z形成的化合
物有CO和CO ,常温下CO难溶于水,CO 能溶于水,故B错误;X的最高价氧化物对应的水化物为硼
2 2
酸,是弱酸,故C错误。
13.已知冰晶石(NaAlF )熔融时的电离方程式为NaAlF===3Na++AlF。现有冰晶石的结构单元如
3 6 3 6
图所示,位于大立方体顶角和面心,位于大立方体的12条棱的中点和8个小立方体的体心, 是图中、中
的一种。下列说法正确的是(N 表示阿伏加德罗常数的值)( )
AA.冰晶石是分子晶体
B.大立方体的体心处 代表AlF
C.与Na+距离相等且最近的Na+有6个
D.冰晶石晶体的密度为 g·cm-3
【答案】D
【解析】由冰晶石熔融时能发生电离,可知冰晶石是离子晶体,A错误;每个晶胞中含有的个数为
8×+6×=4,的个数为12×+8=11,根据冰晶石的化学式可知,AlF与Na+的个数比为1∶3,故 与必然表
示同一种微粒, 代表Na+,B错误;与Na+距离相等且最近的Na+有8个,C错误;晶体的密度为 g·cm
-3= g·cm-3,D正确。
14.X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期,X原子的最外层电
子排布式是2s22p4,Z原子的核外电子数比Y原子少1,下列说法不正确的是( )
A.CX 分子是非极性分子
2
B.ZH 的VSEPR模型名称为三角锥形
3
C.Z 分子是非极性分子
4
D.酸HYO 比酸HZO 的酸性强
2 4 3 4
【答案】B
【解析】X、Y、Z是三种短周期元素,X原子的最外层电子排布式是2s22p4,X为O元素;X、Y位
于同一族,Y为S元素;Y、Z处于同一周期,均为第三周期元素,且Z原子的核外电子数比Y原子少1,
Z的质子数=16-1=15,则Z为P元素,由分析可知,X为O、Y为S、Z为P。CX 的结构式为
2
O==C==O,为直线形结构,结构对称、正负电荷的中心重合,为非极性分子,故A正确;ZH 为PH ,P
3 3
上有1对孤电子对,价层电子对数为4,VSEPR模型为四面体形,分子构型为三角锥形,故B错误;P 为
4
正四面体结构,结构对称、正负电荷的中心重合,为非极性分子,故C正确;非金属性S >P,因此最高价
氧化物对应水化物酸性HSO 比HPO 的强,故D正确。
2 4 3 4
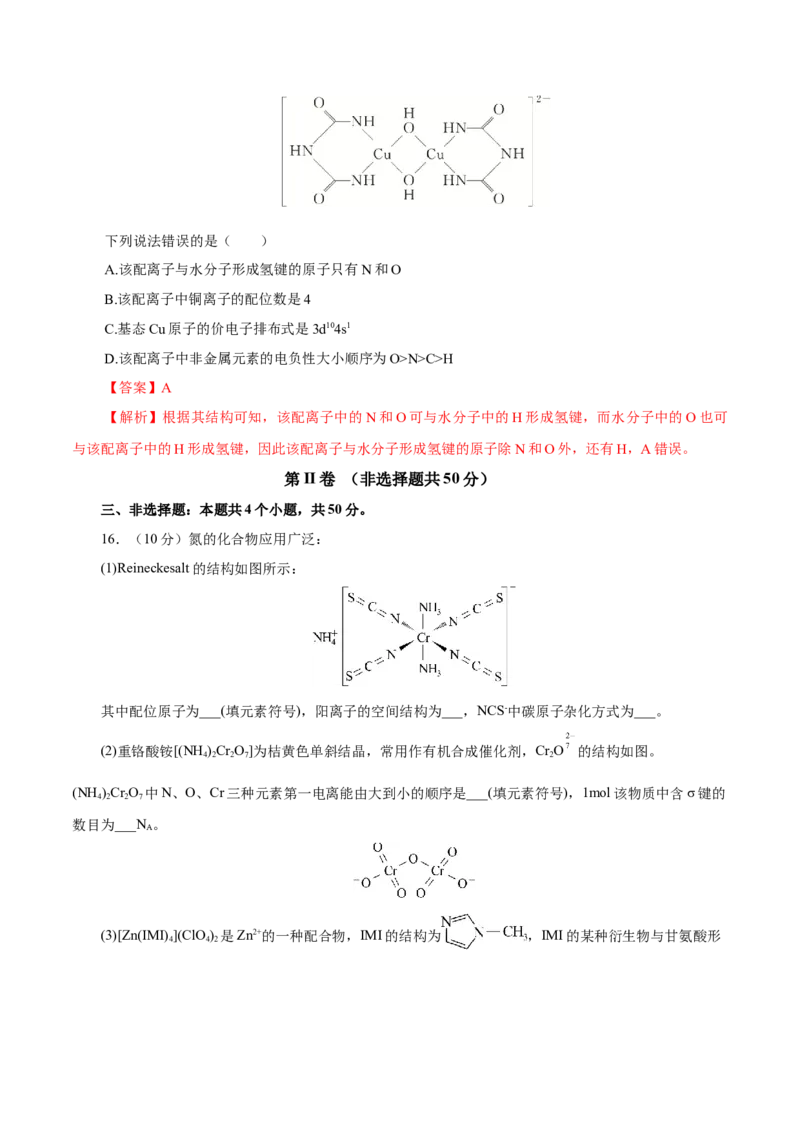
15.在碱性溶液中,Cu2+可以与缩二脲形成紫色配离子,其结构如图所示。下列说法错误的是( )
A.该配离子与水分子形成氢键的原子只有N和O
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中非金属元素的电负性大小顺序为O>N>C>H
【答案】A
【解析】根据其结构可知,该配离子中的N和O可与水分子中的H形成氢键,而水分子中的O也可
与该配离子中的H形成氢键,因此该配离子与水分子形成氢键的原子除N和O外,还有H,A错误。
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)氮的化合物应用广泛:
(1)Reineckesalt的结构如图所示:
其中配位原子为___(填元素符号),阳离子的空间结构为___,NCS-中碳原子杂化方式为___。
(2)重铬酸铵[(NH )Cr O]为桔黄色单斜结晶,常用作有机合成催化剂,Cr O 的结构如图。
4 2 2 7 2
(NH )Cr O 中N、O、Cr三种元素第一电离能由大到小的顺序是___(填元素符号),1mol该物质中含σ键的
4 2 2 7
数目为___N 。
A
(3)[Zn(IMI) ](ClO) 是Zn2+的一种配合物,IMI的结构为 ,IMI的某种衍生物与甘氨酸形
4 4 2成的离子化合物 常温下为液态而非固态。原因是___。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个
原子间运动,形成“离域π键”(或大π键)。大π键可用 表示,其中m、n分别代表参与形成大π键的
原子个数和电子数,如苯分子中大π键表示为 。
①下列微粒中存在“离域Π键”的是_______________。
A.CH=CH—CH=CH B.CCl C.HO D.SO
2 2 4 2 2
②NaN 中阴离子N 与CO 互为等电子体,均为直线型结构,N 中的2个大π键可表示为_________。
3 2
【答案】N 正四面体 sp杂化 N>O>Cr 16 阴阳离子半径大,电荷小,形成的离子
晶体晶格能小,熔点低(或阴阳离子半径大,电荷小,形成的离子键键能小,熔点低) AD Π
【解析】
(1)根据Reineckesalt的结构图可知,配位原子为N,氮原子提供孤电子对;阳离子为铵根离子,根据
价层电子互斥理论,孤电子对数为0,含有4个σ键,采取sp3杂化,可知其空间结构为正四面体;NCS-中
碳原子的价层电子对数为2,孤电子对数为0,属于sp杂化;
(2)N为半满稳定结构,其第一电离能大于O,N、O为非金属,第一电离能均大于金属,所以N、O、
Cr三种元素第一电离能由大到小的顺序是N>O>Cr;1个Cr O 含有8个σ键,1个铵根离子中含有4个
2
σ键,故1mol该物质中含有σ键数目为:(4×2+8) N =16 N ;
A A
(3)常温下,IMI的某种衍生物与甘氨酸形成的离子化合物 为液态而非固
态,原因为阴阳离子半径大,电荷小,形成的离子晶体晶格能小,熔点低(或阴阳离子半径大,电荷小,形
成的离子键键能小,熔点低);
(4)①CH=CH—CH=CH 、SO 分子中各原子共面,且原子之间均有相互平行的p轨道,可以形成大Π
2 2 2
键,水分子中氢原子没有p轨道,不能形成大Π键,CCl 是正四面体构型,各原子不共面,不能形成大Π
4
键,因此微粒中存在“离域Π键”的是AD。②N 与CO 互为等电子体,均为直线型结构,根据二氧化碳的结构可以判断出N 中σ键为2个,该
2
离子中两边的氮原子提供1个电子,中间氮原子提供2个电子形成大Π键,所以形成的2个大π键可表示
为Π 。
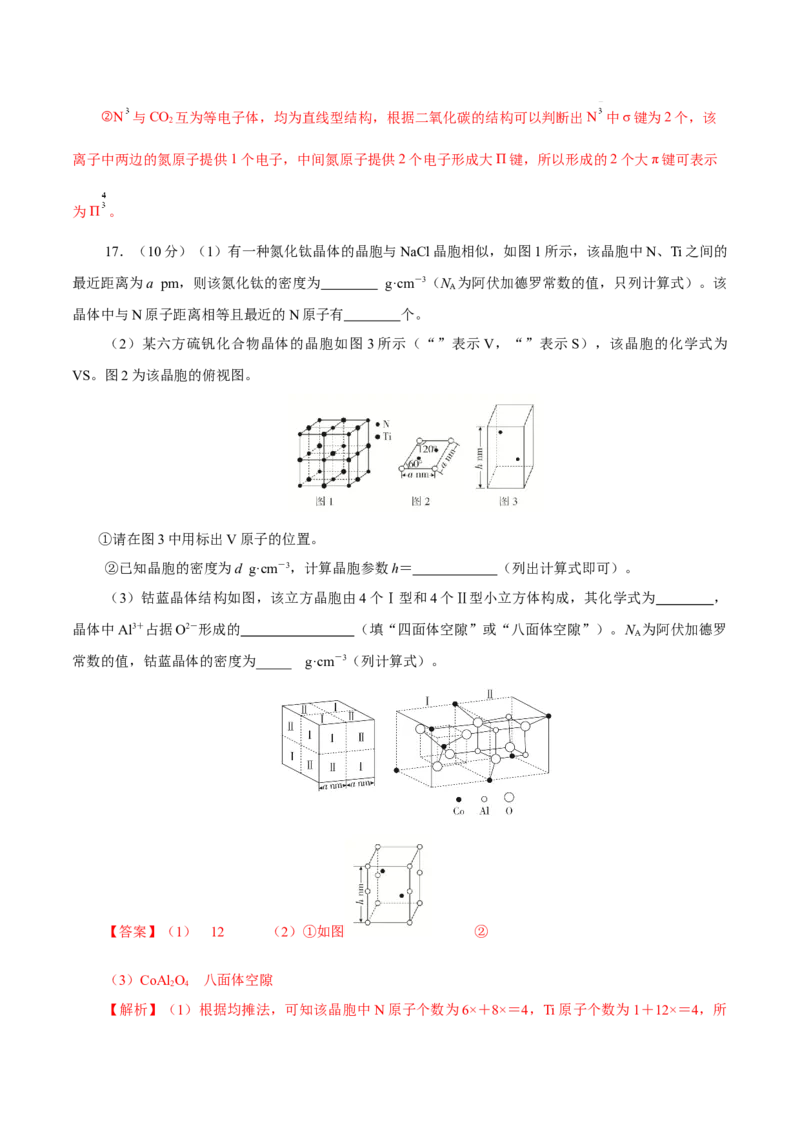
17.(10分)(1)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图1所示,该晶胞中N、Ti之间的
最近距离为a pm,则该氮化钛的密度为 g·cm-3(N 为阿伏加德罗常数的值,只列计算式)。该
A
晶体中与N原子距离相等且最近的N原子有 个。
(2)某六方硫钒化合物晶体的晶胞如图3所示(“”表示V,“”表示S),该晶胞的化学式为
VS。图2为该晶胞的俯视图。
①请在图3中用标出V原子的位置。
②已知晶胞的密度为d g·cm-3,计算晶胞参数h= (列出计算式即可)。
(3)钴蓝晶体结构如图,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为 ,
晶体中Al3+占据O2-形成的 (填“四面体空隙”或“八面体空隙”)。N 为阿伏加德罗
A
常数的值,钴蓝晶体的密度为_____ g·cm-3(列计算式)。
【答案】(1) 12 (2)①如图 ②
(3)CoAl O 八面体空隙
2 4
【解析】(1)根据均摊法,可知该晶胞中N原子个数为6×+8×=4,Ti原子个数为1+12×=4,所以晶胞的质量m= g,而晶胞的体积V=(2a×10-10)3 cm3,所以晶体的密度ρ= g·cm-3。以晶胞顶点N
原子为研究对象,与之距离相等且最近的N原子处于面心位置,每个顶点为8个晶胞共用,每个面为2个
晶胞共用,故与之距离相等且最近的N原子数目为=12。
(2)①该晶胞的化学式为VS,结合该晶胞的俯视图和晶胞结构可知,一个晶胞中含有 2个V原子、
2个S原子,因此V原子的位置是晶胞中8个顶点各一个,4条棱上各一个。②因为一个该晶胞中有2个
VS,所以一个晶胞质量为2×(32+51)× g,根据图2得到晶胞底面积为a×a nm2,所以晶胞的体积为
a×ah nm3=a2h×10-21 cm3,根据公式ρ=可得,d=,所以h=。
(3)根据钴蓝晶体晶胞结构分析,一个晶胞中含有的Co、Al、O个数分别为:4×=8、4×4=16、
8×4=32,所以化学式为CoAl O ;根据结构观察,与Al3+距离最近且相等的O2-有6个,故晶体中Al3+占
2 4
据O2-形成的八面体空隙;该晶胞的体积为(2a×10-7)3 cm3,该晶胞的质量为 g,所以密度为 g·cm-3。
18.(15分)黄铜矿(主要成分为CuFeS)是一种天然矿石。中国在商代或更早就掌握了由它冶炼铜的
2
技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问题:
(1)基态Cu+比Cu2+稳定的原因是___。
(2)SO 的空间构型为___,与SO 互为等电子体的离子是___(写出一种化学式即可)。
(3)图为某阳离子的结构,加热时该离子先失去的配位体是___(填化学式),原因是___。
(4)四方晶系的CuFeS 晶胞结构如图1所示。
2
①CuFeS 中各元素电负性数值从小到大的顺序为___,晶胞中S原子的杂化方式为___。
2
②晶胞中Cu和Fe的投影位置如图2所示。设阿伏伽德罗常数的值为N ,则该晶体的密度为
A
___g·cm-3。
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图
1中原子1的坐标为( , , ),则原子2的坐标为___。晶体中距离Fe最近的S有___个。【答案】
(1)Cu+的价电子为3d10,为全充满状态,稳定,Cu2+的价电子为3d9,较不稳定
(2)三角锥形 PO (或ClO 等)
(3)HO O的电负性强于N元素,NH 更容易提供孤电子对,NH 的配位能力强
2 3 3
(4)Fe<Cu<S sp3 ( ,1, ) 4
【解析】
(1)基态Cu+比Cu2+稳定的原因是Cu+的价电子为3d10,为全充满状态,稳定,Cu2+的价电子为3d9,
较不稳定;
(2)SO 的中心原子价层电子对数为 ,其空间构型为三角锥形,根据等电
子原理S=P-=Cl+,因此与SO 互为等电子体的离子是PO (或ClO 等);
(3)图为某阳离子的结构,其配体分别为上下水分子,四周为氨气分子,由于氧的电负性较大,N电
负性比O小,氨气与铜离子形成配位键比水与铜离子形成配位键稳定,因此加热时该离子先失去的配位体
是HO,原因是O的电负性强于N元素,NH 更容易提供孤电子对,NH 的配位能力强;
2 3 3
(4)①根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此CuFeS 中各元
2
素电负性数值从小到大的顺序为Fe<Cu<S,从图中可以看出S周围都连了四个价键,因此晶胞中S原子
的杂化方式为sp3。②晶胞中Cu和Fe的投影位置如图2所示,铜原子有 ,铁原子有
,硫原子有8个。设阿伏伽德罗常数的值为N ,则该晶体的密度为
A;
③根据原子的分数坐标,如图1中原子1的坐标为( , , ),则原子2的坐标为( ,1, ),根
据图中顶点Fe与硫的关系得到晶体中距离Fe最近的S有4个。
19.(15分) M、Q、R、X、Y为原子序数依次增大的短周期主族元素。M原子核外电子有6种运
动状态,R和X同主族。Z、W是第四周期的过渡元素,Z2+的核外d电子数是W+核外d电子数的一半,
W+核外没有未成对电子。请回答下列问题:
(1)基态W原子的价层电子的轨道表示式为 。
(2)M、Q和R的第一电离能由小到大的顺序是 (用元素符号表示)。
(3)比较简单离子半径:Xn- (填“>”“=”或“<”,下同)Ym-,Rn- P3-。
(4)在上述元素形成的微粒中,与MR 的空间结构相同的是 (写一种);QY 分子的空间
2 3
结构是 。
(5)W的单质晶体的晶胞结构如图所示。W的单质晶体中A、B、C、D围成1个正四面体空隙,该
晶胞中正四面体空隙的数目为 。某种Z的硫化物晶体中S2-以W的单质晶体中W原子的方式堆
积,Z2+填充在正四面体空隙中,则Z2+的填充率(即填充Z2+的正四面体空隙数和正四面体空隙总数的比
值)为 。
【答案】(1)
(2)C <
(4)CS(其他合理答案也可) 三角锥形
2
(5)8 50%
【解析】M原子核外电子有6种运动状态,说明M原子核外有6个电子,即M为C元素;W+核外没
有未成对电子,W是第四周期的过渡元素,因此W为Cu元素;Z2+的核外d电子数是Cu+核外d电子数的一半,则Z原子的价层电子排布式为3d54s2,即Z为Mn元素;R和X同主族,X和Y为第三周期主族元
素,Q与R为第二周期主族元素,因此Q为N元素,R为O元素,X为S元素,Y为Cl元素。
(3)电子层结构相同的简单离子,原子序数越小,简单离子半径越大,故离子半径:S2->Cl-,P3-
>S2-,又同主族元素简单离子的半径随原子序数增大而增大,故离子半径:S2->O2-,即离子半径:O2-