文档内容
电化学中的多室、多池装置
1.交换膜类型及特点
交换膜 特定的
阳膜 阴膜 双极膜
类型 交换膜
中间层中的H O解离出 只允许特定的离子或
2
阳离子移向原电 阴离子移向原电 H+和OH-,H+移向原电 分子通过,如质子交
允许通过的离子及
池的正极(电解池 池的负极(电解 池的正极(电解池的阴 换膜只允许H+通过,
移动方向
的阴极) 池的阳极) 极),OH-移向原电池的 氯离子交换膜只允许
负极(电解池的阳极) Cl-通过
无论是原电池还是电解池中,阳离子均移向得电子的一极,阴离子均移向失电子的
通性
一极
2.离子交换膜的作用
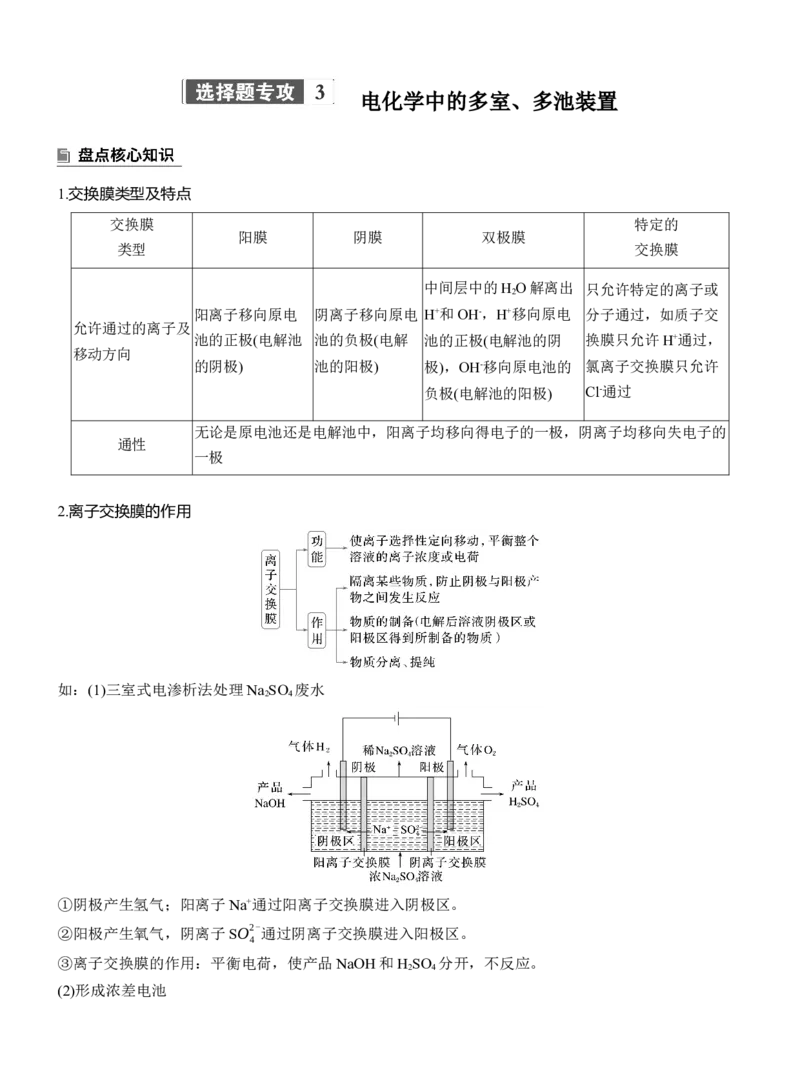
如:(1)三室式电渗析法处理Na SO 废水
2 4
①阴极产生氢气;阳离子Na+通过阳离子交换膜进入阴极区。
②阳极产生氧气,阴离子SO2-通过阴离子交换膜进入阳极区。
4
③离子交换膜的作用:平衡电荷,使产品NaOH和H SO 分开,不反应。
2 4
(2)形成浓差电池①左池为稀AgNO 溶液,左侧Ag电极为负极,右池为浓AgNO 溶液,右侧Ag电极为正极。只有两边
3 3
AgNO 溶液浓度不同,才能形成浓差电池。
3
②正、负电极均为Ag单质。随着反应进行,左右两池浓度的差值逐渐减小,外电路中电流将减小,电
流表指针偏转幅度逐渐变小。当左右两侧离子浓度相等时,电池将停止工作,不再有电流产生,此时
溶液中左、右两边硝酸银溶液的物质的量浓度相等。
③离子交换膜的作用是不允许Ag+穿过,只允许NO-
通过,所以是阴离子交换膜。负极Ag失电子变成
3
Ag+,为了平衡电荷,正极区的NO-
就通过阴离子交换膜向负极移动。
3
(3)物质制备中的离子交换膜
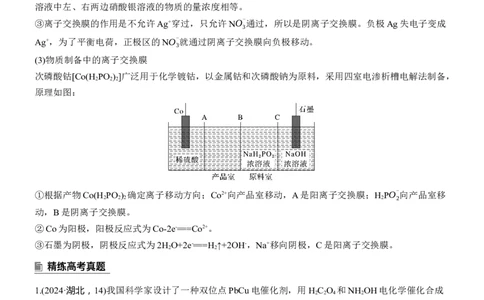
次磷酸钴[Co(H PO ) ]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,
2 2 2
原理如图:
①根据产物Co(H PO ) 确定离子移动方向;Co2+向产品室移动,A是阳离子交换膜;H
PO-
向产品室移
2 2 2 2 2
动,B是阴离子交换膜。
②Co为阳极,阳极反应式为Co-2e-===Co2+。
③石墨为阴极,阴极反应式为2H O+2e-===H ↑+2OH-,Na+移向阴极,C是阳离子交换膜。
2 2
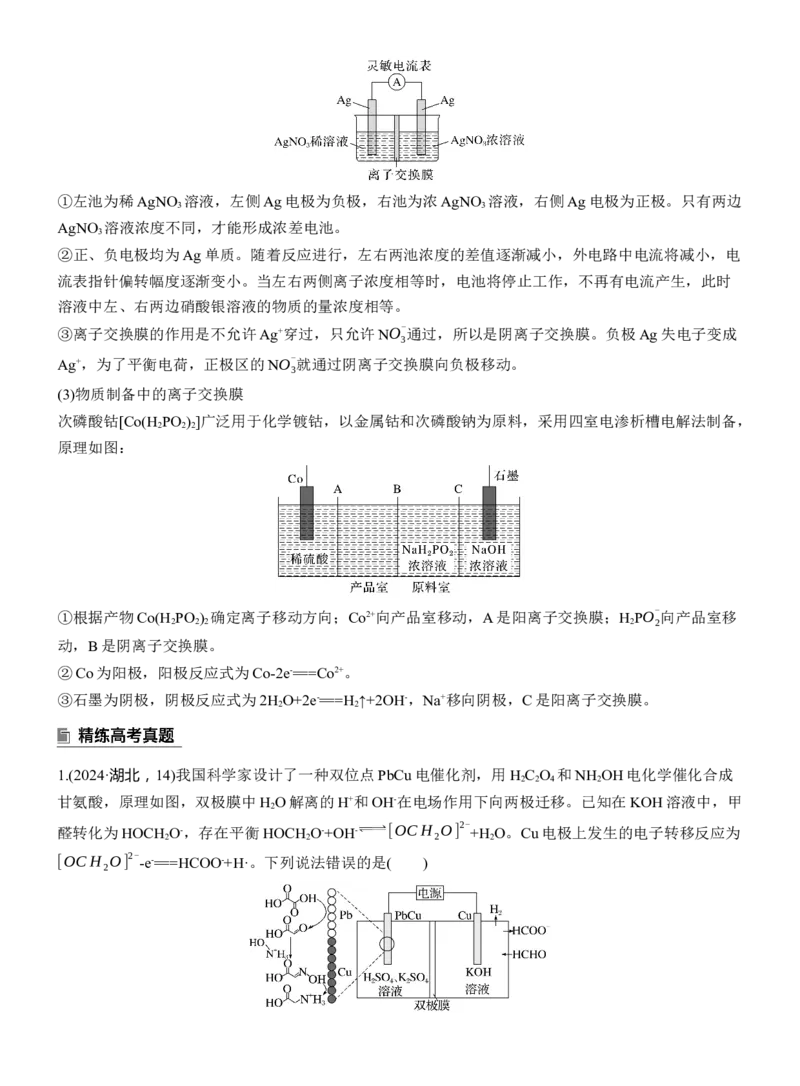
1.(2024·湖北,14)我国科学家设计了一种双位点PbCu电催化剂,用H C O 和NH OH电化学催化合成
2 2 4 2
甘氨酸,原理如图,双极膜中H O解离的H+和OH-在电场作用下向两极迁移。已知在KOH溶液中,甲
2
醛转化为HOCH O-,存在平衡HOCH O-+OH- [OCH O] 2- +H O。Cu电极上发生的电子转移反应为
2 2 2 2
[OCH O] 2- -e-===HCOO-+H·。下列说法错误的是( )
2A.电解一段时间后阳极区c(OH-)减小
B.理论上生成1 mol H N+CH COOH双极膜中有4 mol H O解离
3 2 2
C.阳极总反应式为2HCHO+4OH--2e-===2HCOO-+H ↑+2H O
2 2
D.阴极区存在反应H C O +2H++2e-===OHCCOOH+H O
2 2 4 2
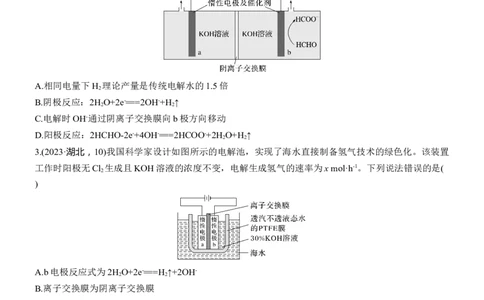
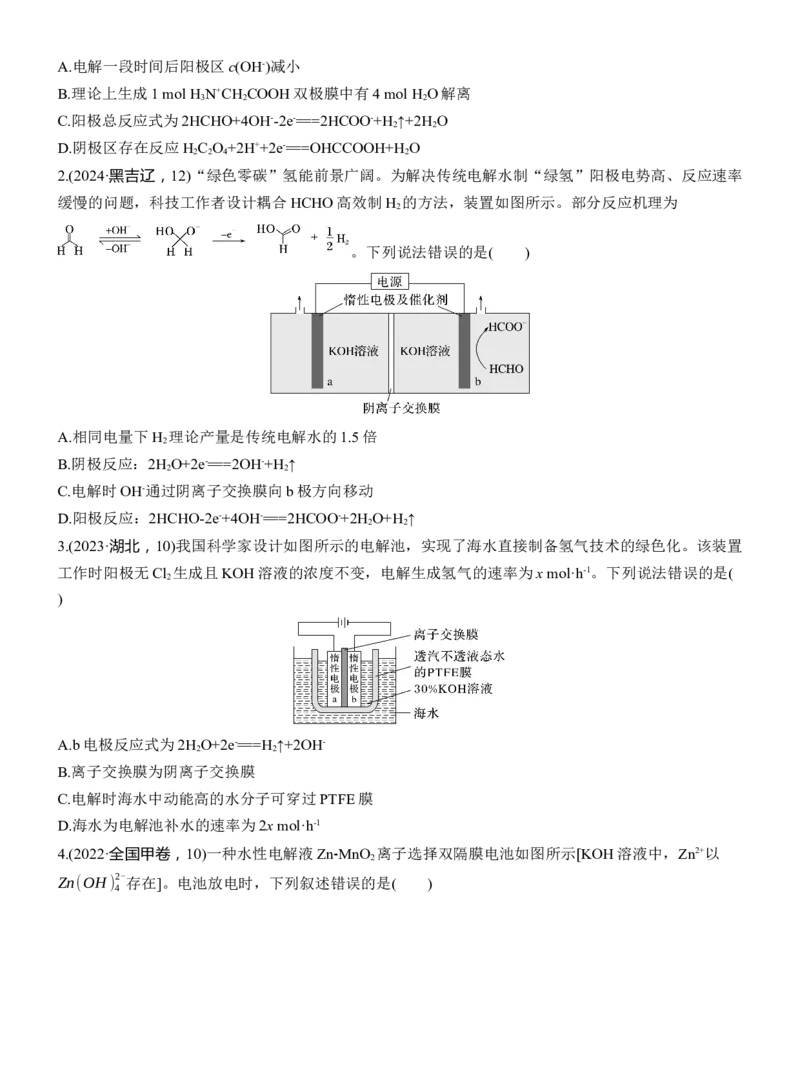
2.(2024·黑吉辽,12)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速率
缓慢的问题,科技工作者设计耦合HCHO高效制H 的方法,装置如图所示。部分反应机理为
2
。下列说法错误的是( )
A.相同电量下H 理论产量是传统电解水的1.5倍
2
B.阴极反应:2H O+2e-===2OH-+H ↑
2 2
C.电解时OH-通过阴离子交换膜向b极方向移动
D.阳极反应:2HCHO-2e-+4OH-===2HCOO-+2H O+H ↑
2 2
3.(2023·湖北,10)我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置
工作时阳极无Cl 生成且KOH溶液的浓度不变,电解生成氢气的速率为x mol·h-1。下列说法错误的是(
2
)
A.b电极反应式为2H O+2e-===H ↑+2OH-
2 2
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过PTFE膜
D.海水为电解池补水的速率为2x mol·h-1
4.(2022·全国甲卷,10)一种水性电解液Zn⁃MnO
2
离子选择双隔膜电池如图所示[KOH溶液中,Zn2+以
Zn(OH) 2- 存在]。电池放电时,下列叙述错误的是( )
4A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO2-通过隔膜向Ⅱ区迁移
4
C.MnO 电极反应:MnO +2e-+4H+===Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+===Zn(OH) 2- +Mn2++2H O
2 4 2答案精析
精练高考真题
1.B [由题意可知,Cu电极为阳极,电极总反应为2HCHO-2e-+4OH-===2HCOO-+H ↑+2H O,阳极区消耗
2 2
OH-、同时生成H O,c(OH-)减小,A、C正确;PbCu电极为阴极,首先HOOC—COOH在Pb上发生得电
2
子的还原反应转化为OHC—COOH:H C O +2e-+2H+===OHC—COOH+H O,OHC—COOH与HO—N+H
2 2 4 2 3
反应生成HOOC—CH==N—OH:OHC—COOH+HO—N+H HOOC—CH==N—OH+H O+H+,HOOC—
3 2
CH N—OH发生得电子的还原反应转化成H N+CH COOH:HOOC—CH==N—OH+4e-+5H+===
3 2
H N+CH COOH+H O,阴极总反应为H C O +NH OH+6e-+7H+===H N+CH COOH+3H O,1 mol H O解离成
3 2 2 2 2 4 2 3 2 2 2
1 mol H+和1 mol OH-,故理论上生成1 mol H N+CH COOH双极膜中有6 mol H O解离,B错误、D正确。]
3 2 2
2.A [据图示可知,b电极上HCHO转化为HCOO-,HCHO发生氧化反应,所以b电极为阳极,a电极为
1
阴极,HCHO为阳极反应物,阳极反应:①HCHO+OH--e-===HCOOH+ H ↑,②HCOOH+OH-===HCOO-
2 2
+H O,阴极反应:2H O+2e-===H ↑+2OH-,即转移2 mol电子时,阴、阳两极各生成1 mol H ,共2 mol
2 2 2 2
H ;而传统电解水:2H O 2H ↑+O ↑,转移2 mol电子,只有阴极生成1 mol H ,所以相同电量下H
2 2 2 2 2 2
理论产量是传统电解水的2倍,故A错误、B正确;由电极反应式可知,电解过程中阴极生成OH-,OH-通
过阴离子交换膜向阳极移动,即向b极方向移动,故C正确;由分析可知阳极反应为2HCHO-2e-+4OH-
===2HCOO-+2H O+H ↑,故D正确。]
2 2
3.D [b电极为阴极,发生还原反应,电极反应为2H O+2e-===H ↑+2OH-,故A正确;该装置工作时阳极
2 2
无Cl 生成且KOH浓度不变,阳极发生的电极反应为4OH--4e-===O ↑+2H O,为保持OH-浓度不变,则阴
2 2 2
极产生的OH-要通过离子交换膜进入阳极室,即离子交换膜应为阴离子交换膜,故B正确;电解时电解槽
中不断有水被消耗,海水中动能高的水以“汽”的形式穿过PTFE膜,为电解池补水,故C正确;由电解
总反应可知,每生成1 mol H 要消耗1 mol H O,生成H 的速率为x mol·h-1,则补水的速率也应是x
2 2 2
mol·h-1,故D错误。]
4.A [根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
===Zn(OH) 2- ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+===Mn2++2H O,K+从Ⅲ区通过隔膜向
4 2 2 2
Ⅱ区迁移,A错误、C正确;Ⅰ区的SO2-
通过隔膜向Ⅱ区迁移,B正确;电池的总反应为Zn+4OH-
4
+MnO +4H+===Zn(OH) 2- +Mn2++2H O,D正确。]
2 4 2