文档内容
专题四 氧化还原反应 专题检验
一、选择题(16×3=48分)
1.(2022·北京·首都师范大学附属中学三模)下列物质在生活中的应用与氧化还原反应无
关的是
A.FeSO 补血剂与维生素C配合使用效果更佳
4
B.用明矾处理污水
C.用84消毒液杀灭细菌
D.还原Fe粉用作食品脱氧剂
2.(2022·北京育才学校三模)下列离子检验利用了氧化还原反应的是
选项 待检验离子 检验试剂
A Fe3+ KSCN溶液
2-
B 稀盐酸、氯化钡溶液
SO4
C I- Cl 、淀粉溶液
2
D + 浓NaOH溶液、湿润的红色石蕊试纸
NH4
3.(2022·青海西宁·一模)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A Cl (HCl) H O、浓H SO
2 2 2 4
B NaCl溶液(MgCl ) NaOH溶液、过滤、稀HCl
2
C 乙醇(乙酸) NaOH溶液、分液
D NO(NO ) H O、无水CaCl
2 2 2
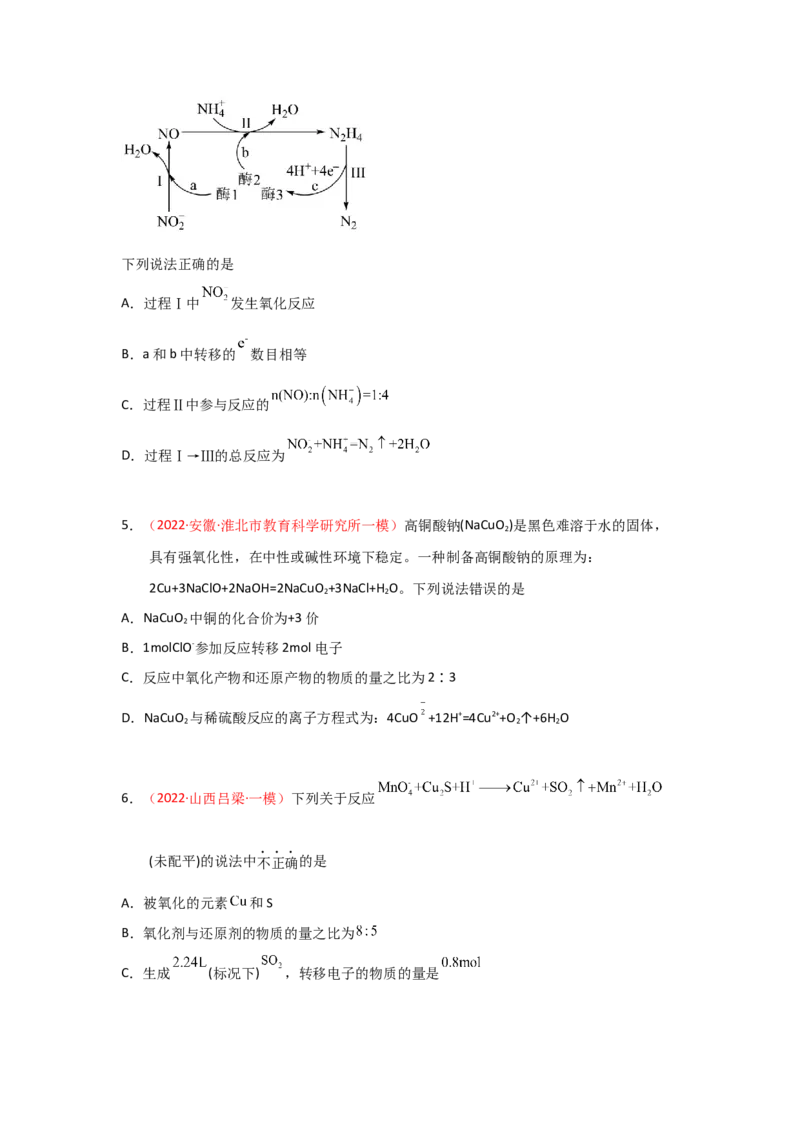
4.(2022·湖南卷)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能
将海洋中的 转化为 进入大气层,反应过程如图所示。下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
5.(2022·安徽·淮北市教育科学研究所一模)高铜酸钠(NaCuO )是黑色难溶于水的固体,
2
具有强氧化性,在中性或碱性环境下稳定。一种制备高铜酸钠的原理为:
2Cu+3NaClO+2NaOH=2NaCuO +3NaCl+H O。下列说法错误的是
2 2
A.NaCuO 中铜的化合价为+3价
2
B.1molClO-参加反应转移2mol电子
C.反应中氧化产物和还原产物的物质的量之比为2∶3
D.NaCuO 与稀硫酸反应的离子方程式为:4CuO +12H+=4Cu2++O ↑+6H O
2 2 2
6.(2022·山西吕梁·一模)下列关于反应
(未配平)的说法中不正确的是
A.被氧化的元素 和S
B.氧化剂与还原剂的物质的量之比为
C.生成 (标况下) ,转移电子的物质的量是D.还原性的强弱关系是:
7.(2022·陕西咸阳·一模) 是一种绿色的饮用水消毒剂。常用下列两种反应原理制
备:
反应1:
反应2:
下列说法正确的是
A.两个反应中 都作氧化剂
B.反应1中氧化剂与还原剂的物质的量之比为1∶2
C.反应2中每转移6mol电子,生成气体的物质的量为15mol
D.制备等量的 ,反应1比反应2转移的电子总数多
8.(2022·北京市十一学校三模)碱式氯化铜 是一种重要的无机杀虫
剂,它可以通过以下步骤制备。
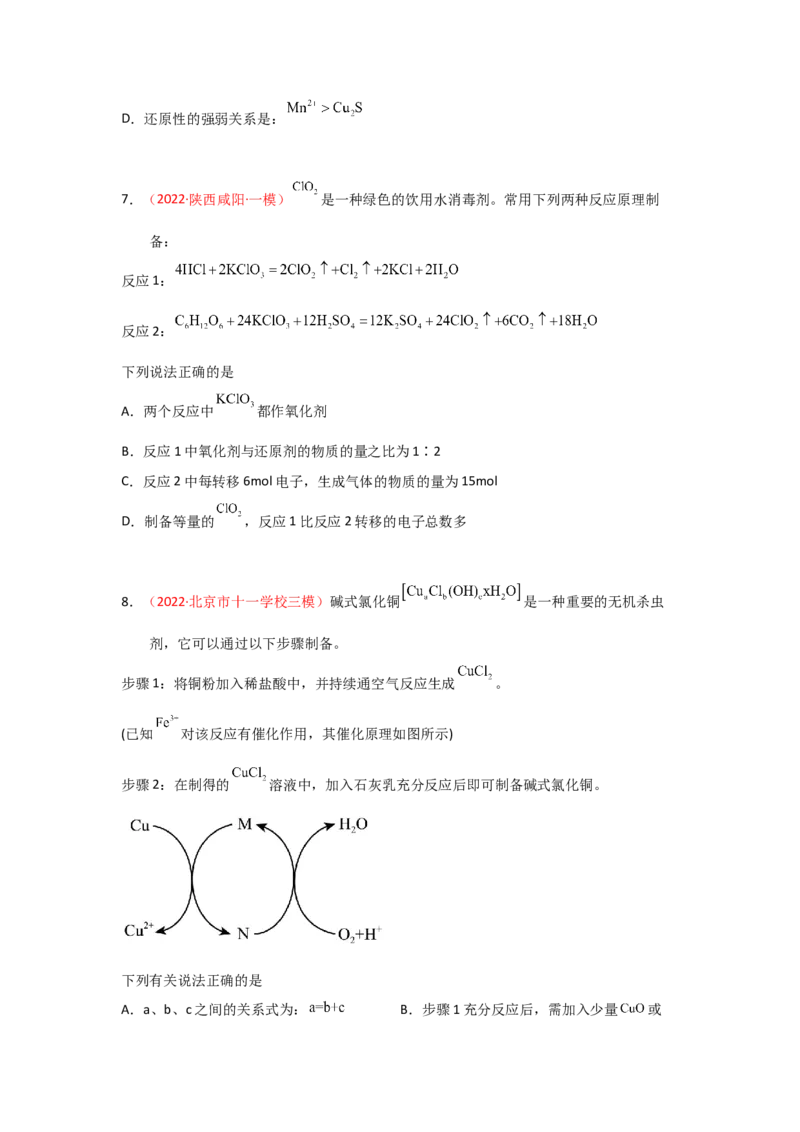
步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成 。
(已知 对该反应有催化作用,其催化原理如图所示)
步骤2:在制得的 溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
下列有关说法正确的是
A.a、b、c之间的关系式为: B.步骤1充分反应后,需加入少量 或C.图中M、N分别为 、 D.制备 的 ,理论上消耗
9.(2022·上海上海·二模)工业硅冶炼炉中存在如下反应:
反应①:SiO +2C Si(熔点1410℃)+2CO↑
2
反应②:SiO +3C SiC(熔点2700℃)+2CO↑
2
已知SiC与Si结构相似,N 表示阿伏加德罗常数的值。
A
关于上述反应说法正确的是
A.反应①中C置换了Si,说明非金属性C>Si
B.反应①与②中氧化剂与还原剂物质的量之比均为1∶2
C.反应①与②中每生成22.4LCO,转移电子数均为2N 个
A
D.SiC熔点明显高于Si是因为两者结构相似,但SiC摩尔质量更大
10.(2022·广东·广州六中三模)中国是稀土大国,铈(Ce)是地壳中含量最高的稀土元素,
主要存在与独居石中。金属铈在空气中易被氧化变暗,能与水反应,常见的化合价为
+3和+4,氧化性: 。下列说法正确的是
A. 、 、 互为同位素
B.可通过电解 溶液制得金属铈
C.铈能从硫酸铜溶液中置换出铜:
D. 溶于氢碘酸的化学方程式可表示为
11.(2022·内蒙古·包钢一中一模)硫元素的几种化合物存在下列转化关系。下列说法正确
的是
浓H SO SO Na SO 溶液 Na S O 溶液 S
2 4 2 2 3 2 2 3A.反应①中生成的SO 具有漂白性,可使溴水褪色
2
B.反应②中若SO 过量,就会生成NaHSO
2 3
C.反应④中生成 S 既是氧化产物,也是还原产物
D.反应④中当消耗 1mol 稀硫酸时,电子转移为4mol
12.(2022·新疆喀什·一模)铅丹(Pb O )可作防锈用涂料,其中铅的化合价为+2价和+4
3 4
价,它与浓盐酸反应的化学方程式为Pb O +8HCl(浓)=3PbCl +Cl ↑+4H O。下列说法正
3 4 2 2 2
确的是
A.Pb O 与浓盐酸反应时,Pb O 作为还原剂
3 4 3 4
B.物质的氧化性:Cl >Pb O
2 3 4
C.Pb O 中+2价的铅与+4价的铅的物质的量之比为2:1
3 4
D.当上述反应中消耗1molPb O 时,生成的氯气为22.4L
3 4
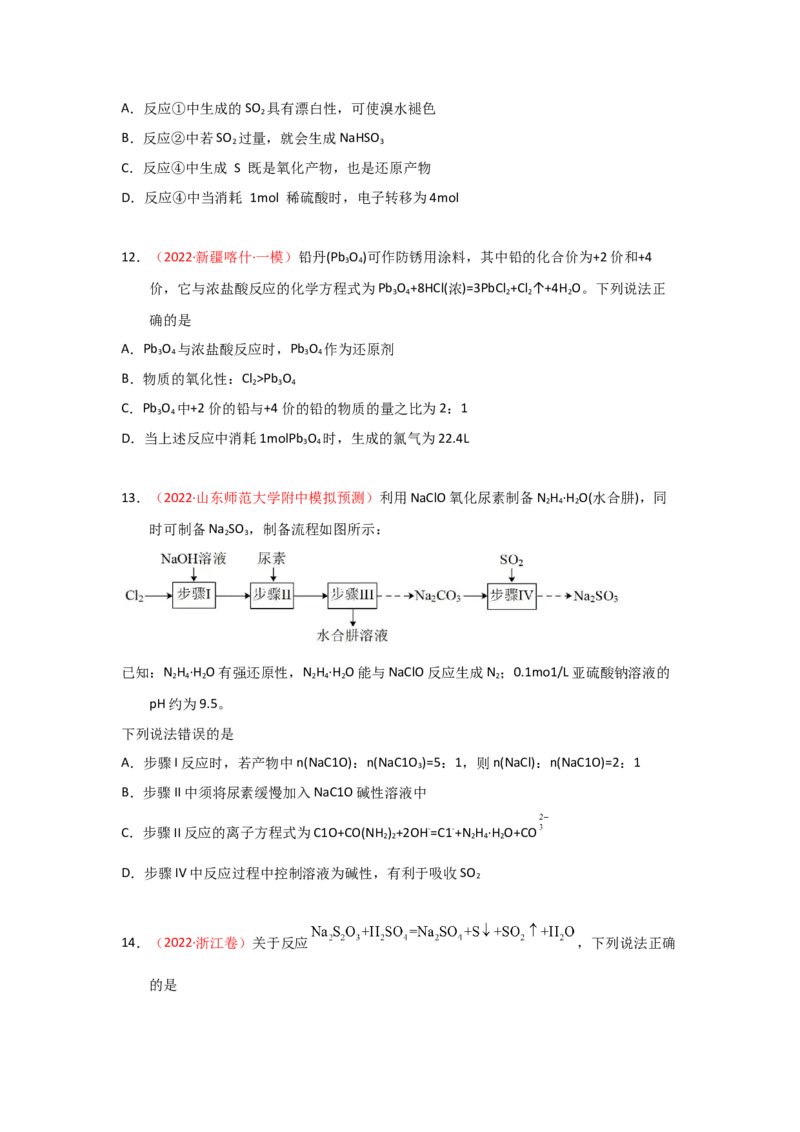
13.(2022·山东师范大学附中模拟预测)利用NaClO氧化尿素制备N H ·H O(水合肼),同
2 4 2
时可制备Na SO ,制备流程如图所示:
2 3
已知:N H ·H O有强还原性,N H ·H O能与NaClO反应生成N ;0.1mo1/L亚硫酸钠溶液的
2 4 2 2 4 2 2
pH约为9.5。
下列说法错误的是
A.步骤I反应时,若产物中n(NaC1O):n(NaC1O )=5:1,则n(NaCl):n(NaC1O)=2:1
3
B.步骤II中须将尿素缓慢加入NaC1O碱性溶液中
C.步骤II反应的离子方程式为C1O+CO(NH ) +2OH-=C1-+N H ·H O+CO
2 2 2 4 2
D.步骤IV中反应过程中控制溶液为碱性,有利于吸收SO
2
14.(2022·浙江卷)关于反应 ,下列说法正确
的是A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
15.(2022·河南信阳·二模)化学上常用标准电极电势数据φθ(氧化型/还原型)比较物质氧
化能力。φθ值越高,氧化型物质氧化能力越强,φθ值与体系pH有关。利用表格所给
数据分析,以下说法错误的是
氧化型/还原型 φθ(Co3+/Co2+) φθ(HClO/Cl—
酸性介质 1.84V 1.49V
氧化型/还原型 φθ[Co(OH) /Co(OH) ] φθ(ClO—/Cl—)
3 2
碱性介质 0.17V x
A.推测:x<1.49V
B.Co O 与浓盐酸发生反应:Co O +8H+=Co2++2Co3++4H O
3 4 3 4 2
C.若x=0.81V,碱性条件下可发生反应:2Co(OH) +NaClO+H O=2Co(OH) +NaCl
2 2 3
D.从图中数据可知氧化剂物质的氧化性随着溶液酸性增强而增强
16.(2022·河南郑州·一模)甲酸钙[(HCOO) Ca]是一种新型猪饲料添加剂。实验室制取甲酸
2
钙方法之一,是将Ca(OH) 和甲醛溶液依次加入质量分数为30%~70%的H O 中。下列
2 2 2
说法错误的是
A.反应温度不宜过高
B.该反应中被还原的元素只有O
C.参加反应的氧化剂与还原剂的物质的量之比为1:1
D.每生成26 g (HCOO) Ca,反应转移电子的物质的量为0.4 mol
2
二、主观题(4×13=42分)
17.(2022·山东省青岛市4区市教学研究室高三联考)党十九大报告中首次将树立和践行
“绿水青山就是金山银山”的理念写入党代会报告,治理污染减少排放具有十分重要的意义。回答下列问题:
(1)下面是消除NO 排放的三个案例:
x
①利用纯碱溶液可以吸收硝酸厂废气中的NO和NO [n(NO):n(NO )=1:1],该过程中发生
2 2
反应的化学方程式为___________。
②三元催化可以将汽车尾气中的CO和NO 进行净化处理,该过程中发生反应的化学方程式
x
为___________。
③利用尿素消除NO 污染的转化反应为Ⅰ.NO+O →NO ,Ⅱ.NO +CO(NH ) →无污染气体。
x 2 2 2 3 2
尿素中C元素的化合价___________,反应Ⅱ的化学方程式为___________。
(2)为测定热电厂排放气中SO 的含量,进行了如下实验:标准状况下,将排放气匀速通入
2
100mL0.5mol/L酸性KMnO 溶液中。若排放气的流速为 ,经过bmin溶液恰好
4
褪色,则该排放气中SO 的含量为___________g/L。
2
(3)通过如下流程可实现SO 和NO综合处理并获得保险粉(Na S O )和硝铵。
2 2 2 4
①装置Ⅲ中生成Ce4+与S O 2-的物质的量之比为___________。
2 4
②装置Ⅳ中溶液含有a mol·Lˉ1NO -和b mol·Lˉ1NO -,欲将cL该溶液完全转化为硝铵,需要通
2 3
入O 与NH 的体积比为___________(同温同压下)。
2 3
18.(2022·上海市第二中学高一月考)实验室可通过置换反应完成卤素单质活泼性比较的实
验。某实验小组设计了装置如图,回答下列问题:
(1)已知:常温下KClO 与浓盐酸反应可制取氯气,反应如下。配平该化学方程式,标出电
3
子转移的方向和数目。
反应①___________KClO +___________HCl(浓)=___________KCl + ___________Cl ↑+
3 2
___________H O___________
2该反应中氧化剂为___________,被还原的元素是___________。
(2)该装置中,吸有KI淀粉溶液的棉球颜色变为___________。吸有NaBr溶液的棉球中发生
反应的离子方程式为___________。
(3)由反应现象能否得出活泼性Br >I 的结论?回答并说明理由___________。
2 2
(4)实验室还可通过以下反应制取氯气:
反应② 2KMnO +16HCl=2KCl + 2MnCl +5Cl ↑+ 8H O;
4 2 2 2
反应③ MnO +4HCl(浓) MnCl +Cl ↑+ 2H O;
2 2 2 2
若要制得相同质量的氯气,反应②和③中电子转移的数目之比为___________。
(5)通过反应①~③,比较反应中氧化剂的氧化性强弱___________,(用“>”、“<”或
“=”连接)说明判断依据:___________。
(6)通过反应①~③,可以知道HCl的还原性强弱与___________、___________等因素有关。
19.(2022·安徽芜湖·三模)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分
为含锰化合物及FeS)与氧化锰矿(主要成分为MnO 等锰的氧化物)为原料制备硫酸锰的
2
工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O 、MgO。
4 2 3 2 3
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
物质 Fe(OH) Fe(OH) Mn(OH) Al(OH)
3 2 2 3
开始沉淀的pH 1.9 7.6 7.3 3.0
完全沉淀的pH 3.2 9.6 9.3 5.2
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______(2)若试剂a为MnO ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步
2
骤,造成的影响是_______。
(3)“中和除杂”时,应控制溶液的pH范围是_______。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1。则溶液中c(Mg2+)和c(Ca2+)的比值
=_______(已知:K (MgF )=6.4×10-10;K (CaF )=3.6×10-12)
sp 2 sp 2
(5)“碳化结晶”时发生反应的离子方程式为_______,选择NH HCO 而不选择Na CO 溶液的
4 3 2 3
原因是_______。
20.(2022·安徽芜湖·三模)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分
为含锰化合物及FeS)与氧化锰矿(主要成分为MnO 等锰的氧化物)为原料制备硫酸锰的
2
工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O 、MgO。
4 2 3 2 3
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
物质 Fe(OH) Fe(OH) Mn(OH) Al(OH)
3 2 2 3
开始沉淀的pH 1.9 7.6 7.3 3.0
完全沉淀的pH 3.2 9.6 9.3 5.2
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______
(2)若试剂a为MnO ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步
2
骤,造成的影响是_______。
(3)“中和除杂”时,应控制溶液的pH范围是_______。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1。则溶液中c(Mg2+)和c(Ca2+)的比值=_______(已知:K (MgF )=6.4×10-10;K (CaF )=3.6×10-12)
sp 2 sp 2
(5)“碳化结晶”时发生反应的离子方程式为_______,选择NH HCO 而不选择Na CO 溶液的
4 3 2 3
原因是_______。