文档内容
专题四 阿伏伽德罗常数
核心考点1、阿伏伽德罗常数易错陷阱
1.气体摩尔体积的概念
在标准状况( 0℃、101kPa)下,1mol任何气体所占的体积都约为22.4L,叫做该气体的摩尔体积,单位
是L/mol,用V 表示,即标准状况下( STP) 气体摩尔体积为22.4L/mol。因此,遇到体积与22.4L相关的
m
数据时要注意以下两种情况,免误入陷阱。
(1)温度和压强:
a. 考查气体时,一定要注意是标准状况(0℃,1.01×105Pa)还是非标准状况。题目经常会设置陷阱
——在常温常压下( 即25℃、101kPa)。
b. 温度和压强影响气体的体积,但不影响气体的质量和物质的量,因此,如果讨论物质的量、质量与
微粒数目的关系时,与标准状况无关。
(2)物质状态:
考查气体摩尔体积时,要注意在标准状况下①冰醋酸为固态,HO、HO 、Br 、四氯化碳、氯仿、二
2 2 2 2
氯甲烷、苯、二硫化碳、乙醇等为液体。②大于4而小于16的烃为液态(新戊烷除外),大于或等于16
的烃为固态。③SO 在标准状况下为固态,常温常压下为液态;④在常见有机物中C≤4 的烃、新戊烷、
3
CHCl、甲醛为气态。
3
3、不定体系
一些物质间的变化具有一定的隐蔽性,有时需要借助方程式分析才能挖掘出隐含的变化情况。如
“NO和O 的混合气”、“NO 气体有时应考虑2 NO (g) NO (g)”等。
2 2 2 2 4
4、物质中的粒子数的考查
当考查一定量的物质中含有的微粒数( 分子、原子、离子、质子、中子、电子等) 时,一定要明确物
质的结构,需注意以下问题。
(1) 单质组成:
气体单质的组成除常见的双原子分子(Cl、O、N 等)外,还有单原子分子(如稀有气体Ne)、三原
2 2 2
子分子(如O)、四原子分子(如P)等。
3 4
(2)具有相同最简式的物质:
如NO 和NO、乙烯与与丙烯、同分异构体、乙炔与苯、乙酸与葡萄糖等,只要总质量一定,则其中
2 2 4所含原子数与两者比例无关。
(3)某些物质的摩尔质量比较特殊:
要注意同位素引入时,同位素原子的中子数变化对质量数变化的影响,核电荷数和核外电子数未发生变化。
多涉及一定物质的量或一定质量的物质(DO、TO、18O、14CO、D 等)中含有多少粒子(分子、原子、离
2 2 2 2 2
子、质子、中子、电子等)的计算。如:20g重水(D O)和H18O均含有10N 个电子。
2 2 A
(4)离子数目的判断:
①特殊物质: Na O( 阳离子与阴离子之比为2:1) ,CaC ( 阳离子与阴离子之比为1: 1) ,BaO( 阳离子与
2 2 2 2
阴离子之比为1: 1)
②电离、水解等常识:考查弱电解质电离、盐类的水解等引起微粒数目的改变。
如:1L0.1 mol /L 的氨水含有0.1N 个OH- ( 解析: NH ·H O是弱碱,弱电解质部分电离,小于0.1N 个,
A 3 2 A
故错误) ;1mol FeCl 完全水解生成N 个Fe(OH) 胶粒(解析:忽视了CO2-水解及胶粒的组成特点,故错
3 A 3 3
误)
5、物质结构(特殊物质中的化学键的数目)
(1)要熟记某些无机物中的化学键
SiO( 1mol含4mol Si-O) 、金刚石(1mol C成2mol C-C)、Si(1mol Si成2mol Si-Si)、石墨、CH、
2 4
P( 1mol含6molP-P) 等较为复杂的物质的化学键数目。
4
(2)要熟记某些有机物中的化学键
①烷烃( C H )中, C-H键为: 2n + 2(与H原子数相同) ,C-C键为: n-1(比C原子数少1) ,总键数为:
n 2n + 2
3n+1;
②烯烃或环烷烃( C H )中, C-H 键为: 2n(与H原子数相同),C-C( 视双键为两条单键) 为n,总键数为: 3n ;
n 2n
③炔烃( C H ) 中,C-H 键为: 2n-2(与H原子数相同),C-C( 视三键为三条单键) 为: n + 1,总键数为:
n 2n-2
3n-1。
6、氧化还原反应或电化学中电子转移数目
要熟悉常见元素的化合价,正确分析氧化还原反应及电极反应中电子转移与反应物或生成物之间的定
量关系。歧化反应、归中反应、有变价金属(Fe、Cu等)参与的反应是高频考点。需要提醒学生以下几个
问题:
①Cl 与碱或水反应时: 1molCl 转移1mol电子;Cl 与还原性的物质反应时: 1molCl 转移2mol 电子。
2 2 2 2
②Cu、Fe 等是变价金属,在与强氧化剂反应时分别为+ 2、+ 3 价( 如Cl、HNO 等) ,而在与弱氧化剂反
2 3
应时分别为+ l、+ 2 价( 如H+、S、I 等) 。
2
③NaO 与HO、CO 反应时转移电子,如:2NaO+2H O=4NaOH+O ↑,每生成1mol O 转移2mol电子等。
2 2 2 2 2 2 2 2 2④HO 分解时: 1molH O 转移1mol 电子;HO 与强氧化剂反应时: 1molH O 转移2mol电子。
2 2 2 2 2 2 2 2
1.【2022年海南卷】在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下
A
列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
2.【2022年6月浙江卷】 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
3.(2021·湖南真题) 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
4.(2021·广东真题)设 为阿伏加德罗常数的值。下列说法正确的是
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
5.【2022年全国甲卷】 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
6.【2022年辽宁卷】设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为
1.(2023·四川绵阳·二模)为防止水体富营养化,常用 除去水体中过量氨氮(以 表示),气体产
物为 。设 为阿伏加德罗常数的值。下列有关叙述正确的是
A. 所含电子数均为
B. 的 溶液中 数目为
C.反应消耗 ,水体将增加 个D.除氨氮过程中,当生成 时转移电子数为
2.(2023·湖南永州·统考二模)设 为阿伏加德罗常数的值,下列说法正确的是
A. 中所含质子数为
B. 的烃分子中含有 σ键的数目一定为
C. 与足量的 反应,转移的电子数为
D.室温下 蔗糖完全水解形成的葡萄糖分子数为
3.(2023·湖北·统考一模) 表示阿伏加德罗常数的值。下列叙述正确的是
A. 固体中所含阳离子数为
B. 乙烷和丙烯的混合气体中所含 键数为
C.3.9gK在氧气中完全反应转移电子数为
D. 与足量 充分反应生成的 分子数为
4.(2017新课标Ⅲ卷) 为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol 的 中,含有 个中子
B.pH=1的HPO 溶液中,含有 个H+
3 4
C.2.24L(标准状况)苯在O 中完全燃烧,得到 个CO 分子
2 2
D.密闭容器中1 mol PCl 与1 mol Cl 反应制备 PCl (g),增加 个P-Cl键
3 2 5
5.(2016新课标Ⅰ卷)设N 为阿伏加德罗常数值。下列有关叙述正确的是( )
A
A.14 g乙烯和丙烯混合气体中的氢原子数为2N
A
B.1 molN 与4 mol H 反应生成的NH 分子数为2N
2 2 3 A
C.1 molFe溶于过量硝酸,电子转移数为2N
AD.标准状况下,2.24 LCCl 含有的共价键数为0.4N
4 A
核心考点2一定物质的量浓度溶液的配制
1.七种仪器需记牢
托盘天平、量筒、玻璃棒、容量瓶、胶头滴管、烧杯、药匙。
2.实验步骤要理清
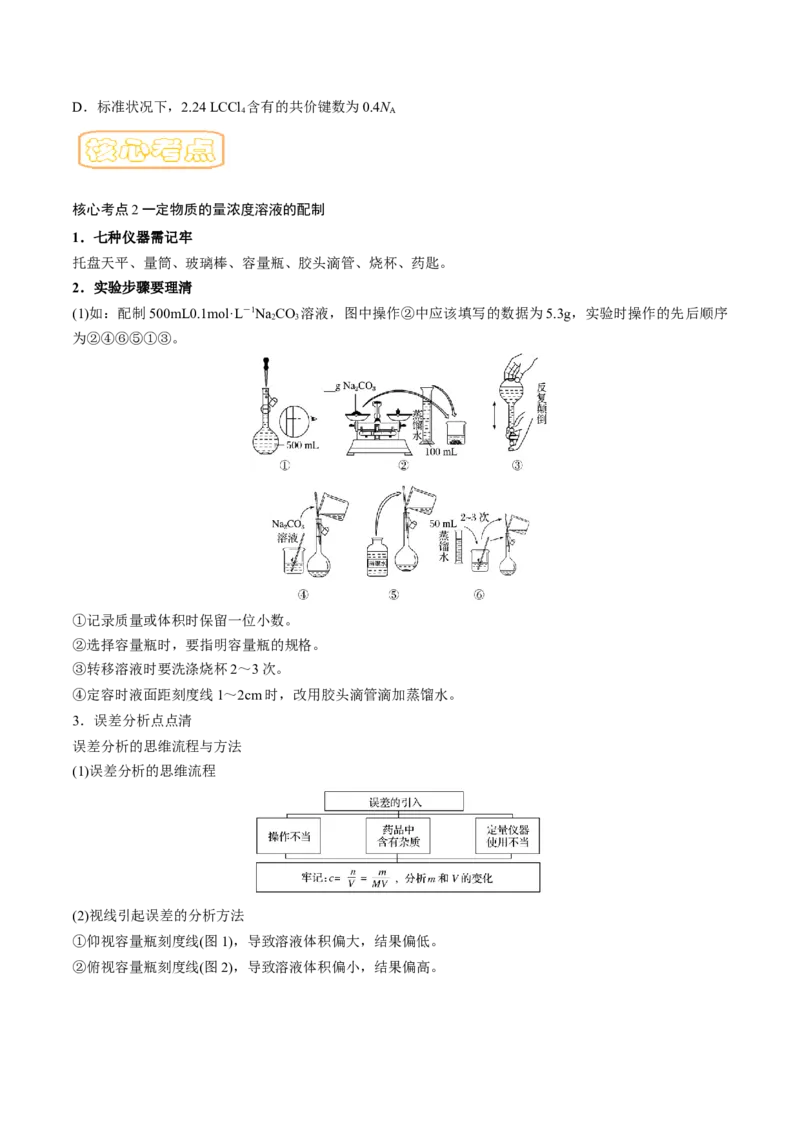
(1)如:配制500mL0.1mol·L-1NaCO 溶液,图中操作②中应该填写的数据为5.3g,实验时操作的先后顺序
2 3
为②④⑥⑤①③。
①记录质量或体积时保留一位小数。
②选择容量瓶时,要指明容量瓶的规格。
③转移溶液时要洗涤烧杯2~3次。
④定容时液面距刻度线1~2cm时,改用胶头滴管滴加蒸馏水。
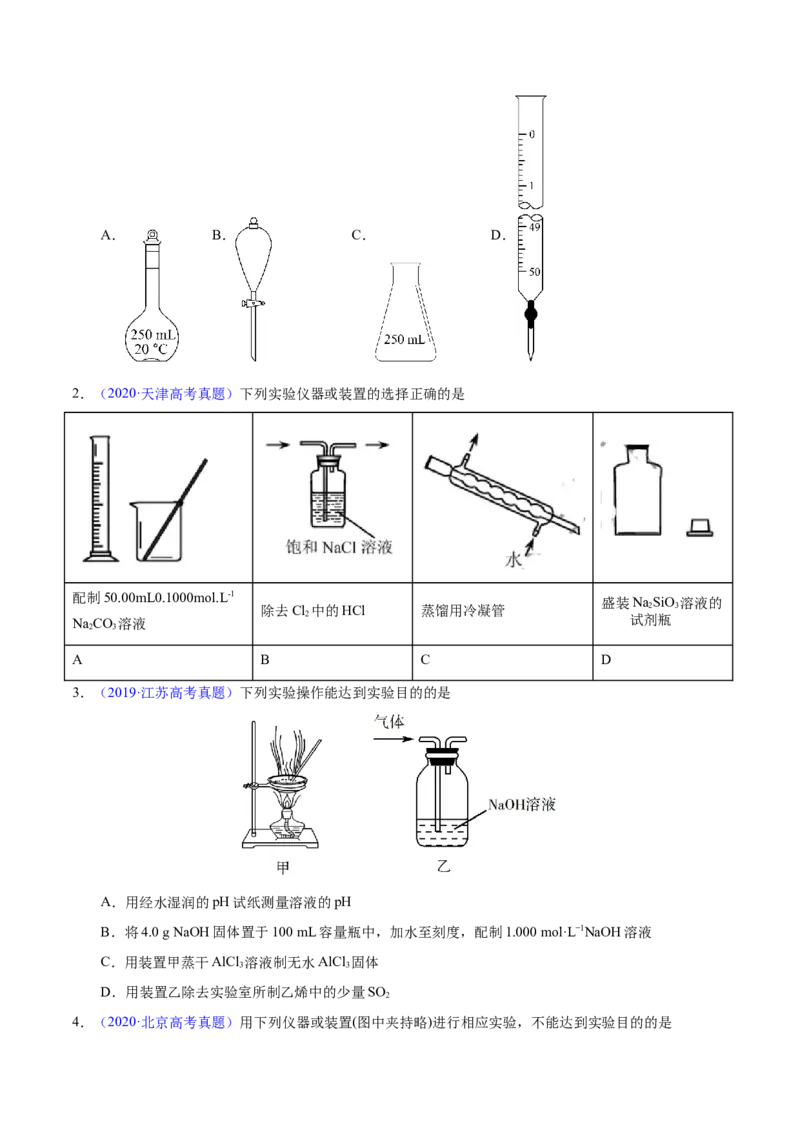
3.误差分析点点清
误差分析的思维流程与方法
(1)误差分析的思维流程
(2)视线引起误差的分析方法
①仰视容量瓶刻度线(图1),导致溶液体积偏大,结果偏低。
②俯视容量瓶刻度线(图2),导致溶液体积偏小,结果偏高。(3)用“偏高”“偏低”或“无影响”填空:
①砝码生锈:偏高。
②定容时,溶液温度高:偏高。
③定容时俯视容量瓶刻度线:偏高。
④称量时物码颠倒且使用游码:偏低。
⑤未洗涤烧杯、玻璃棒:偏低。
⑥称量易吸水物质时间过长:偏低。
⑦转移时,有液体溅出:偏低。
⑧滴加蒸馏水超过容量瓶刻度线,再用胶头滴管吸出:偏低。
⑨定容摇匀后,液面低于刻度线,再加水至刻度线:偏低。
⑩容量瓶内有少量水:无影响。
4.换算关系会推导
(1)气体溶质物质的量浓度的计算:
标准状况下,1L水中溶解某气体VL,所得溶液的密度为ρg·cm-3,气体的摩尔质量为Mg·
mol-1,则c=mol·L-1。
(2)溶液中溶质的质量分数与物质的量浓度之间的换算:
c=(c为溶质的物质的量浓度/mol·L-1,ρ为溶液的密度/g·cm-3,w为溶质的质量分数,M为溶质的摩尔质
量/g·mol-1)。
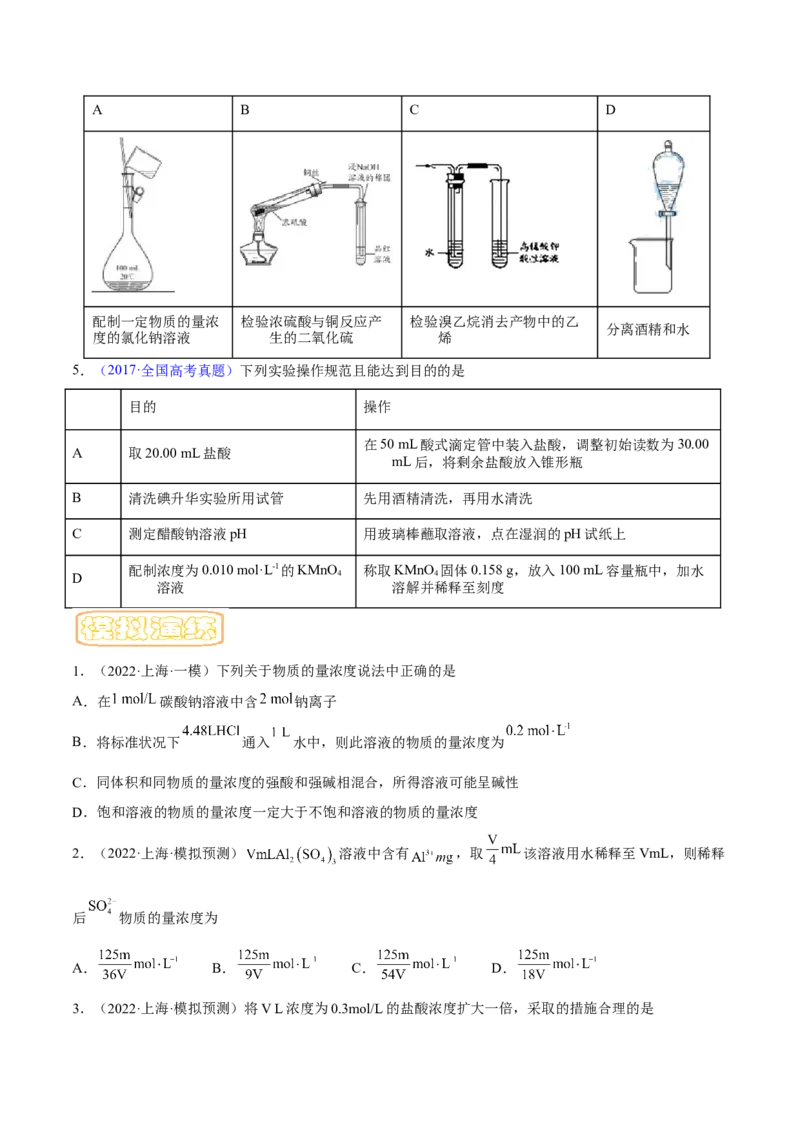
1.(2021·广东真题)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
上述操作中,不需要用到的仪器为A. B. C. D.
2.(2020·天津高考真题)下列实验仪器或装置的选择正确的是
配制50.00mL0.1000mol.L-1
盛装NaSiO 溶液的
除去Cl 中的HCl 蒸馏用冷凝管 2 3
2 试剂瓶
NaCO 溶液
2 3
A B C D
3.(2019·江苏高考真题)下列实验操作能达到实验目的的是
A.用经水湿润的pH试纸测量溶液的pH
B.将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L−1NaOH溶液
C.用装置甲蒸干AlCl 溶液制无水AlCl 固体
3 3
D.用装置乙除去实验室所制乙烯中的少量SO
2
4.(2020·北京高考真题)用下列仪器或装置(图中夹持略)进行相应实验,不能达到实验目的的是A B C D
配制一定物质的量浓 检验浓硫酸与铜反应产 检验溴乙烷消去产物中的乙
分离酒精和水
度的氯化钠溶液 生的二氧化硫 烯
5.(2017·全国高考真题)下列实验操作规范且能达到目的的是
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00
A 取20.00 mL盐酸
mL后,将剩余盐酸放入锥形瓶
B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010 mol·L-1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量瓶中,加水
D 4 4
溶液 溶解并稀释至刻度
1.(2022·上海·一模)下列关于物质的量浓度说法中正确的是
A.在 碳酸钠溶液中含 钠离子
B.将标准状况下 通入 水中,则此溶液的物质的量浓度为
C.同体积和同物质的量浓度的强酸和强碱相混合,所得溶液可能呈碱性
D.饱和溶液的物质的量浓度一定大于不饱和溶液的物质的量浓度
2.(2022·上海·模拟预测) 溶液中含有 ,取 该溶液用水稀释至VmL,则稀释
后 物质的量浓度为
A. B. C. D.
3.(2022·上海·模拟预测)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
4.(2019·陕西安康·统考一模)已知某饱和NaCl溶液的体积为VmL,密度为 ,质量分数为
w%,溶液中含NaCl的质量为m g。则下列表达式正确的是
A. B.
C. D.
5. 用20 18.4 mol·L-1的浓硫酸与铜共热一段时间后,冷却,过滤除去多余的铜,将滤液加水稀释到
100 ,所得溶液中 的浓度为3.18 mol·L-1,则此时溶液中 的物质的量浓度为
A.0.50 mol·L-1 B.0.75 mol·L-1 C.1.00 mol·L-1 D.3.18 mol·L-1
6.(2022·浙江·模拟预测)为确定某碱式碳酸镁 的组成,某同学取23.3g样品
置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 为
),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
(1)98%的硫酸溶液物质的量浓度是___________;
(2)根据实验测定的数据,求出碱式碳酸镁化学式中X、Y、Z的比值(要求写出计算过程)___________。