文档内容
专题突破卷 02 物质的量
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.清末成书的《化学鉴原》中有一段描述:“各原质(元素)化合所用之数名曰′分剂数′。养气(氧气)以
八分为一分剂(即分剂数为八)……一分剂轻气(氢气)为一……并之即水,一分剂为九”。其中与“分剂数”
一词最接近的现代化学概念是( )
A.摩尔质量 B.物质的量
C.化合价 D.质量分数
【答案】A
【解析】根据“各原质(元素)化合所用之数名曰′分剂数′。氧气八分为一分剂,氢气一分为一分剂,水
九分为一分剂”,则氧气的分剂数为八,氢气的分剂数为一,水的分剂数为九,即八份氧气与一份氢气化
合生成九份水,满足O +2H===2H O中的质量守恒,因此与“分剂数”一词最接近的现代化学概念为摩
2 2 2
尔质量。
2.下列关于决定物质体积的因素的说法不正确的是( )
A.物质的体积取决于微粒的数目、微粒的大小和微粒之间的距离
B.在相同条件下,微粒数相同的任何气体都具有相同体积
C.在同温同压下,1 mol任何物质所占有的体积均相同
D.等质量的H,压强越小、温度越高,气体所占体积越大
2
【答案】C
【解析】从微观角度来说,物质的体积由微粒的数目、微粒的大小和微粒之间的距离决定,A正确;微粒
数相同的气体的物质的量相同,相同条件下体积也相同,B正确;C项结论只适用于气态物质,C错误;
压强越小、温度越高,气体的体积越大,D正确。
3.(2024·陕西高三普通高中学业水平合格考试模拟)下列以物质的量为中心的计算正确的是
A.0.1mol·L-1CaCl 溶液中,c(Cl-)为0.05mol·L-1
2
B.22g干冰中约含有3.01×1023个CO 分子
2
C.常温常压下,11.2LO 的质量为16g
2
D.1molNH 的质量为10g
3
【答案】B
【解析】氯离子的浓度为氯化钙浓度的2倍,所以0.1mol·L-1CaCl 溶液中,c(Cl-)为0.2mol·L-1,A错误;
2
22g干冰物质的量为0.5mol,所以约含有3.01×1023个CO 分子,B正确;常温常压下,11.2LO 物质的量不
2 2是0.5mol,所以质量不是16g,C错误;1molNH 的质量为17g,D错误。
3
4.(2023·福建福州模拟)用质量分数为6%的氯化钠溶液(密度约为1.04 g/cm3),配制50 g质量分数为3%的
氯化钠溶液,下列说法正确的是( )
A.图中仪器有四种是不需要的,还需一种图中未画出的玻璃仪器
B.量取水时俯视读数会使所配溶液质量分数偏小
C.需要量取50 mL水配制3%氯化钠溶液
D.需要量取的6%氯化钠溶液的体积为24 mL
【答案】D
【解析】配制该溶液所需仪器主要有烧杯、玻璃棒、量筒、胶头滴管,故图中的 a圆底烧瓶、b酸式滴定
管、c碱式滴定管、d分液漏斗、f托盘天平、g容量瓶六种仪器均不需要,还需要的玻璃仪器有玻璃棒、
量筒、胶头滴管,A错误。用量筒量取水时,俯视读数,实际液体体积比读数偏小,则所配溶液质量分数
偏大,B错误。配制时需要6%的氯化钠溶液:50 g×3%÷6%=25 g,25 g÷1.04 g/cm3≈24 mL,水:50 g-25
g=25 g,C错误,D正确。
5.打火机里装有液态的丙烷和丁烷。下列说法错误的是( )
A.打开打火机开关,分子间距变大
B.摩擦打火石,达到气体的着火点
C.1 mol丙烷完全燃烧需要氧气的体积约为112 L
D.若n(丙烷)∶n(丁烷)=1∶9,则该混合物的平均摩尔质量为56.6 g·mol-1
【答案】C
【解析】打开打火机开关,压强减小,燃料汽化,分子间距变大,A正确;B.摩擦打火石,使温度达到
气体的着火点,从而引燃燃料,B正确;C.没有说明具体的温度和压强,不能判断1 mol丙烷完全燃烧需
要氧气的体积,C错误;D.若n(丙烷)∶n(丁烷)=1∶9,则该混合物的平均摩尔质量为=56.6 g·mol-1,D正
确。
6.(2024·海南华侨中学高三三模)反应 (未配平)可为火箭发射提供动力,下
列说法错误的是
A.17g 溶液中含有氧原子的数目为
B.0.1mol 中含有质子的数目为C.常温常压下,3.2g 中含有共用电子对的数目为0.5
D.标准状况下,生成22.4L 时转移电子的数目为4
【答案】A
【解析】17g 溶液中含有水分子,水分子还有氧原子,氧原子的数目大于 ,A错误;1个 含有
10个质子,0.1mol 中含有质子的数目为 ,B正确;3.2g 的物质的量为0.1mol,1个 含有
5个共用电子对,故3.2g 中含有共用电子对的数目为0.5 ,C正确;生成1个 ,转移4个电子,
标准状况下,生成22.4L 时转移电子的数目为4 ,D正确。
7.一定温度和压强下,用m g的CH 、CO 、O 、SO 四种气体分别吹出四个体积大小不同的气球(如
4 2 2 2
图),下列说法中正确的是( )
A.气球②中装的是O
2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
【答案】D
【解析】m g的CH、CO、O、SO 四种气体的物质的量分别为 mol、 mol、 mol、 mol。根据阿伏加德
4 2 2 2
罗定律及其推论可知,同温同压下气体的体积与其物质的量成正比,结合四个气球的体积推知,①是
SO ,②是CO ,③是O ,④是CH ,A项错误;气球①和气球③中气体分子数之比为∶=1∶2,B项错
2 2 2 4
误;气球①和气球④中气体物质的量之比为∶=1∶4,C项错误;气球③和气球④中气体密度之比等于其摩
尔质量之比,D项正确。
8.(2024·安徽名校教研联盟高三3月月考)已知 为阿伏加德罗常数的值,下列说法正确的是
A. 葡萄糖( 中含有羟基的数目为
B. 甲苯分子中含有 键的数目为C. 的 溶液中 的数目为
D. 醋酸钠固体溶于稀醋酸至溶液呈中性,醋酸根的数目为
【答案】D
【解析】葡萄糖为五羟基醛, 葡萄糖 中含有羟基的数目为 ,A项错误;苯环中不是3
个 键,是1个6中心6电子的大 键,B项错误; 的 溶液中
,数目为 ,C项错误;根据溶液呈电中性可得:
,则 ,D项正确。
9.某温度下,向图中所示a、b、c、d中通入等质量的CH、CO、O、SO 四种气体中的一种(已知密封隔
4 2 2 2
板Ⅰ、Ⅱ、Ⅲ、Ⅳ可自由滑动,且与容器内壁摩擦不计)。下列说法中错误的是( )
A.d中通入的气体是CH
4
B.a和b中原子个数之比为16∶11
C.a和c容器体积之比为1∶2
D.c和d中气体密度之比为2∶1
【答案】B
【解析】A项,设四种气体的质量都为m g,则CH、CO、O、SO 的物质的量分别表示为 mol、 mol、
4 2 2 2
mol、 mol,同温同压下,气体体积比等于物质的量之比,则a、b、c、d中分别为SO 、CO、O、CH。
2 2 2 4
由此可知d中通入的气体是CH;B项,二者物质的量之比= mol∶ mol=11∶16,则原子个数之比=
4
(11×3)∶(16×3)=11∶16;C项,同温同压下,气体体积之比等于物质的量之比,则a和c容器体积之比=
mol∶ mol=1∶2;D项,同温同压下,两种气体的密度之比等于摩尔质量之比,因此c和d中气体密度之比
=32∶16=2∶1。
10.配制250 mL 0.10 mol·L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏小的是( )
①将NaOH固体放在纸上称量,再转移到烧杯中溶解 ②烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯
③实验用的容量瓶洗净后未干燥,里面含有少量水 ④定容时采用俯视
A.①② B.①②④ C.①③ D.①④【答案】A
【解析】①部分氢氧化钠粘在纸上,溶质质量偏小,所得的溶液浓度偏小;②容量瓶中溶质偏少,所得的
溶液浓度偏小;③由于定容时需要加入蒸馏水,对溶液浓度无影响;④溶液体积偏小,所得的溶液浓度偏
大。
11.(2024·江苏镇江调研)向三个密闭容器中分别充入Ne、H、O 三种气体,下列有关这三种气体的叙述正
2 2
确的是 ( )
A.温度、压强相同时,三种气体的密度关系:ρ(H )>ρ(Ne)>ρ(O )
2 2
B.温度、密度相同时,三种气体的压强关系:p(H )>p(Ne)>p(O )
2 2
C.质量、温度、压强均相同时,三种气体的体积关系:V(O )>V(Ne)>V(H )
2 2
D.温度、压强、体积均相同时,三种气体的质量关系:m(H )>m(Ne)>m(O )
2 2
【答案】B
【解析】根据阿伏加德罗定律的推论pV=nRT=RT可知,则pM=ρRT,即温度、压强相同时,气体的密
度与其摩尔质量成正比,A项错误;同理,温度、密度相同时,气体的压强与其摩尔质量成反比,B项正
确;质量、温度、压强均相同时,气体的体积与其摩尔质量成反比,C项错误;温度、压强、体积均相同
时,气体的质量与其摩尔质量成正比,D项错误。
12.(2024·湖南岳阳一模)常温下,某氮的气态氧化物15.6 L与过量的氢气混合,在一定条件下反应,使之
生成液态水和无污染的气体单质。恢复到原状态,反应后气体体积比反应前气体体积减小了46.8 L,则原
氮的氧化物的化学式为( )
A.NO B.NO
2 3 2
C.NO D.NO
2
【答案】A
【解析】设该氮氧化合物的分子式为NO,化学方程式为NO+xH===N +xHO,相同条件下参加反应
2 x 2 x 2 2 2
的气体的体积之比等于其物质的量之比也等于其化学计量数之比,
NO+xH===N +xHO ΔV
2 x 2 2 2
1 x
15.6 L 46.8 L
则1∶x=15.6 L∶46.8 L,x=3,所以其化学式为NO。
2 3
13.现有A、B、C三种化合物,各取40 g相混合,完全反应后,容器中只有18 g B、49 g C,还有D生
成,已知D的相对分子质量为106。下列说法中不正确的是( )
A.化学方程式一定是A+B===C+D
B.生成D的物质的量为0.5 mol
C.若化学方程式为2A+B===C+D,则A的摩尔质量为40 g·mol-1
D.若D是碳酸钠,则钠离子的质量为23 g
【答案】A
【解析】现有A、B、C三种化合物,各取40 g相混合,完全反应后,容器中只有18 g B、49 g C,还有D
生成,则40 g A完全反应,参加反应的B的质量为40 g-18 g=22 g,生成的C的质量为49 g-40 g=9
g,根据质量守恒定律反应生成的D的质量为40 g+22 g-9 g=53 g。由分析知A和B是反应物,C和D是生成物,但无法确定A、B、C、D的物质的量之比,即反应方程式不一定为 A+B===C+D,故A错
误;反应生成的D的质量为53 g,D的相对分子质量为106,则生成D的物质的量为=0.5 mol,故B正
确;若化学方程式为2A+B===C+D,结合D的物质的量为0.5 mol,则A的物质的量为1 mol,其摩尔质
量为 =40 g·mol-1,故C正确;若D是碳酸钠,物质的量为0.5 mol,则钠离子的物质的量为1 mol,质量
为23 g,故D正确。
14.(2024·江苏苏州高三月考)下列叙述正确的是( )
①标准状况下,1 L HCl和1 L H O的物质的量相同
2
②常温常压下,1 g H 和14 g N 的体积相同
2 2
③28 g CO的体积为22.4 L
④若两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑤同温同压下,相同体积的任何气体单质所含的原子数目相同
⑥同温同压下,气体的密度与气体的相对分子质量成正比
A.①④⑥ B.②⑥
C.⑤⑥ D.①⑤⑥
【答案】B
【解析】①标准状况下,1 L HCl的物质的量为 mol,但标准状况下水为液体,不能利用气体摩尔体积计
算其物质的量,①错误;②1 g H 的物质的量为0.5 mol,14 g N 的物质的量为0.5 mol,常温常压下,气
2 2
体的物质的量相同时,其体积相同,②正确;③未说明是在标准状况下,不能确定28 g CO的体积,③错
误;④物质的状态不确定,体积可能相同,也可能不同,④错误;⑤同温同压下,相同体积的任何气体单
质的物质的量相同,所含的分子数目相同,但原子数目不一定相同,⑤错误;⑥根据阿伏加德罗定律及推
论可知,同温同压下,气体的密度与气体的相对分子质量成正比,⑥正确。
15.(2024·山东临沂高三第二次高考模拟)[Co(NH )Cl]Cl (M=250.5g/mol)是一种易溶于热水,难溶于乙
3 5 2
醇的紫红色晶体。
(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入ag研细的CoCl ·6H O(M=238g/mol),得
2 2
到[Co(NH )]Cl 沉淀。边搅拌边慢慢滴入足量30%H O 溶液,得到[Co(NH )HO]Cl 溶液。慢慢注入适量
3 6 2 2 2 3 5 2 3
浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到bg产品。
(2)钴的测定:取5.0g样品于锥形瓶中,加入NaOH溶液并加热使钴(Ⅲ)完全沉淀,后加入HSO 和HO 将
2 4 2 2
其还原为钴(Ⅱ),再加入VmLcmol/LEDTA,用cmol/LZnCl 标准溶液滴定过量的EDTA,消耗ZnCl 溶液
1 1 2 2 2
平均体积为VmL(EDTA与金属阳离子1:1反应)。
2
下列有关计算正确的是
A.[Co(NH )Cl]Cl 的产率为 B.[Co(NH )Cl]Cl 的产率为
3 5 2 3 5 2C.样品中钴的质量分数为 D.样品中钴的质量分数为
【答案】C
【解析】根据Co元素守恒可知,ag研细的CoCl ·6H O(M=238g/mol)完全反应理论上能够生成的
2 2
[Co(NH )Cl]Cl 的质量为: = ,而实际生成bg[Co(NH )Cl]Cl ,故
3 5 2 3 5 2
[Co(NH )Cl]Cl 的产率为 ×100%= ×100%,A错误;由A项分析可知,[Co(NH )Cl]Cl 的产
3 5 2 3 5 2
率为 ×100%,B错误;由题干步骤(2)信息可知,5.0g样品中含有Co的物质的量为:(c V-c V)×10-
1 1 2 2
3mol,故样品中钴的质量分数为: = ,C正确;由C项
分析可知,样品中钴的质量分数为 ,D错误。
二、非选择题(本题包括4小题,共55分)
16.(14分)实验室需要配制0.50 mol·L-1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整
个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为5 g)、药匙、烧杯、________、
________、________、________以及等质量的两片同种纸片。
(2)计算。配制该溶液需取NaCl晶体________ g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将试剂倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是_______________________
_________________________________________________。
(5) 转 移 、 洗 涤 。 在 转 移 时 应 使 用 玻 璃 棒 引 流 , 需 要 洗 涤 烧 杯 2 ~ 3 次 是 为 了
________________________________________________________________________。
(6)定容。向容量瓶中加水至液面接近刻度线________处,改用________加水,使溶液凹液面与刻度线相
切。(7)摇匀、装瓶。
【答案】(1)500 mL容量瓶 (1分) 量筒(1分) 胶头滴管(1分) 玻璃棒(1分)
(2)14.6(2分)
(3)①
(1分)
②左盘(1分)
(4)搅拌,加速NaCl溶解(2分)
(5)保证溶质全部转入容量瓶中(2分)
(6)1~2 cm(1分) 胶头滴管(1分)
【解析】配制480 mL 0.50 mol·L-1的NaCl溶液,必须用500 mL的容量瓶。m(NaCl)=0.50 mol·L-1×0.5
L×58.5 g·mol-1≈14.6 g(托盘天平精确到0.1 g)。用托盘天平称量时,物品放在左盘。配制一定物质的量浓度
溶液的一般步骤为计算→称量(或量取)→溶解、冷却→转移、洗涤→定容、摇匀→装瓶贴签。
17.(18分)填写下列空白。
(1)将等物质的量的NH 和CH 混合,混合气体中NH 与CH 的质量比为________。
3 4 3 4
(2)要使NH 与CH 含相同数目的H原子,则NH 和CH 的物质的量之比为________。
3 4 3 4
(3)标准状况下,密度为0.75 g·L-1的NH 与CH 组成的混合气体中,NH 的体积分数为_________,该混合
3 4 3
气体对氢气的相对密度为________。
(4)已知a g A和b g B恰好完全反应生成 0.2 mol C和d g D,则C的摩尔质量为________________。
(5)同温同压下,已知O 的密度为ρ g·L-1,则CO 的密度为____________。
2 2
(6)现有下列三种气体:①32 g CH ;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6 L
4
O。请按物理量由小到大的顺序排列:
2
a.质量:____________(填标号,下同);
b.分子数目:____________;
c.相同状况下气体的体积:____________。
【答案】(1)17∶16(2分)
(2)4∶3(2分)
(3)80%(2分)8.4(2分)
(4)5(a+b-d)g·mol-1(2分)
(5) g·L-1(2分)
(6)①<②<③(2分)②<③<①(2分)②<③<①(2分)
【解析】(1)将等物质的量(设为n mol)的NH 和CH 混合,混合气体中NH 与CH 的质量比为(n mol×17
3 4 3 4
g·mol-1)∶(n mol×16 g·mol-1)=17∶16。(2)要使NH 与CH 含相同数目的H原子,则NH 和CH 的物质的量
3 4 3 4
之比为4∶3。(3)混合气体的平均摩尔质量为0.75 g·L-1×22.4 L·mol-1=16.8 g·mol-1,设NH 的体积分数为
3
x,则17x+16(1-x)=16.8,解得x=0.8,即80%;该混合气体对氢气的相对密度为=8.4。(4)根据质量守
恒定律,C的质量为(a+b-d)g,则C的摩尔质量为=5(a+b-d)g·mol-1。(5)同温同压下,已知O 的密度
2
为ρ g·L-1,而=,则ρ(CO)== g·L-1。(6)①32 g CH 的物质的量为=2 mol;②约含有6.02×1023个HCl
2 4分子的氯化氢气体的物质的量为=1 mol,其质量为36.5 g·mol-1×1 mol=36.5 g;③标准状况下33.6 L O 的
2
物质的量为=1.5 mol,其质量为32 g·mol-1×1.5 mol=48 g。a.根据上述分析可知,三种物质的质量大小为
①<②<③。b.根据N=nN 可知,气体分子数与其物质的量成正比,气体的物质的量大小为②<③<①,
A
则三种气体含有分子数目大小为②<③<①。c.根据V=nV 可知,相同条件下气体的体积与物质的量成正
m
比,气体的物质的量大小为②<③<①,则三种气体的体积大小为②<③<①。
18.(8分)为了测定某铜银合金的组成,将30.0 g合金溶于80.0 mL 13.5 mol·L-1的浓硝酸中。待合金完
全溶解后,收集到NO和NO 的混合气体6.72 L(标准状况下)并测得H+浓度为1 mol·L-1。假设反应后溶液
2
的体积为80.0 mL,不考虑2NO NO,试计算:
2 2 4
(1)被还原的硝酸的物质的量为______________。
(2)合金中银的质量分数为_____________。
(3)确定6.72 L气体中各成分的物质的量:____________。
【答案】(1)0.3 mol(2分)
(2)36%(2分)
(3)n(NO)=0.2 mol,n(NO )=0.1 mol(4分)
2
【解析】(1)根据氮原子守恒可知被还原的硝酸的物质的量即生成气体的物质的量,所以被还原的硝酸的物
质的量为=0.3 mol。
(2)剩余硝酸是 1 mol·L-1×0.08 L=0.08 mol,则参加反应的硝酸为 13.5 mol·L-1×0.08 L-0.08 mol=1.0
mol。设合金中Cu和Ag的物质的量分别为x mol和y mol,则64.0x+108y=30.0,根据氮原子守恒可知
2x+y=1.0-0.3=0.7,解得:x=0.3、y=0.1,所以银的质量分数为×100%=36%。
(3)设混合气体中NO、NO 的物质的量分别是a mol、b mol,则a+b=0.3,根据得失电子守恒可知3a+b
2
=0.3×2+0.1,解得a=0.2、b=0.1,即6.72 L气体中n(NO)为0.2 mol,n(NO )为0.1 mol。
2
19.(15分)(2024·福建七市质检)一水草酸钙(CaC O·H O)可用作分离稀有金属的载体。回答下列问题:
2 4 2
(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙
沉淀,过滤,用热水洗涤,在105 ℃干燥得产品。
①已知CaCl 溶液中CaCl 质量浓度为1.11 g·L-1,则该溶液中CaCl 的物质的量浓度为__________。
2 2 2
②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:
__________________________________________________________________。
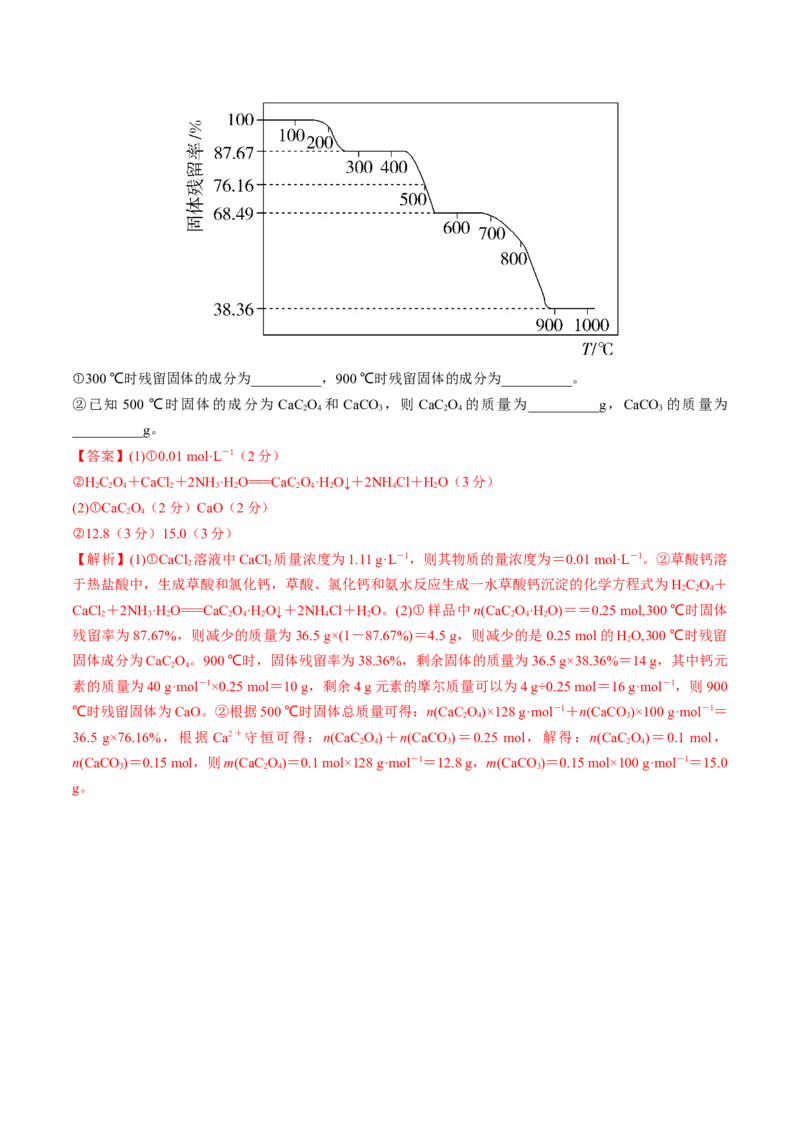
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取 36.5 g样品加热,样品的固体残留率随温度
的变化如图所示。①300 ℃时残留固体的成分为__________,900 ℃时残留固体的成分为__________。
②已知 500 ℃时固体的成分为 CaC O 和 CaCO ,则 CaC O 的质量为__________g,CaCO 的质量为
2 4 3 2 4 3
__________g。
【答案】(1)①0.01 mol·L-1(2分)
②H C O+CaCl +2NH ·H O===CaC O·H O↓+2NH Cl+HO(3分)
2 2 4 2 3 2 2 4 2 4 2
(2)①CaC O(2分)CaO(2分)
2 4
②12.8(3分)15.0(3分)
【解析】(1)①CaCl 溶液中CaCl 质量浓度为1.11 g·L-1,则其物质的量浓度为=0.01 mol·L-1。②草酸钙溶
2 2
于热盐酸中,生成草酸和氯化钙,草酸、氯化钙和氨水反应生成一水草酸钙沉淀的化学方程式为HC O +
2 2 4
CaCl +2NH ·H O===CaC O·H O↓+2NH Cl+HO。(2)①样品中n(CaC O·H O)==0.25 mol,300 ℃时固体
2 3 2 2 4 2 4 2 2 4 2
残留率为87.67%,则减少的质量为36.5 g×(1-87.67%)=4.5 g,则减少的是0.25 mol的HO,300 ℃时残留
2
固体成分为CaC O。900 ℃时,固体残留率为38.36%,剩余固体的质量为36.5 g×38.36%=14 g,其中钙元
2 4
素的质量为40 g·mol-1×0.25 mol=10 g,剩余4 g元素的摩尔质量可以为4 g÷0.25 mol=16 g·mol-1,则900
℃时残留固体为CaO。②根据500 ℃时固体总质量可得:n(CaC O)×128 g·mol-1+n(CaCO)×100 g·mol-1=
2 4 3
36.5 g×76.16%,根据 Ca2+守恒可得:n(CaC O)+n(CaCO)=0.25 mol,解得:n(CaC O)=0.1 mol,
2 4 3 2 4
n(CaCO)=0.15 mol,则m(CaC O)=0.1 mol×128 g·mol-1=12.8 g,m(CaCO)=0.15 mol×100 g·mol-1=15.0
3 2 4 3
g。