文档内容
专题突破卷 08 化学反应与能量(二)
——电解池、金属的腐蚀与防护 电化学原理的综合应用 多池、多室的电化学装置
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.湖北省随州市出土的曾侯乙编钟,是战国早期的青铜编钟,主要由铜锡合金冶炼铸造而成,保存完
好。下列有关说法错误的是( )
A.锡青铜的熔点比纯铜低
B.在自然环境中,锡青铜中的锡可对铜起保护作用
C.青铜文物在潮湿环境中的腐蚀比干燥环境中快
D.锡青铜表面生成Cu (OH) Cl覆盖物的过程属于化学腐蚀
2 3
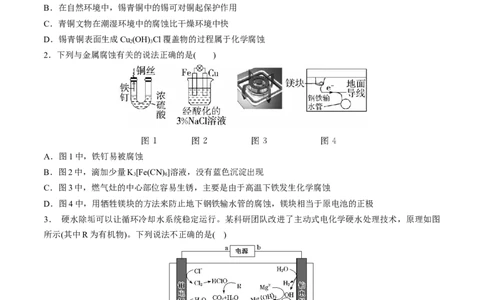
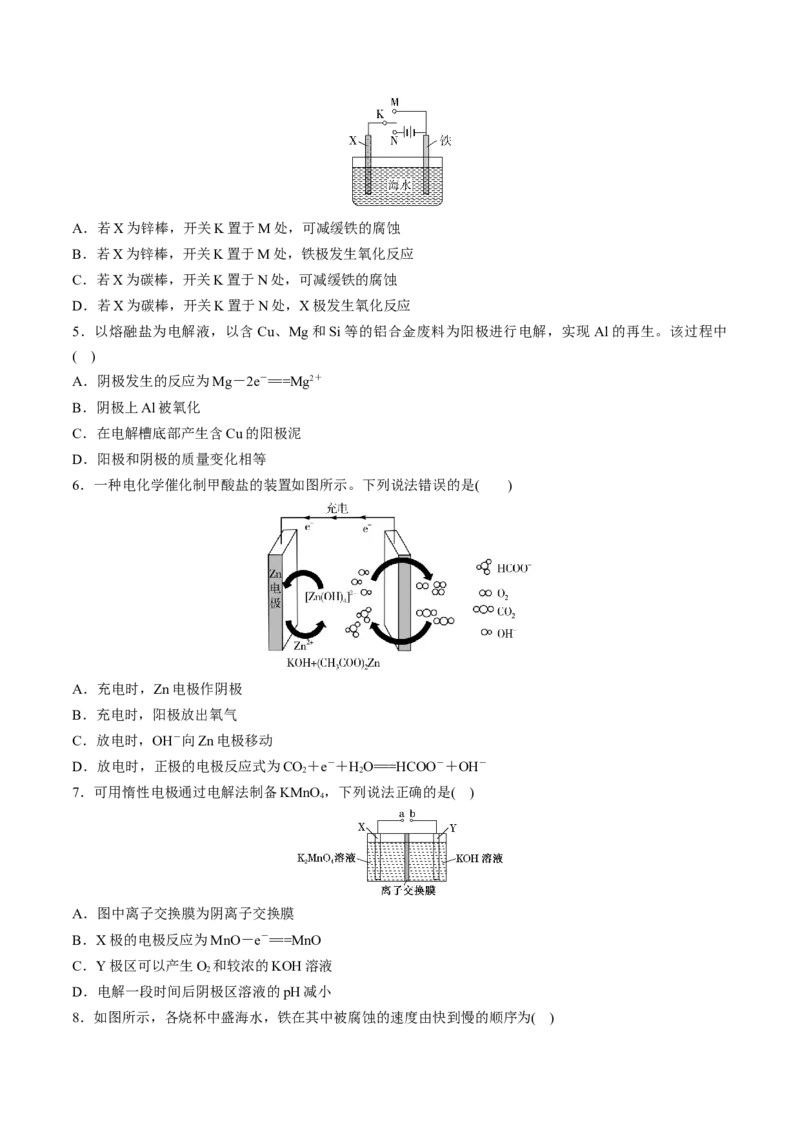
2.下列与金属腐蚀有关的说法正确的是( )
A.图1中,铁钉易被腐蚀
B.图2中,滴加少量K[Fe(CN) ]溶液,没有蓝色沉淀出现
3 6
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁输水管的腐蚀,镁块相当于原电池的正极
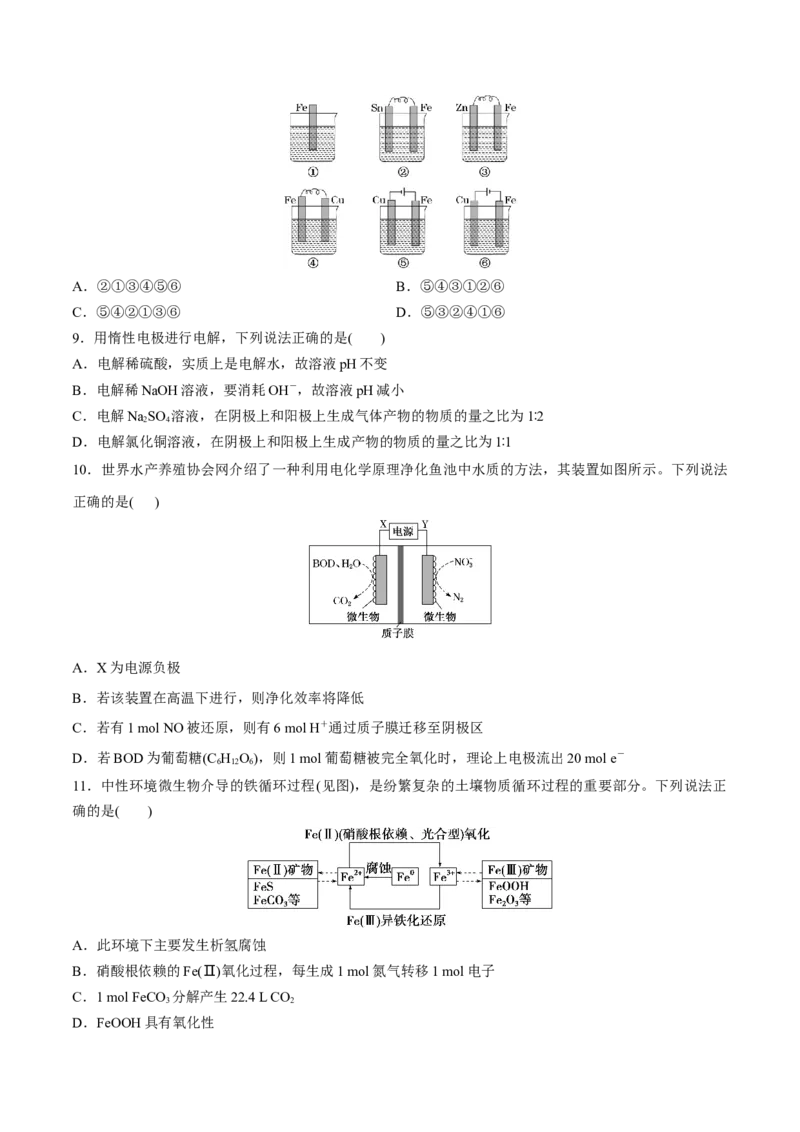
3. 硬水除垢可以让循环冷却水系统稳定运行。某科研团队改进了主动式电化学硬水处理技术,原理如图
所示(其中R为有机物)。下列说法不正确的是( )
A.b端为电源正极,处理后的水垢沉淀在阳极底部
B.处理过程中Cl-可循环利用
C.流程中发生离子反应:HCO+Ca2++OH-===CaCO ↓+HO,Mg2++2OH-===Mg(OH) ↓
3 2 2
D.若R为CO(NH),则消耗1 mol CO(NH ) 生成N 时,铂电极N处产生的H 应大于3 mol
2 2 2 2 2 2
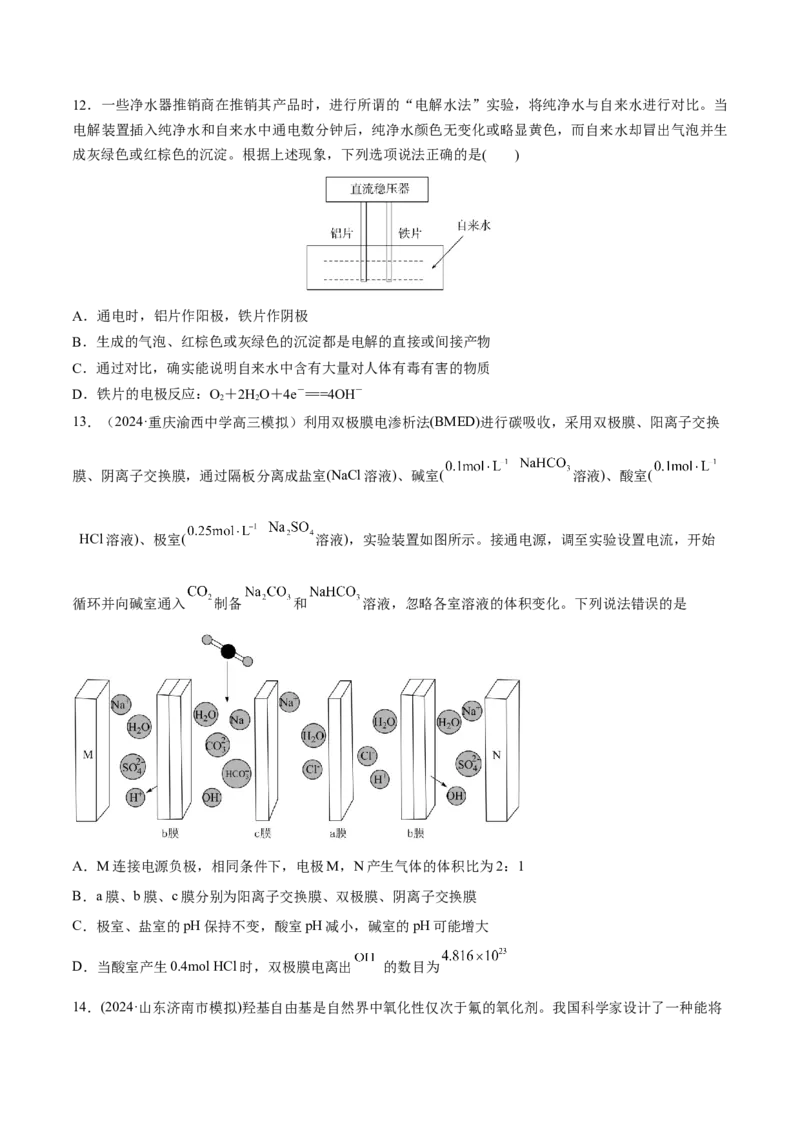
4.利用如图装置可以模拟铁的电化学防护。下列说法错误的是( )A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀
B.若X为锌棒,开关K置于M处,铁极发生氧化反应
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀
D.若X为碳棒,开关K置于N处,X极发生氧化反应
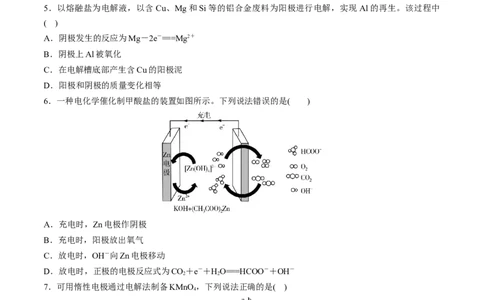
5.以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实现Al的再生。该过程中
( )
A.阴极发生的反应为Mg-2e-===Mg2+
B.阴极上Al被氧化
C.在电解槽底部产生含Cu的阳极泥
D.阳极和阴极的质量变化相等
6.一种电化学催化制甲酸盐的装置如图所示。下列说法错误的是( )
A.充电时,Zn电极作阴极
B.充电时,阳极放出氧气
C.放电时,OH-向Zn电极移动
D.放电时,正极的电极反应式为CO+e-+HO===HCOO-+OH-
2 2
7.可用惰性电极通过电解法制备KMnO ,下列说法正确的是( )
4
A.图中离子交换膜为阴离子交换膜
B.X极的电极反应为MnO-e-===MnO
C.Y极区可以产生O 和较浓的KOH溶液
2
D.电解一段时间后阴极区溶液的pH减小
8.如图所示,各烧杯中盛海水,铁在其中被腐蚀的速度由快到慢的顺序为( )A.②①③④⑤⑥ B.⑤④③①②⑥
C.⑤④②①③⑥ D.⑤③②④①⑥
9.用惰性电极进行电解,下列说法正确的是( )
A.电解稀硫酸,实质上是电解水,故溶液pH不变
B.电解稀NaOH溶液,要消耗OH-,故溶液pH减小
C.电解NaSO 溶液,在阴极上和阳极上生成气体产物的物质的量之比为1∶2
2 4
D.电解氯化铜溶液,在阴极上和阳极上生成产物的物质的量之比为1∶1
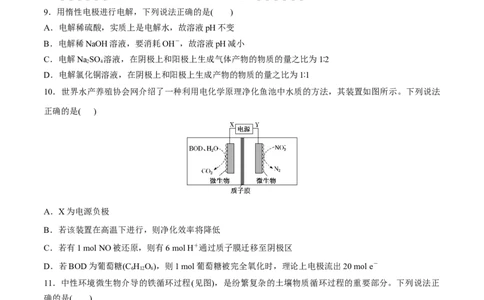
10.世界水产养殖协会网介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。下列说法
正确的是( )
A.X为电源负极
B.若该装置在高温下进行,则净化效率将降低
C.若有1 mol NO被还原,则有6 mol H+通过质子膜迁移至阴极区
D.若BOD为葡萄糖(C H O),则1 mol葡萄糖被完全氧化时,理论上电极流出20 mol e-
6 12 6
11.中性环境微生物介导的铁循环过程(见图),是纷繁复杂的土壤物质循环过程的重要部分。下列说法正
确的是( )
A.此环境下主要发生析氢腐蚀
B.硝酸根依赖的Fe(Ⅱ)氧化过程,每生成1 mol氮气转移1 mol电子
C.1 mol FeCO 分解产生22.4 L CO
3 2
D.FeOOH具有氧化性12.一些净水器推销商在推销其产品时,进行所谓的“电解水法”实验,将纯净水与自来水进行对比。当
电解装置插入纯净水和自来水中通电数分钟后,纯净水颜色无变化或略显黄色,而自来水却冒出气泡并生
成灰绿色或红棕色的沉淀。根据上述现象,下列选项说法正确的是( )
A.通电时,铝片作阳极,铁片作阴极
B.生成的气泡、红棕色或灰绿色的沉淀都是电解的直接或间接产物
C.通过对比,确实能说明自来水中含有大量对人体有毒有害的物质
D.铁片的电极反应:O+2HO+4e-===4OH-
2 2
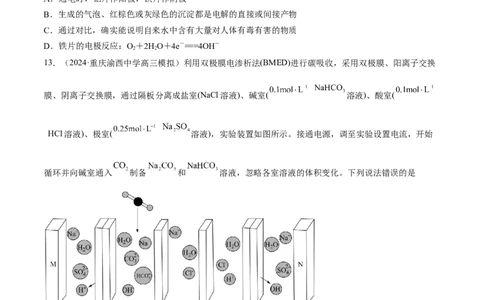
13.(2024·重庆渝西中学高三模拟)利用双极膜电渗析法(BMED)进行碳吸收,采用双极膜、阳离子交换
膜、阴离子交换膜,通过隔板分离成盐室(NaCl溶液)、碱室( 溶液)、酸室(
HCl溶液)、极室( 溶液),实验装置如图所示。接通电源,调至实验设置电流,开始
循环并向碱室通入 制备 和 溶液,忽略各室溶液的体积变化。下列说法错误的是
A.M连接电源负极,相同条件下,电极M,N产生气体的体积比为2:1
B.a膜、b膜、c膜分别为阳离子交换膜、双极膜、阴离子交换膜
C.极室、盐室的pH保持不变,酸室pH减小,碱室的pH可能增大
D.当酸室产生0.4mol HCl时,双极膜电离出 的数目为
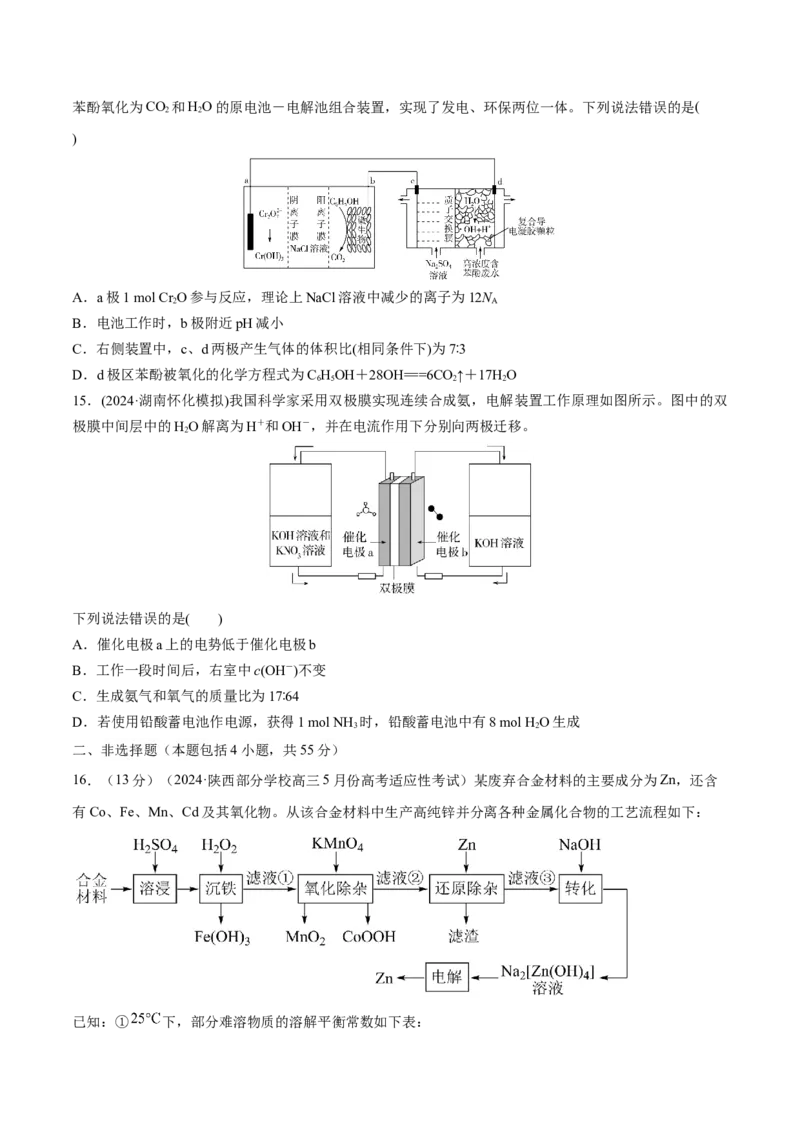
14.(2024·山东济南市模拟)羟基自由基是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为CO 和HO的原电池-电解池组合装置,实现了发电、环保两位一体。下列说法错误的是(
2 2
)
A.a极1 mol Cr O参与反应,理论上NaCl溶液中减少的离子为12N
2 A
B.电池工作时,b极附近pH减小
C.右侧装置中,c、d两极产生气体的体积比(相同条件下)为7∶3
D.d极区苯酚被氧化的化学方程式为C HOH+28OH===6CO ↑+17HO
6 5 2 2
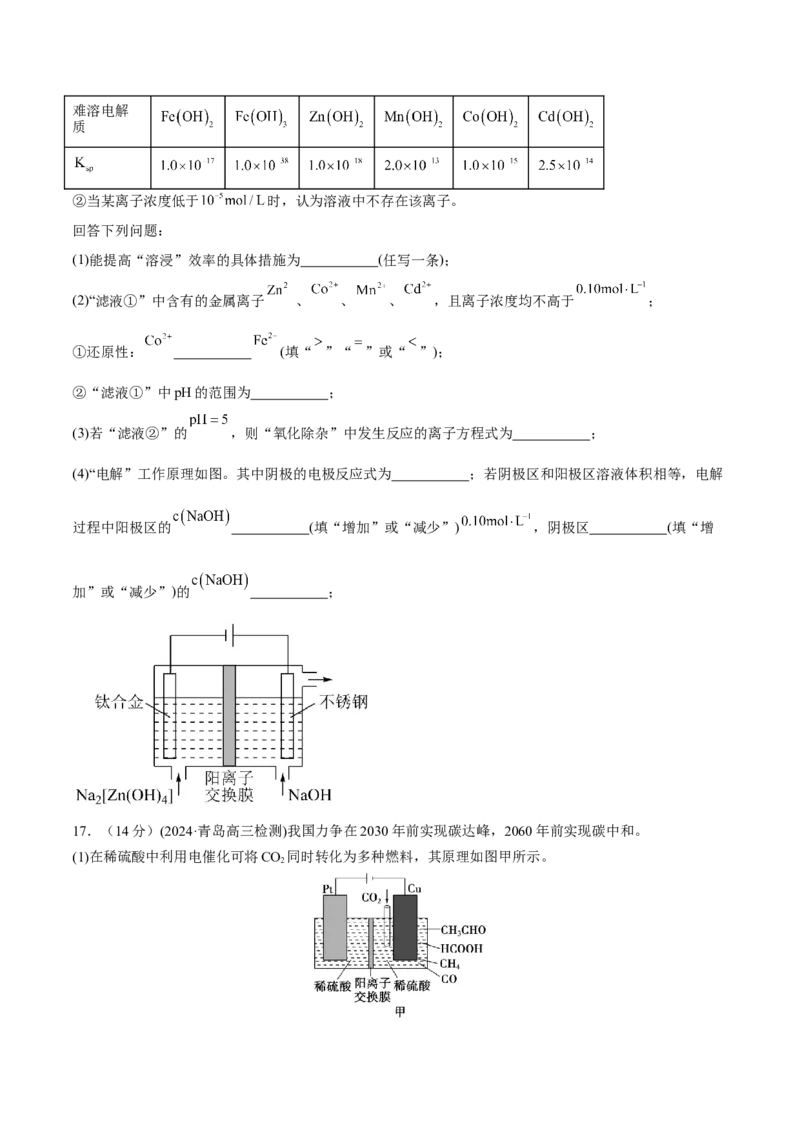
15.(2024·湖南怀化模拟)我国科学家采用双极膜实现连续合成氨,电解装置工作原理如图所示。图中的双
极膜中间层中的HO解离为H+和OH-,并在电流作用下分别向两极迁移。
2
下列说法错误的是( )
A.催化电极a上的电势低于催化电极b
B.工作一段时间后,右室中c(OH-)不变
C.生成氨气和氧气的质量比为17∶64
D.若使用铅酸蓄电池作电源,获得1 mol NH 时,铅酸蓄电池中有8 mol H O生成
3 2
二、非选择题(本题包括4小题,共55分)
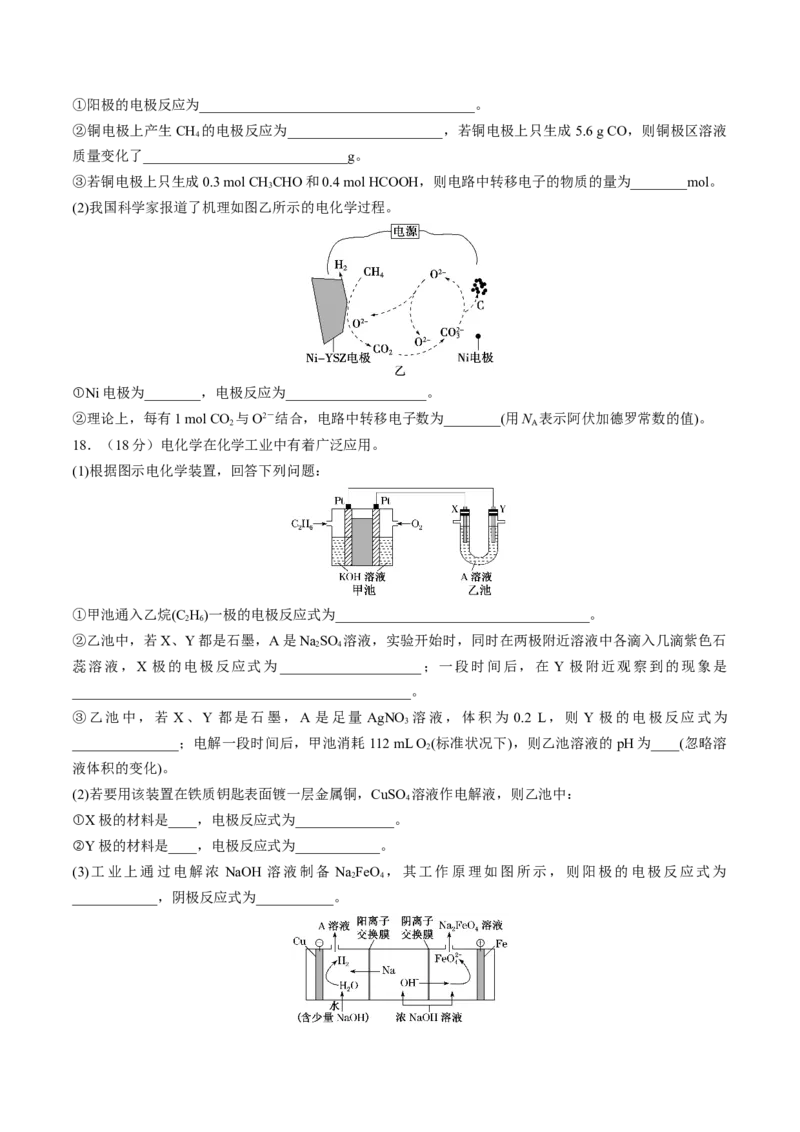
16.(13分)(2024·陕西部分学校高三5月份高考适应性考试)某废弃合金材料的主要成分为Zn,还含
有Co、Fe、Mn、Cd及其氧化物。从该合金材料中生产高纯锌并分离各种金属化合物的工艺流程如下:
已知:① 下,部分难溶物质的溶解平衡常数如下表:难溶电解
质
②当某离子浓度低于 时,认为溶液中不存在该离子。
回答下列问题:
(1)能提高“溶浸”效率的具体措施为 (任写一条);
(2)“滤液①”中含有的金属离子 、 、 、 ,且离子浓度均不高于 ;
①还原性: (填“ ”“ ”或“ ”);
②“滤液①”中pH的范围为 ;
(3)若“滤液②”的 ,则“氧化除杂”中发生反应的离子方程式为 ;
(4)“电解”工作原理如图。其中阴极的电极反应式为 ;若阴极区和阳极区溶液体积相等,电解
过程中阳极区的 (填“增加”或“减少”) ,阴极区 (填“增
加”或“减少”)的 ;
17.(14分)(2024·青岛高三检测)我国力争在2030年前实现碳达峰,2060年前实现碳中和。
(1)在稀硫酸中利用电催化可将CO 同时转化为多种燃料,其原理如图甲所示。
2①阳极的电极反应为_______________________________________。
②铜电极上产生CH 的电极反应为______________________,若铜电极上只生成5.6 g CO,则铜极区溶液
4
质量变化了_____________________________g。
③若铜电极上只生成0.3 mol CH CHO和0.4 mol HCOOH,则电路中转移电子的物质的量为________mol。
3
(2)我国科学家报道了机理如图乙所示的电化学过程。
①Ni电极为________,电极反应为____________________。
②理论上,每有1 mol CO 与O2-结合,电路中转移电子数为________(用N 表示阿伏加德罗常数的值)。
2 A
18.(18分)电化学在化学工业中有着广泛应用。
(1)根据图示电化学装置,回答下列问题:
①甲池通入乙烷(C H)一极的电极反应式为____________________________________。
2 6
②乙池中,若X、Y都是石墨,A是NaSO 溶液,实验开始时,同时在两极附近溶液中各滴入几滴紫色石
2 4
蕊溶液,X 极的电极反应式为____________________;一段时间后,在 Y 极附近观察到的现象是
________________________________________________。
③乙池中,若 X、Y 都是石墨,A 是足量 AgNO 溶液,体积为 0.2 L,则 Y 极的电极反应式为
3
_______________;电解一段时间后,甲池消耗112 mL O (标准状况下),则乙池溶液的pH为____(忽略溶
2
液体积的变化)。
(2)若要用该装置在铁质钥匙表面镀一层金属铜,CuSO 溶液作电解液,则乙池中:
4
①X极的材料是____,电极反应式为______________。
②Y极的材料是____,电极反应式为____________。
(3)工业上通过电解浓 NaOH 溶液制备 NaFeO ,其工作原理如图所示,则阳极的电极反应式为
2 4
____________,阴极反应式为___________。19.(10分)如图所示,通电5 min后,电极5的质量增加2.16 g,请回答下列问题。
(1)a 为电源的________(填“正”或“负”)极,C 池是________池。A 池阳极的电极反应为
________________,C池阴极的电极反应为________________。
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电
前溶液中Cu2+的物质的量浓度为________。
(3)如果 A 池溶液是 200 mL 足量的食盐水(电解过程溶液体积不变),则通电 5 min 后,溶液的 pH 为
________。