文档内容
专题讲座(一) 化学计算的常用方法
第一部分:高考真题感悟
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2018·海南·高考真题)某工业废气所含氮氧化物(N O)的氮氧质量比为7∶4,该NO 可表示为
x y x y
A.NO B.NO C.NO D.NO
2 2 3 2
3.(2014·上海·高考真题)含有砒霜(As O)的试样和锌、盐酸混合反应,生成的砷化氢(AsH)在热玻璃管
2 3 3
中完全分解成单质砷和氢气。若砷的质量为1.50mg,则
A.被氧化的砒霜为1.98mg
B.分解产生的氢气为0.672ml
C.和砒霜反应的锌为3.90mg
D.转移的电子总数为6×10―5N
A
4.(2010·湖南·高考真题)把500 有BaCl 和KCl的混合溶液分成5等份,取一份加入含 硫酸钠
2
的溶液,恰好使钡离子完全沉淀;另取一份加入含 硝酸银的溶液,恰好使氯离子完全沉淀。则该混
合溶液中钾离子浓度为
A. B.
C. D.
5.(2010·海南·高考真题)把V L含有MgSO 和KSO 的混合溶液分成两等份,一份加入含a mol NaOH
4 2 4
的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl 的溶液,恰好使硫酸根离子完全沉
2
淀为硫酸钡。则原混合溶液中钾离子的浓度为
A. (b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(2b-a)/V mol·L-1 D.2(b-a)/V mol·L-1
7.(2011·上海·高考真题)过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体
质量增加了28 g,反应中有关物质的物理量正确的是(N 表示阿伏加德罗常数)
A
二氧化碳 碳酸钠 转移的电子
A 1mol N
A
B 22.4L 1molC 106 g 1mol
D 106g 2N
A
8.(2017·上海·高考真题)有3克镁铝合金完全溶于盐酸后得到标准状况下的氢气3360 mL,在所得的溶
液中加入足量的浓氨水可得沉淀质量_________克。
9.(2017·上海·高考真题)10.7g 氯化铵和足量的氢氧化钙混合后充分加热,再将所生成的气体完全溶于
水后得 50 mL 溶液,计算:
(1)可生成标准状况下的氨气多少升?______________
(2)所得溶液的物质的量浓度是多少? ______________
10.(2017·上海·高考真题)6克冰醋酸完全溶于水配成500毫升溶液,用此醋酸溶液滴定20毫升某一未
知浓度的氢氧化钠溶液,共消耗这种醋酸溶液30毫升。求:
(1)醋酸溶液的物质的量的浓度_________。
(2)未知氢氧化钠溶液的物质的量的浓度________________。
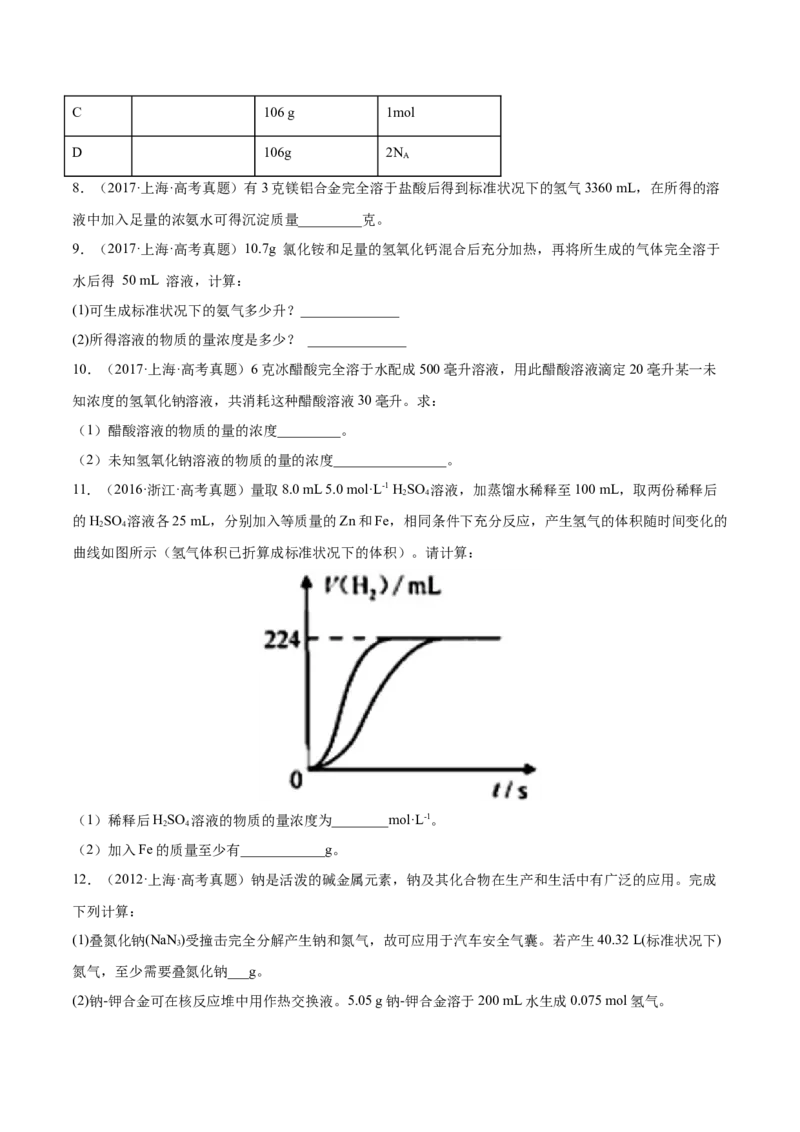
11.(2016·浙江·高考真题)量取8.0 mL 5.0 mol·L-1 HSO 溶液,加蒸馏水稀释至100 mL,取两份稀释后
2 4
的HSO 溶液各25 mL,分别加入等质量的Zn和Fe,相同条件下充分反应,产生氢气的体积随时间变化的
2 4
曲线如图所示(氢气体积已折算成标准状况下的体积)。请计算:
(1)稀释后HSO 溶液的物质的量浓度为________mol·L-1。
2 4
(2)加入Fe的质量至少有____________g。
12.(2012·上海·高考真题)钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成
下列计算:
(1)叠氮化钠(NaN )受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)
3
氮气,至少需要叠氮化钠___g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。①计算溶液中氢氧根离子的物质的量浓度________ (忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式________。
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:
2NaAl(OH) +CO →2Al(OH) ↓ +Na CO+H O。已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)
4 2 3 2 3 2 3
和15 mol Na CO,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH) 和NaCO 的物质的
2 3 3 2 3
量之比________。
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过
程中产品无损失。
氢氧化钠质量(g) 氯化钠质量(g)
① 2.40 3.51
② 2.32 2.34
③ 3.48 3.51
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出
结论________。
13.(2020·天津·高考真题)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ.甲方案
实验原理:
实验步骤:
(1)判断 沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO )=________mol‧L-1。
4
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_________(填“偏高”、“偏低”或“无影
4
响”)。
Ⅱ.乙方案实验原理: ,
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H 体积为bmL,已知实验条件下 ,则c(CuSO )______mol‧L-1(列
2 4
出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )________(填“偏高”、“偏低”或
4
“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:_________(填“是”或“否”)。
4
第二部分:最新模拟精练
1.(2022·全国·模拟预测)将1.92g铜粉与一定量的浓硝酸反应,硝酸的还原产物为NO和NO ,当铜粉
2
完全反应时收集到混合气体1.12L(气体体积折算为标准状况)。则所消耗硝酸的物质的量是A.0.08mol B.0.09mol C.0.11mol D.0.12mol
2.(2022·湖南娄底·模拟预测)取X、Y两种醇各0.1mol,分别与足量的钠反应,在同温同压下收集到H
2
体积分别为VmL、VmL。根据上述数据,不能推知下列相关量之比的是
1 2
A.X、Y消耗钠的质量之比 B.X、Y分子所含羟基数目之比
C.X、Y反应中转移电子数之比 D.X、Y的摩尔质量之比
3.(2022·全国·模拟预测)室温下,将1 L某气态烃与4 L氧气混合,引燃后将生成的气体通过浓硫酸,
剩余气体恢复至室温时体积变为2 L,则该气体是:①乙烷;②乙烯;③乙炔;④甲烷
A.只有② B.只有①②③ C.只有④ D.以上均不可能
4.(2022·山东聊城·二模)镓(Ga)位于周期表中第四周期第IIIA族,与强酸、强碱溶液均能反应生成H,
2
是一种应用广泛的金属元素,可用于制造半导体材料氮化镓、砷化镓、磷化镓等。同温同压下,
分别与 浓度均为 的盐酸和氢氧化钠溶液充分反应,生成H 的体积分别为 和
2
。下列说法错误的是
A.
B.转移的电子数之比为
C.消耗酸和碱的物质的量之比为
D.反应前后两溶液的质量变化相等
5.(2022·湖南·长沙一中一模)将铁、氧化铁、氧化铜组成的混合物粉末mg放入盛 盐酸
的烧杯中,充分反应后产生2.24L H (标准状况),残留固体2.56g。过滤,滤液中无Cu2+。将滤液加水稀释
2
到500mL,测得其中c(H+)为 。下列说法正确的是
A.m=15.36
B.烧杯中转移电子的物质的量共为0.28mol
C.若将反应后的溶液倒入蒸发皿中直接蒸干可得到0.2mol FeCl
2
D.过滤时需要用到的玻璃仪器有烧杯、玻璃棒、漏斗、锥形瓶
6.(2022·北京·牛栏山一中模拟预测)镁与不同浓度的硝酸溶液反应可得到 、 、 、 、等还原产物(每种情况只考虑生成一种还原产物),下列说法错误的是
A.24g镁与足量某浓度的硝酸溶液充分反应生成 时消耗
B.消耗等量的镁生成的还原产物物质的量最多的是
C.生成氢气时所用硝酸浓度应小于生成其它产物时所用硝酸浓度
D.生成等物质的量的 和 消耗镁的物质的量之比为3:4
7.(2022·湖南·模拟预测)常温常压下,0.5mol铝、0.5mol铁分别与足量稀硫酸完全反应,生成氢气的体
积分别为 和 ( 为阿伏加德罗常数的值)。下列说法正确的是
A. L
B.
C.铝、铁消耗硫酸的物质的量相等
D.反应生成的硫酸铝水解形成 胶体,胶体粒子数目为0.5
8.(2022·山东临沂·三模)以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。下列说法正
确的是
A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率
B.反应②的原子利用率为100%
C.生成1.0 mol NH NO 至少需要0.75 mol CH
4 3 4
D.反应③理论上当n( NH):n(O )= 4:3时,恰好完全反应
3 2
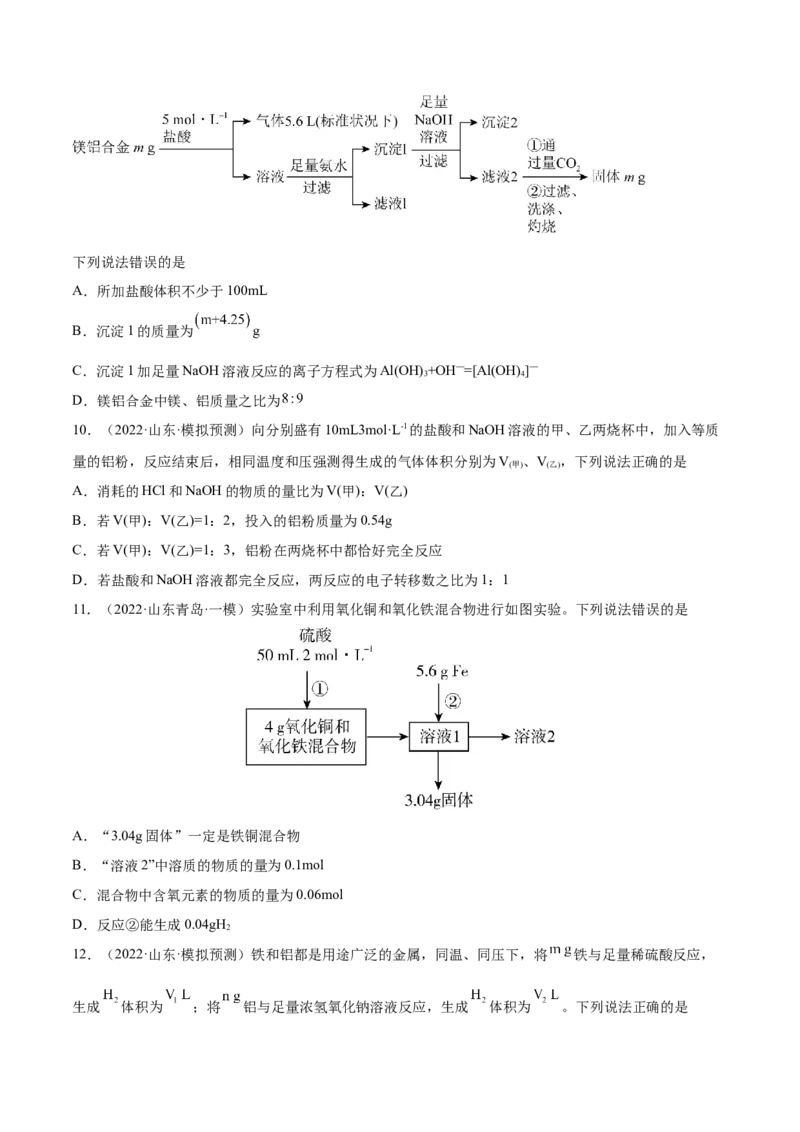
9.(2022·山东青岛·二模)实验室为测定镁铝合金中镁、铝含量,设计如下流程:下列说法错误的是
A.所加盐酸体积不少于100mL
B.沉淀1的质量为 g
C.沉淀1加足量NaOH溶液反应的离子方程式为Al(OH) +OH—=[Al(OH) ]—
3 4
D.镁铝合金中镁、铝质量之比为
10.(2022·山东·模拟预测)向分别盛有10mL3mol·L-1的盐酸和NaOH溶液的甲、乙两烧杯中,加入等质
量的铝粉,反应结束后,相同温度和压强测得生成的气体体积分别为V 、V ,下列说法正确的是
(甲) (乙)
A.消耗的HCl和NaOH的物质的量比为V(甲):V(乙)
B.若V(甲):V(乙)=1:2,投入的铝粉质量为0.54g
C.若V(甲):V(乙)=1:3,铝粉在两烧杯中都恰好完全反应
D.若盐酸和NaOH溶液都完全反应,两反应的电子转移数之比为1:1
11.(2022·山东青岛·一模)实验室中利用氧化铜和氧化铁混合物进行如图实验。下列说法错误的是
A.“3.04g固体”一定是铁铜混合物
B.“溶液2”中溶质的物质的量为0.1mol
C.混合物中含氧元素的物质的量为0.06mol
D.反应②能生成0.04gH
2
12.(2022·山东·模拟预测)铁和铝都是用途广泛的金属,同温、同压下,将 铁与足量稀硫酸反应,
生成 体积为 ;将 铝与足量浓氢氧化钠溶液反应,生成 体积为 。下列说法正确的是A.两反应生成 的物质的量之比为
B. 铁与足量稀硫酸反应,生成 的物质的量一定为
C.保持温度压强不变,将 铝与足量稀硫酸反应,生成 体积大于
D.参加反应的铁与铝的质量比
二、主观题(共4小题,共40分)
13.(10分)(2022·浙江·模拟预测) 在不同温度下失水和分解,随着温度升高分别生成
,现称取 在敞口容器加热一定时间后,得到 固体,
测得生成的 的体积为 (已折算为标准标况),求:
(1)固体的成分和物质的量比_______。
(2)标准状态下生成 的体积_______。
14.(10分)(2022·浙江台州·二模)已知某加碘盐(含 的食盐)中含碘量为 。现有
1000kg该加碘盐,计算:
(1)该加碘食盐中至少含碘_______mol
(2)若用 与 反应制 ,标准状况至少需要消耗 _______L(写出计算过程)。
15.(10分)(2022·浙江杭州·二模)以下方法常用于对废水中的苯酚进行定量测定:取 含苯酚废
水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用 标
准溶液滴定至终点,消耗 溶液 .已知
(三溴苯酚). 和 溶液颜色均为无色.
(1)消耗 的物质的量为________.
(2)废水中苯酚的物质的量浓度为_______(写出简要计算过程).
16.(10分)(2022·浙江·模拟预测)现有一瓶常见一元酸形成的铵盐固体,为测定其中的含氮量可以采用
“甲醛法”,即: (未配平)。现称取4g该铵盐溶于水,加入足量的
甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入 的NaOH溶液,当
滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
(1)过程中消耗的甲醛物质的量为_______mol。
(2)该铵盐中氮的质量分数是_______%。(写出计算过程)