文档内容
专题讲座(七) 常考速率、平衡图像题解题策略
第一部分:高考真题感悟
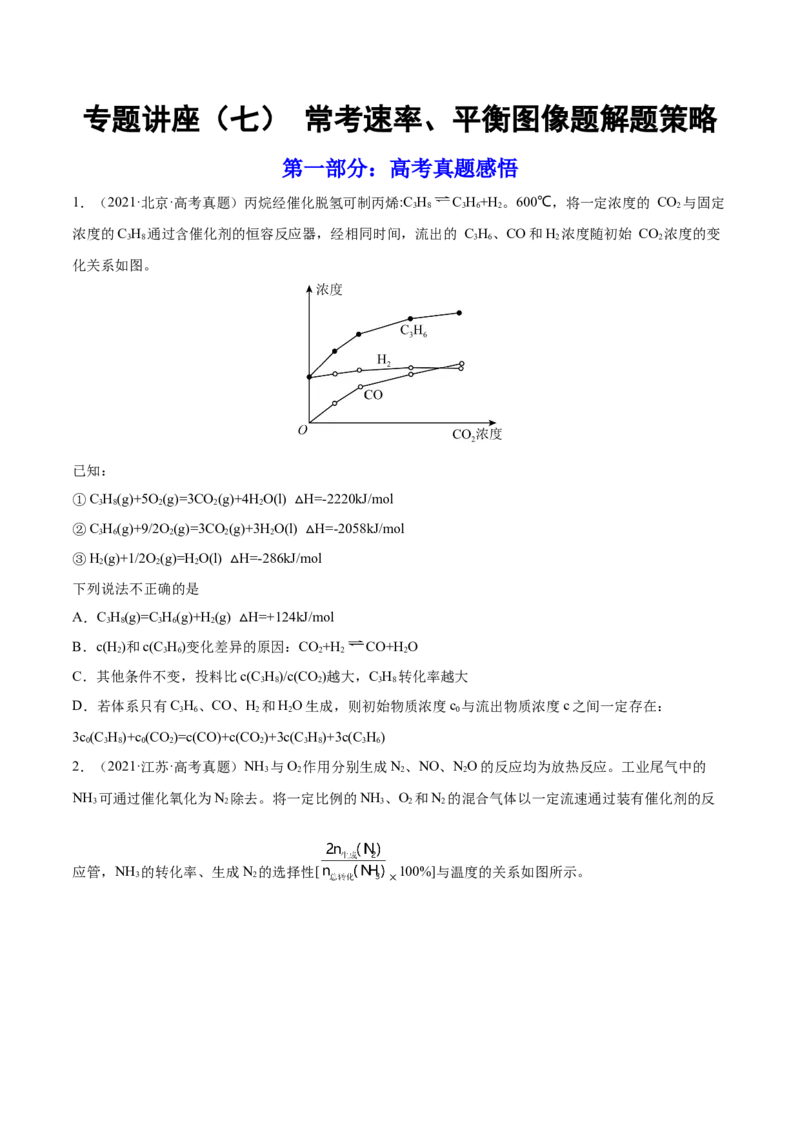
1.(2021·北京·高考真题)丙烷经催化脱氢可制丙烯:C H C H+H 。600℃,将一定浓度的 CO 与固定
3 8 3 6 2 2
浓度的C H 通过含催化剂的恒容反应器,经相同时间,流出的 C H、CO和H 浓度随初始 CO 浓度的变
3 8 3 6 2 2
化关系如图。
已知:
①C H(g)+5O(g)=3CO (g)+4HO(l) H=-2220kJ/mol
3 8 2 2 2
②C
3
H
6
(g)+9/2O
2
(g)=3CO
2
(g)+3H
2
O(l)△ H=-2058kJ/mol
③H
2
(g)+1/2O
2
(g)=H
2
O(l) H=-286kJ/m△ol
下列说法不正确的是 △
A.C H(g)=C H(g)+H(g) H=+124kJ/mol
3 8 3 6 2
B.c(H
2
)和c(C
3
H
6
)变化差异△的原因:CO
2
+H
2
CO+H
2
O
C.其他条件不变,投料比c(C H)/c(CO )越大,C H 转化率越大
3 8 2 3 8
D.若体系只有C H、CO、H 和HO生成,则初始物质浓度c 与流出物质浓度c之间一定存在:
3 6 2 2 0
3c(C H)+c (CO)=c(CO)+c(CO )+3c(C H)+3c(C H)
0 3 8 0 2 2 3 8 3 6
2.(2021·江苏·高考真题)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的
3 2 2 2
NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反
3 2 3 2 2
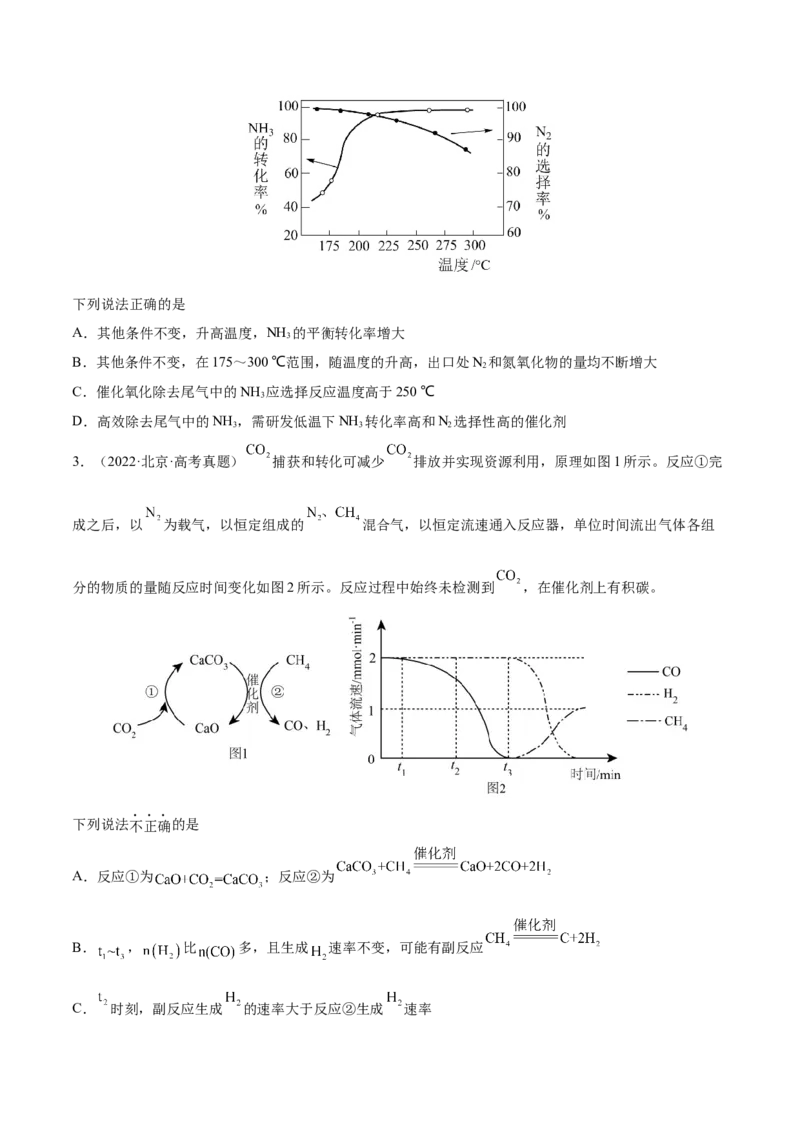
应管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
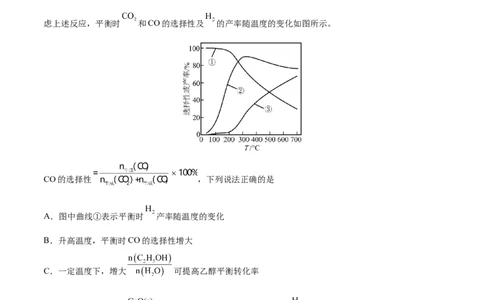
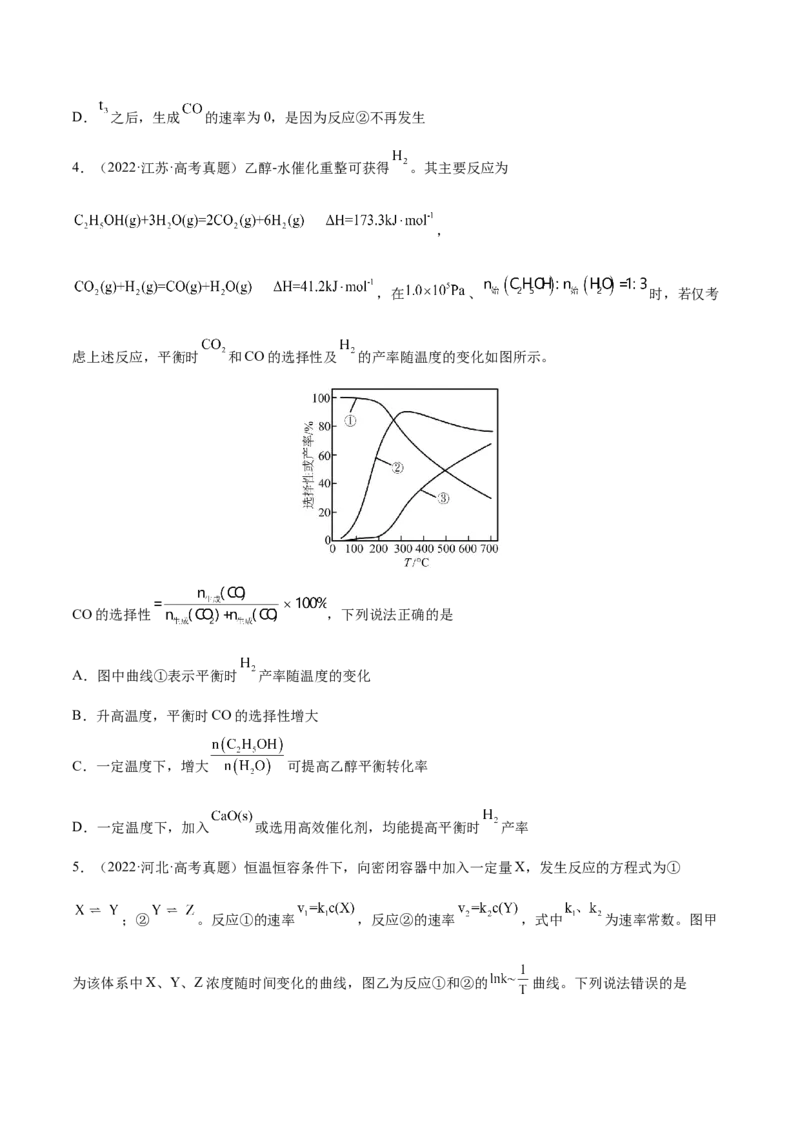
3.(2022·北京·高考真题) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完
成之后,以 为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组
分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A.反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率D. 之后,生成 的速率为0,是因为反应②不再发生
4.(2022·江苏·高考真题)乙醇-水催化重整可获得 。其主要反应为
,
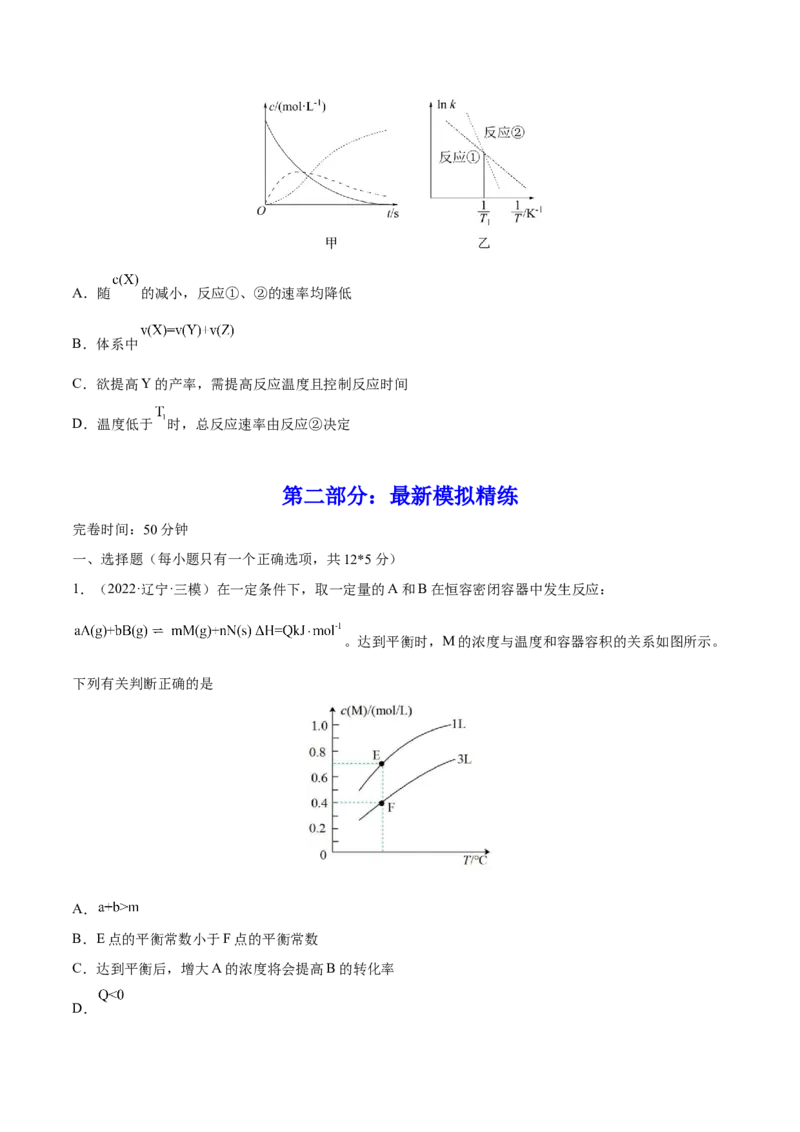
,在 、 时,若仅考
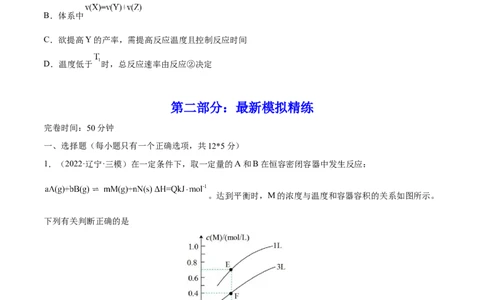
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
5.(2022·河北·高考真题)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①
;② 。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲
为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于 时,总反应速率由反应②决定
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
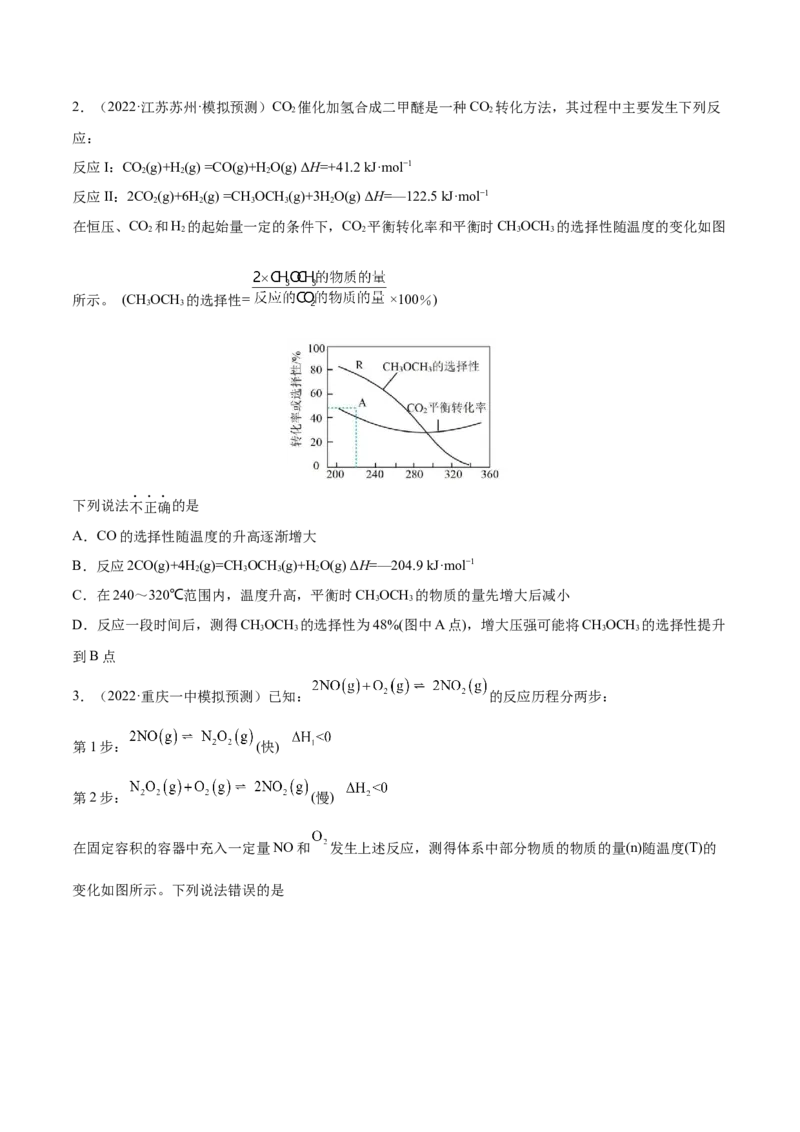
1.(2022·辽宁·三模)在一定条件下,取一定量的A和B在恒容密闭容器中发生反应:
。达到平衡时,M的浓度与温度和容器容积的关系如图所示。
下列有关判断正确的是
A.
B.E点的平衡常数小于F点的平衡常数
C.达到平衡后,增大A的浓度将会提高B的转化率
D.2.(2022·江苏苏州·模拟预测)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下列反
2 2
应:
反应I:CO(g)+H(g) =CO(g)+H O(g) ΔH=+41.2 kJ·mol−1
2 2 2
反应II:2CO(g)+6H(g) =CH OCH (g)+3HO(g) ΔH=—122.5 kJ·mol−1
2 2 3 3 2
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CHOCH 的选择性随温度的变化如图
2 2 2 3 3
所示。 (CHOCH 的选择性= ×100%)
3 3
下列说法不正确的是
A.CO的选择性随温度的升高逐渐增大
B.反应2CO(g)+4H(g)=CH OCH (g)+HO(g) ΔH=—204.9 kJ·mol−1
2 3 3 2
C.在240~320℃范围内,温度升高,平衡时CHOCH 的物质的量先增大后减小
3 3
D.反应一段时间后,测得CHOCH 的选择性为48%(图中A点),增大压强可能将CHOCH 的选择性提升
3 3 3 3
到B点
3.(2022·重庆一中模拟预测)已知: 的反应历程分两步:
第1步: (快)
第2步: (慢)
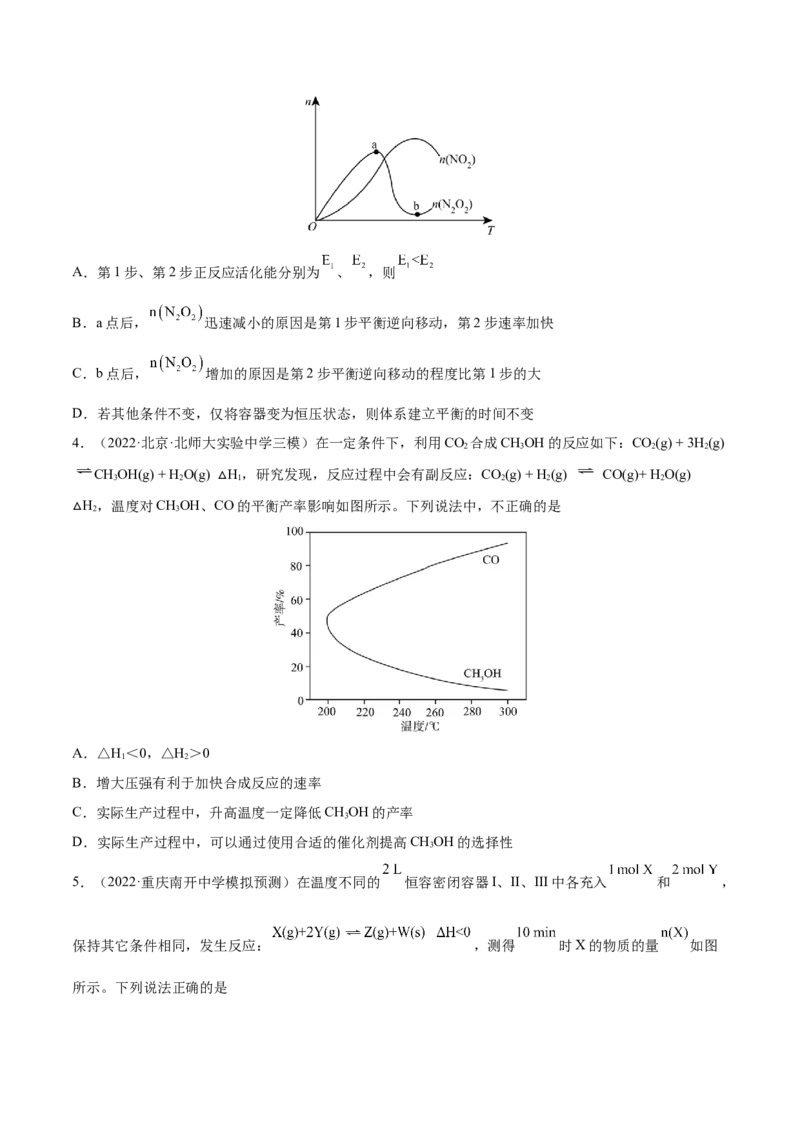
在固定容积的容器中充入一定量NO和 发生上述反应,测得体系中部分物质的物质的量(n)随温度(T)的
变化如图所示。下列说法错误的是A.第1步、第2步正反应活化能分别为 、 ,则
B.a点后, 迅速减小的原因是第1步平衡逆向移动,第2步速率加快
C.b点后, 增加的原因是第2步平衡逆向移动的程度比第1步的大
D.若其他条件不变,仅将容器变为恒压状态,则体系建立平衡的时间不变
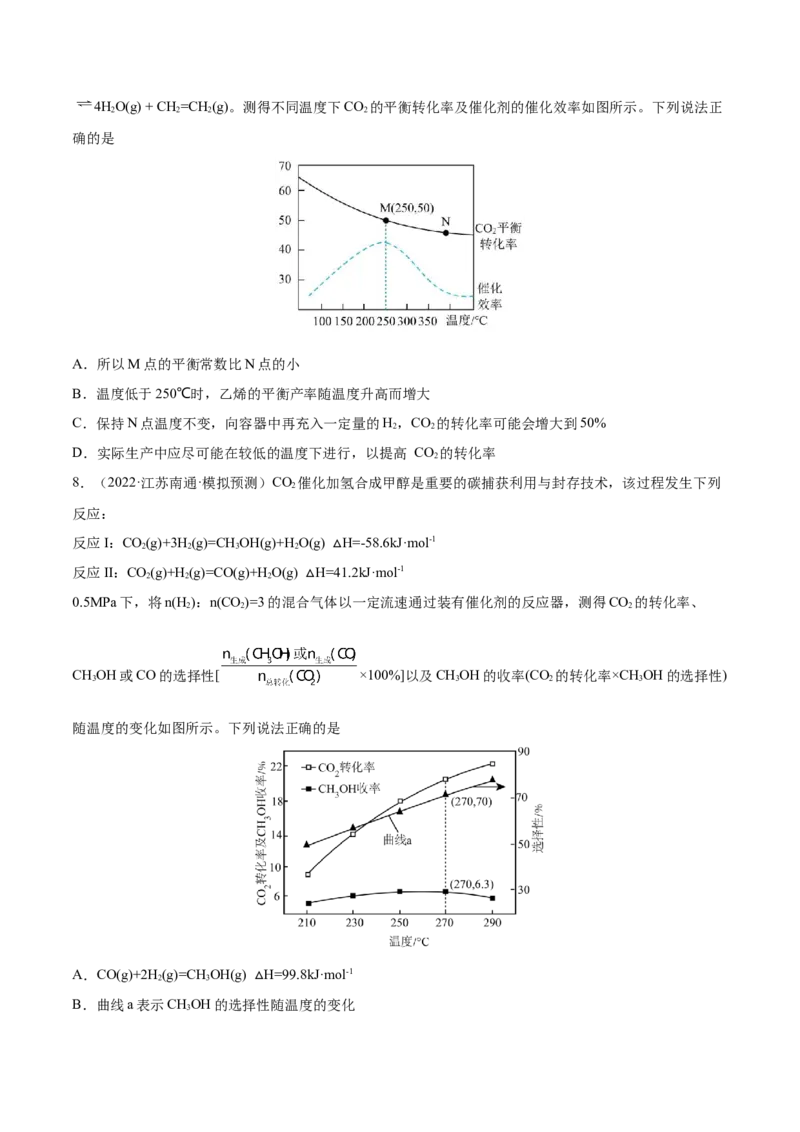
4.(2022·北京·北师大实验中学三模)在一定条件下,利用CO 合成CHOH的反应如下:CO(g) + 3H(g)
2 3 2 2
CHOH(g) + H O(g) H,研究发现,反应过程中会有副反应:CO(g) + H(g) CO(g)+ H O(g)
3 2 1 2 2 2
H,温度对CHOH、C△O的平衡产率影响如图所示。下列说法中,不正确的是
2 3
△
A.△H<0,△H>0
1 2
B.增大压强有利于加快合成反应的速率
C.实际生产过程中,升高温度一定降低CHOH的产率
3
D.实际生产过程中,可以通过使用合适的催化剂提高CHOH的选择性
3
5.(2022·重庆南开中学模拟预测)在温度不同的 恒容密闭容器I、II、III中各充入 和 ,
保持其它条件相同,发生反应: ,测得 时X的物质的量 如图
所示。下列说法正确的是A.逆反应速率:
B.b点一定满足:
C.再向容器III中充入 和 的转化率不变
D.从容器III中移走 的体积分数减小
6.(2022·江苏泰州·模拟预测)CH—CO 重整反应能够有效去除大气中 CO,是实现“碳中和”的重要
4 2 2
途径之一,发生的反应如下:
重整反应 CH(g)+CO (g)=2CO(g)+2H(g) ΔH
4 2 2
积炭反应Ⅰ 2CO(g)=CO(g)+C(s) ΔH =―172 kJ·mol-1
2 1
积炭反应Ⅱ CH(g)=C(s)+2H (g) ΔH =+75kJ·mol-1
4 2 2
在恒压、起始投料比 =1条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。
下列说法正确的是
A.重整反应的反应热ΔH=-247 kJ·mol-1
B.曲线B表示CH 平衡时物质的量随温度的变化
4
C.积炭会导致催化剂失活,降低CH 的平衡转化率
4
D.低于600℃时,降低温度有利于减少积炭的量并去除CO 气体
2
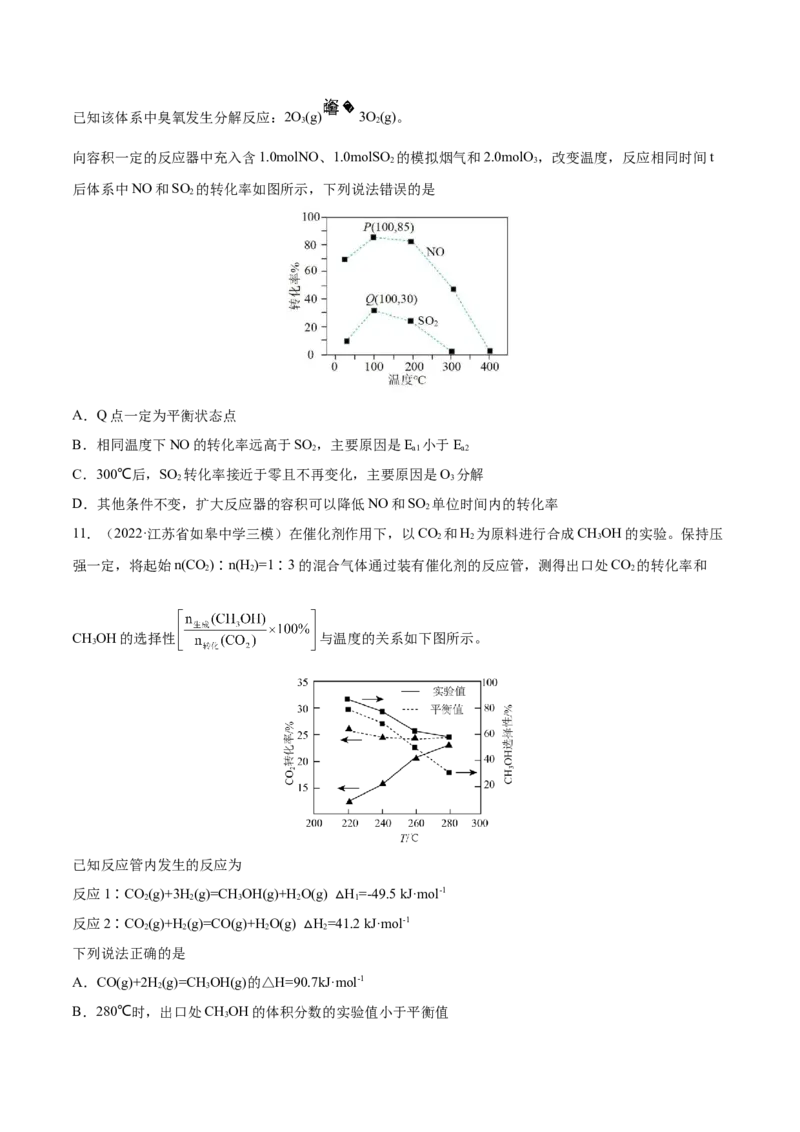
7.(2022·上海奉贤·二模)向恒容密闭容器中充入体积比为1:3的CO 和H,发生反应2CO(g) + 6H(g)
2 2 2 24HO(g) + CH =CH (g)。测得不同温度下CO 的平衡转化率及催化剂的催化效率如图所示。下列说法正
2 2 2 2
确的是
A.所以M点的平衡常数比N点的小
B.温度低于250℃时,乙烯的平衡产率随温度升高而增大
C.保持N点温度不变,向容器中再充入一定量的H,CO 的转化率可能会增大到50%
2 2
D.实际生产中应尽可能在较低的温度下进行,以提高 CO 的转化率
2
8.(2022·江苏南通·模拟预测)CO 催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程发生下列
2
反应:
反应I:CO(g)+3H(g)=CH OH(g)+H O(g) H=-58.6kJ·mol-1
2 2 3 2
反应II:CO
2
(g)+H
2
(g)=CO(g)+H
2
O(g) H=△41.2kJ·mol-1
0.5MPa下,将n(H
2
):n(CO
2
)=3的混合△气体以一定流速通过装有催化剂的反应器,测得CO
2
的转化率、
CHOH或CO的选择性[ ×100%]以及CHOH的收率(CO 的转化率×CH OH的选择性)
3 3 2 3
随温度的变化如图所示。下列说法正确的是
A.CO(g)+2H(g)=CH OH(g) H=99.8kJ·mol-1
2 3
B.曲线a表示CH
3
OH的选择△性随温度的变化C.图中所示270℃时,对应CO 的转化率为21%
2
D.在210℃~250℃之间,CHOH的收率增大是由于CHOH的选择性增大导致
3 3
9.(2022·江苏·模拟预测)二氧化碳催化加氢制甲醇是一种实现“碳中和”的有效方法。在 和 催
化制甲醇反应体系中,主要发生的反应的热化学方程式为
反应I:
反应II:
将1mol 和3mol 混和气体通入恒压、密闭容器中,在 的催化下反应,平衡时 转
化率、 和CO选择率随温度变化如图所示(选择率:转化的 中生成 或CO的百分比)。下
列说法错误的是
A. 选择率对应的曲线是b
B.
C.图中M点时, 的平衡转化率为25%,则 的转化率为33.3%
D.提高 转化为 的转化率,需要研发在低温区高效的催化剂
10.(2022·江苏·启东中学模拟预测)某科研小组研究臭氧脱除SO 和NO工艺,反应原理及反应热、活化
2
能数据如下:
反应I:NO(g)+O (g) NO (g)+O(g) H=-200.9kJ·mol-1 E =+3.2kJ·mol-1
3 2 2 1 a1
△
反应II:SO (g)+O(g) SO (g)+O(g) H=-241.6kJ·mol-1 E =+58kJ·mol-1
2 3 3 2 2 a2
△已知该体系中臭氧发生分解反应:2O(g) 3O(g)。
3 2
向容积一定的反应器中充入含1.0molNO、1.0molSO 的模拟烟气和2.0molO,改变温度,反应相同时间t
2 3
后体系中NO和SO 的转化率如图所示,下列说法错误的是
2
A.Q点一定为平衡状态点
B.相同温度下NO的转化率远高于SO ,主要原因是E 小于E
2 a1 a2
C.300℃后,SO 转化率接近于零且不再变化,主要原因是O 分解
2 3
D.其他条件不变,扩大反应器的容积可以降低NO和SO 单位时间内的转化率
2
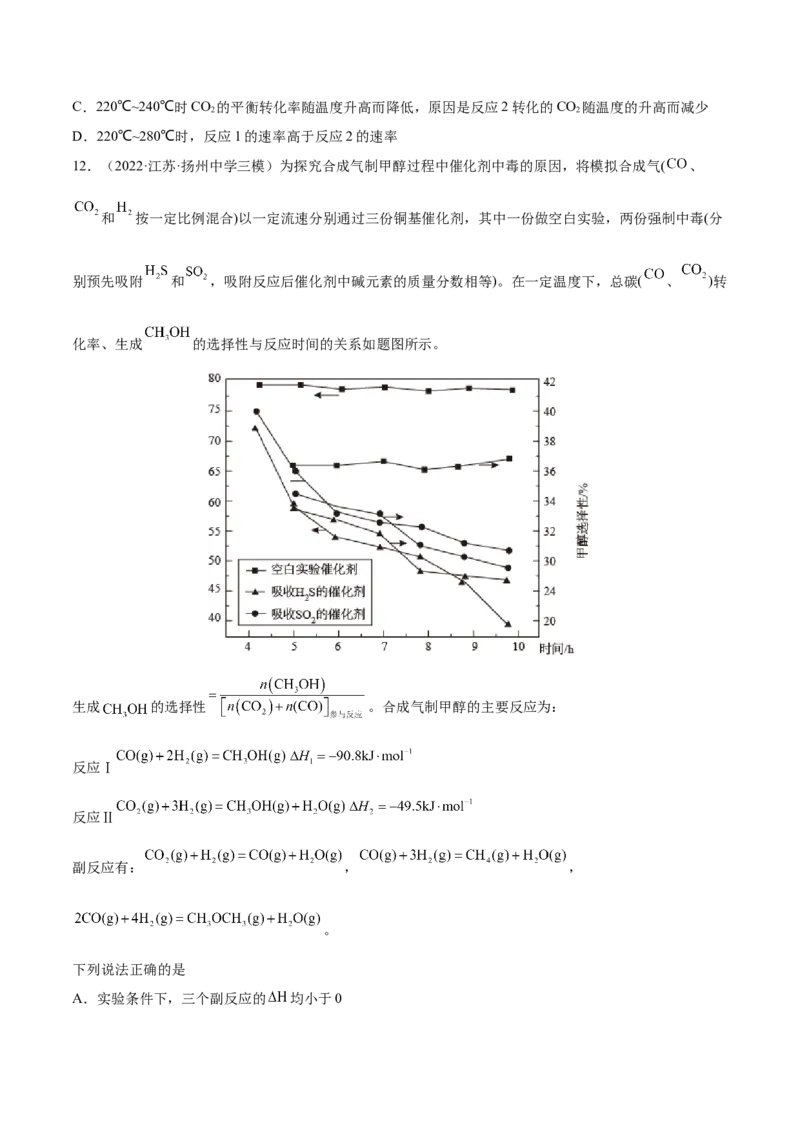
11.(2022·江苏省如皋中学三模)在催化剂作用下,以CO 和H 为原料进行合成CHOH的实验。保持压
2 2 3
强一定,将起始n(CO)∶n(H )=1∶3的混合气体通过装有催化剂的反应管,测得出口处CO 的转化率和
2 2 2
CHOH的选择性 与温度的关系如下图所示。
3
已知反应管内发生的反应为
反应1∶CO(g)+3H(g)=CH OH(g)+H O(g) H=-49.5 kJ·mol-1
2 2 3 2 1
反应2∶CO
2
(g)+H
2
(g)=CO(g)+H
2
O(g) H
2
=△41.2 kJ·mol-1
下列说法正确的是 △
A.CO(g)+2H(g)=CH OH(g)的△H=90.7kJ·mol-1
2 3
B.280℃时,出口处CHOH的体积分数的实验值小于平衡值
3C.220℃~240℃时CO 的平衡转化率随温度升高而降低,原因是反应2转化的CO 随温度的升高而减少
2 2
D.220℃~280℃时,反应1的速率高于反应2的速率
12.(2022·江苏·扬州中学三模)为探究合成气制甲醇过程中催化剂中毒的原因,将模拟合成气( 、
和 按一定比例混合)以一定流速分别通过三份铜基催化剂,其中一份做空白实验,两份强制中毒(分
别预先吸附 和 ,吸附反应后催化剂中碱元素的质量分数相等)。在一定温度下,总碳( 、 )转
化率、生成 的选择性与反应时间的关系如题图所示。
生成 的选择性 。合成气制甲醇的主要反应为:
反应Ⅰ
反应Ⅱ
副反应有: , ,
。
下列说法正确的是
A.实验条件下,三个副反应的 均小于0B.空白实验时,若其他条件不变,升高温度,总碳转化率一定减小
C.相同条件下, 对催化剂的毒害作用大于
D.为提高生成 的选择性,可研发不与含硫物反应的催化剂
二、主观题(共3小题,共40分)
13.(2022·上海杨浦·一模)(12分)氧硫化碳( ),用于合成除草剂、杀虫剂等,还能作为粮食熏蒸
剂。完成下列填空:
、 分别与 反应均能制得 ,反应如下:
反应Ⅰ:
反应Ⅱ:
已知:在相同条件下,
向两个容积相同的密闭容器中按下表投料( 不参与反应),分别发生上述反应。
反应Ⅰ 反应Ⅱ
起始投料
起始物质的量( ) 1 1 3 1 1 3
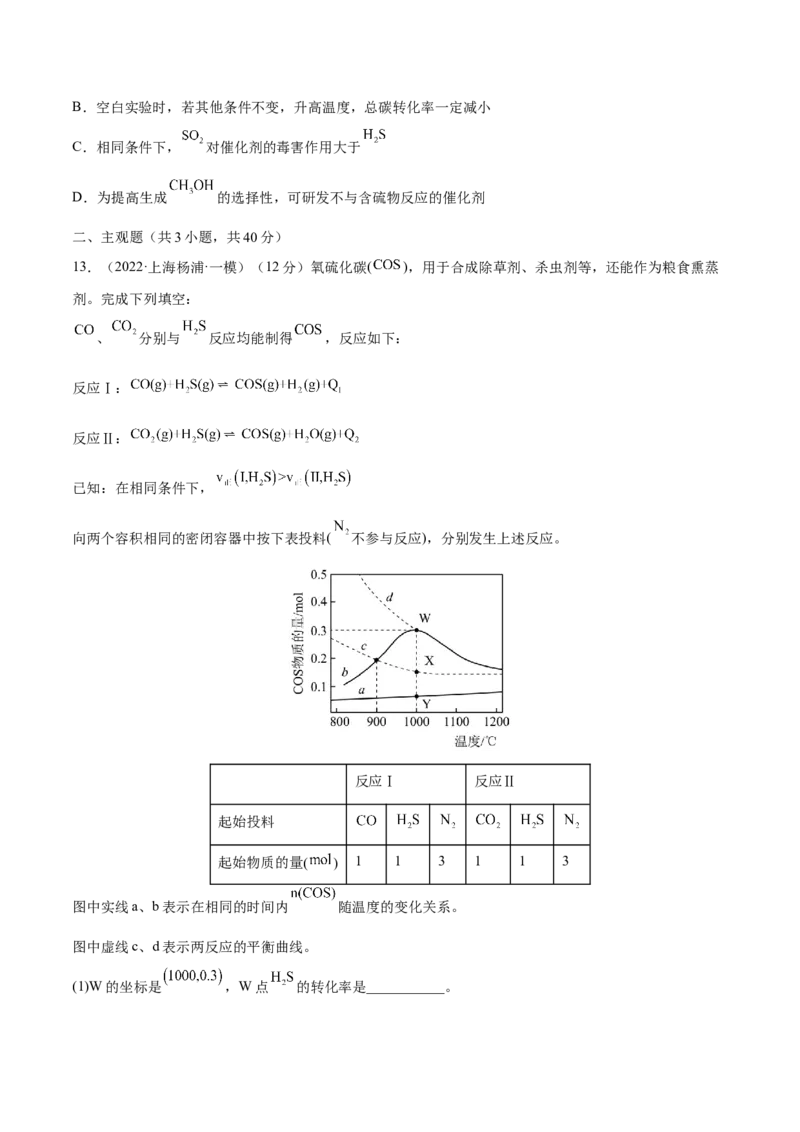
图中实线a、b表示在相同的时间内 随温度的变化关系。
图中虚线c、d表示两反应的平衡曲线。
(1)W的坐标是 ,W点 的转化率是___________。(2)a是反应___________(填“Ⅰ”或“Ⅱ”)的 随温度的变化关系,依据是:___________。
(3) ___________0(填“>”或“<”),理由是:___________。
(4)下列结论正确的是___________(选填选项)。A.曲线d为反应I的平衡曲线
B. 时,平衡常数
C.相同条件下,延长反应时间也不能使反应体系中Y点 的量达到W点
D.恒温恒容下,向W点表示的反应体系中增大 ,能提高 的转化率
14.(2022·浙江·模拟预测)(14分) 在工业生产中具有重要作用。
(1)
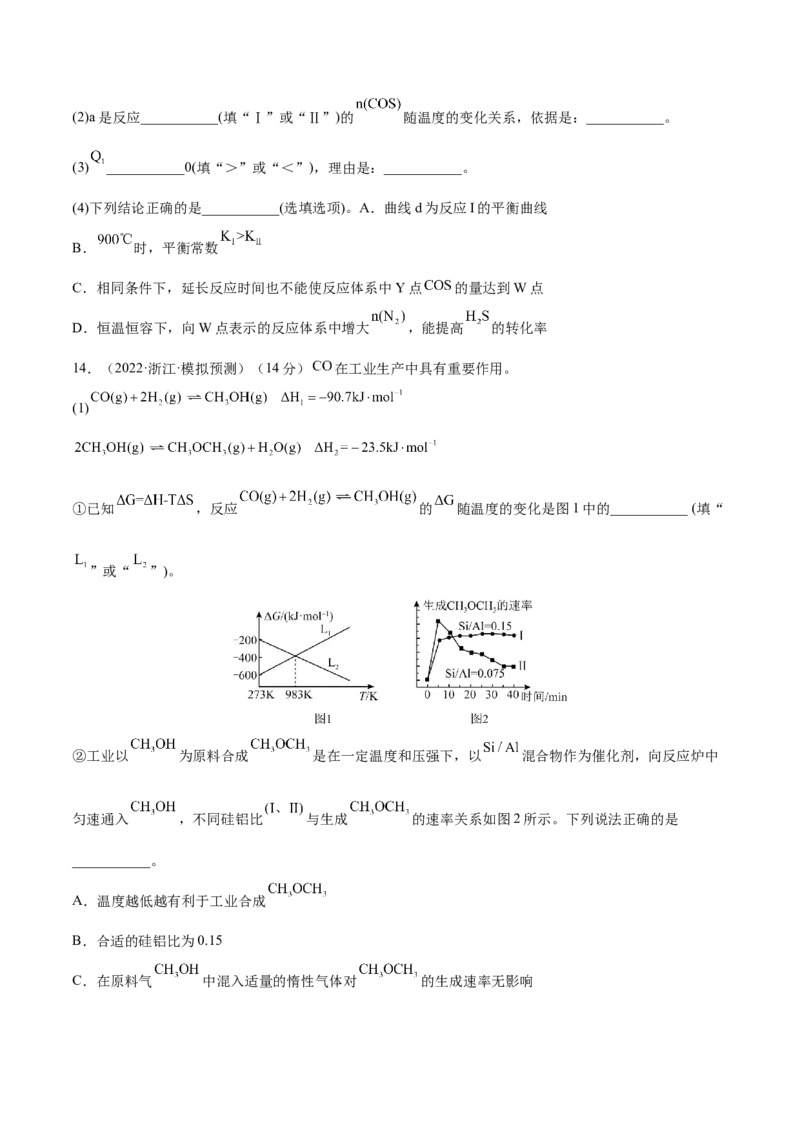
①已知 ,反应 的 随温度的变化是图1中的___________ (填“
”或“ ”)。
②工业以 为原料合成 是在一定温度和压强下,以 混合物作为催化剂,向反应炉中
匀速通入 ,不同硅铝比 与生成 的速率关系如图2所示。下列说法正确的是
___________。
A.温度越低越有利于工业合成
B.合适的硅铝比为0.15
C.在原料气 中混入适量的惰性气体对 的生成速率无影响D. 内, 的产量
(2)已知在催化剂M作用下, 。
①一定温度下,假设正逆反应速率与浓度关系为 只与
温度相关,则反应的平衡常数 ___________(用含 的式子表示)。
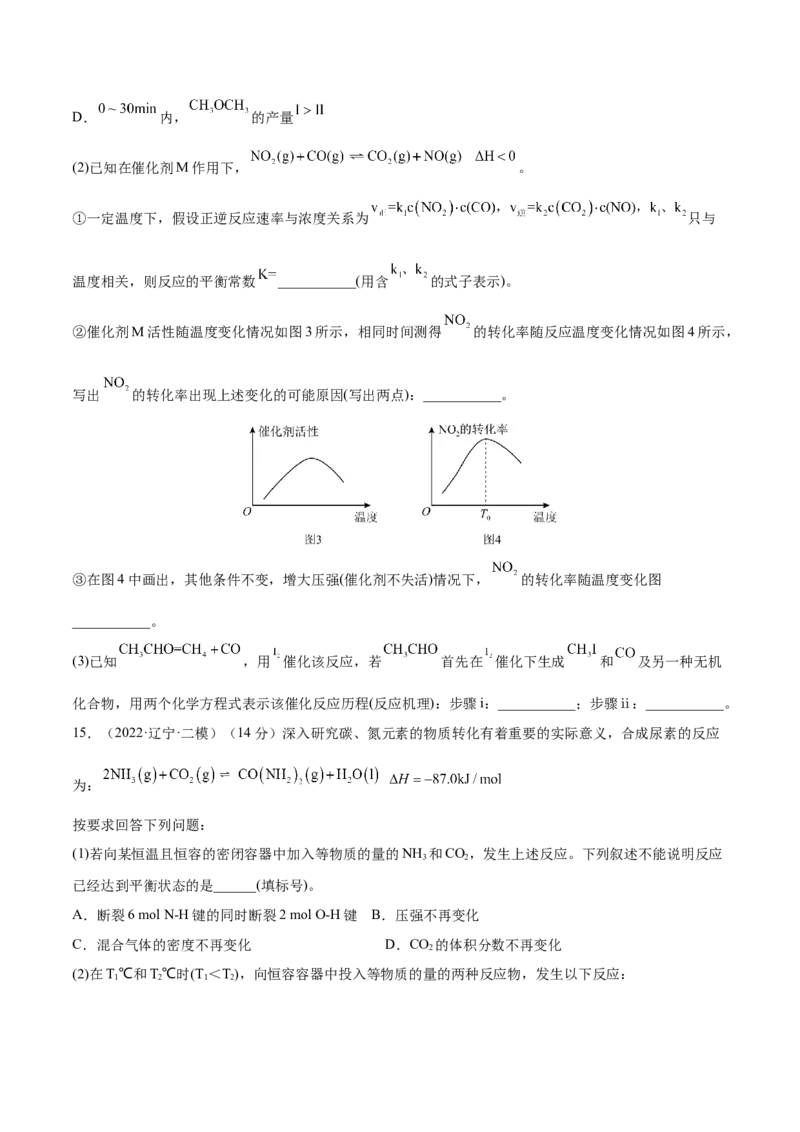
②催化剂M活性随温度变化情况如图3所示,相同时间测得 的转化率随反应温度变化情况如图4所示,
写出 的转化率出现上述变化的可能原因(写出两点):___________。
③在图4中画出,其他条件不变,增大压强(催化剂不失活)情况下, 的转化率随温度变化图
___________。
(3)已知 ,用 催化该反应,若 首先在 催化下生成 和 及另一种无机
化合物,用两个化学方程式表示该催化反应历程(反应机理):步骤i:___________;步骤ⅱ:___________。
15.(2022·辽宁·二模)(14分)深入研究碳、氮元素的物质转化有着重要的实际意义,合成尿素的反应
为:
按要求回答下列问题:
(1)若向某恒温且恒容的密闭容器中加入等物质的量的NH 和CO,发生上述反应。下列叙述不能说明反应
3 2
已经达到平衡状态的是______(填标号)。
A.断裂6 mol N-H键的同时断裂2 mol O-H键 B.压强不再变化
C.混合气体的密度不再变化 D.CO 的体积分数不再变化
2
(2)在T℃和T℃时(T <T),向恒容容器中投入等物质的量的两种反应物,发生以下反应:
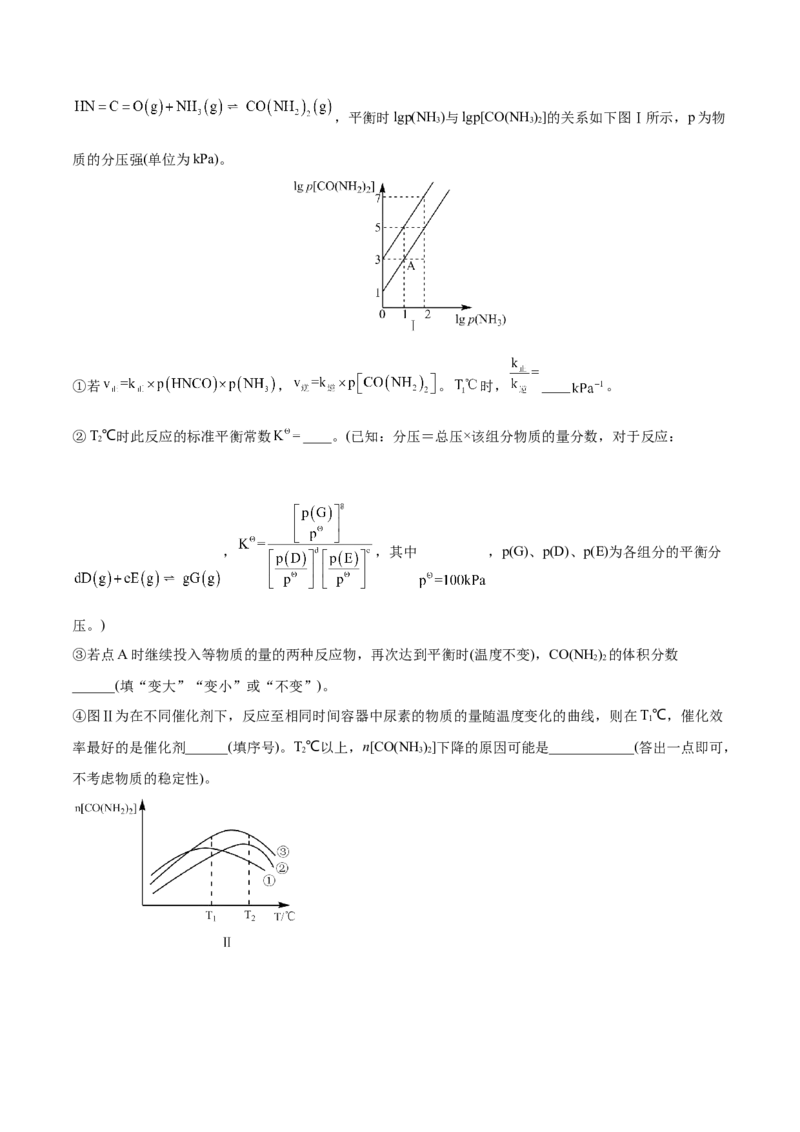
1 2 1 2,平衡时lgp(NH )与lgp[CO(NH )]的关系如下图Ⅰ所示,p为物
3 3 2
质的分压强(单位为kPa)。
①若 , 。 时, ____ 。
②T℃时此反应的标准平衡常数 ____。(已知:分压=总压×该组分物质的量分数,对于反应:
2
, ,其中 ,p(G)、p(D)、p(E)为各组分的平衡分
压。)
③若点A时继续投入等物质的量的两种反应物,再次达到平衡时(温度不变),CO(NH) 的体积分数
2 2
______(填“变大”“变小”或“不变”)。
④图Ⅱ为在不同催化剂下,反应至相同时间容器中尿素的物质的量随温度变化的曲线,则在T℃,催化效
1
率最好的是催化剂______(填序号)。T℃以上,n[CO(NH)]下降的原因可能是____________(答出一点即可,
2 3 2
不考虑物质的稳定性)。