文档内容
专题讲座(六) 隔膜在电化学的作用
第一部分:高考真题感悟
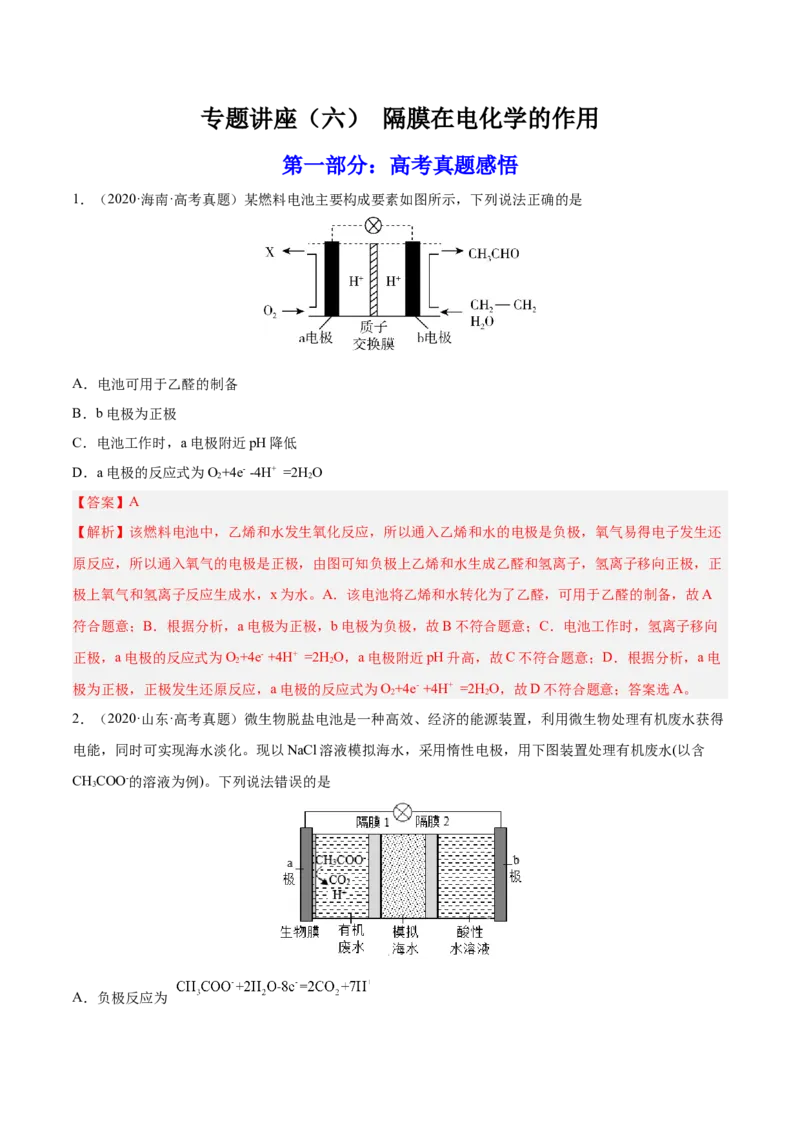
1.(2020·海南·高考真题)某燃料电池主要构成要素如图所示,下列说法正确的是
A.电池可用于乙醛的制备
B.b电极为正极
C.电池工作时,a电极附近pH降低
D.a电极的反应式为O+4e- -4H+ =2H O
2 2
【答案】A
【解析】该燃料电池中,乙烯和水发生氧化反应,所以通入乙烯和水的电极是负极,氧气易得电子发生还
原反应,所以通入氧气的电极是正极,由图可知负极上乙烯和水生成乙醛和氢离子,氢离子移向正极,正
极上氧气和氢离子反应生成水,x为水。A.该电池将乙烯和水转化为了乙醛,可用于乙醛的制备,故A
符合题意;B.根据分析,a电极为正极,b电极为负极,故B不符合题意;C.电池工作时,氢离子移向
正极,a电极的反应式为O+4e- +4H+ =2H O,a电极附近pH升高,故C不符合题意;D.根据分析,a电
2 2
极为正极,正极发生还原反应,a电极的反应式为O+4e- +4H+ =2H O,故D不符合题意;答案选A。
2 2
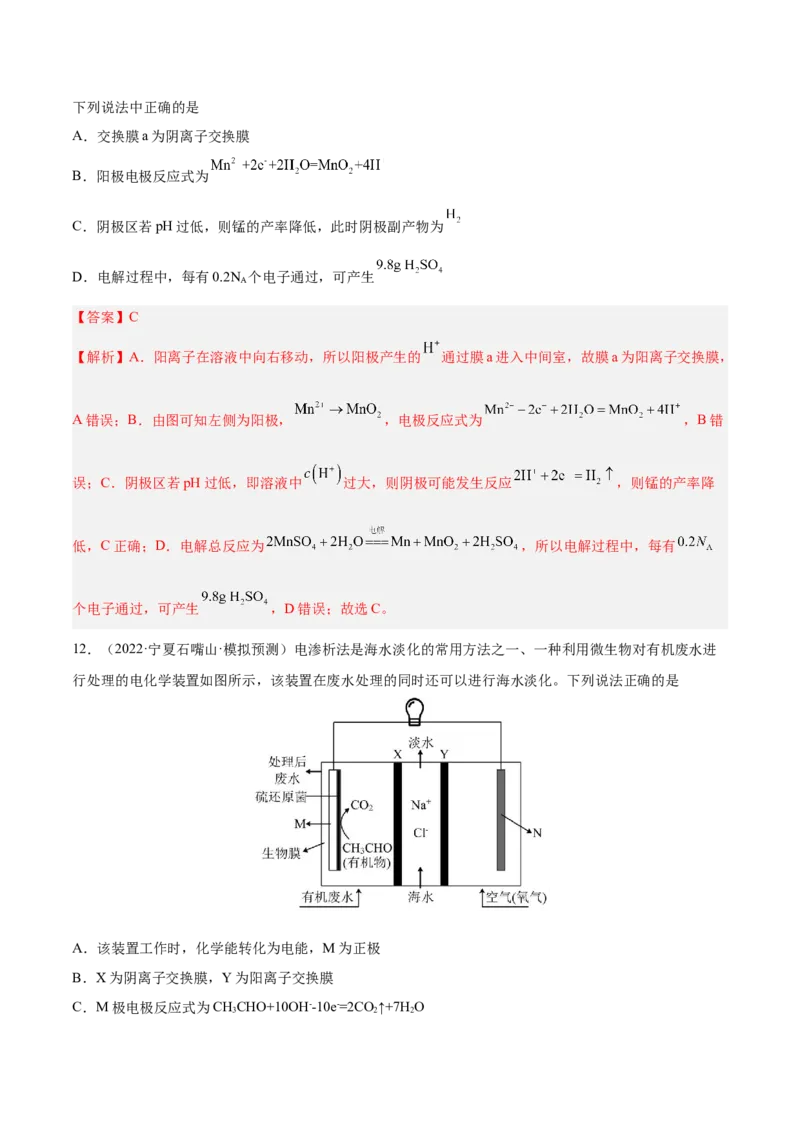
2.(2020·山东·高考真题)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得
电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含
CHCOO-的溶液为例)。下列说法错误的是
3
A.负极反应为B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
【答案】B
【解析】据图可知a极上CHCOOˉ转化为CO 和H+,C元素被氧化,所以a极为该原电池的负极,则b极
3 2
为正极。A.a极为负极,CHCOOˉ失电子被氧化成CO 和H+,结合电荷守恒可得电极反应式为
3 2
CHCOOˉ+2H O-8eˉ=2CO↑+7H+,故A正确;B.为了实现海水的淡化,模拟海水中的氯离子需要移向负
3 2 2
极,即a极,则隔膜1为阴离子交换膜,钠离子需要移向正极,即b极,则隔膜2为阳离子交换膜,故B
错误;C.当电路中转移1mol电子时,根据电荷守恒可知,海水中会有1molClˉ移向负极,同时有
1molNa+移向正极,即除去1molNaCl,质量为58.5g,故C正确;D.b极为正极,水溶液为酸性,所以氢
离子得电子产生氢气,电极反应式为2H++2eˉ=H↑,所以当转移8mol电子时,正极产生4mol气体,根据
2
负极反应式可知负极产生2mol气体,物质的量之比为4:2=2:1,故D正确;故答案为B。
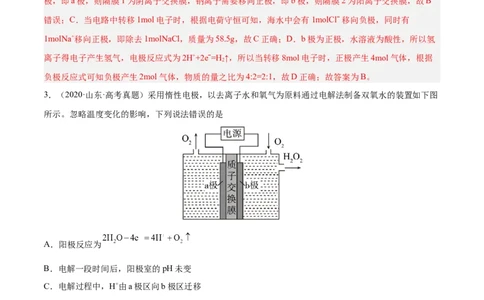
3.(2020·山东·高考真题)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图
所示。忽略温度变化的影响,下列说法错误的是
A.阳极反应为
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
【答案】D
【解析】a极析出氧气,氧元素的化合价升高,做电解池的阳极,b极通入氧气,生成过氧化氢,氧元素的
化合价降低,被还原,做电解池的阴极。A.依据分析a极是阳极,属于放氧生酸性型的电解,所以阳极的
反应式是2HO-4e-=4H++O ↑,故A正确,但不符合题意;B.电解时阳极产生氢离子,氢离子是阳离子,通
2 2
过质子交换膜移向阴极,所以电解一段时间后,阳极室的pH值不变,故B正确,但不符合题意;C.有B
的分析可知,C正确,但不符合题意;D.电解时,阳极的反应为:2HO-4e-=4H++O ↑,阴极的反应为:
2 2O+2e-+2H+=H O,总反应为:O+2H O=2HO,要消耗氧气,即是a极生成的氧气小于b极消耗的氧气,
2 2 2 2 2 2 2
故D错误,符合题意;故选:D。
4.(2021·天津·高考真题)如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列
2 2 3
判断错误的是
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当 完全溶解时,至少产生气体336mL (折合成标准状况下)
【答案】C
【解析】通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,说明石墨电极Ⅱ为阳极,则电源b为正极,a为
2 2 3
负极,石墨电极Ⅰ为阴极。A.由分析可知,a是电源的负极,故A正确;B.石墨电极Ⅱ为阳极,通电一
段时间后,产生氧气和氢离子,所以向石墨电极Ⅱ附近滴加石蕊溶液,出现红色,故B正确;C.随着电
解的进行,铜离子在阴极得电子生成铜单质,所以CuCl 溶液浓度变小,故C错误;D.当
2
完全溶解时,消耗氢离子为0.06mol,根据阳极电极反应式 ,产生氧气为0.015mol,
体积为336mL (折合成标准状况下),故D正确;故选C。
5.(2022·山东·高考真题)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生
成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
【答案】BD
【解析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池。
A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,同时生成H+,电极反应式为
2
CHCOO--8 e-+2 H O =2CO ↑+7 H+,H+通过阳膜进入阴极室,甲室的电极反应式为Co2++2e-=Co,因此,甲
3 2 2
室溶液pH逐渐减小,A错误;B.对于乙室,正极上LiCoO 得到电子,被还原为C o2+,同时得到Li+,
2
其中的O2-与溶液中的H+结合HO,电极反应式为2LiCoO +2e-+8H+=2Li++2Co2++4H O,负极发生的反应为
2 2 2
CHCOO--8 e-+2 H O =2CO ↑+7 H+,负极产生的H+通过阳膜进入正极室,但是乙室的H+浓度仍然是减小的,
3 2 2
因此电池工作一段时间后应该补充盐酸,B正确;C.电解质溶液为酸性,不可能大量存在OH-,乙室电极
反应式为:LiCoO +4H+=Li++Co2++2H O,C错误;D.若甲室Co2+减少200 mg,则电子转移物质的量为
2 2
n(e-)= ;若乙室Co2+增加300 mg,则转移电子的物质的量为n(e-)=
,由于电子转移的物质的量不等,说明此时已进行过溶液转移,即将乙室部分溶液
转移至甲室,D正确;故合理选项是BD。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)1.(2022·广西柳州·模拟预测)科学家近年发明了一种新型 水介质电池。电池示意图如下,电极
为金属锌和选择性催化材料。放电时,温室气体 被转化为储氢物质甲酸等,为解决环境和能源问题提
供了一种新途径。下列说法正确的是
A.放电时,负极区pH升高
B.放电时,1mol 转化为HCOOH,转移的电子数为4mol
C.充电时,Zn电极连电源正极
D.充电时,产生22.4L(标准状况下) ,生成的Zn为130g
【答案】D
【解析】A.负极上Zn失电子,生成Zn2+,Zn2+结合OH-生成 ,消耗了溶液中的氢氧根离子,负
极区pH下降,A错误;B.放电时,正极反应为 ,1molCO 转化为HCOOH,
2
转移的电子数为2mol,B错误;C.充电时,Zn电极连接电源负极,阴极反应为
,C错误;D.充电时总反应式为
,生成1mol氧气的同时,生成Zn2mol,即生成的Zn为
130g,D正确;故答案选D。
2.(2022·广西玉林·一模)水是鱼类赖以生存的环境,较好的水质能减少鱼类疾病的发生,更有利于鱼类
的生长和生存。世界水产养殖协会网介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。下列说法正确的是
A.Y为电源的正极
B.阴极反应式为2 +10e-+12H+=N ↑+6H O
2 2
C.将该装置放置于高温下,可以提高其净化效率
D.若BOD为葡萄糖(C H O),则1mol葡萄糖被完全氧化时,理论上电极上流出22mole-
6 l2 6
【答案】B
【解析】从装置图中可知,X电极连接的电极上发生反应是微生物作用下BOD、HO生成CO,Y电极连
2 2
接电极上,微生物作用下,硝酸根离子生成了氮气,氮元素化合价降低,发生还原反应,为电解池的阴极,
则Y为负极,X为正极。A.Y电极连接电极上,微生物作用下,硝酸根离子生成了氮气,氮元素化合价
降低,发生还原反应,为电解池的阴极,则Y为电源的负极,故A错误;B.阴极是硝酸根离子生成了氮
气,氮元素化合价降低,发生还原反应,阴极反应式为2 +10e-+12H+=N ↑+6H O,故B正确;C.若该
2 2
装置在高温下进行,催化剂微生物被灭活,则净化效率将降低,故C错误;D.若BOD为葡萄糖
(C H O),则1mol葡萄糖被完全氧化时,碳元素化合价0价变化为+4价,理论上电极上流出电子的物质的
6 l2 6
量:4e-×6=24mol e-,故D错误;故选:B。
3.(2022·河南河南·二模)天津大学某科研团队利用电解原理,实现了两电极体系中甲酸和辛腈的高选择
性合成,其工作原理如下图所示。下列说法正确的是注:不考虑电极的副反应。
A.Ni P电极与直流电源的负极相连
2
B.通电一段时间后, In/In O 电极附近溶液的pH不变
2 3-x
C.工作时,每转移2mol电子阴极室和阳极室中溶液的质量变化相差46g
D.理论上整个反应过程的原子利用率为100%
【答案】D
【解析】有机反应中:加氧去氢为氧化,加氢去氧为还原,左侧In/In O 电极上是CO 加氢生成
2 3-x 2
HCOOH,发生还原反应,故该电极是电解池阴极,右侧Ni P电极上是CH(CH)NH 去氢生成
2 3 2 7 2
CH(CH)CN,发生氧化反应,故该电极是电解池阳极;A.根据分析,Ni P电极是阳极,所以所连直流电
3 2 6 2
源正极,A错误;B.通电一段时间后,In/In O 电极附近HCOOH浓度变高,其电离的H+变多,所以溶
2 3-x
液pH变小,B错误;C.阳极电极反应式为 ,阴极电极反应
式为 ,每转移2mol电子,根据电极反应式可以看到,阴极会有1molCO 进入结
2
合H+生成HCOOH,增加质量为44g,阳极会生成2molH+,且H+会通过阳离子交换膜转移至阴极区,阴极
区质量增加2g,阳极区质量减少2g,所以两极室质量差是48g,C错误;D.理论上,电路上每转移2mol
电子,阳极损失2molH+,H+全部转移至阴极区结合CO 生成HCOOH,没有任何材料浪费,所以原子利用
2
率为100%,D正确;综上,本题选D。
4.(2022·江西江西·模拟预测)我国学者开发了一种新型高效电解析氢(HER)催化剂,大幅降低了电解所
需的电压,同时可将 气体变废为宝。其工作原理如图所示,下列说法正确的是A.Y电极可选择铁
B.X的电极反应式为
C.吸收 的反应的离子方程式为
D.当回收32t硫时,理论上有 通过M由a流向b
【答案】C
【解析】根据图示,左侧氢离子得电子生成氢气,故左侧X为阴极,右侧Y为阳极,亚铁离子失去电子生
成铁离子,铁离子与HS发生氧化还原反应得到S。A.Y为电解池阳极,若选择铁作电极,则电极反应式
2
为 ,A错误;B.X的电极反应式为 ,B错误;C.吸收 反应的离子方
程式为 ,C正确;D.当回收32t硫时,S元素化合价由-2价升高为0价,转
移电子数为: ,故理论上有 通过M由b流向a,D错误;故选
C。
5.(2022·河南开封·一模)K-O 电池结构如图所示,a和b为两个电极,其中之一为单质钾。关于该电池,
2
下列说法错误的是A.正极反应式为O+2e—+K+=KO
2 2
B.隔膜允许K+通过,不允许O 通过
2
C.放电时,电流由b电极沿导线流向a电极
D.用此电池电解CuCl 溶液,理论上消耗3.9gK时,产生3.2gCu
2
【答案】A
【解析】由图可知,a电极为原电池的负极,钾失去电子发生氧化反应生成钾离子,电极反应式为K—e—
=K+,b电极为正极,氧气在钾离子作用下得到电子发生还原反应生成超氧化钾,电极反应式为O+e—
2
+K+=KO。A.由分析可知,b电极为正极,氧气在钾离子作用下得到电子发生还原反应生成超氧化钾,电
2
极反应式为O+e—+K+=KO,故A错误;B.钾是活泼金属,易与氧气反应,所以电池工作时,隔膜允许
2 2
钾离子通过,不允许氧气通过,故B正确;C.由分析可知,放电时,a电极为原电池的负极,b电极为正
极,电流由正极b电极沿导线流向负极a电极,故C正确;D.由得失电子数目守恒可知,用此电池电解
氯化铜溶液,理论上消耗3.9g钾时,阴极产生铜的质量为 × ×64g/mol=3.2g,故D正确;故选
A。
6.(2022·河南焦作·一模)磷酸铁锂(LiFePO )电池因特别适于作动力方面的应用,故称作磷酸铁锂动力电
4
池。磷酸铁锂电池的内部结构如图所示,充电时总反应是C +LiFePO =Li FePO +Li C ,下列说法中错
6 4 1-x 4 x 6
误的是A.LiFePO 作为电池的正极,与铝箔相连
4
B.聚合物隔膜将正、负极隔开,可使电子通过
C.放电时,正极反应式为Li FePO +xLi++xe- =LiFePO
1-x 4 4
D.放电时,Li+从负极移向正极
【答案】B
【解析】充电时总反应是C +LiFePO =Li FePO +Li C 放电时总反应是Li FePO +Li C = C
6 4 1-x 4 x 6, 1-x 4 x 6 6
+LiFePO ,负极反应式为:LiC -xe-= C +xLi+,正极反应式为Li FePO +xLi++xe- =LiFePO ;A.由图及
4 x 6 6 1-x 4 4
电极反应式分析可知,LiFePO 作为电池的正极,与铝箔相连,故A正确;B.电池放电时为原电池,负极
4
中的Li+通过聚合物隔膜向正极迁移,电子不能通过聚合物隔膜,故B错误;C.由电池总反应可知,正极上
Li FePO 得电子发生还原反应,所以正极电极反应式为Li FePO +xLi++xe- =LiFePO ,故C正确;D.磷酸
1-x 4 1-x 4 4
铁锂电池不含重金属和稀有金属,是一种安全无毒无污染的绿色环保电池,故D正确;故答案选B。
7.(2022·安徽池州·模拟预测)我国科学家最近研发出一种新型纳米硅锂电池,可反复充电3万次,电池
容量只衰减了不到10%。电池反应式为Li TiO+Li Si LiTiO +Si。下列说法错误的是
1-x 2 x 2A.电池放电时,Li+由N极移向M极
B.电池放电时,电池正极反应式为Li TiO+xLi++xe-=LiTiO
1-x 2 2
C.精制的饱和食盐水通入阳极室
D.负极质量减轻7g时,理论上最多可制得40gNaOH
【答案】A
【解析】电池反应式为Li TiO+Li Si LiTiO +Si,M极为负极,电极反应式为LiSi-xe-=xLi+
1-x 2 x 2 x
+Si,N极为正极,电极反应式Li TiO+xLi++xe-=LiTiO,电解池中,左侧为阳极,电极反应式为2Cl--2e-
1-x 2 2
=Cl↑,右侧电极为2HO+2e-=H ↑+2OH-。A. 电池放电时,阳离子向正极N移动,故A错误;B. 电池
2 2 2
放电时,N极为正极,电池正极反应式为Li TiO+xLi++xe-=LiTiO,故B正确;C. 电解池中左侧电极为
1-x 2 2
阳极,电极反应式为2Cl--2e-=Cl↑,故阳极室通入精制的饱和食盐水,故C正确;D. 负极质量减轻7g时,
2
转移电子 ×1=1mol,电解池中转移1mol电子生成1molNaOH,即生成1mol×40g/mol=40g,故D正
确;故选:A。
8.(2022·湖南·模拟预测)“四室电渗析法”可用来制备某些化工产品,原理如图所示,阳极室中电解质
溶液为稀硫酸,阴极室中电解质溶液为稀NaOH溶液。下列说法正确的是
A.阴极材料起导电作用,也可以换成铜、铁、铝锂等金属材料
B.若原料室加入浓NaI溶液,产品室每得到1 mol HI,阳极室溶液减少9 g
C.该装置的优点之一为电解后在阴极一定可以得到较浓的氢氧化钠溶液
D.若原料室加入浓NaH PO 溶液,阳极室电解质溶液用HPO 溶液代替稀硫酸,并撤去阳极室与产品室
2 2 3 2
间的阳膜,会更有利于制备HPO
3 2
【答案】B
【解析】由电池装置图可知,该电池为电解池,左侧石墨电极为阳极,水失去电子生成氧气和氢离子,右
侧石墨电极为阴极,水得到电子生成氢气和氢氧根离子。A.铝会和NaOH反应,锂会与水反应,不可以
作阴极,A项错误;B.阳极电极反应:2HO-4e-=O ↑+4H+,产品室得到1molHI,则有1mol氢离子通过阳
2 2膜转移到产品室,即阳极转移1mol电子,生成氧气8g同时转移氢离子1g,阳极室溶液减少9g,B项正确;
C.阴极要得到浓的氧氧化钠溶液,原料室加入的溶液必须为钠盐,C项错误;D.撤掉阳极与产品室的阳
膜,HPO 或HPO 在阳极可能会失电子被氧化成PO ,不利于制备HPO ,D项错误;故答案选B。
3 2 3 3 2
9.(2022·吉林吉林·模拟预测)利用如图HCOOH燃料电池装置,获得电能的同时还可以得到KHCO 、
3
KSO 。下列说法错误的是
2 4
A.通入O 的电极为电池正极
2
B.放电过程中需补充的物质X为HSO
2 4
C.负极电极反应式为HCOO-+2OH-_2e-=HCO +HO
2
D.每生成1 mol KHCO,有1 mol K+通过阳离子膜
3
【答案】D
【解析】A.燃料电池中燃料失电子作负极,氧气得电子作正极,A正确;B.由图示可知,放电过程中正
极有KSO 生成,因此需补充的物质X为HSO ,B正确;C.由图示可知,负极HCOOH失电子生成
2 4 2 4
HCO ,负极电极反应式为:HCOO-+2OH-_2e-=HCO +HO,C正确;D.每生成1 mol KHCO,转移
2 3
2mol电子,则有2 mol K+通过阳离子膜,D错误;答案选D。
10.(2022·陕西·西安中学模拟预测)乙醛酸是一种重要的化工中间体,可采用如下图所示的电化学装置
合成。图中的双极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法不
2
正确的是A.铅电极连接电源正极,发生氧化反应
B.阳极区,Br 是氧化剂,把乙二醛氧化成乙醛酸
2
C.双极膜中间层中的OH-在外电场作用下向石墨电极方向迁移
D.外电路中迁移2mol电子,理论上能制得2mol乙醛酸
【答案】A
【解析】A.乙二酸的分子式为C HO,乙醛酸的分子式为C HO,碳原子的化合价由乙二酸的+3价变为
2 2 4 2 2 3
乙醛酸的+2价,化合价降低得到电子发生还原反应,则铅电极与电源负极相连,为电解池的阴极,A项错
误;B.石墨电极为电解池的阳极,阳极失去电子化合价升高,乙二醛的分子式为C HO,碳原子的化合
2 2 2
价为+1价,则Br 是氧化剂把乙二醛氧化成乙醛酸,B项正确;C.阴离子向阳极移动,则氢氧根离子向石
2
墨电极移动,C项正确;D.阴极电极反应式为: ,阳极的电极反应式:
,整个电路中电荷守恒,外电路中迁移2mol电子,阳极上产生1mol
的乙醛酸,阴极上产生1mol的乙醛酸,理论上能制得2mol乙醛酸,D项正确;答案选A。
11.(2022·湖北·华中师大一附中模拟预测)利用硫酸锰溶液可通过离子交换膜组合工艺获得Mn、
、 ,原理如图所示:下列说法中正确的是
A.交换膜a为阴离子交换膜
B.阳极电极反应式为
C.阴极区若pH过低,则锰的产率降低,此时阴极副产物为
D.电解过程中,每有0.2N 个电子通过,可产生
A
【答案】C
【解析】A.阳离子在溶液中向右移动,所以阳极产生的 通过膜a进入中间室,故膜a为阳离子交换膜,
A错误;B.由图可知左侧为阳极, ,电极反应式为 ,B错
误;C.阴极区若pH过低,即溶液中 过大,则阴极可能发生反应 ,则锰的产率降
低,C正确;D.电解总反应为 ,所以电解过程中,每有
个电子通过,可产生 ,D错误;故选C。
12.(2022·宁夏石嘴山·模拟预测)电渗析法是海水淡化的常用方法之一、一种利用微生物对有机废水进
行处理的电化学装置如图所示,该装置在废水处理的同时还可以进行海水淡化。下列说法正确的是
A.该装置工作时,化学能转化为电能,M为正极
B.X为阴离子交换膜,Y为阳离子交换膜
C.M极电极反应式为CHCHO+10OH--10e-=2CO ↑+7H O
3 2 2D.当有1molNa+通过离子交换膜时,N极消耗的空气体积约为26.7L
【答案】B
【解析】A.由图可知,该装置为原电池,是将化学能转化为电能,电极N中氧气发生还原反应,作正极;
电极M甲醛发生氧化反应做负极;故A项错误;B.电极N中氧气发生还原反应,电极反应式为5O+20 e-
2
+10H O =20OH-,生成阴离子,故钠离子向N极移动,Y为阳离子交换膜,电极M甲醛发生氧化反应,电
2
极反应式为CHCHO+3H O-10e-=2CO ↑+10H+,X为阴离子交换膜,故B项正确;C.电极M甲醛发生氧
3 2 2
化反应,电极反应式为2CHCHO+6H O-20e-=4CO ↑+20H+,故C项错误;D.N电极反应式为5O+20 e-
3 2 2 2
+10H O =20OH-,当有20molNa+通过离子交换膜时,标准状况消耗氧气的体积为5 ;标准状况,
2
当有1molNa+通过离子交换膜时,N极消耗的空气体积约为5 ,选项无标准状况这一前提,
故D项错误。故答案选B。
二、主观题(共3小题,共40分)
13.(2020·河北·磁县第二中学模拟预测)(14分)钢铁工业是国家工业的基础,钢铁生锈现象却随处可
见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:_____________
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R
可以采用________。
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的__________极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如
图所示:①电镀装置图的“直流电源”中,______ 填“a”或“b” 是正极。Fe电极反应式为_________;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、
烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为________。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:______。
【答案】(1)O+2H O+4e-==4OH-
2 2
(2)C
(3)负
(4)①a Cu2++2e-=Cu ②0.08mol ③铁比铜活泼,铁与铜构成原电池的两个电极,铁作负极,更易
被腐蚀
【详解】(1)钢铁腐蚀的吸氧腐蚀,是金属吸收空气中的氧气发生的反应,正极得电子,化合价降低,
故吸氧腐蚀过程中的正极电极反应式为:O+2H O+4e-==4OH-;
2 2
(2)图①所示的方案为牺牲阳极的阴极保护法,故添加的物质应该比铁更活泼,但钠易与水发生剧烈反
应,不安全,故焊接在铁闸门上的固体材料R可以采用锌,答案选C;
(3)图②所示的方案是外加电源的阴极保护法,故铁闸门应该连接在直流电源的负极,做阴极,答案为:
负;
(4))①电镀时电源正极连接的电极为阳极,故a为正极;铁连接负极,故Fe电极发生的电极反应为:
Cu2++2e-=Cu;②阳极溶解的铜的质量等于阴极上析出的铜的质量,故阳极溶解的铜为2.56 g,即0.04
mol,故电镀过程中电路中通过的电子的物质的量为0.08 mol;③镀件镀层破损后,镀层金属与镀件金属在
周围环境中形成原电池,活泼性较强的金属更容易被腐蚀;故答案为:a;Cu2++2e-=Cu;0.08mol;铁比铜活
泼,铁与铜构成原电池的两个电极,铁作负极,更易被腐蚀。
14.(2021·北京·模拟预测)(12分)回答下列问题
(1)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用
下,阴、阳膜复合层间的HO解离成H+和OH-;AB为离子交换膜。
2①B膜最佳应选择___________。
②阳极的电极反应式是___________。
③少量的I-因浓度差通过BPM膜,若撤去A膜,其缺点是___________。
(2)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚(C HOH)废水更加高效,装置如
6 5
下图所示。已知a极主要发生的反应是O 生成HO,然后在电解液中产生·OH并迅速与苯酚反应。
2 2 2
①b极连接电源的___________极(填“正”或“负”)。
②a极的电极反应式为___________。
③除电极反应外,电解液中主要发生的反应方程式有___________。
【答案】(1)Na+交换膜 2HO-4e-=O ↑+4H+ I-会在阳极失电子得到碘单质,沉积在阳
2 2
极表面,损伤阳极板
(2)正 O+2e-+2H+=H O C HO+28·OH=6CO ↑+17HO
2 2 2 6 6 2 2
【解析】(1)①从图上看,右端的BPM膜和B膜之间产生NaOH,BPM膜提供OH-,B膜最好是Na+交换
膜;②阳极附近溶液为硫酸溶液,水电离出的氢氧根离子失电子,故阳极的电极反应式为2HO-4e-=O ↑
2 2
+4H+;③A膜应为阳离子交换膜,阳极产生的H+透过A膜和少量的I-反应得到少量的HI,若撤去A膜,
I-会在阳极失电子得到碘单质,沉积在阳极表面,损伤阳极板。
(2)①a极主要发生的反应是O 生成HO,O元素化合价降低、得到电子、发生还原反应,则a电极为阴极、
2 2 2
与电源负极相接,所以b电极为阳极、与电源正极相接;②a电极为阴极,O 得到电子生成HO,电解质
2 2 2
溶液显酸性,电极反应式为O+2e-+2H+=H O;③HO 分解产生·OH,化学方程式为HO=2·OH,·OH
2 2 2 2 2 2 2除去苯酚生成无毒的氧化物,该氧化物为CO,反应的化学方程式为C HO+28·OH=6CO ↑+17HO。
2 6 6 2 2
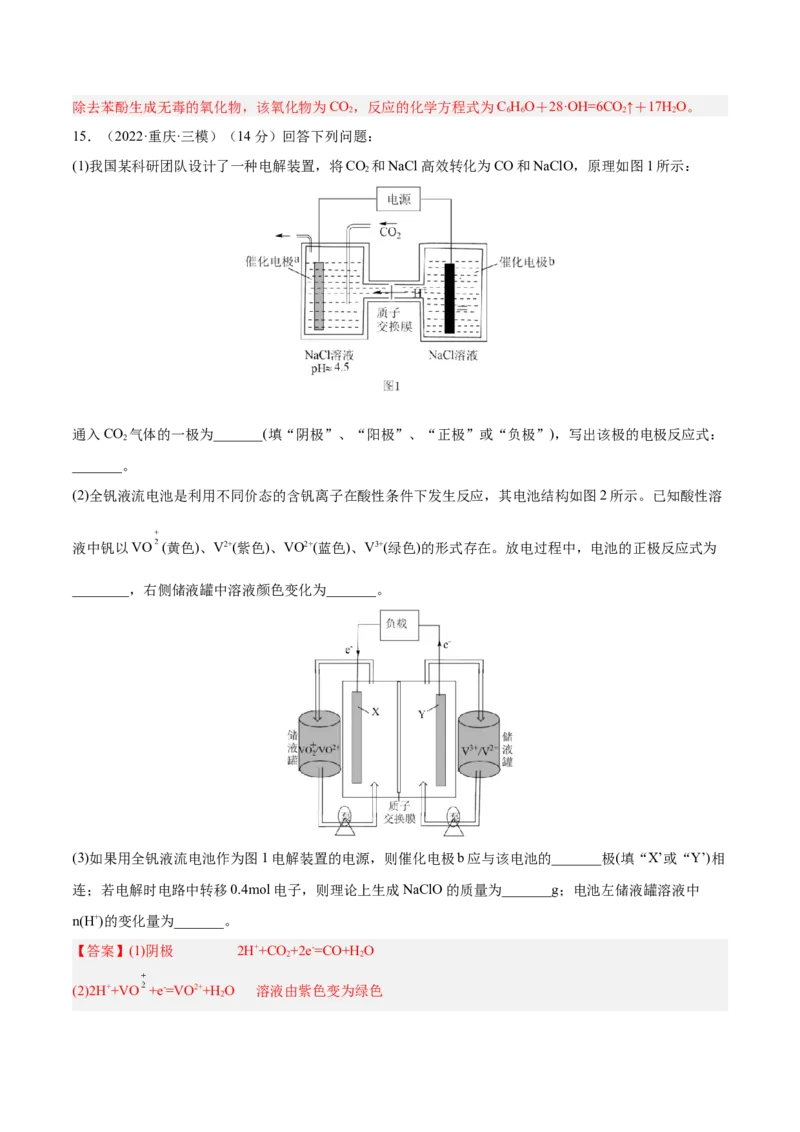
15.(2022·重庆·三模)(14分)回答下列问题:
(1)我国某科研团队设计了一种电解装置,将CO 和NaCl高效转化为CO和NaClO,原理如图1所示:
2
通入CO 气体的一极为_______(填“阴极”、“阳极”、“正极”或“负极”),写出该极的电极反应式:
2
_______。
(2)全钒液流电池是利用不同价态的含钒离子在酸性条件下发生反应,其电池结构如图2所示。已知酸性溶
液中钒以VO (黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
________,右侧储液罐中溶液颜色变化为_______。
(3)如果用全钒液流电池作为图1电解装置的电源,则催化电极b应与该电池的_______极(填“X’或“Y’)相
连;若电解时电路中转移0.4mol电子,则理论上生成NaClO的质量为_______g;电池左储液罐溶液中
n(H+)的变化量为_______。
【答案】(1)阴极 2H++CO +2e-=CO+H O
2 2
(2)2H++VO +e-=VO2++H O 溶液由紫色变为绿色
2(3)X 14.9 0.4mol
【解析】(1)该装置为电解池,CO→CO,碳元素化合价降低,发生还原反应,则通入CO 气体的一极为阴
2 2
极,电极反应式:2H++CO +2e-=CO+H O;
2 2
(2)由电子流入的一极为正极,则X为正极,放电时正极上反应式:2H++VO +e-=VO2++H O;放电过程中,
2
右罐为负极,反应式:V2+-e-═V3+,则溶液颜色逐渐由紫色变为绿色;
(3)图2是原电池,Y极电子流出,则Y为负极,X为正极,图1是电解池,催化电极b是阳极,由电解池
的阳极接原电池的正极,则催化电极b应与该电池的X极,催化电极b的电极反应式为:HO+Cl--2e-
2
=HClO+H+,电路中转移0.4mol电子,则理论上生成0.2mol NaClO,质量
为m=nM=0.2mol×74.5g/mol=14.9g,充电时,左槽正极上反应式:2H++VO +e-=VO2++H O,若转移电子
2
0.4mol,消耗氢离子为0.8mol,通过交换膜定向移动通过0.4mol电子,则左槽溶液中n(H+)的变化量为
0.8mol-0.4mol=0.4mol。