文档内容
专题讲座(十二) 晶胞参数、坐标参数的分析与应用
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 晶胞参数与晶体密度间的互算
高频考点2 原子空间利用率的计算
高频考点3 晶胞中原子坐标的确定
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
【知识梳理】
知识点一、常见晶体结构分析
1.常见原子晶体结构分析
晶体 晶体结构 结构分析
(1)每个C与相邻4个C以共价键结合,形成正四面体结构
(2)键角均为109°28′
金刚石 (3)最小碳环由6个C组成且6个C不在同一平面内
(4)每个C参与4个C—C键的形成,C原子数与C—C键数之比为1∶2
(5)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个Si与4个O以共价键结合,形成正四面体结构
(2)每个正四面体占有1个Si,4个“O”,因此二氧化硅晶体中Si与O的个
SiO
数比为1∶2
2
(3)最小环上有12个原子,即6个O,6个Si
(4)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
SiC、BP、 (1)每个原子与另外4个不同种类的原子形成正四面体结构
AlN
(2)密度:ρ(SiC)=;ρ(BP)=;ρ(AlN)=(a为晶胞边长,N 为阿伏加德罗
A常数)
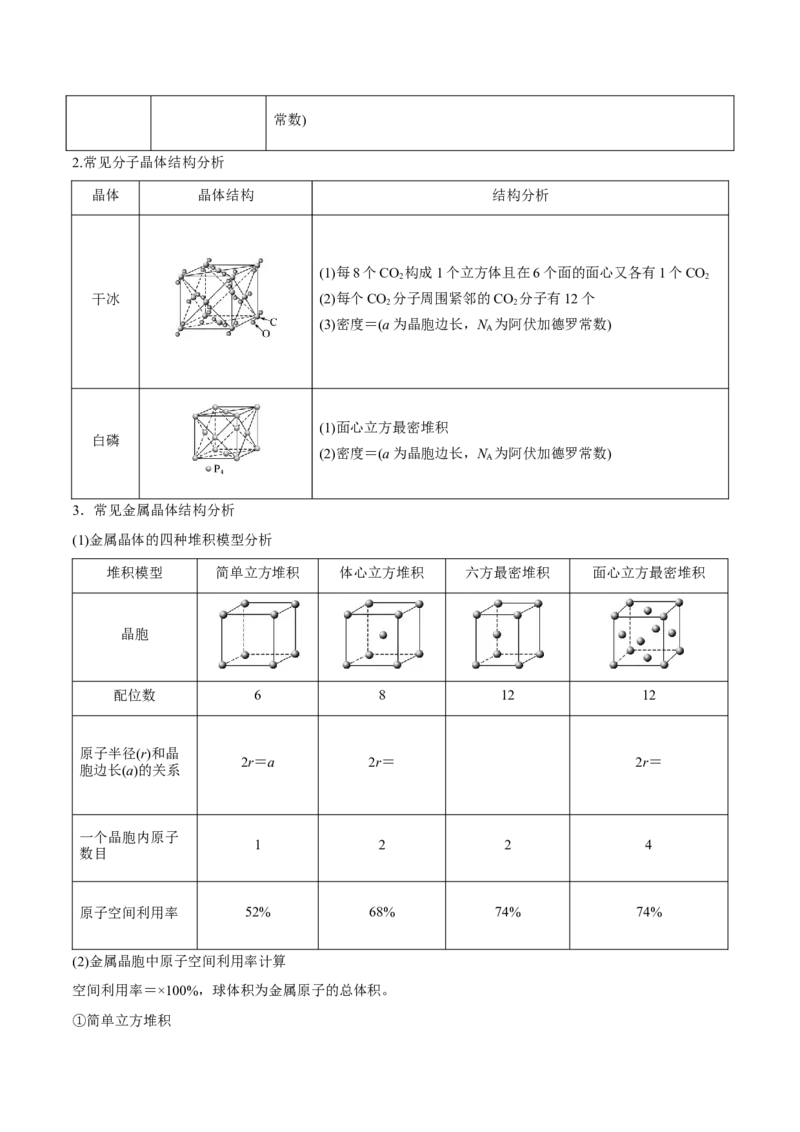
2.常见分子晶体结构分析
晶体 晶体结构 结构分析
(1)每8个CO 构成1个立方体且在6个面的面心又各有1个CO
2 2
干冰 (2)每个CO 分子周围紧邻的CO 分子有12个
2 2
(3)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
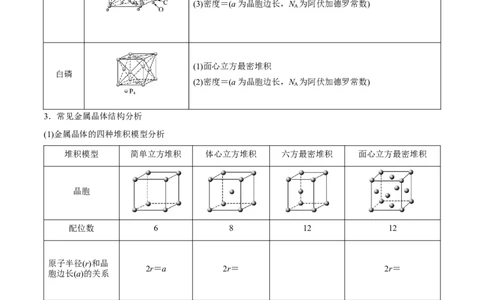
(1)面心立方最密堆积
白磷
(2)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
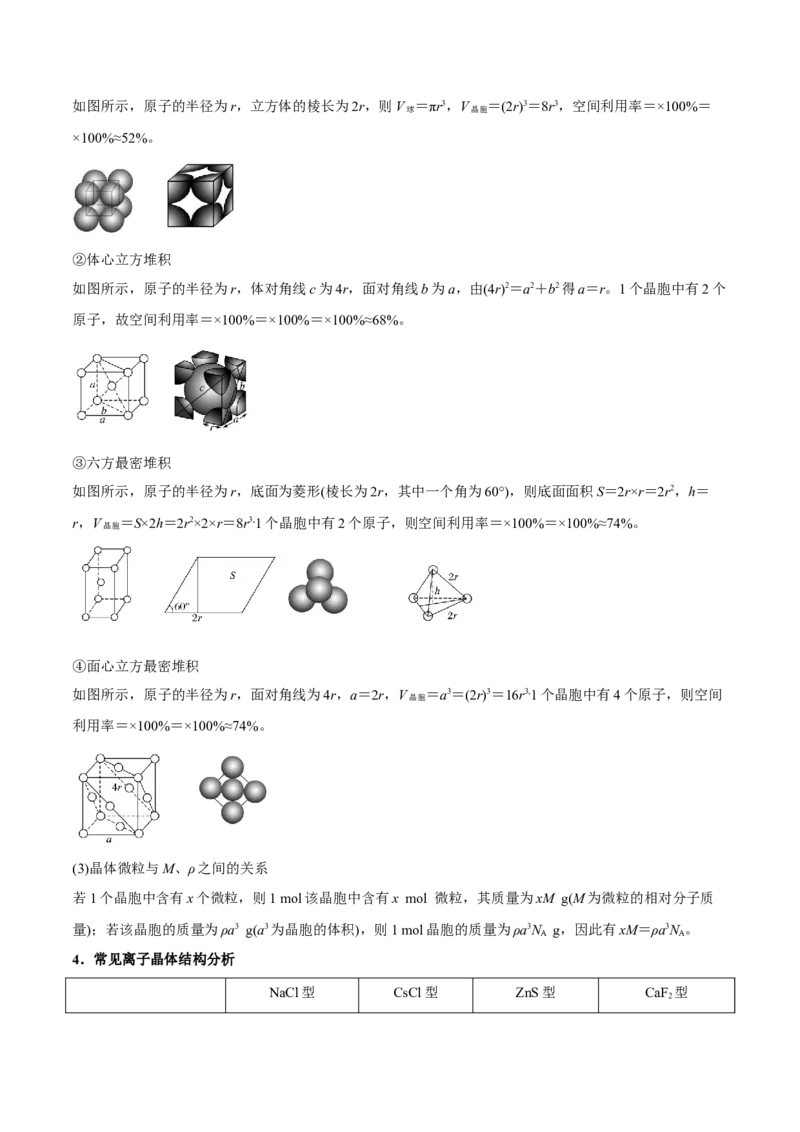
3.常见金属晶体结构分析
(1)金属晶体的四种堆积模型分析
堆积模型 简单立方堆积 体心立方堆积 六方最密堆积 面心立方最密堆积
晶胞
配位数 6 8 12 12
原子半径(r)和晶
2r=a 2r= 2r=
胞边长(a)的关系
一个晶胞内原子
1 2 2 4
数目
原子空间利用率 52% 68% 74% 74%
(2)金属晶胞中原子空间利用率计算
空间利用率=×100%,球体积为金属原子的总体积。
①简单立方堆积如图所示,原子的半径为r,立方体的棱长为2r,则V =πr3,V =(2r)3=8r3,空间利用率=×100%=
球 晶胞
×100%≈52%。
②体心立方堆积
如图所示,原子的半径为r,体对角线c为4r,面对角线b为a,由(4r)2=a2+b2得a=r。1个晶胞中有2个
原子,故空间利用率=×100%=×100%=×100%≈68%。
③六方最密堆积
如图所示,原子的半径为r,底面为菱形(棱长为2r,其中一个角为60°),则底面面积S=2r×r=2r2,h=
r,V =S×2h=2r2×2×r=8r3,1个晶胞中有2个原子,则空间利用率=×100%=×100%≈74%。
晶胞
④面心立方最密堆积
如图所示,原子的半径为r,面对角线为4r,a=2r,V =a3=(2r)3=16r3,1个晶胞中有4个原子,则空间
晶胞
利用率=×100%=×100%≈74%。
(3)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒的相对分子质
量);若该晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有xM=ρa3N 。
A A
4.常见离子晶体结构分析
NaCl型 CsCl型 ZnS型 CaF 型
2晶胞
配位数 6 8 4 F-:4;Ca2+:8
配位数及
影响因素 影响 阳离子与阴离子的半径比值越大,配位数越多,另外配位数还与阴、阳离子的电
因素 荷比有关等
密度的计算(a为晶胞边
长,N 为阿伏加德罗常
A
数)
知识点二、原子分数坐标参数
1.概念
原子分数坐标参数,表示晶胞内部各原子的相对位置。
2.原子分数坐标的确定方法
(1)依据已知原子的坐标确定坐标系取向。
(2)一般以坐标轴所在正方体的棱长为1个单位。
(3)从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标。
3.金刚石晶胞中碳原子坐标的确定
以金刚石晶胞结构为例,金刚石晶体整体上是正四面体立体网状结构。每个碳原子L能层的4个电子
采用sp3杂化,形成4个等同的杂化轨道,相邻的两个碳原子之间形成σ键。这样每个碳原子与周围4个碳
原子形成4个σ键,每个碳原子都是直接相连的4个碳原子的重心。
在一个金刚石晶胞中有8个碳原子位于立方体的顶点,6个碳原子位于面心,4个碳原子位于晶胞内部。
每个晶胞中8个顶点中有4个顶点、6个面心和4个晶胞内部的碳原子形成4个正四面体,每个正四面体的
4个顶点分别是一个晶胞顶点和这个顶点所在平面的面心,正四面体中心是晶胞内的1个碳原子。
用解析几何知识研究晶体中各个微粒间的位置关系更具体更直接。以底面一个顶点的碳原子(通常取后
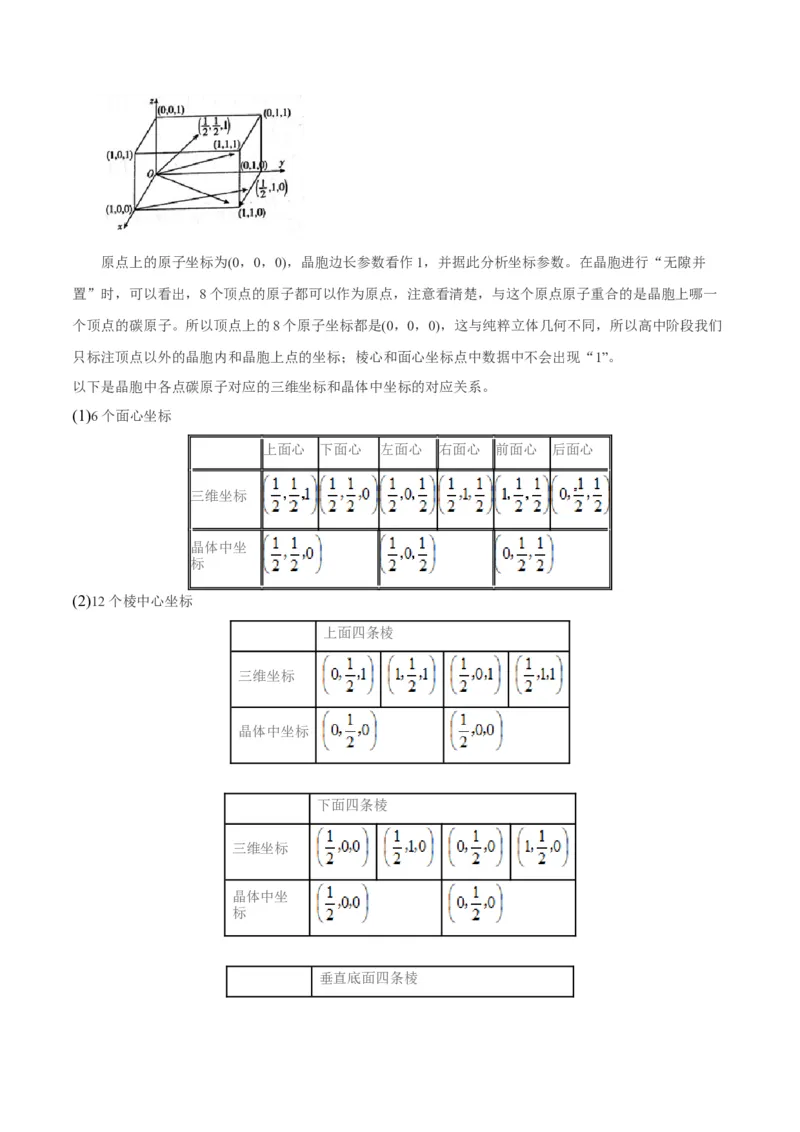
左下)为原点建立一个三维坐标系。原点上的原子坐标为(0,0,0),晶胞边长参数看作1,并据此分析坐标参数。在晶胞进行“无隙并
置”时,可以看出,8个顶点的原子都可以作为原点,注意看清楚,与这个原点原子重合的是晶胞上哪一
个顶点的碳原子。所以顶点上的8个原子坐标都是(0,0,0),这与纯粹立体几何不同,所以高中阶段我们
只标注顶点以外的晶胞内和晶胞上点的坐标;棱心和面心坐标点中数据中不会出现“1”。
以下是晶胞中各点碳原子对应的三维坐标和晶体中坐标的对应关系。
(1)6个面心坐标
上面心 下面心 左面心 右面心 前面心 后面心
三维坐标
晶体中坐
标
(2)12个棱中心坐标
上面四条棱
三维坐标
晶体中坐标
下面四条棱
三维坐标
晶体中坐
标
垂直底面四条棱三维坐标
晶体中坐
标
(3)晶胞内部4个碳原子的坐标
金刚石晶胞有两种取向,由于金刚石晶胞内部有4个碳原子,在空间分布是不对称的,所以从不同方
向观察晶胞时,内部的4个碳原子的位置是不相同的。我们把左边的图叫作取向1,右边的图叫作取向2
它们各自绕竖直中心轴旋转90°,就能够变为对方。金刚石晶胞内4个碳原子坐标:
取向1:
取向2:
所以金刚石晶胞的取向不同时,晶胞内部不对称的4个原子的坐标会发生改变。
4.常见晶胞的原子坐标
1)金刚石晶胞的原子坐标
(1)取向一:
金刚石晶胞中碳原子的坐标:
8个顶点碳原子的坐标:0,0,0;
6个面中心碳原子的坐标:1/2,0,1/2;1/2,1/2,0;0,1/2,1/2;
4个内部碳原子的坐标:1/4,1/4,3/4;3/4,1/4,1/4;3/4,3/4,3/4;1/4,3/4,1/4;(2)取向二:
金刚石晶胞中碳原子的坐标:
8个顶点碳原子的坐标:0,0,0;
6个面中心碳原子的坐标:1/2,0,1/2;1/2,1/2,0;0,1/2,1/2;
4个内部碳原子的坐标:1/4,1/4,1/4;3/4,3/4,1/4;3/4,1/4,3/4;1/4,3/4,3/4;
注:金刚石晶胞的取向不同时,即使都是取前左下的顶点原子作原点,晶胞内部不对称的4个碳原子的坐
标,也会发生改变。
2)氟化钙晶体:
每个CaF 晶胞有4个Ca2+和8个F-原子分数坐标如下:
2
Ca2+: 0,0,0 1/2,1/2,0 1/2,0,1/2 0,1/2,1/2
F-: 1/4,1/4,1/4 3/4,1/4,1/4 1/4,3/4,1/4 1/4,1/4,3/4
3/4,3/4,1/4 3/4,1/4,3/4 1/4,3/4,3/4 3/4,3/4,3/4
3)氯化钠晶胞:
每个晶胞含有4个Cl-和4个Na+,它们的原子分数坐标为:
Na+: 1/2,1/2,1/2 1/2,0,0 0,1/2,0 0,0,1/2Cl-: 0,0,0 1/2,1/2,0 0,1/2,1/2 1/2,0,1/2
注:碱金属的卤化物、氢化物,碱土金属的氧化物、硫化物、硒化物、碲化物,过渡金属的氧化物、硫化
物,以及间隙型碳化物、氮化物都属NaCl型结构。
知识点三、宏观晶体密度与微观晶胞参数的关系
1.密度的计算式:
2.计算类型
晶体的密度有两种计算形式,一种是知道晶胞边长和晶胞结构进行的计算,一种是知道原子或离子半
径和晶胞结构进行的计算。
1)知道晶胞边长和晶胞结构进行的计算
若晶胞为正方体,边长为a pm,含有b个分子,分子的相对分子质量为M,则密度的计算过程为(别记结
论,学会计算过程)
晶胞的体积为:(a×10-12m)3= a3×10-36m3
晶胞中分子的总质量为:m=nM=(b/N )M= bM/6.02×1023g
A
ρ=M/V=(bM/6.02×1023g) /( a3×10-36m3)=(bM×1013)/(6.02×a3)g/m3
(1)CO 分子晶体的密度计算:
2
已知CO 分子晶体的结构如下图(面心立方),晶胞边长为572pm(计算数据)。
2
①晶胞中的分子数目计算:8×1/8+6×1/2=4
一个晶胞中有4个CO。
2
②晶体密度计算:m=nM=[4/(6.02×1023/mol)]×44g/mol=2.9236×10-22g
V=(572×10-12)3m3=1.8715×10-28m3
ρ=m/V=2.9236×10-22g /1.8715×10-28m3=1.562×106g/m3=1.562g/ cm3。
(2)Po(钋),相对原子质量为209,晶胞边长为336pm。
①晶胞中原子数目计算:8×1/8=1。
②密度计算:
m=nM=[1/(6.02×1023/mol)]×209g/mol=3.472×10-22g
V=(336×10-12)3m3=3.7933×10-29m3
ρ=m/V=3.472×10-22g /3.7933×10-29m3=9.153 ×106g/m3=9.153g/cm3
2)知道原子或离子半径和晶胞结构进行的计算
先用原子或离子的半径计算出晶胞的边长,然后再进行密度计算。
(1)Na的体心立方
Na的原子半径r=186pm。
①晶胞中的原子数目计算:8×1/8+1=2。
②密度计算:
先计算晶胞的边长a:根据体对角线=√3a=4r,
边长a=4r/√3=4×186pm/√3=429.56pm。
m=nM=[2/(6.02×1023/mol)]×23g/mol=7.6412×10-23g
V=(429.56×10-12)3m3=7.9263×10-29m3
ρ=m/V=7.6412×10-23g /7.9263×10-29m3=9.64 ×105g/m3=0.964g/cm3
(2)Zn的六方堆积:Zn的范德华半径为139pm。
①正六棱柱中原子数目计算:12×1/6+2×1/2+3=6
②密度计算:六方最密堆积不是正方体晶胞,不能用正方体的公式计算。
用上面的正六棱柱计算,正六棱柱的边长为278pm。
若边长为r,体积为24√2 r3。(计算式见空间利用率计算的(3))
V=24√2 r3=24√2×(139×10-12m)3=9.1153×10-29m3
m=nM=[6/(6.02×1023/mol)]×65.38g/mol=6.5163×10-22g
ρ=m/V=6.5163×10-22g /9.1153×10-29m3=7.15 ×106g/m3=7.15g/cm3
(3)金刚石原子晶体的结构
①晶胞中的原子数目计算:8×1/8+6×1/2+4=8
②密度计算:以金刚石结构为例,C的共价半径为77pm。
大立方体的边长为8r/√3,即355.65 pm。(计算式见空间利用率计算的(4))
m=nM=[8/(6.02×1023/mol)]×12g/mol=1.5947×10-22g
V=(355.65×10-12)3m3=4.4985×10-29m3
ρ=m/V=1.5947×10-22g /4.4985×10-29m3=3.545 ×106g/m3=3.545g/cm3
(4)离子晶体的密度计算:①NaCl:Na+的离子半径为95pm,Cl-的离子半径为181pm
晶胞边长的计算:2r(Na+)+2r(Cl-)=552pm。
其中含Na+4个,Cl-4个。
m=nM=[4/(6.02×1023/mol)]×23g/mol+[4/(6.02×1023/mol)]×35.45g/mol=3.8837×10-22g
V=(552×10-12)3m3=1.682×10-28m3
ρ=m/V=3.8837×10-22g /1.682×10-28m3=2.309×106g/m3=2.309g/cm3
②CsCl:Cs+的离子半径为169pm,Cl-的离子半径为181pm。
晶胞边长的计算:[2r(Cs+)+2r(Cl-)]/√3=404.15pm。
其中含Cs+1个,Cl-1个。
m=nM=[1/(6.02×1023/mol)]×132.9g/mol+[1/(6.02×1023/mol)]×35.45g/mol=2.7965×10-22g
V=(404.15×10-12)3m3=6.6013×10-29m3
ρ=m/V=2.7965×10-22g /6.6013×10-29m3=4.236×106g/m3=4.236g/cm3
③CaF :Ca2+的离子半径为99pm,F-的离子半径为136pm。
2
右侧为晶胞的八分之一
晶胞边长计算为2{[2r(Ca2+)+2r(F-)]/√3}=542.71pm。
其中含Ca2+4个,F-8个,则密度为
M=nm=[4/(6.02×1023/mol)]×40g/mol+[8/(6.02×1023/mol)]×19g/mol=5.1827×10-22gV=(542.71×10-12)3m3=1.5985×10-28m3
ρ=m/V=5.1827×10-22g /1.5985×10-28m3=3.242×106g/m3=3.242g/cm3
知能点四 晶体中堆积方式不同的棱长与原子半径的关系
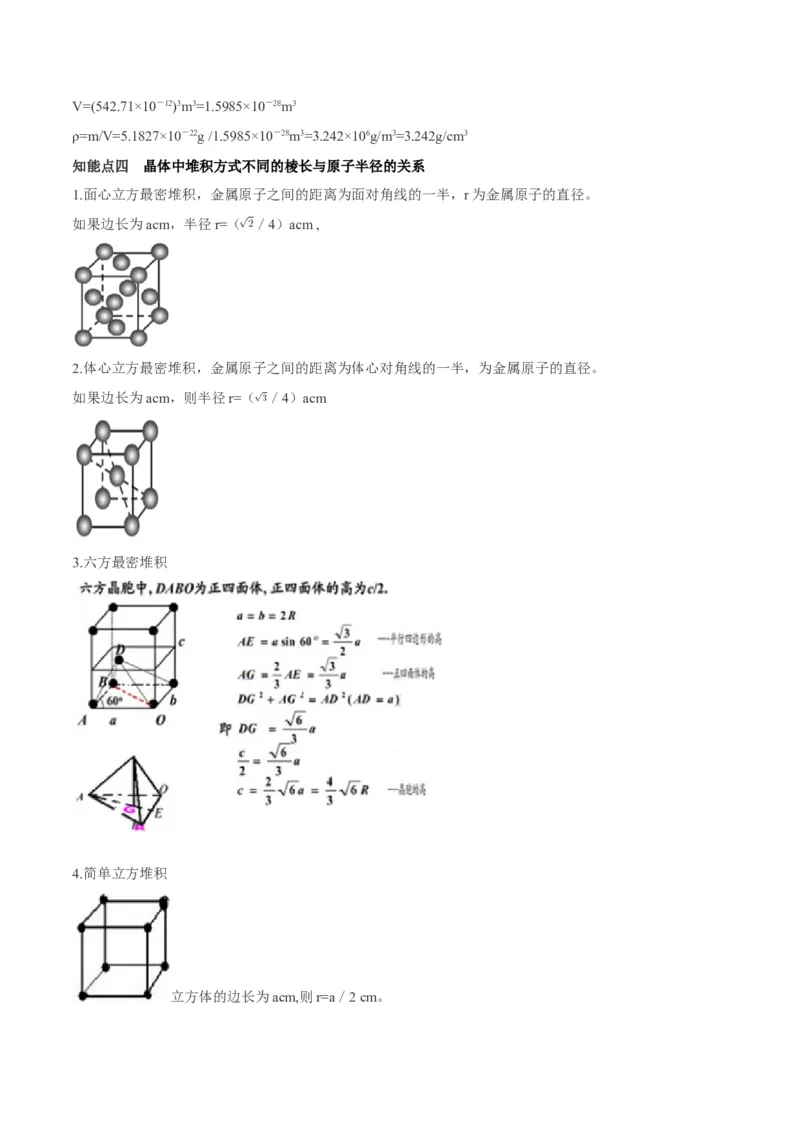
1.面心立方最密堆积,金属原子之间的距离为面对角线的一半,r为金属原子的直径。
如果边长为acm,半径r=( /4)acm ,
2.体心立方最密堆积,金属原子之间的距离为体心对角线的一半,为金属原子的直径。
如果边长为acm,则半径r=( /4)acm
3.六方最密堆积
4.简单立方堆积
立方体的边长为acm,则r=a/2 cm。5.金刚石
图中原子均为碳原子,这种表示为更直观。如边长为acm,碳原子的半径为( /8)acm。
知识点五 空间利用率的计算
1、空间利用率的计算式
若原子的半径为R,晶胞中原子有n个,立方晶胞的边长为a:
单个原子的体积为4πr3/3,立方晶胞的体积为a。
3
则空间利用率为
2、各种晶胞的空间利用率计算
(1)金属晶体的简单立方
①晶胞中原子数目计算:8×1/8=1。
②空间利用率计算:设球的半径为r,则正方体的边长为2r。
原子的总体积为4πr3/3。正方体的体积为8r3。
空间利用率为(4πr3/3)/(8 r3)=π/6=52.36%
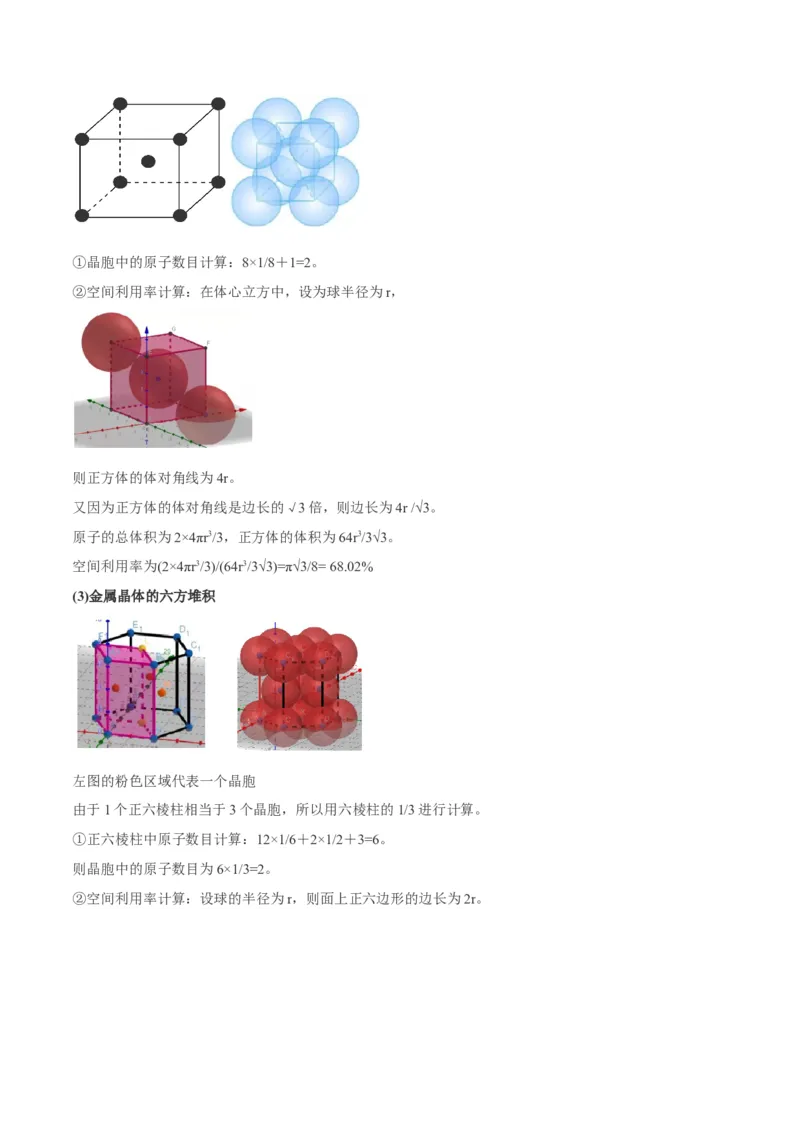
(2)金属晶体的体心立方①晶胞中的原子数目计算:8×1/8+1=2。
②空间利用率计算:在体心立方中,设为球半径为r,
则正方体的体对角线为4r。
又因为正方体的体对角线是边长的√3倍,则边长为4r /√3。
原子的总体积为2×4πr3/3,正方体的体积为64r3/3√3。
空间利用率为(2×4πr3/3)/(64r3/3√3)=π√3/8= 68.02%
(3)金属晶体的六方堆积
左图的粉色区域代表一个晶胞
由于1个正六棱柱相当于3个晶胞,所以用六棱柱的1/3进行计算。
①正六棱柱中原子数目计算:12×1/6+2×1/2+3=6。
则晶胞中的原子数目为6×1/3=2。
②空间利用率计算:设球的半径为r,则面上正六边形的边长为2r。正六棱柱的高的计算:
正六棱柱的高为两个边长为2r的正四面体的高。边长2r的正四面体的体高为2√6r/3,则正六棱柱的高为
4√6r/3。
正六边形的面积为6×√3r2=6√3r2。
正六棱柱的体积为(6√3r2)×(4√6r/3)=24√2 r3。
晶胞体积为正六棱柱的1/3,为8√2r3。
原子的总体积为2×4πr3/3=8πr3/3。
空间利用率为(8πr3/3)/(8√2r3)=π/3√2= 74.05%
(4)金刚石原子晶体的结构
①晶胞中的原子数目计算:8×1/8+6×1/2+4=8
②空间利用率计算:根据两个C之间紧密相邻,若C的原子半径为r,则C-C为2r。
大立方体切8个小立方体,其中一个如右图。中间球位于小立方体的中心。小立方体的体对角线为4r(自己
思考一下),则小立方体的边长为4r/√3。
求得大立方体的边长为8r/√3,体积为512r3/3√3。
大立方体内的碳原子数为8,碳原子的总体积为8×4πr3/3=32πr3/3。
所以空间利用率为(32πr3/3)/(512 r3/3√3)=π√3/16=34.01%
第三部分:典型例题剖析
高频考点1 晶胞参数与晶体密度间的互算
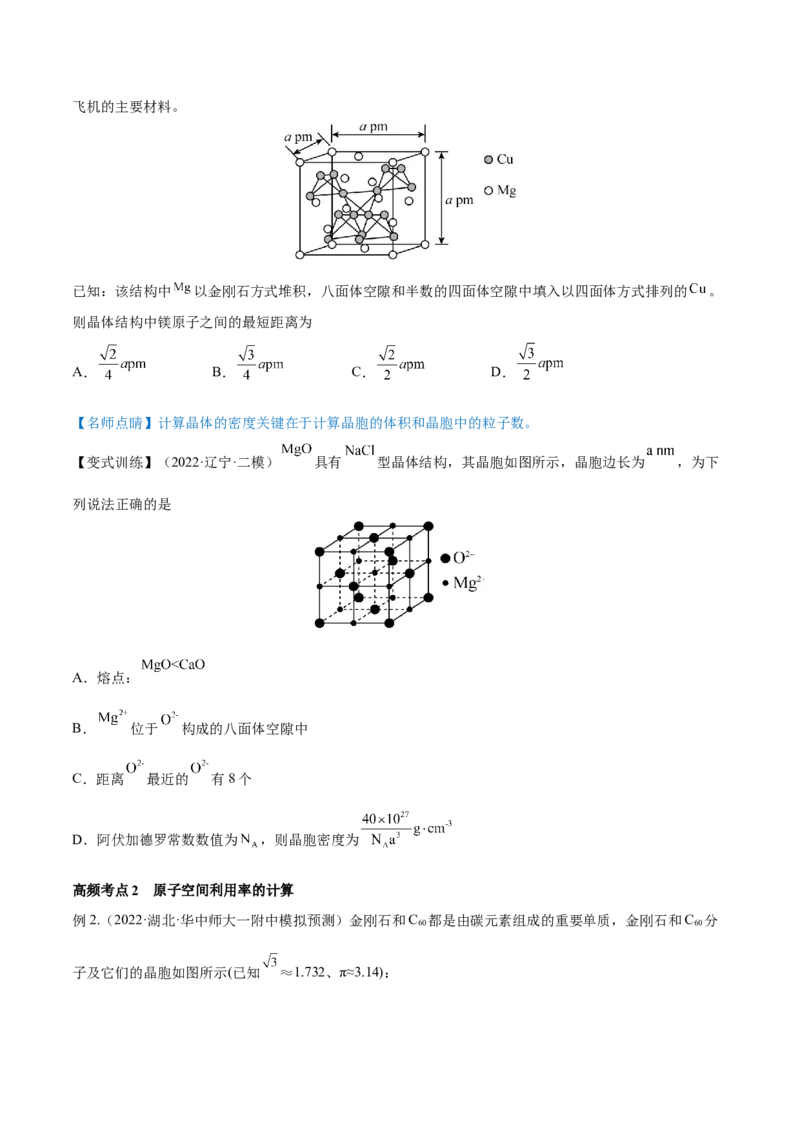
例1.(2022·辽宁辽阳·二模)在普通铝中加入少量 和 后,形成一种称为拉维斯相的 (结构如
图)微小晶粒,其分散在 中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,“坚铝”是制造飞机的主要材料。
已知:该结构中 以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入以四面体方式排列的 。
则晶体结构中镁原子之间的最短距离为
A. B. C. D.
【名师点睛】计算晶体的密度关键在于计算晶胞的体积和晶胞中的粒子数。
【变式训练】(2022·辽宁·二模) 具有 型晶体结构,其晶胞如图所示,晶胞边长为 ,为下
列说法正确的是
A.熔点:
B. 位于 构成的八面体空隙中
C.距离 最近的 有8个
D.阿伏加德罗常数数值为 ,则晶胞密度为
高频考点2 原子空间利用率的计算
例2.(2022·湖北·华中师大一附中模拟预测)金刚石和C 都是由碳元素组成的重要单质,金刚石和C 分
60 60
子及它们的晶胞如图所示(已知 ≈1.732、π≈3.14):下列说法正确的是
A.每个金刚石晶胞中含有4个碳原子
B.每个C 分子含有90个σ键
60
C.金刚石和C 晶胞中微粒间的作用力均只有共价键
60
D.每个金刚石晶胞原子的空间利用率为74.05%
【名师点睛】解答原子空间利用率的计算问题要掌握以下四方面知识:①四种堆积的切割模型; ②晶胞
参数(边长)与金属原子半径的关系; ③六方最密堆积晶胞所含原子数及晶胞体积;④空间利用率计算
方法;
【变式训练】(2022·全国·高三专题练习)有四种不同堆积方式的金属晶体的晶胞如图所示(原子半径为
rcm),下列叙述错误的是
A.晶胞中原子的配位数分别为:①6,②8,③12,④12
B.晶胞①的空间利用率:
C.晶胞中含有的原子数分别为:③2,④4,
D.金属晶体是一种“巨分子”,可能存在分子间作用力
高频考点3 晶胞中原子坐标的确定
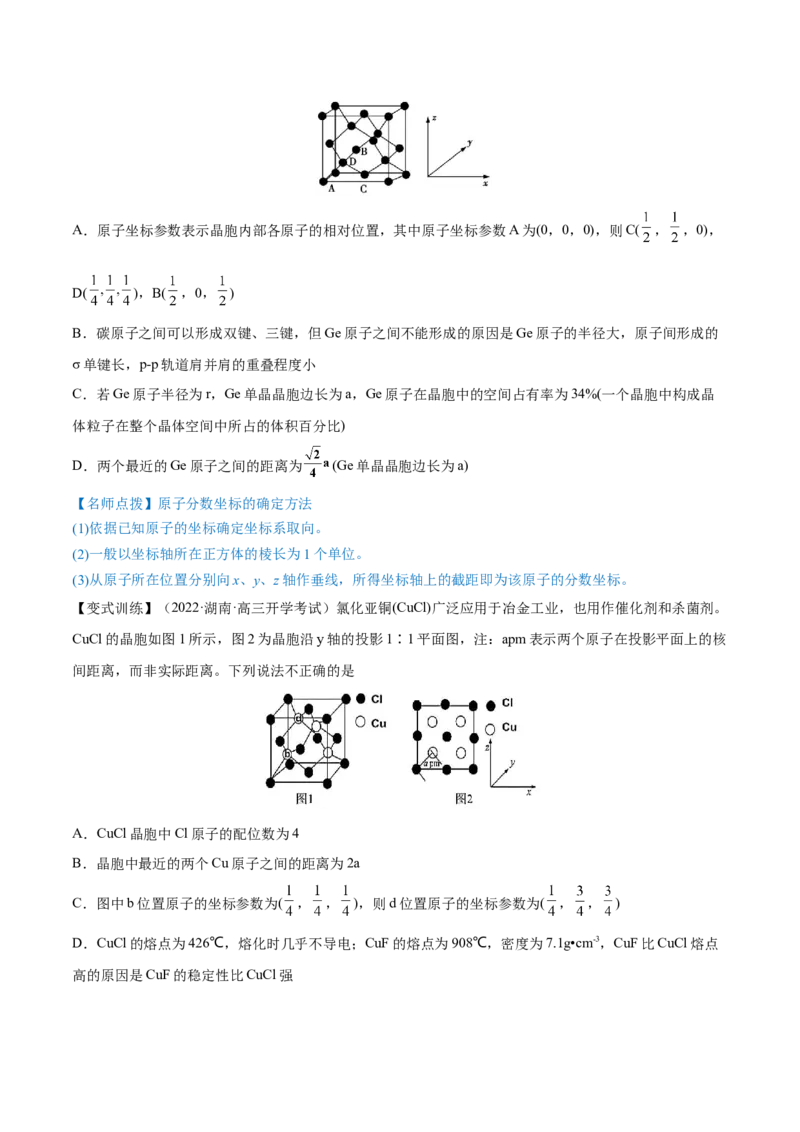
例3.(2022·辽宁·二模)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。Ge与碳是同族元素,
碳原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。Ge单晶的晶胞结构类似于金刚石,
如图。( =1.732,π=3.14)(注:晶胞中所有的球是等径硬球,且A球和D球相切)下列说法错误的是A.原子坐标参数表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),则C( , ,0),
D( ),B( ,0, )
B.碳原子之间可以形成双键、三键,但Ge原子之间不能形成的原因是Ge原子的半径大,原子间形成的
σ单键长,p-p轨道肩并肩的重叠程度小
C.若Ge原子半径为r,Ge单晶晶胞边长为a,Ge原子在晶胞中的空间占有率为34%(一个晶胞中构成晶
体粒子在整个晶体空间中所占的体积百分比)
D.两个最近的Ge原子之间的距离为 (Ge单晶晶胞边长为a)
【名师点拨】原子分数坐标的确定方法
(1)依据已知原子的坐标确定坐标系取向。
(2)一般以坐标轴所在正方体的棱长为1个单位。
(3)从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标。
【变式训练】(2022·湖南·高三开学考试)氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。
CuCl的晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图,注:apm表示两个原子在投影平面上的核
间距离,而非实际距离。下列说法不正确的是
A.CuCl晶胞中Cl原子的配位数为4
B.晶胞中最近的两个Cu原子之间的距离为2a
C.图中b位置原子的坐标参数为( , , ),则d位置原子的坐标参数为( , , )
D.CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3,CuF比CuCl熔点
高的原因是CuF的稳定性比CuCl强