文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(河北专用)
化 学
考情速递
高考·新考法:
第13-14题,以锂离子电池为命题情境,分别考查电化学的有关计算和电极反应以及反应历程,体现
了对常规考点的创新糅合。
高考·新情境:
本套试卷情境丰富,如第1题以河北博物院馆藏文物为情境考查硅酸盐材料。第3题以CH 与Cl 在光
4 2
照发生的反应为情境考查阿伏加德罗常数。第17题以实现“双碳”目标为情境考查热化学方程式、化学
平衡状态、转化率、化学平衡常数等。
命题·大预测:
预测2025年高考河北卷化学试题继续保持稳中求新风格,试卷结构和试题难度保持相对稳定。高考
情境化试题比例将增加,彰显学科的价值引领。在备考时,注重教材知识在具体问题解决过程中的理解和
应用。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li7 Be9 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
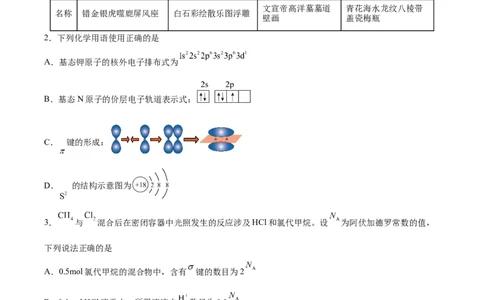
1.燕赵大地历史悠久,文化灿烂。下列河北博物院馆藏文物的主要成分属于硅酸盐的是
选项 A B C D文物
朝代 战国(1977年出土) 五代(1995年出土) 北齐(1989年出土) 元(1964年出土)
文宣帝高洋墓墓道 青花海水龙纹八棱带
名称 错金银虎噬鹿屏风座 白石彩绘散乐图浮雕
壁画 盖瓷梅瓶
2.下列化学用语使用正确的是
A.基态钾原子的核外电子排布式为
B.基态N原子的价层电子轨道表示式:
C. 键的形成:
D. 的结构示意图为
3. 与 混合后在密闭容器中光照发生的反应涉及HCl和氯代甲烷。设 为阿伏加德罗常数的值,
下列说法正确的是
A.0.5mol氯代甲烷的混合物中,含有 键的数目为2
B.0.1mol HCl溶于水,所得溶液中 数目为0.1
C.1mol 溶于水,充分反应后转移电子的数目为
D.1mol 与1mol 在密闭容器中反应后,容器内分子总数大于2
4.下列离子方程式错误的是
A. 通入冷的 溶液中:B.向苯酚钠 溶液中通入少量 :
C.用 溶液吸收少量 :
D. 溶液与少量的 溶液混合:
5.下列实验装置的使用或操作正确且能达到实验目的的是
A.测定原电池电压 B.分离铁粉和 C.碱式滴定管排气泡 D.测定中和反应的反应热
6.下列化学实验中的操作、现象及结论都正确的是
选
操作 现象 结论
项
向1-溴丙烷中加入KOH溶液,加热并充分振荡, 溶液中出现棕黑色
A AgBr为棕黑色
然后取少量液体滴入 溶液中 沉淀
向甲基环己烷和甲苯中分别滴加少量酸性 溶 前者下层溶液为紫红色, 苯环使甲基变活
B
液,充分振荡 后者溶液为无色 泼
探究氯水颜色成因:取少量黄绿色的新制氯水,向 产生白色沉淀,溶液变无 氯水颜色与
C
其中滴加 溶液至过量 色 有关
试管底部固体消失,试管 固体受
D 将盛有 固体的试管加热
口有晶体凝结 热易升华
7.化合物M(如图所示)是一种医药中间体。下列关于M的说法错误的是
A.不含手性碳原子
B.能发生取代反应和氧化反应
C.分子中C原子有2种杂化方式
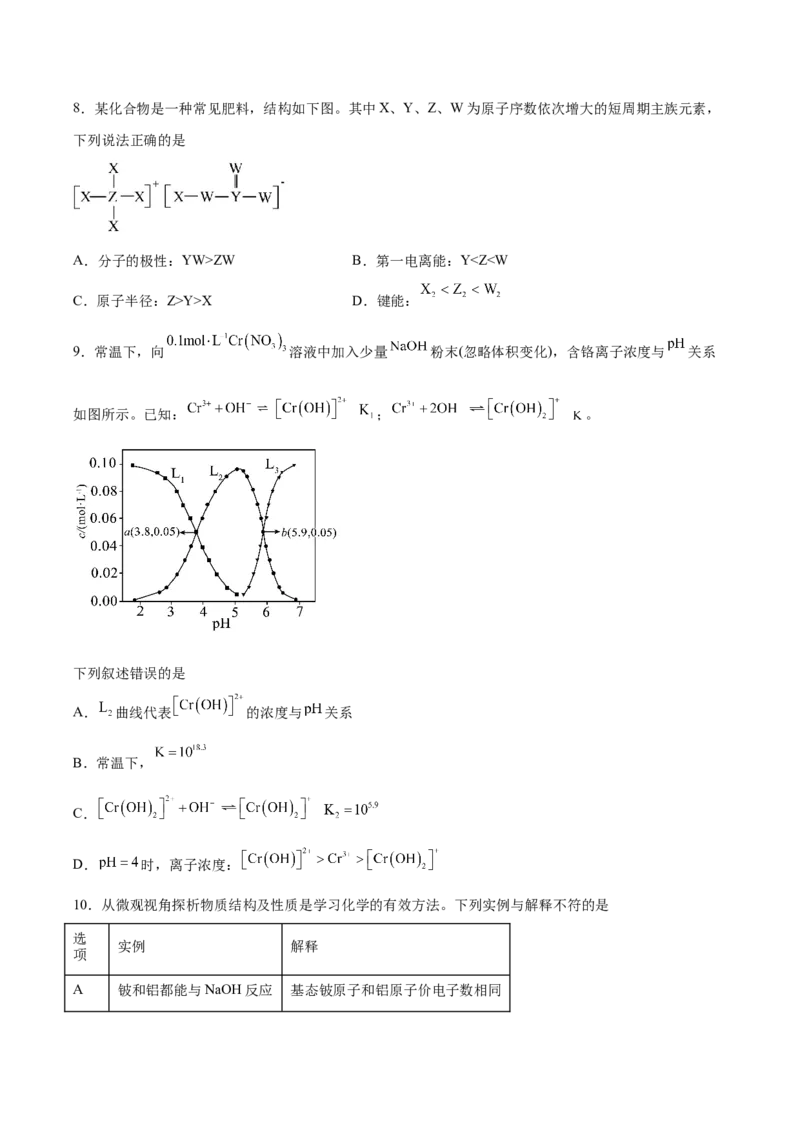
D.1mol M最多消耗 或NaOH的物质的量相等8.某化合物是一种常见肥料,结构如下图。其中X、Y、Z、W为原子序数依次增大的短周期主族元素,
下列说法正确的是
A.分子的极性:YW>ZW B.第一电离能:YY>X D.键能:
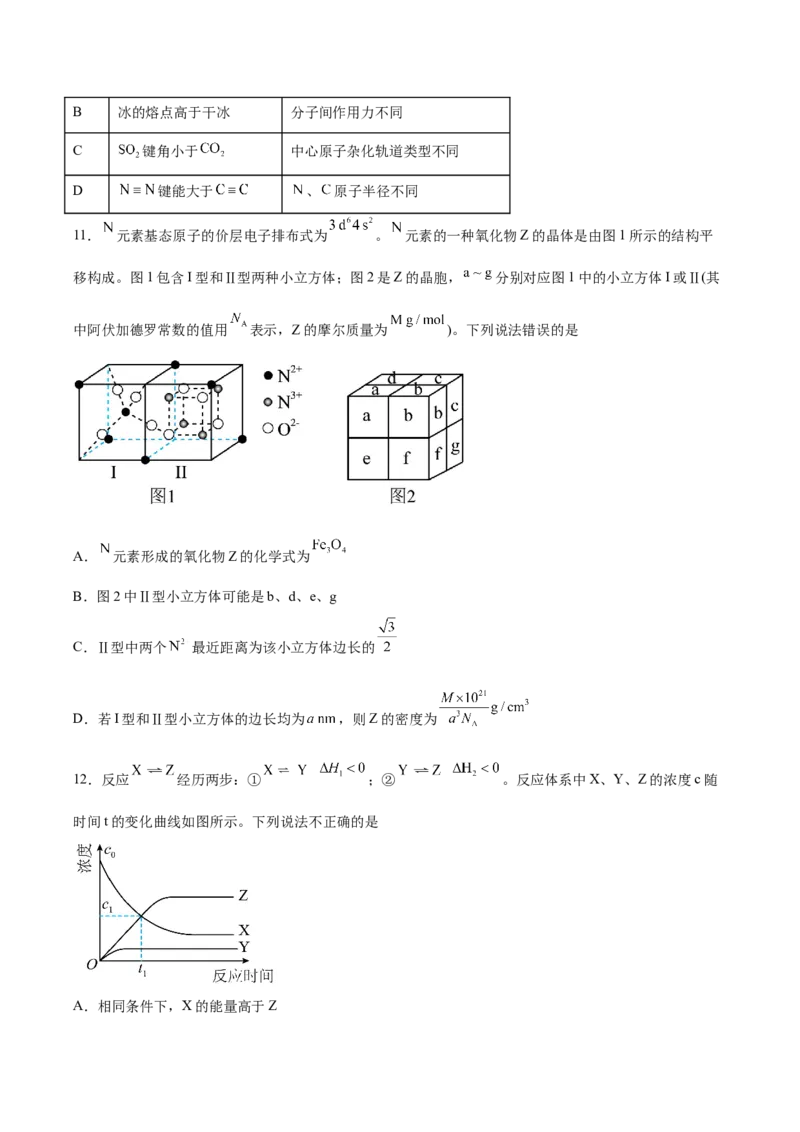
9.常温下,向 溶液中加入少量 粉末(忽略体积变化),含铬离子浓度与 关系
如图所示。已知: ; 。
下列叙述错误的是
A. 曲线代表 的浓度与 关系
B.常温下,
C.
D. 时,离子浓度:
10.从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是
选
实例 解释
项
A 铍和铝都能与NaOH反应 基态铍原子和铝原子价电子数相同B 冰的熔点高于干冰 分子间作用力不同
C 键角小于 中心原子杂化轨道类型不同
D 键能大于 、 原子半径不同
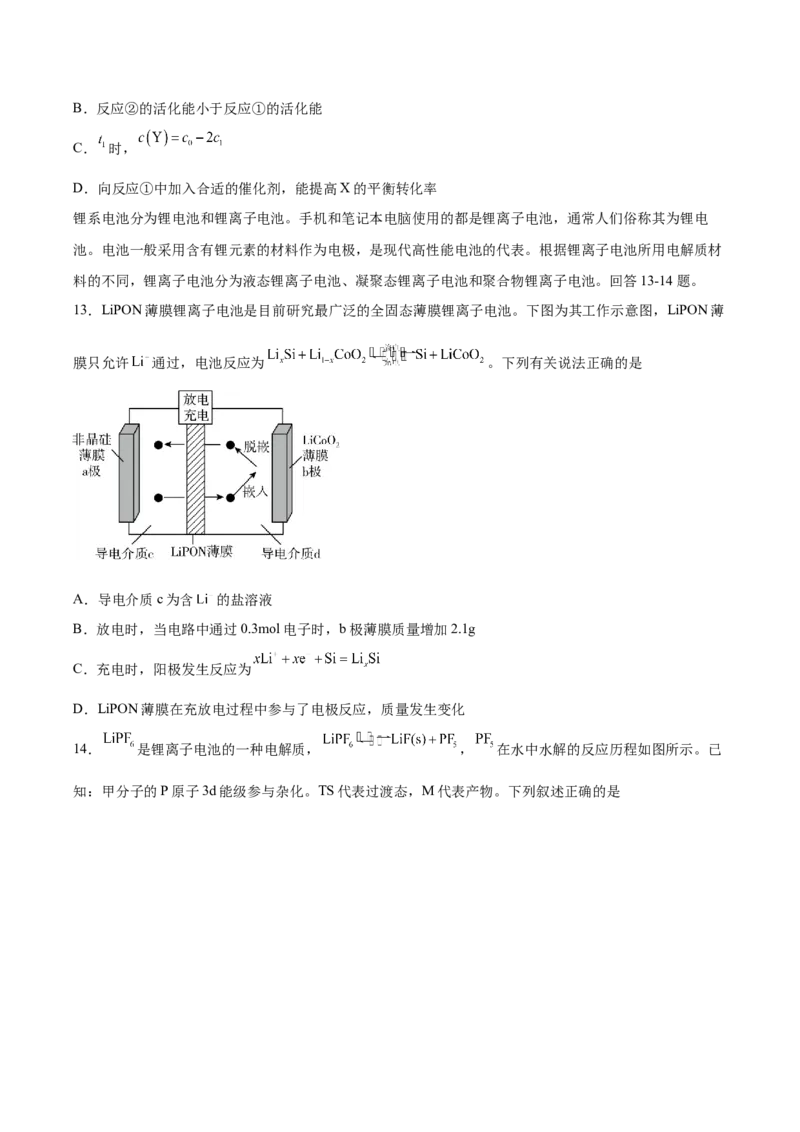
11. 元素基态原子的价层电子排布式为 。 元素的一种氧化物Z的晶体是由图1所示的结构平
移构成。图1包含I型和Ⅱ型两种小立方体;图2是Z的晶胞, 分别对应图1中的小立方体I或Ⅱ(其
中阿伏加德罗常数的值用 表示,Z的摩尔质量为 )。下列说法错误的是
A. 元素形成的氧化物Z的化学式为
B.图2中Ⅱ型小立方体可能是b、d、e、g
C.Ⅱ型中两个 最近距离为该小立方体边长的
D.若I型和Ⅱ型小立方体的边长均为 ,则Z的密度为
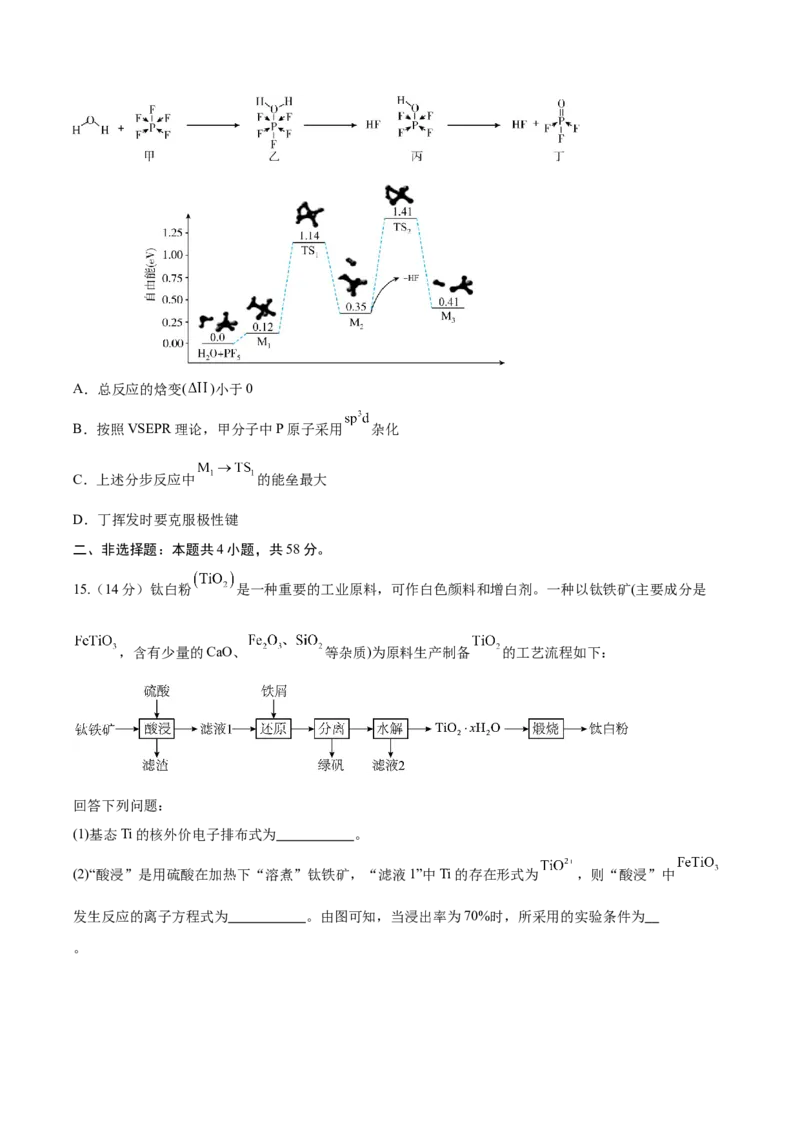
12.反应 经历两步:① ;② 。反应体系中X、Y、Z的浓度c随
时间t的变化曲线如图所示。下列说法不正确的是
A.相同条件下,X的能量高于ZB.反应②的活化能小于反应①的活化能
C. 时,
D.向反应①中加入合适的催化剂,能提高X的平衡转化率
锂系电池分为锂电池和锂离子电池。手机和笔记本电脑使用的都是锂离子电池,通常人们俗称其为锂电
池。电池一般采用含有锂元素的材料作为电极,是现代高性能电池的代表。根据锂离子电池所用电解质材
料的不同,锂离子电池分为液态锂离子电池、凝聚态锂离子电池和聚合物锂离子电池。回答13-14题。
13.LiPON薄膜锂离子电池是目前研究最广泛的全固态薄膜锂离子电池。下图为其工作示意图,LiPON薄
膜只允许 通过,电池反应为 。下列有关说法正确的是
A.导电介质c为含 的盐溶液
B.放电时,当电路中通过0.3mol电子时,b极薄膜质量增加2.1g
C.充电时,阳极发生反应为
D.LiPON薄膜在充放电过程中参与了电极反应,质量发生变化
14. 是锂离子电池的一种电解质, , 在水中水解的反应历程如图所示。已
知:甲分子的P原子3d能级参与杂化。TS代表过渡态,M代表产物。下列叙述正确的是A.总反应的焓变( )小于0
B.按照VSEPR理论,甲分子中P原子采用 杂化
C.上述分步反应中 的能垒最大
D.丁挥发时要克服极性键
二、非选择题:本题共4小题,共58分。
15.(14分)钛白粉 是一种重要的工业原料,可作白色颜料和增白剂。一种以钛铁矿(主要成分是
,含有少量的CaO、 等杂质)为原料生产制备 的工艺流程如下:
回答下列问题:
(1)基态Ti的核外价电子排布式为 。
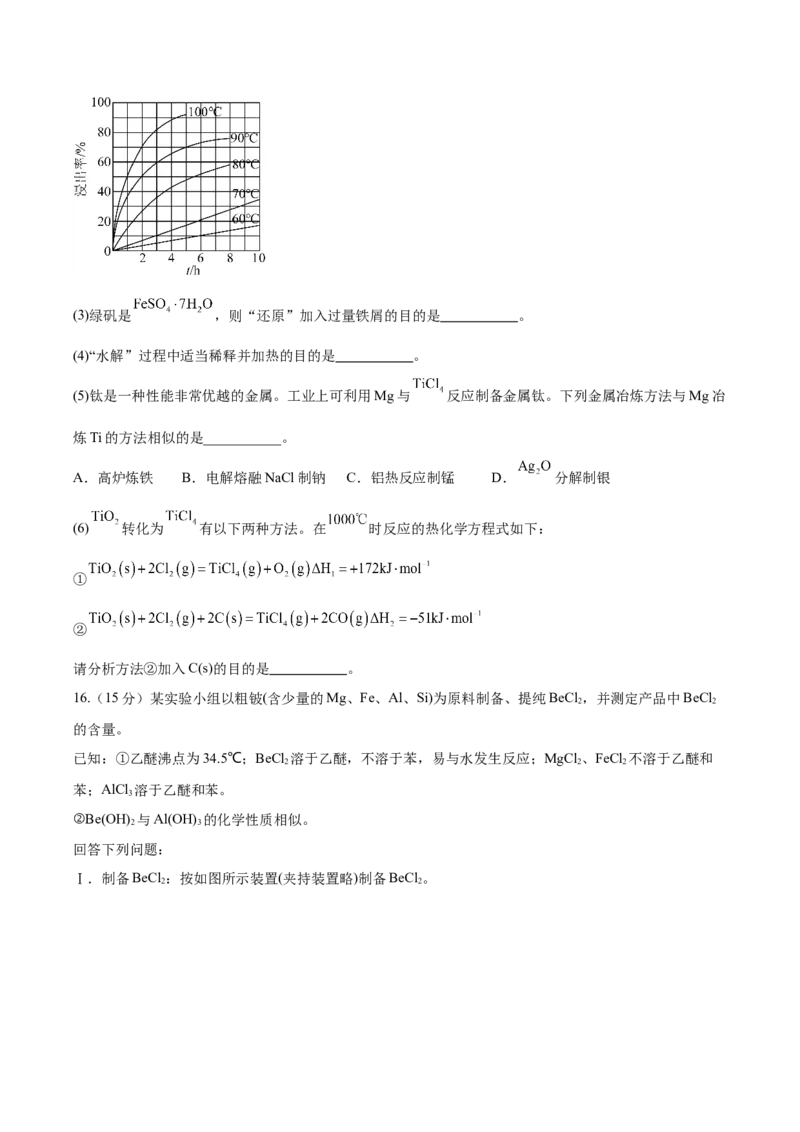
(2)“酸浸”是用硫酸在加热下“溶煮”钛铁矿,“滤液1”中Ti的存在形式为 ,则“酸浸”中
发生反应的离子方程式为 。由图可知,当浸出率为70%时,所采用的实验条件为
。(3)绿矾是 ,则“还原”加入过量铁屑的目的是 。
(4)“水解”过程中适当稀释并加热的目的是 。
(5)钛是一种性能非常优越的金属。工业上可利用Mg与 反应制备金属钛。下列金属冶炼方法与Mg冶
炼Ti的方法相似的是___________。
A.高炉炼铁 B.电解熔融NaCl制钠 C.铝热反应制锰 D. 分解制银
(6) 转化为 有以下两种方法。在 时反应的热化学方程式如下:
①
②
请分析方法②加入C(s)的目的是 。
16.(15分)某实验小组以粗铍(含少量的Mg、Fe、Al、Si)为原料制备、提纯BeCl ,并测定产品中BeCl
2 2
的含量。
已知:①乙醚沸点为34.5℃;BeCl 溶于乙醚,不溶于苯,易与水发生反应;MgCl 、FeCl 不溶于乙醚和
2 2 2
苯;AlCl 溶于乙醚和苯。
3
②Be(OH) 与Al(OH) 的化学性质相似。
2 3
回答下列问题:
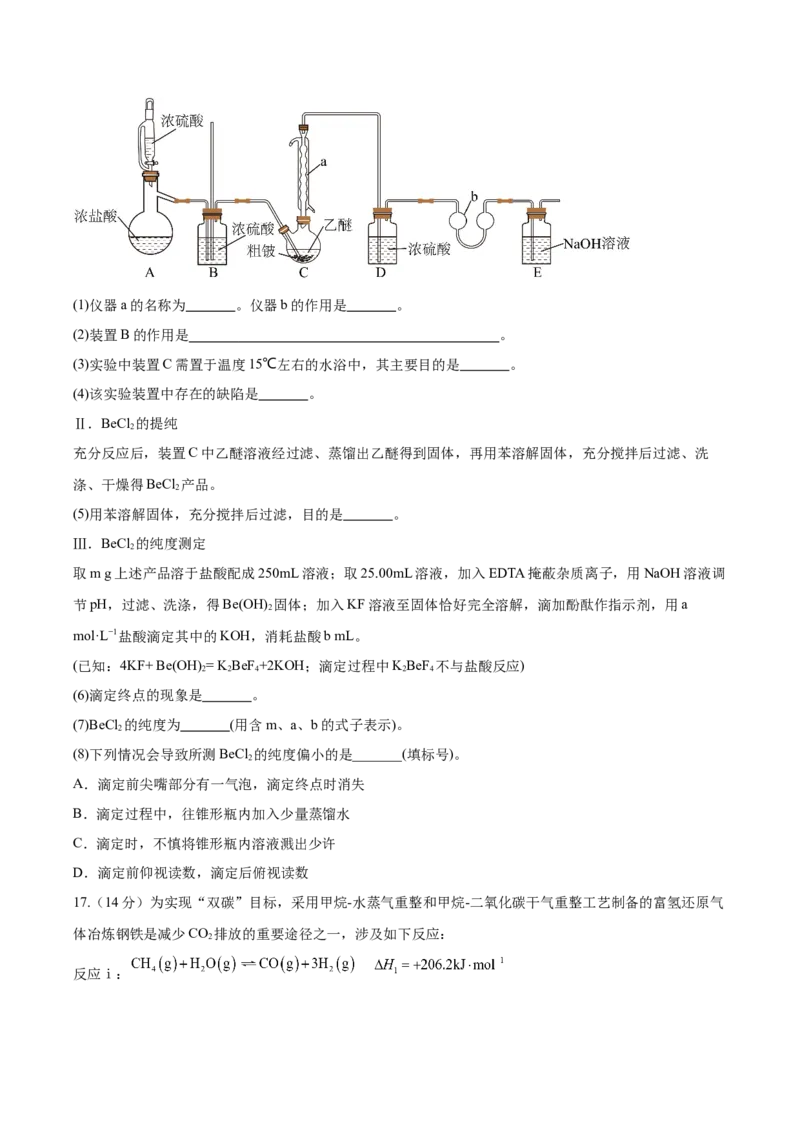
Ⅰ.制备BeCl :按如图所示装置(夹持装置略)制备BeCl 。
2 2(1)仪器a的名称为 。仪器b的作用是 。
(2)装置B的作用是 。
(3)实验中装置C需置于温度15℃左右的水浴中,其主要目的是 。
(4)该实验装置中存在的缺陷是 。
Ⅱ.BeCl 的提纯
2
充分反应后,装置C中乙醚溶液经过滤、蒸馏出乙醚得到固体,再用苯溶解固体,充分搅拌后过滤、洗
涤、干燥得BeCl 产品。
2
(5)用苯溶解固体,充分搅拌后过滤,目的是 。
Ⅲ.BeCl 的纯度测定
2
取m g上述产品溶于盐酸配成250mL溶液;取25.00mL溶液,加入EDTA掩蔽杂质离子,用NaOH溶液调
节pH,过滤、洗涤,得Be(OH) 固体;加入KF溶液至固体恰好完全溶解,滴加酚酞作指示剂,用a
2
mol·L−1盐酸滴定其中的KOH,消耗盐酸b mL。
(已知:4KF+ Be(OH) = K BeF +2KOH;滴定过程中KBeF 不与盐酸反应)
2 2 4 2 4
(6)滴定终点的现象是 。
(7)BeCl 的纯度为 (用含m、a、b的式子表示)。
2
(8)下列情况会导致所测BeCl 的纯度偏小的是_______(填标号)。
2
A.滴定前尖嘴部分有一气泡,滴定终点时消失
B.滴定过程中,往锥形瓶内加入少量蒸馏水
C.滴定时,不慎将锥形瓶内溶液溅出少许
D.滴定前仰视读数,滴定后俯视读数
17.(14分)为实现“双碳”目标,采用甲烷-水蒸气重整和甲烷-二氧化碳干气重整工艺制备的富氢还原气
体冶炼钢铁是减少CO 排放的重要途径之一,涉及如下反应:
2
反应ⅰ:反应ⅱ:
反应ⅲ:
回答下列问题:
(1)CO(g)将HO(g)还原为H(g)的热化学方程式为 。
2 2
(2)反应ⅰ中,减小压强,CH 的平衡转化率 (填“增大”“减小”或“不变”),原因是
4
。
(3)一定温度下,一定量的CH 和CO 在恒容密闭容器中发生反应ⅲ,下列叙述能说明反应ⅲ已达到平衡状
4 2
态的是___________(填标号)。
A.单位时间内消耗1mol CH 的同时生成2mol H
4 2
B.混合气体的密度保持不变
C.
D.混合气体的平均摩尔质量不再变化
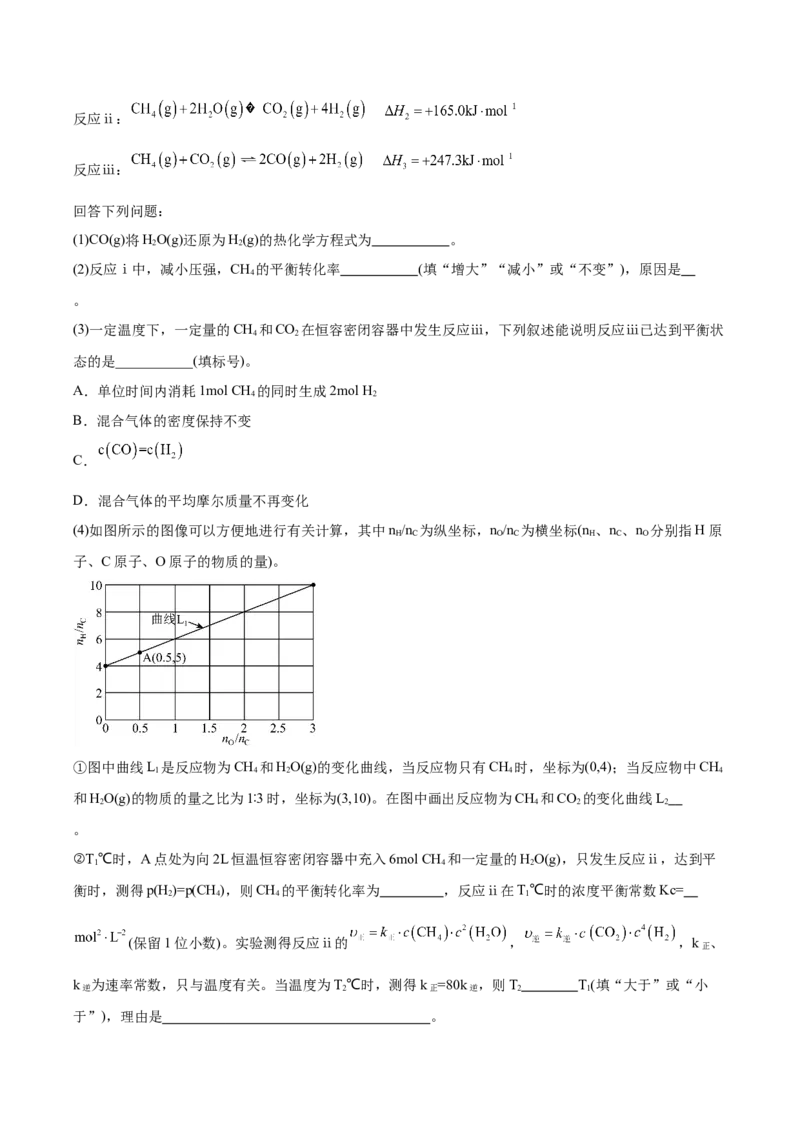
(4)如图所示的图像可以方便地进行有关计算,其中n /n 为纵坐标,n /n 为横坐标(n 、n 、n 分别指H原
H C O C H C O
子、C原子、O原子的物质的量)。
①图中曲线L 是反应物为CH 和HO(g)的变化曲线,当反应物只有CH 时,坐标为(0,4);当反应物中CH
1 4 2 4 4
和HO(g)的物质的量之比为1∶3时,坐标为(3,10)。在图中画出反应物为CH 和CO 的变化曲线L
2 4 2 2
。
②T ℃时,A点处为向2L恒温恒容密闭容器中充入6mol CH 和一定量的HO(g),只发生反应ⅱ,达到平
1 4 2
衡时,测得p(H )=p(CH ),则CH 的平衡转化率为 ,反应ⅱ在T℃时的浓度平衡常数Kc=
2 4 4 1
(保留1位小数)。实验测得反应ⅱ的 , ,k 、
正
k 为速率常数,只与温度有关。当温度为T℃时,测得k =80k ,则T T(填“大于”或“小
逆 2 正 逆 2 1
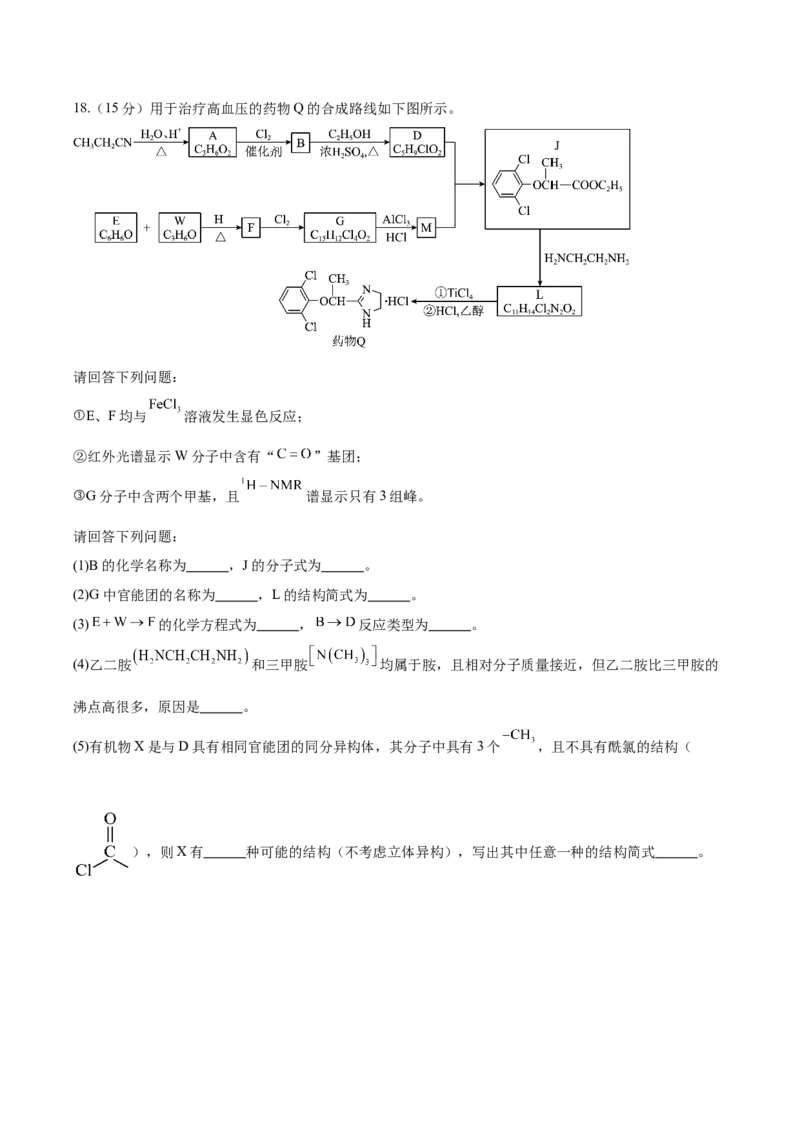
于”),理由是 。18.(15分)用于治疗高血压的药物Q的合成路线如下图所示。
请回答下列问题:
①E、F均与 溶液发生显色反应;
②红外光谱显示W分子中含有“ ”基团;
③G分子中含两个甲基,且 谱显示只有3组峰。
请回答下列问题:
(1)B的化学名称为 ,J的分子式为 。
(2)G中官能团的名称为 ,L的结构简式为 。
(3) 的化学方程式为 , 反应类型为 。
(4)乙二胺 和三甲胺 均属于胺,且相对分子质量接近,但乙二胺比三甲胺的
沸点高很多,原因是 。
(5)有机物X是与D具有相同官能团的同分异构体,其分子中具有3个 ,且不具有酰氯的结构(
),则X有 种可能的结构(不考虑立体异构),写出其中任意一种的结构简式 。