文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(河北专用)
化 学
考情速递
高考·新考法:
第13-14题,以锂离子电池为命题情境,分别考查电化学的有关计算和电极反应以及反应历程,体现
了对常规考点的创新糅合。
高考·新情境:
本套试卷情境丰富,如第1题以河北博物院馆藏文物为情境考查硅酸盐材料。第3题以CH 与Cl 在光
4 2
照发生的反应为情境考查阿伏加德罗常数。第17题以实现“双碳”目标为情境考查热化学方程式、化学
平衡状态、转化率、化学平衡常数等。
命题·大预测:
预测2025年高考河北卷化学试题继续保持稳中求新风格,试卷结构和试题难度保持相对稳定。高考
情境化试题比例将增加,彰显学科的价值引领。在备考时,注重教材知识在具体问题解决过程中的理解和
应用。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li7 Be9 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.燕赵大地历史悠久,文化灿烂。下列河北博物院馆藏文物的主要成分属于硅酸盐的是
选项 A B C D文物
朝代 战国(1977年出土) 五代(1995年出土) 北齐(1989年出土) 元(1964年出土)
文宣帝高洋墓墓道 青花海水龙纹八棱带
名称 错金银虎噬鹿屏风座 白石彩绘散乐图浮雕
壁画 盖瓷梅瓶
【答案】D
【解析】“错金银虎噬鹿屏风座”的主要材料是金属材料,A项不符合题意;“白石彩绘散乐图浮雕”的
主要材料是汉白玉(主要成分是 ),B项不符合题意;壁画的主要材料是颜料,如各种颜色的无机物,
C项不符合题意;“青花海水龙纹八棱带盖瓷梅瓶”的主要材料是陶瓷材料,其主要成分为硅酸盐,D项
符合题意;故选D。
2.下列化学用语使用正确的是
A.基态钾原子的核外电子排布式为
B.基态N原子的价层电子轨道表示式:
C. 键的形成:
D. 的结构示意图为
【答案】C
【解析】3d能级的能量大于4s能级,核外电子排布时,电子应先进入4s能级,再进入3d能级,故基态钾
原子的电子排布式为 ,A错误;基态N原子的价层电子排布式为2s22p3,则价层电子的
轨道表示式为 ,B错误;π键是p-p原子轨道以“肩并肩”方式重叠形成,即为,C正确;S2-的质子数为16,由S原子得到2个电子后形成,则S2-的核外电子数为
18,结构示意图为 ,D错误;故选C。
3. 与 混合后在密闭容器中光照发生的反应涉及HCl和氯代甲烷。设 为阿伏加德罗常数的值,
下列说法正确的是
A.0.5mol氯代甲烷的混合物中,含有 键的数目为2
B.0.1mol HCl溶于水,所得溶液中 数目为0.1
C.1mol 溶于水,充分反应后转移电子的数目为
D.1mol 与1mol 在密闭容器中反应后,容器内分子总数大于2
【答案】A
【解析】每个氯代甲烷分子中均含有4个 键,故0.5mol氯代甲烷的混合物中,含有 键的数目为2 ,
A项正确;盐酸中存在水的电离,故0.1mol HCl溶于水,所得溶液中 数目大于0.1 ,B项错误;
溶于水,不能与水完全反应 ,故1mol 溶于水,充分反应后转移电子的数目
小于 ,C项错误;由反应原理和原子守恒知,1mol 与1mol 在密闭容器中反应后,容器内分子
总数为2 ,D项错误;故选A。
4.下列离子方程式错误的是
A. 通入冷的 溶液中:
B.向苯酚钠 溶液中通入少量 :
C.用 溶液吸收少量 :D. 溶液与少量的 溶液混合:
【答案】D
【解析】 与冷的 反应生成NaCl和NaClO,反应离子方程式为: ,故
A正确;因酸性:HCO> >HCO ,苯酚钠 溶液中通入少量 ,反应生成苯酚和碳
2 3
酸氢钠,离子方程式为: ,故B正确; 溶液与少量 反
应,氯气被还原为氯离子,部分亚硫酸根被氧化为硫酸根,同时生成的氢离子与亚硫酸根结合成 ,
反应离子方程式为: ,故C正确;少量的物质完全反应,应按少量的
物质的电离比例书写离子方程式, 溶液与少量 溶液混合生成碳酸钡沉淀、水和碳酸根离
子: ,故D错误;故选D。
5.下列实验装置的使用或操作正确且能达到实验目的的是
A.测定原电池电压 B.分离铁粉和 C.碱式滴定管排气泡 D.测定中和反应的反应热
【答案】C
【解析】该装置未形成闭合回路,不能构成原电池装置,故A错误;铁粉与碘单质加热时发生反应,无法
分离,故B错误;碱式滴定管排气泡时,尖嘴向上倾斜,挤压玻璃珠快速放液,赶出气泡,故C正确;该
装置缺少保温措施,未使用环形玻璃搅拌器,会导致热量损失,无法准确测定反应热,故D错误;故选
C。
6.下列化学实验中的操作、现象及结论都正确的是
选
操作 现象 结论
项向1-溴丙烷中加入KOH溶液,加热并充分振荡, 溶液中出现棕黑色
A AgBr为棕黑色
然后取少量液体滴入 溶液中 沉淀
向甲基环己烷和甲苯中分别滴加少量酸性 溶 前者下层溶液为紫红色, 苯环使甲基变活
B
液,充分振荡 后者溶液为无色 泼
探究氯水颜色成因:取少量黄绿色的新制氯水,向 产生白色沉淀,溶液变无 氯水颜色与
C
其中滴加 溶液至过量 色 有关
试管底部固体消失,试管 固体受
D 将盛有 固体的试管加热
口有晶体凝结 热易升华
【答案】B
【解析】1-溴丙烷中加入KOH溶液,加热可发生水解反应,应在酸性溶液中检验溴离子,因为KOH与硝
酸银反应生成沉淀,由实验及现象不能证明1-溴丙烷中混有杂质,故A项错误;向甲基环己烷和甲苯中分
别滴加少量酸性KMnO 溶液,充分振荡,甲苯被氧化成苯甲酸,甲基环己烷酸性KMnO 溶液不反应,说
4 4
明苯环使甲基变活泼,故B项正确;新制氯水中存在 ,向其中滴加AgNO 溶液至
3
过量,氯离子浓度降低,平衡正向移动,氯气浓度变小,氯水黄绿色消失,故C项错误;加热盛有氯化铵
固体的试管,氯化铵受热分解生成氨气和HCl,试管底部固体消失;氨气和HCl在试管口又重新化合生成
氯化铵,导致有固体凝结,此过程并不是氯化铵固体受热升华,故D项错误; 故选B。
7.化合物M(如图所示)是一种医药中间体。下列关于M的说法错误的是
A.不含手性碳原子
B.能发生取代反应和氧化反应
C.分子中C原子有2种杂化方式
D.1mol M最多消耗 或NaOH的物质的量相等
【答案】D
【解析】由结构知,M中不含手性碳原子,A项正确;羧基能发生取代反应,燃烧属于氧化反应,B项正
确;分子中单键C原子为 杂化,羧基、酰胺基中的C为 杂化,C项正确;羧基可与碳酸氢钠反应,1mol M最多能消耗1mol ,M中含有酰胺基,故1mol M消耗NaOH的物质的量大于1mol,D项
错误;故选D。
8.某化合物是一种常见肥料,结构如下图。其中X、Y、Z、W为原子序数依次增大的短周期主族元素,
下列说法正确的是
A.分子的极性:YW>ZW B.第一电离能:YY>X D.键能:
【答案】A
【解析】根据该物质中各元素的成键特点及所带电荷数可知,X为H元素,Y为C元素,Z为N元素,W
为O元素。YW为CO,ZW为NO,周期表中同周期从左到右电负性依次增大,,同主族从上到
下,电负性依次减小,C、N、O属同一周期,电负性:O>N>C,电负性差值越大,极性越
强,则极性:CO>NO,故A项正确;同一周期元素的第一电离能随着原子序数的增大而呈增大的趋
势,但第IIA族和第VA族元素的第一电离能大于相邻元素, Y为C元素, Z为N元素,W为O元素,
则第一电离能为:N>O>C,故B项错误;同周期从左到右半径依次减小,从上到下半径依次增大,X为
H元素,Y为C元素, Z为N元素,则原子半径:C>N>H,故C项错误;双原子分子键能大小与其分子
结构中键的类型和数量有关,三键、双键、单键键能依次减弱,氮分子中含有N≡N键,氧分子中含有
O=O键,氢分子中含有H-H键,则键能: ,故D项错误;故选A。
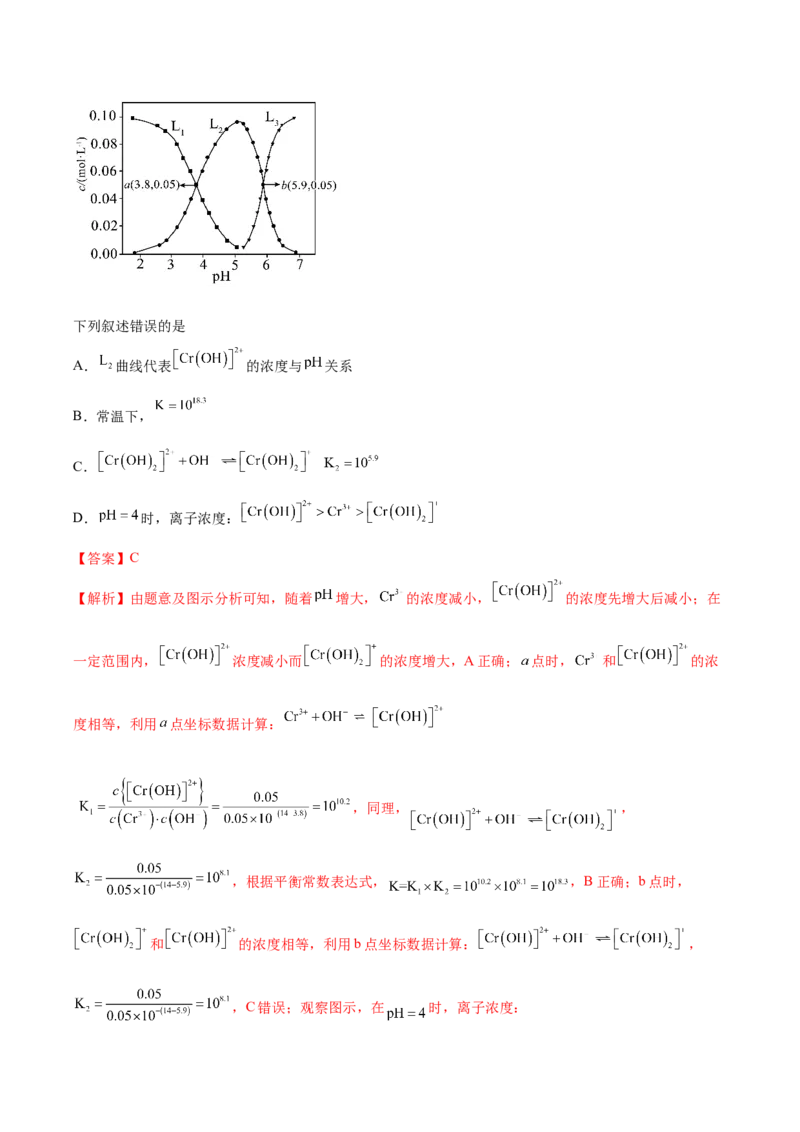
9.常温下,向 溶液中加入少量 粉末(忽略体积变化),含铬离子浓度与 关系
如图所示。已知: ; 。下列叙述错误的是
A. 曲线代表 的浓度与 关系
B.常温下,
C.
D. 时,离子浓度:
【答案】C
【解析】由题意及图示分析可知,随着 增大, 的浓度减小, 的浓度先增大后减小;在
一定范围内, 浓度减小而 的浓度增大,A正确; 点时, 和 的浓
度相等,利用 点坐标数据计算:
,同理, ,
,根据平衡常数表达式, ,B正确;b点时,
和 的浓度相等,利用b点坐标数据计算: ,
,C错误;观察图示,在 时,离子浓度:,D正确;故选C。
10.从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是
选
实例 解释
项
A 铍和铝都能与NaOH反应 基态铍原子和铝原子价电子数相同
B 冰的熔点高于干冰 分子间作用力不同
C 键角小于 中心原子杂化轨道类型不同
D 键能大于 、 原子半径不同
【答案】A
【解析】基态铍原子和铝原子的价电子数分别为2、3,价电子数不相同, 正确的解释应该是根据对角线规
则,铍和铝的化学性质相似,都能表现出两性,因此都能与NaOH反应,A错误;冰分子间存在氢键和范
德华力,干冰分子间只存在范德华力,二者作用力类型不同,作用力类型强度不同,B正确; 中硫原
子的孤电子对数为 、价层电子对数为2+1=3,则杂化轨道类型为 ,呈V形, 中碳原子
的孤电子对数为 、价层电子对数为2+0=2,杂化轨道类型为 杂化、呈直线形,C正确;氮原
子半径小于碳原子,导致 比 的键长短,键能大,D正确; 故选A。
11. 元素基态原子的价层电子排布式为 。 元素的一种氧化物Z的晶体是由图1所示的结构平
移构成。图1包含I型和Ⅱ型两种小立方体;图2是Z的晶胞, 分别对应图1中的小立方体I或Ⅱ(其
中阿伏加德罗常数的值用 表示,Z的摩尔质量为 )。下列说法错误的是A. 元素形成的氧化物Z的化学式为
B.图2中Ⅱ型小立方体可能是b、d、e、g
C.Ⅱ型中两个 最近距离为该小立方体边长的
D.若I型和Ⅱ型小立方体的边长均为 ,则Z的密度为
【答案】C
【解析】N元素基态原子的价层电子排布式为 ,则N是Fe元素,Ⅰ型立体结构中Fe2+位于顶点和体
心,离子数是4× +1,O2-位于晶胞内,离子数是4,Ⅱ型立方体中Fe2+位于顶点,离子数是4× ,O2-位于
晶胞内,离子数是4,Fe3+位于晶胞内,离子数是4,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,所
以1个晶胞含有Fe2+数是8、O2-数是32、Fe3+数是16。由分析可知,晶体中三种离子个数比
N(Fe2+)∶N(Fe3+)∶N(O2-)=8∶16∶32= 1∶2∶4,故化学式为 ,A正确;由图可知,晶胞中Ⅰ型立体结构、Ⅱ型
立方体交叉排列,所以Ⅱ型小立方体可能是b、d、e、g,B正确;Ⅱ型小立方体中Fe2+位于顶点,最近距
离两个Fe2+为小立方体的面对角线,为边长的 倍,C错误;由分析可知,图2所示晶胞质量为
,晶胞体积为 ,所以密度为 ,则 的密度为
,D正确。故选C。
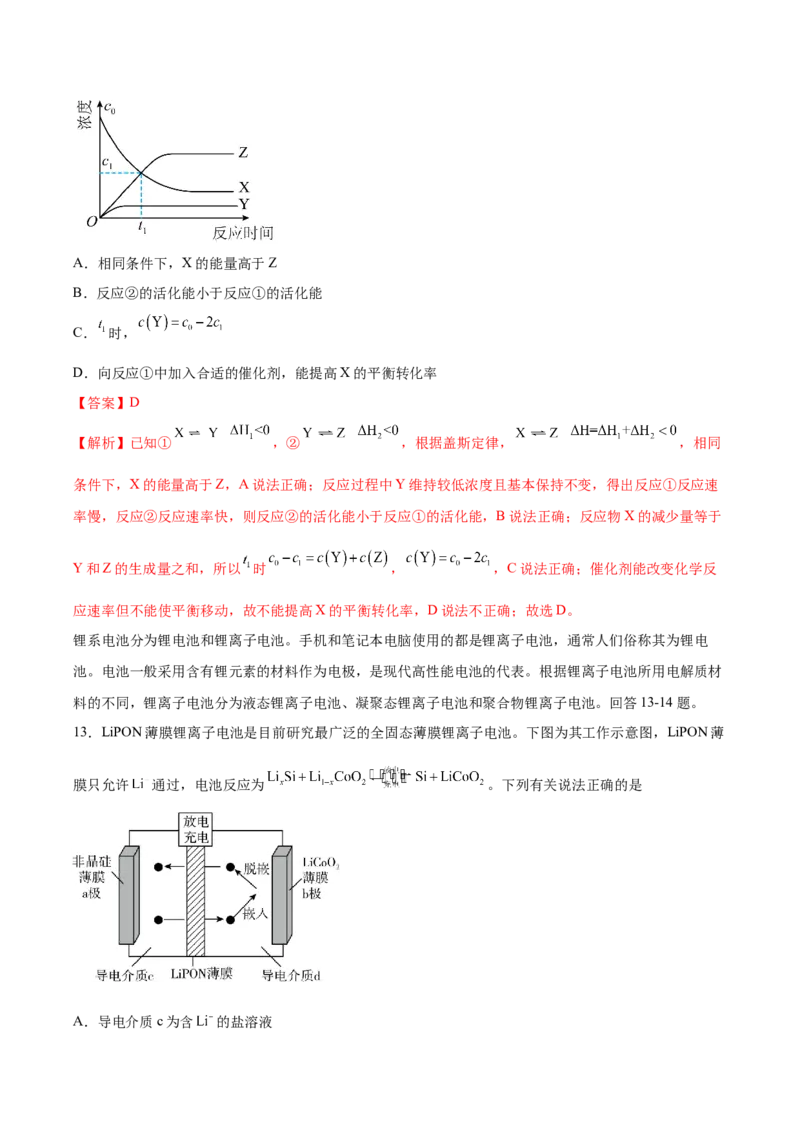
12.反应 经历两步:① ;② 。反应体系中X、Y、Z的浓度c随
时间t的变化曲线如图所示。下列说法不正确的是A.相同条件下,X的能量高于Z
B.反应②的活化能小于反应①的活化能
C. 时,
D.向反应①中加入合适的催化剂,能提高X的平衡转化率
【答案】D
【解析】已知① ,② ,根据盖斯定律, ,相同
条件下,X的能量高于Z,A说法正确;反应过程中Y维持较低浓度且基本保持不变,得出反应①反应速
率慢,反应②反应速率快,则反应②的活化能小于反应①的活化能,B说法正确;反应物X的减少量等于
Y和Z的生成量之和,所以 时 , ,C说法正确;催化剂能改变化学反
应速率但不能使平衡移动,故不能提高X的平衡转化率,D说法不正确;故选D。
锂系电池分为锂电池和锂离子电池。手机和笔记本电脑使用的都是锂离子电池,通常人们俗称其为锂电
池。电池一般采用含有锂元素的材料作为电极,是现代高性能电池的代表。根据锂离子电池所用电解质材
料的不同,锂离子电池分为液态锂离子电池、凝聚态锂离子电池和聚合物锂离子电池。回答13-14题。
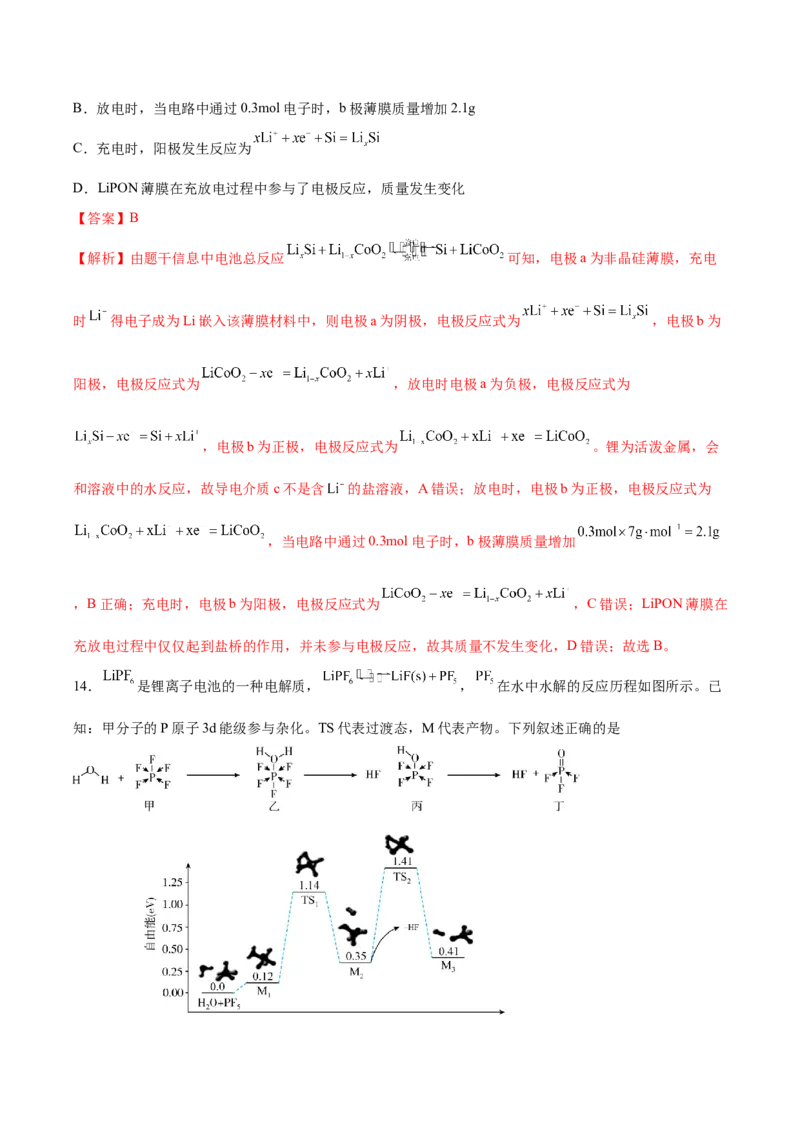
13.LiPON薄膜锂离子电池是目前研究最广泛的全固态薄膜锂离子电池。下图为其工作示意图,LiPON薄
膜只允许 通过,电池反应为 。下列有关说法正确的是
A.导电介质c为含 的盐溶液B.放电时,当电路中通过0.3mol电子时,b极薄膜质量增加2.1g
C.充电时,阳极发生反应为
D.LiPON薄膜在充放电过程中参与了电极反应,质量发生变化
【答案】B
【解析】由题干信息中电池总反应 可知,电极a为非晶硅薄膜,充电
时 得电子成为Li嵌入该薄膜材料中,则电极a为阴极,电极反应式为 ,电极b为
阳极,电极反应式为 ,放电时电极a为负极,电极反应式为
,电极b为正极,电极反应式为 。锂为活泼金属,会
和溶液中的水反应,故导电介质c不是含 的盐溶液,A错误;放电时,电极b为正极,电极反应式为
,当电路中通过0.3mol电子时,b极薄膜质量增加
,B正确;充电时,电极b为阳极,电极反应式为 ,C错误;LiPON薄膜在
充放电过程中仅仅起到盐桥的作用,并未参与电极反应,故其质量不发生变化,D错误;故选B。
14. 是锂离子电池的一种电解质, , 在水中水解的反应历程如图所示。已
知:甲分子的P原子3d能级参与杂化。TS代表过渡态,M代表产物。下列叙述正确的是A.总反应的焓变( )小于0
B.按照VSEPR理论,甲分子中P原子采用 杂化
C.上述分步反应中 的能垒最大
D.丁挥发时要克服极性键
【答案】B
【解析】根据图示,总反应为 ,反应物的总能量小于生成物的总能量,总反应为吸
热反应,总反应的焓变大于0,A错误; 分子中P的价层电子对数为 ,P原子的3d
能级参与杂化,则 中P原子采取 杂化,B正确; 的能垒为 ,
的能垒为 ,故 的能垒最大,C错误;丁( )是由分子构成
的物质,挥发时克服分子间作用力,不需要克服极性键,D错误;故选B。
二、非选择题:本题共4小题,共58分。
15.(14分)钛白粉 是一种重要的工业原料,可作白色颜料和增白剂。一种以钛铁矿(主要成分是
,含有少量的CaO、 等杂质)为原料生产制备 的工艺流程如下:
回答下列问题:
(1)基态Ti的核外价电子排布式为 。
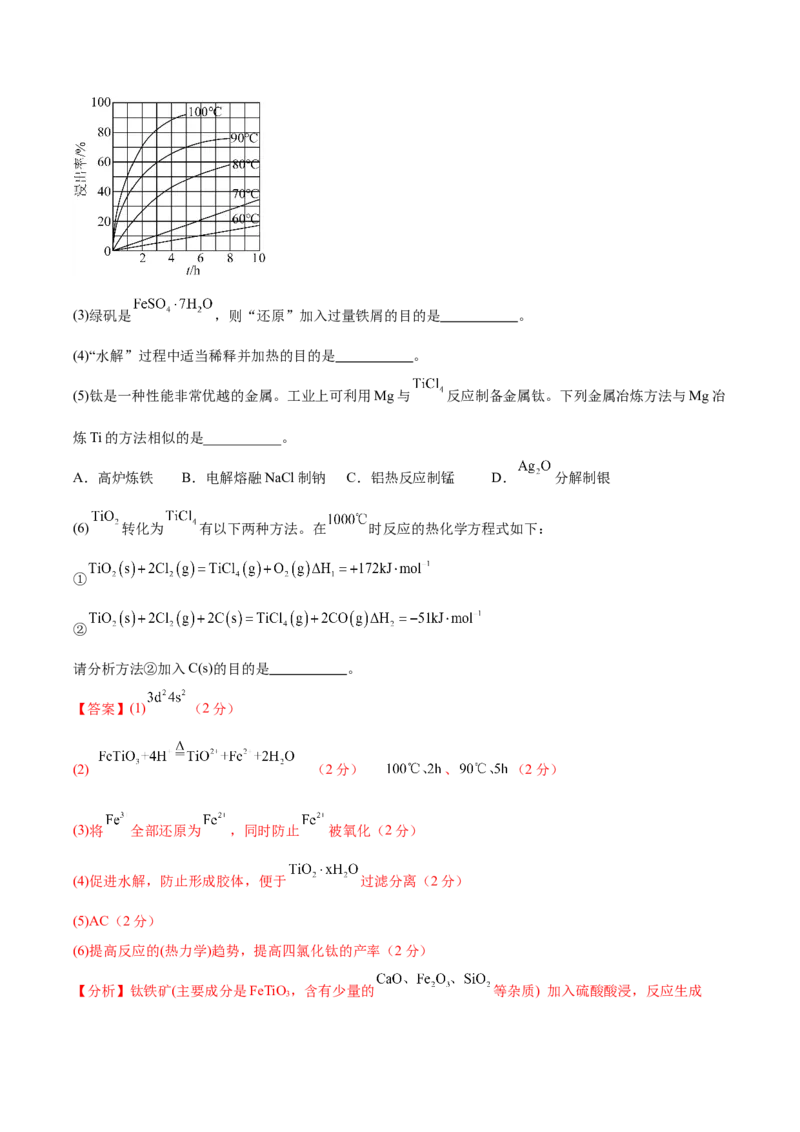
(2)“酸浸”是用硫酸在加热下“溶煮”钛铁矿,“滤液1”中Ti的存在形式为 ,则“酸浸”中
发生反应的离子方程式为 。由图可知,当浸出率为70%时,所采用的实验条件为
。(3)绿矾是 ,则“还原”加入过量铁屑的目的是 。
(4)“水解”过程中适当稀释并加热的目的是 。
(5)钛是一种性能非常优越的金属。工业上可利用Mg与 反应制备金属钛。下列金属冶炼方法与Mg冶
炼Ti的方法相似的是___________。
A.高炉炼铁 B.电解熔融NaCl制钠 C.铝热反应制锰 D. 分解制银
(6) 转化为 有以下两种方法。在 时反应的热化学方程式如下:
①
②
请分析方法②加入C(s)的目的是 。
【答案】(1) (2分)
(2) (2分) 、 (2分)
(3)将 全部还原为 ,同时防止 被氧化(2分)
(4)促进水解,防止形成胶体,便于 过滤分离(2分)
(5)AC(2分)
(6)提高反应的(热力学)趋势,提高四氯化钛的产率(2分)
【分析】钛铁矿(主要成分是FeTiO,含有少量的 等杂质) 加入硫酸酸浸,反应生成
3、 、 和微溶的 , 不与酸反应,过滤后所得滤液1中加入铁屑,将三价
铁转化为二价铁,再将绿矾 分离出来, 经过水解后得到 和硫酸,最后烧
得到钛白粉( );
【解析】(1)Ti是第22号元素,基态 的价层电子排布式为 ;
(2)“酸浸”是硫酸与 发生反应,离子方程式为 ;当Fe的浸出
率为70%时,可对应 和 两条曲线,故实验条件为: 、 ;
(3)加入过量铁粉是为了将 全部还原为 ,同时防止 被氧化;
(4)“水解”过程中适当稀释并加热是为了促进水解,防止形成胶体,便于 过滤分离;
(5)工业上可利用Mg与 反应制备金属钛,利用的是热还原法,B为电解法,D为热分解法,故选
AC;
(6)方法①为吸热反应,方法②为放热反应,加入 可以使反应①氧气减少,促进反应正向移动,反
应②为熵增反应,故加 的目的是提高反应的热力学趋势,提高四氯化钛的产率。
16.(15分)某实验小组以粗铍(含少量的Mg、Fe、Al、Si)为原料制备、提纯BeCl ,并测定产品中BeCl
2 2
的含量。
已知:①乙醚沸点为34.5℃;BeCl 溶于乙醚,不溶于苯,易与水发生反应;MgCl 、FeCl 不溶于乙醚和
2 2 2
苯;AlCl 溶于乙醚和苯。
3
②Be(OH) 与Al(OH) 的化学性质相似。
2 3
回答下列问题:
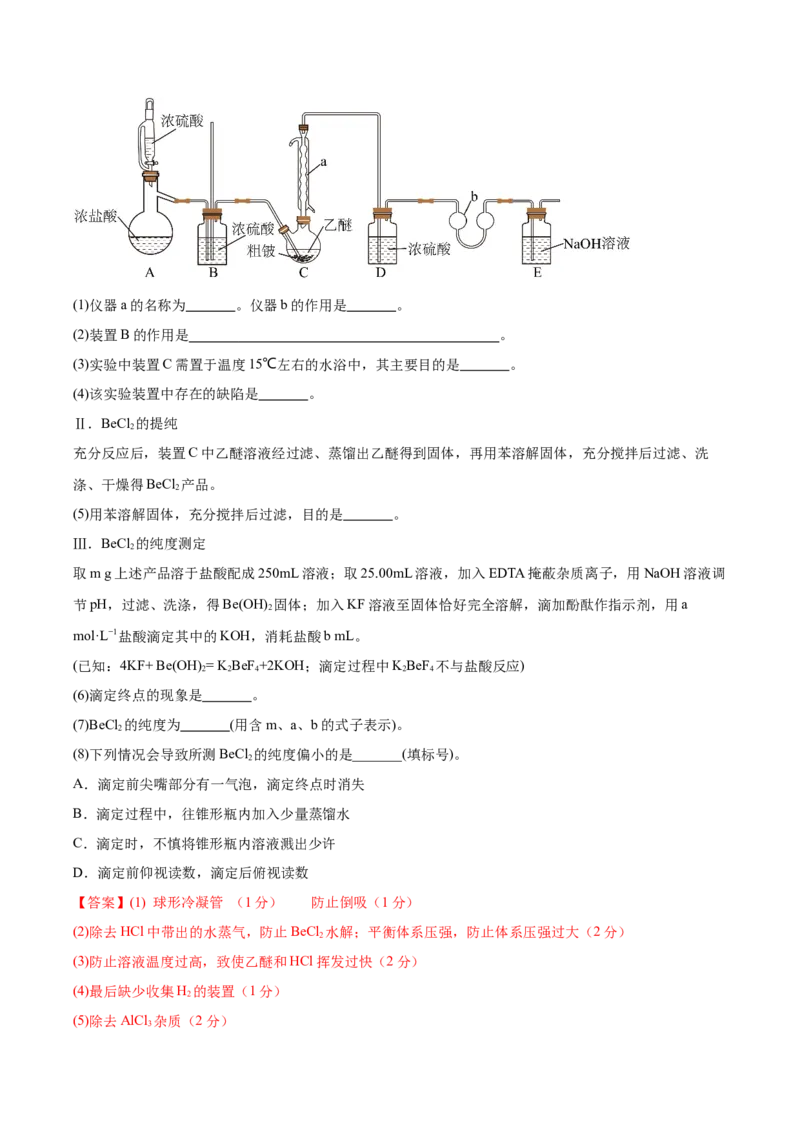
Ⅰ.制备BeCl :按如图所示装置(夹持装置略)制备BeCl 。
2 2(1)仪器a的名称为 。仪器b的作用是 。
(2)装置B的作用是 。
(3)实验中装置C需置于温度15℃左右的水浴中,其主要目的是 。
(4)该实验装置中存在的缺陷是 。
Ⅱ.BeCl 的提纯
2
充分反应后,装置C中乙醚溶液经过滤、蒸馏出乙醚得到固体,再用苯溶解固体,充分搅拌后过滤、洗
涤、干燥得BeCl 产品。
2
(5)用苯溶解固体,充分搅拌后过滤,目的是 。
Ⅲ.BeCl 的纯度测定
2
取m g上述产品溶于盐酸配成250mL溶液;取25.00mL溶液,加入EDTA掩蔽杂质离子,用NaOH溶液调
节pH,过滤、洗涤,得Be(OH) 固体;加入KF溶液至固体恰好完全溶解,滴加酚酞作指示剂,用a
2
mol·L−1盐酸滴定其中的KOH,消耗盐酸b mL。
(已知:4KF+ Be(OH) = K BeF +2KOH;滴定过程中KBeF 不与盐酸反应)
2 2 4 2 4
(6)滴定终点的现象是 。
(7)BeCl 的纯度为 (用含m、a、b的式子表示)。
2
(8)下列情况会导致所测BeCl 的纯度偏小的是_______(填标号)。
2
A.滴定前尖嘴部分有一气泡,滴定终点时消失
B.滴定过程中,往锥形瓶内加入少量蒸馏水
C.滴定时,不慎将锥形瓶内溶液溅出少许
D.滴定前仰视读数,滴定后俯视读数
【答案】(1) 球形冷凝管 (1分) 防止倒吸(1分)
(2)除去HCl中带出的水蒸气,防止BeCl 水解;平衡体系压强,防止体系压强过大(2分)
2
(3)防止溶液温度过高,致使乙醚和HCl挥发过快(2分)
(4)最后缺少收集H 的装置(1分)
2
(5)除去AlCl 杂质(2分)
3(6)当滴入最后一滴盐酸,溶液由浅红色褪为无色,且半分钟不恢复原色(2分)
(7) (2分)
(8)CD(2分)
【分析】装置A中,将浓硫酸通过恒压滴液漏斗加入蒸馏烧瓶中,浓硫酸吸水放热,降低HCl的溶解度,
从而制取HCl气体;装置B中,用浓硫酸吸收HCl中混有的水蒸气,同时平衡内外压强;装置C中,粗铍
中的Be、Al、Mg、Fe都能与HCl发生反应,而Si不反应,用球形冷凝管使乙醚、HCl冷凝回流;装置D
用于防止E中产生的水蒸气的进入;双球U形管用于防止倒吸;装置E用于吸收未反应的HCl,但没有对
反应生成的H 进行收集,会带来安全隐患。
2
【解析】(1)仪器a为内管呈球形的冷凝管,名称为:球形冷凝管。仪器b为双球U形管,作用是:防止
倒吸。
(2)题干信息显示,BeCl 易发生水解,浓盐酸产生的HCl气体中常带有水蒸气,长玻璃导管能起调节瓶
2
内外压强的作用,则装置B的作用是:除去HCl中带出的水蒸气,防止BeCl 水解;平衡体系压强,防止
2
体系压强过大。
(3)在装置C中,HCl与铍、铝、铁、镁等都能发生反应,但HCl和乙醚的沸点低,所以装置C需置于
温度15℃左右的水浴中,其主要目的是:防止溶液温度过高,致使乙醚和HCl挥发过快。
(4)H 是易燃气体,会带来安全隐患,则该实验装置中存在的缺陷是:最后缺少收集H 的装置。
2 2
(5)BeCl 溶于乙醚,不溶于苯,易与水发生反应;MgCl 、FeCl 不溶于乙醚和苯;AlCl 溶于乙醚和苯。
2 2 2 3
反应结束后,充分搅拌过滤出不溶的MgCl 、FeCl ,此时BeCl 、AlCl 仍溶解在乙醚中,蒸馏出乙醚,得
2 2 2 3
到二种固体盐。用苯溶解固体,将AlCl 溶解,得到不溶的BeCl ,则此操作的目的是:除去AlCl 杂质。
3 2 3
(6)滴定前,溶液呈碱性,酚酞变红色,滴定终点时,酚酞的红色褪去,则现象是:当滴入最后一滴盐
酸,溶液由浅红色褪为无色,且半分钟不恢复原色。
(7)由反应可建立关系式:BeCl —Be(OH) —2KOH—2HCl,n(HCl)=a mol·L−1×b ×10-3L=ab×10-3mol,
2 2
n(BeCl )= ab×10-3mol,则BeCl 的纯度为 = 。
2 2
(8)A.滴定前尖嘴部分有一气泡,滴定终点时消失,则读取消耗盐酸的体积偏大,测定结果偏大,A不
符合题意;
B.滴定过程中,往锥形瓶内加入少量蒸馏水,对KOH的物质的量不产生影响,不影响滴加盐酸的体积,
测定结果不变,B不符合题意;C.滴定时,不慎将锥形瓶内溶液溅出少许,则KOH的物质的量减小,消耗盐酸的体积减小,测定结果偏
小,C符合题意;
D.滴定前仰视读数,滴定后俯视读数,则读取消耗盐酸的体积偏小,测定结果偏小,D符合题意;
故选CD。
17.(14分)为实现“双碳”目标,采用甲烷-水蒸气重整和甲烷-二氧化碳干气重整工艺制备的富氢还原气
体冶炼钢铁是减少CO 排放的重要途径之一,涉及如下反应:
2
反应ⅰ:
反应ⅱ:
反应ⅲ:
回答下列问题:
(1)CO(g)将HO(g)还原为H(g)的热化学方程式为 。
2 2
(2)反应ⅰ中,减小压强,CH 的平衡转化率 (填“增大”“减小”或“不变”),原因是
4
。
(3)一定温度下,一定量的CH 和CO 在恒容密闭容器中发生反应ⅲ,下列叙述能说明反应ⅲ已达到平衡状
4 2
态的是___________(填标号)。
A.单位时间内消耗1mol CH 的同时生成2mol H
4 2
B.混合气体的密度保持不变
C.
D.混合气体的平均摩尔质量不再变化
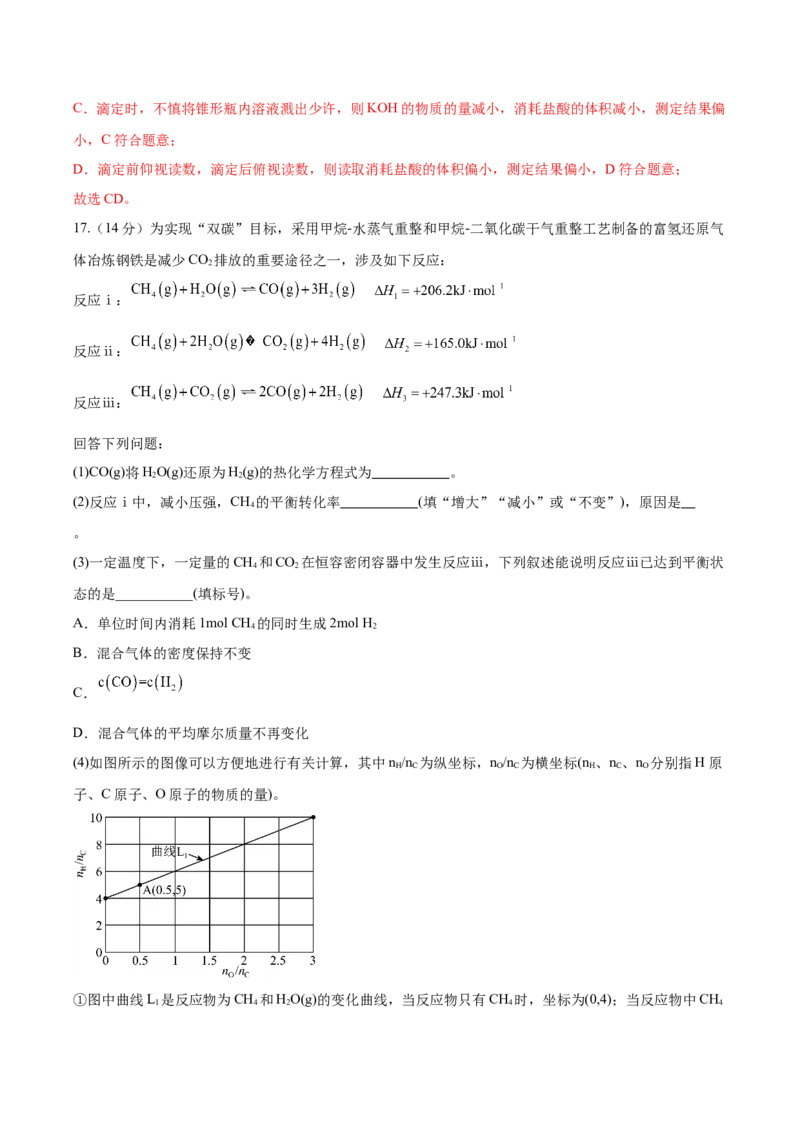
(4)如图所示的图像可以方便地进行有关计算,其中n /n 为纵坐标,n /n 为横坐标(n 、n 、n 分别指H原
H C O C H C O
子、C原子、O原子的物质的量)。
①图中曲线L 是反应物为CH 和HO(g)的变化曲线,当反应物只有CH 时,坐标为(0,4);当反应物中CH
1 4 2 4 4和HO(g)的物质的量之比为1∶3时,坐标为(3,10)。在图中画出反应物为CH 和CO 的变化曲线L
2 4 2 2
。
②T ℃时,A点处为向2L恒温恒容密闭容器中充入6mol CH 和一定量的HO(g),只发生反应ⅱ,达到平
1 4 2
衡时,测得p(H )=p(CH ),则CH 的平衡转化率为 ,反应ⅱ在T℃时的浓度平衡常数Kc=
2 4 4 1
(保留1位小数)。实验测得反应ⅱ的 , ,k 、
正
k 为速率常数,只与温度有关。当温度为T℃时,测得k =80k ,则T T(填“大于”或“小
逆 2 正 逆 2 1
于”),理由是 。
【答案】(1) (2分)
(2) 增大 (1分) 该反应为气体分子数增多的反应,减小压强,平衡向正反应方向移动,CH 的平衡
4
转化率增大(2分)
(3)D(1分)
(4) (2分) 20% (2分) 92.2 (2分) 小于 (1分)
反应ⅱ为吸热反应,降低温度,平衡向反应ⅱ的逆反应方向移动,平衡常数减小,T℃时该反应的浓度平
2
衡常数 (T ℃时该反应的浓度平衡常数),故T 小于T(2分)
1 2 1
【解析】(1)由题干已知信息可知,反应ⅰ:
反应ⅱ: 可知反应ii-反应i可得CO(g)将
HO(g)还原为H(g)的反应方程式: ,根据盖斯定律可知,该反应的反
2 2应热 = =165.0-206.2=-41.2kJ/mol,故该反应的热化学方程式为:
=-41.2kJ/mol,故答案为:
=-41.2kJ/mol;
(2)由题干已知信息可知,反应ⅰ 正反应是一个气体体积增大的方
向,则减小压强,上述平衡正向移动,则CH 的平衡转化率增大,故答案为:增大;该反应为气体分子数
4
增多的反应,减小压强,平衡向正反应方向移动,CH 的平衡转化率增大;
4
(3)由题干已知信息可知,反应ⅲ: 正反
应是一个气体体积增大的吸热反应,据此分析解题:
A.化学反应平衡的本质特征为正、逆反应速率相等,而消耗CH 和生成H 均为正反应,故单位时间内消
4 2
耗1mol CH 的同时生成2mol H 不能说明反应达到化学平衡,A不合题意;
4 2
B.反应前后气体的质量不变,在恒容密闭容器中反应则气体的体积不变,即反应过程中混合气体的密度
始终保持不变,故混合气体的密度保持不变不能说明反应达到化学平衡,B不合题意;
C.化学反应平衡的本质特征之一为各组分的浓度保持不变而不是相等或成比例,故当 不能
说明反应达到化学平衡,C不合题意;
D.该反应前后气体的物质的量一直改变,混合气体的质量保持不变,即混合气体的平均摩尔质量一直改
变,则混合气体的平均摩尔质量不再变化说明反应达到化学平衡,D符合题意;故选D;
(4)①图中曲线L 是反应物为CH 和HO(g)的变化曲线,当反应物只有CH 时,坐标为(0,4)即n /n =4,
1 4 2 4 H C
n /n =0;当反应物中CH 和HO(g)的物质的量之比为1∶3时,坐标为(3,10) n /n = =10,n /n =3;在
O C 4 2 H C O C
反应物为CH 和CO 则当反应物只有CH 时,则坐标仍为(0,4),当反应物只有CO 时,则坐标仍为(2, 0),
4 2 4 2
故变化曲线L 如图所示: ;
2②T ℃时,由题干图示信息可知,A点处为n /n =5,n /n =0.5,即CH 和HO的物质的量之比为2:1,向
1 H C O C 4 2
2L恒温恒容密闭容器中充入6mol CH 和一定量的HO(g),只发生反应ⅱ,根据三段式分析:
4 2
达到平衡时,测得p(H )=p(CH )即n(H )=n(CH )即6-x=4x,解得x=1.2mol,则CH 的平衡转化率为
2 4 2 4 4
×100%=20%,反应ⅱ在T℃时的浓度平衡常数Kc= =
1
=92.2 (保留1位小数),实验测得反应ⅱ的 , ,
k 、k 为速率常数,只与温度有关,当温度为T℃时,测得k =80k ,化学平衡的本质特征为:
正 逆 2 正 逆
,则有 =K( )=80<K( ),
T2 T2
则T 小于T,故答案为:20%;92.2;小于;反应ⅱ为吸热反应,降低温度,平衡向反应ⅱ的逆反应方向
2 1
移动,平衡常数减小,T℃时该反应的浓度平衡常数 (T ℃时该反应的浓度平衡常数),故
2 1
T 小于T。
2 1
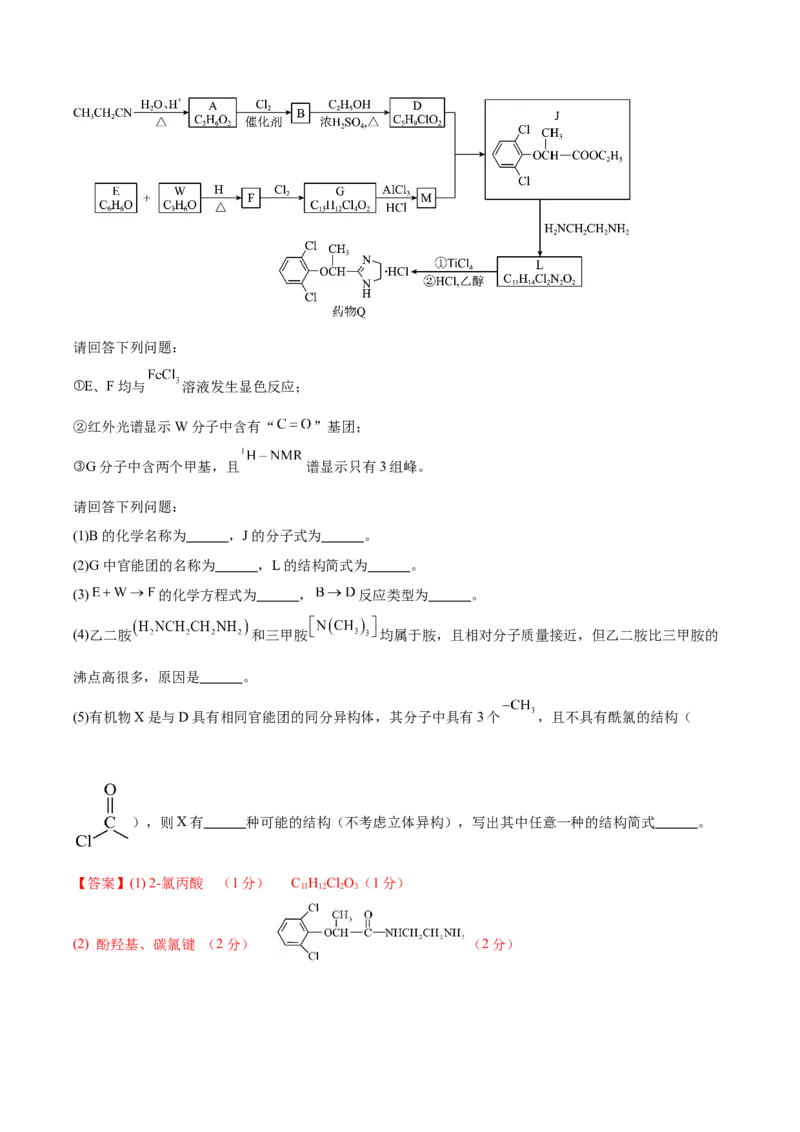
18.(15分)用于治疗高血压的药物Q的合成路线如下图所示。请回答下列问题:
①E、F均与 溶液发生显色反应;
②红外光谱显示W分子中含有“ ”基团;
③G分子中含两个甲基,且 谱显示只有3组峰。
请回答下列问题:
(1)B的化学名称为 ,J的分子式为 。
(2)G中官能团的名称为 ,L的结构简式为 。
(3) 的化学方程式为 , 反应类型为 。
(4)乙二胺 和三甲胺 均属于胺,且相对分子质量接近,但乙二胺比三甲胺的
沸点高很多,原因是 。
(5)有机物X是与D具有相同官能团的同分异构体,其分子中具有3个 ,且不具有酰氯的结构(
),则X有 种可能的结构(不考虑立体异构),写出其中任意一种的结构简式 。
【答案】(1) 2-氯丙酸 (1分) C H ClO(1分)
11 12 2 3
(2) 酚羟基、碳氯键 (2分) (2分)(3) (2分) 取代反应(酯化反应)(1分)
(4)乙二胺存在分子间氢键而三甲胺不存在分子间氢键(2分)
(5)2 (2分) 、 (2分)
【解析】CHCHCN在酸性条件下水解生成A为CHCHCOOH,A与氯气在催化剂作用下反应生成B,B
3 2 3 2
与乙醇在浓硫酸、加热条件下反应生成D,则B生成D的反应为酯化反应,结合J的结构简式可知,D的
结构简式为CHCHClCOOCH CH,则B的结构简式为CHCHClCOOH。E、F均与氯化铁溶液发生显色反
3 2 3 3
应,E为苯酚,W中含有C=O基团,则W为丙酮,D和M反应生成J,根据J和D的结构简式可知,M
为 ,G与AlCl 、HCl反应生成M,且G分子中含两个甲基,有3组峰,G为
3
,则F为 。J与HNCH CHNH 反应生成L,结合L的分子式
2 2 2 2
可知L为 ,L经过①、②两步反应生成Q。
(1)B的结构简式为CHCHClCOOH,其名称为2-氯丙酸。根据J的结构简式可知其分子式为
3
C H ClO。
11 12 2 3
(2)G的结构简式为 ,其中官能团名称为酚羟基、碳氯键。L的结构简式为
。
(3)E和W分别为苯酚和丙酮,两者在酸性、加热条件下反应生成F 和水,化学方程式为 。根据分析可知,B与乙醇发生酯化反应
生成D,反应类型为取代反应(酯化反应)。
(4)乙二胺中N与H直接相连,该H原子呈正电性,容易与另一个乙二胺中的N原子形成分子间氢键,
而三甲胺中H未与N原子直接相连,无法形成分子间氢键,因此乙二胺比三甲胺的沸点高很多。
(5)有机物X与D具有相同的官能团且互为同分异构体,则X中存在酯基,分子中存在三个甲基,且不
具有酰氯的结构,则满足条件的同分异构体为 、 ,共两种。